ANTECEDENTES
El angioedema hereditario es un trastorno autosómico dominante causado por la deficiencia del inhibidor C1 (AEH tipo 1) o disminución de su función (AEH tipo 2); sin embargo, se han reportado casos de enfermedad en pacientes con concentraciones normales del inhibidor C1. El Angioedema hereditario tipo 1 representa el 85% de los casos. Es importante señalar que los pacientes no siempre tienen antecedentes familiares de la enfermedad, y aproximadamente el 25 % de los casos de angioedema hereditario tienen enfermedad de novo.1
El angioedema hereditario es una enfermedad excepcional, con una prevalencia de 1.1 y 1.6 por cada 50,000 habitantes en América del Norte y Europa, respectivamente.2 En Latinoamérica, por tratarse de una enfermedad subdiagnosticada, no se cuenta con demasiada información, pero en México se documentó una prevalencia estimada de 0.805 por cada 50,000 habitantes en el año 2019, donde el 84.2% correspondieron al tipo 1, el 14.9% al tipo 2 y el 0.9% con inhibidor C1 normal. En Colombia se desconoce la prevalencia de angioedema hereditario.3
Dentro de la fisiopatología de la enfermedad, se manifiesta con alteración del inhibidor C1, que regula la vía del complemento, con subsiguiente aumento de la producción de bradicinina, alteración en la permeabilidad capilar, edema generalizado en los tejidos blandos y las mucosas, sin urticaria.4
Para el tratamiento de la enfermedad, según las guías de la Asociación Estadounidense de Angioedema Hereditario y la guía internacional WAO/EAACI, en los episodios agudos se estipulan concentrados de C1INH derivados del plasma (pdC1INH, Berinert) y el C1INH humano recombinante (rhC1INH, Ruconest), que se administran por vía endovenosa; además del inhibidor de la calicreína plasmática (Ecallantide) y el antagonista del receptor de bradicinina B2 (Icatibant), aplicados por vía subcutánea.5,6
El tratamiento profiláctico de primera línea, a largo plazo, consiste en Lanadelumab (anticuerpo monoclonal de la calicreína plasmática), Cinryze (tratamiento de reemplazo de pdC1INH por vía intravenosa) y Haegarda (tratamiento de reemplazo de pdC1INH por vía subcutánea). El tratamiento de segunda línea incluye Danazol por vía oral, que potencia la síntesis hepática de inhibidor C1, y los antifibrinolíticos (ácido tranexámico o ácido épsilon aminocaproico).7,8
En la bibliografía se han documentado casos de reacción adversa al tratamiento con Lanadelumab, casi siempre de tipo leve y con baja incidencia.9 Es así como en el estudio HELP se informaron reacciones adversas al medicamento en menos del 20% de los pacientes, la mayor parte leves en el 98.8%,10 por ejemplo: dolor en el sitio de aplicación, infecciones virales de la vía respiratoria alta, cefalea, entre otros; sin embargo, del total de pacientes estudiados se informó solo un evento de reacción de hipersensibilidad, con interrupción del tratamiento. Este tipo de hallazgos fueron similares en el estudio de seguimiento posterior, es decir, el HELP OLE.11
Dentro de las escalas para la compresión del control de la enfermedad en pacientes con angioedema recurrente destaca el AECT (Angioedema Control Test), que analiza 4 ítems (frecuencia de los síntomas, afectación en la calidad de vida, impredictibilidad de aparición del cuadro y control de los síntomas con el tratamiento en las últimas 4 semanas); la puntuación mayor de 10 indica buen control y el valor menor de 10 evidencia mal control de la enfermedad.12 Incluso se cuenta con el AE-QoL (The Angioedema QoL Questionnaire), que consta de 17 preguntas en 4 dominios, donde se evalúa: funcionamiento, fatiga-estado de ánimo, miedo-vergüenza y comida durante las 4 semanas anteriores; la puntuación se interpreta mediante una escala lineal que va de 0 a 100, donde el valor de 100 indica el peor deterioro posible.13
REPORTE DE CASO
Paciente masculino de 53 años, originario de Toca, Boyacá, Colombia, sin antecedentes patológicos previos; antecedente de consumo frecuente de alcohol, sin exposición al tabaco, quien labora como agricultor. Inició con un cuadro clínico a los 20 años de edad, consistente en episodios de edema recurrente en la cara, las extremidades inferiores y el escroto, asociado con dolor abdominal, sin eritema, que desaparecían de forma espontánea entre 24 y 48 horas, por lo que nunca asistió a consulta médica. Debido a los antecedentes en familiares de primer grado de consanguinidad (hermano, sobrinos e hijos) de angioedema hereditario tipo 1 (AEH-1), se le realizaron estudios de laboratorio en 2015 que reportaron concentraciones elevadas de proteína plasmática (antigénica) y C1-INH funcional, y concentraciones bajas del complemento C4 (Cuadro 1), en quien dado contexto clínico, antecedentes familiares del paciente, se consideró paciente cursaba con cuadro de Angioedema hereditario tipo 1, al paciente no le fueron repetidas las pruebas de laboratorio confirmatorio ni toma de pruebas genéticas por disentimiento del paciente.
Cuadro 1. Resultados de laboratorio efectuados en 2015
| C1 inhibidor funcional | Referencia: normal mayor de 67 | Resultado: 24 mg/dL |
| C1 inhibidor antígeno | Referencia:19.0-37.0 | Resultado: menor a 3 mg/dL |
| Complemento C4 | Referencia: 10-40 | Resultado: 0.0 mg/dL |
En 2016 inició el protocolo para los episodios de edema con Icatibant (30 mg) por vía subcutánea, con adecuada respuesta y desaparición de los síntomas 20 minutos después de recibir el tratamiento. En el año 2021 se evidenció aumento de la frecuencia de los episodios (tres episodios en cuatro meses), con predominio de síntomas gastrointestinales, por lo que se decidió iniciar el tratamiento profiláctico a largo plazo con Danazol, en dosis de 100 mg cada 3 días por 3 semanas. Sin embargo, tuvo reacción adversa a la medicación, con aumento de las transaminasas. Tomando en cuenta el alto riesgo de hepatotoxicidad (antecedente de consumo de alcohol), se decidió cambiar el tratamiento a Lanadelumab, en dosis de 300 mg por vía subcutánea.
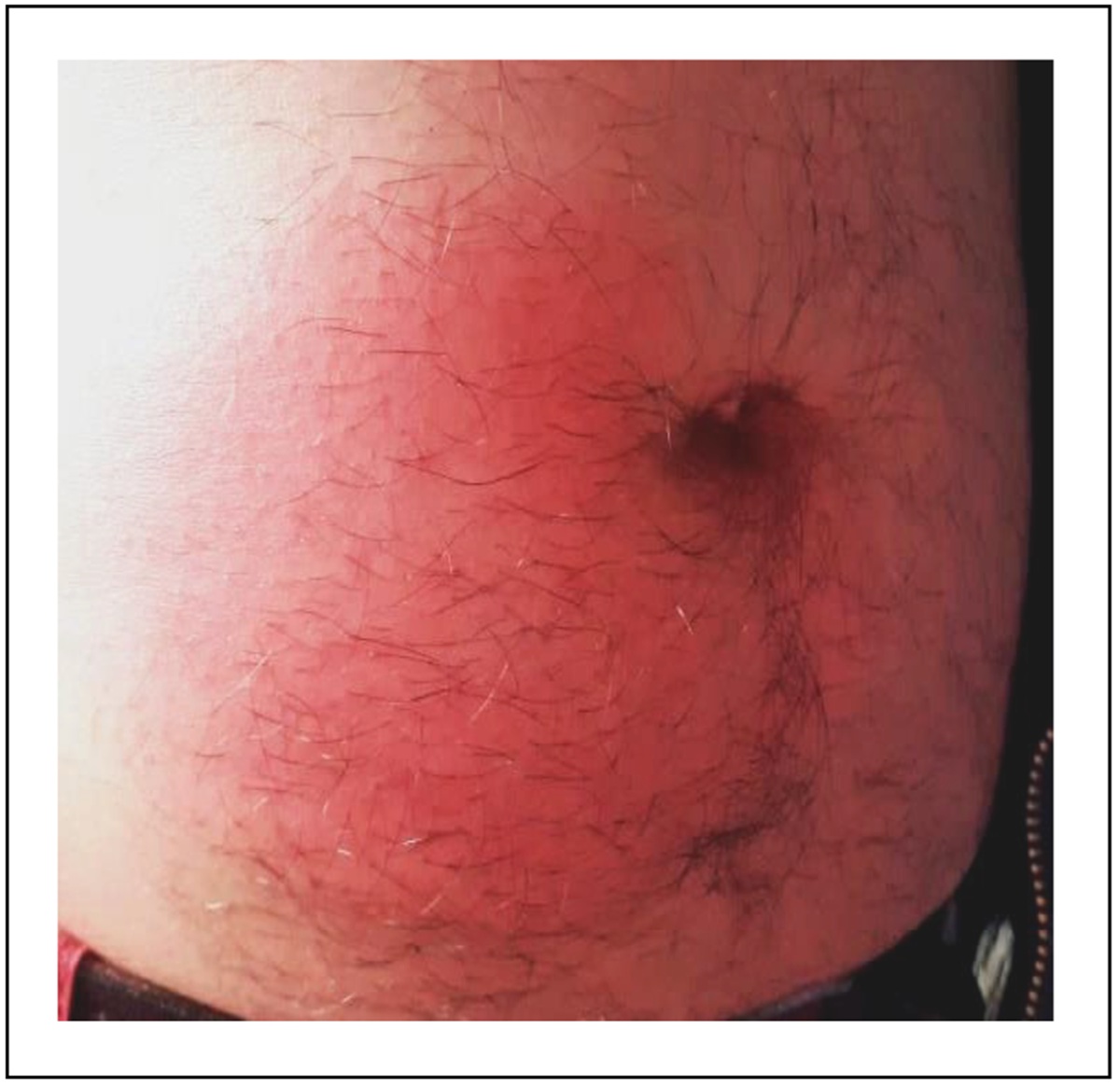
Desde la primera dosis manifestó eritema e induración en el sitio de aplicación, con posterior prurito generalizado (Figura 1). Se intentó administrar en dos ocasiones el medicamento, con la misma dosis, en un intervalo de dos semanas, pero siguió manifestando la misma reacción, por lo que se decidió suspender el tratamiento con Lanadelumab.
En la actualidad, el paciente manifiesta cinco episodios al año (el último se registró en junio de 2023), con dolor abdominal, para lo que recibe Icatibant con adecuada respuesta. Hoy día permanece en seguimiento trimestral en el servicio de Alergología, en Tunja, Boyacá, Colombia, con buen apego al tratamiento médico. La última valoración, llevada a cabo en julio de 2023, informó: AECT: 16 - AE-QoL:13, evidenciando buen control de la enfermedad y mejoría en la calidad de vida. Es importante destacar que al momento de establecer el diagnóstico de la enfermedad, las escalas de clinimetría no fueron documentadas en la historia clínica, por lo que no se hizo la comparación de las mismas.
DISCUSIÓN
El caso aquí expuesto supone un desafío clínico significativo al abordar el angioedema hereditario tipo 1, en un paciente con antecedentes familiares de la enfermedad. La manifestación clínica se caracteriza por episodios recurrentes de edema facial y abdominal desde una edad temprana, y coincide con la bibliografía acerca del tema.
La mayor parte de los estudios emprendidos en 2015 reportaron concentraciones bajas del inhibidor funcional C1, antígeno y complemento C4, validando en angioedema hereditario tipo 1 en el paciente. El tratamiento inicial con Icatibant para el control de los episodios fue efectivo; sin embargo, la progresión de la enfermedad motivó la exploración de opciones profilácticas. La introducción de Danazol en 2021 no demostró eficacia, lo que llevó a la transición a Lanadelumab. Aunque esta terapia parecía prometedora, los efectos adversos locales persistieron (evidenciados por eritema e induración), por lo que se decidió suspenderlo. Esta reacción atípica plantea interrogantes de la variabilidad en las respuestas individuales al tratamiento y subraya la rareza de los efectos adversos locales significativos, especialmente en una terapia que se considera bien tolerada.
Es importante destacar que, actualmente en Colombia, dentro de la práctica clínica, Danazol y Lanadelumab se prescriben como tratamiento profiláctico a largo plazo. Si bien Lanadelumab es un medicamento de primera línea, en Colombia tiene disponibilidad limitada, debido al alto costo, por lo que al inicio del tratamiento no le fue indicado al paciente. Danazol es un fármaco con excelente costo-beneficio y de fácil disponibilidad, por lo que se le indicó al paciente de primera intención, a pesar de ser suponer un tratamiento de segunda línea.
La complejidad del angioedema hereditario tipo 1 se refleja en la diversidad de respuestas al tratamiento, y resalta la importancia de considerar enfoques personalizados, según el contexto clínico de cada paciente. La limitación principal en este caso radica en la falta de éxito con los tratamientos profilácticos prescritos hasta el momento.
Es importante realizar estudios e investigaciones adicionales acerca del angioedema hereditario tipo 1, con la finalidad de comprender mejor la patogénesis y, por ende, mejorar las estrategias de tratamiento actuales.
CONCLUSIONES
Del caso aquí reportado destaca la necesidad de un enfoque integral para el tratamiento del angioedema hereditario tipo 1, incorporando evaluaciones continuas y adaptando las estrategias terapéuticas según la evolución del paciente. La rareza de los efectos adversos locales recalca la importancia de la vigilancia estrecha y exploración de alternativas de tratamiento en pacientes con angioedema hereditario tipo 1 de difícil control.