Introducción
La caña de azúcar se emplea como materia prima para la producción de azúcar y etanol (Zavala et al. 2021). Este cultivo se produce en regiones tropicales y subtropicales (Assureira y Assureira 2022); su cosecha coincide con los meses más fríos y secos para garantizar el máximo contenido de sacarosa en el tallo (Alokika et al. 2021). Alrededor de 70% del azúcar que se consume en el mundo depende del cultivo de la caña de azúcar (Cabrera y Zuaznábar 2010) con elevada tasa de formación de biomasa debido a la anatomía de sus hojas, mismas que representan 60% del residuo generado por el cultivo (Carvalho et al. 2017).
Los ingenios azucareros mexicanos procesan 5 957 170 t de azúcar provenientes de 777 078 hectáreas. Las hojas de caña se han empleado tradicionalmente en la alimentación animal como forraje para el ganado bovino y ovino (Alokika al. 2021) semi estabulado y estabulado, pero su baja densidad, de 17 kg/m3 dificulta su manipulación (Assureira y Assureira 2022) e indica altos contenidos de fibra. Las hojas, son consideradas un rastrojo y cuando se ofrecen como único alimento muestran limitaciones nutricionales, que sugieren buscar metodologías para aprovechar su potencial.
Los tratamientos químicos en forrajes mejoran la disponibilidad de los carbohidratos estructurales, reducen el contenido de fibra y aumentan la digestibilidad ruminal. Así mismo, buscan disminuir costos y ser una opción viable y sustentable para la alimentación del ganado (Samadi et al. 2016, Alokika et al. 2021). Se encontraron pocas investigaciones sobre el tratamiento de los residuos de caña de azúcar con ácido fosfórico H3PO4 (Hermiati et al. 2022). Otros residuos lignocelulósicos como el rastrojo de bambú se han tratado con H3PO4 y se observa que mejora su digestibilidad enzimática (Huang et al. 2019). Pero no se encontraron estudios sobre la degradabilidad y digestibilidad de hojas de caña de azúcar tratadas con ácido fosfórico. Por tanto, el objetivo del presente estudio fue evaluar la degradabilidad ruminal y digestibilidad de las hojas de caña de azúcar tratadas con H3PO4 durante 1 a 7 días, y determinar la degradabilidad ruminal y la digestibilidad.
Materiales y métodos
Ubicación del experimento
El estudio se realizó en el laboratorio de Nutrición Animal del Departamento de Zootecnia de la Universidad Autónoma Chapingo, ubicada en el municipio de Texcoco de Mora, Estado de México.
Obtención de muestras
Se utilizaron hojas de caña de azúcar (Saccharum officinarumL.) cv cubana, del Campo Paredones, ejido de Cuautlixco, Cuautla, Morelos. Estas se obtuvieron de cosecha manual sin quema, durante la temporada febrero/marzo 2023. Las hojas con tres semanas postcosecha se transportaron al Laboratorio de Nutrición Animal, se secaron al sol por una semana y tres días en estufa (Tecsa®, modelo HFT-18) a 60 °C. El material vegetal se molió (molino de laboratorio Wiley Mill®, modelo 4), con criba de 3.0 mm, obteniéndose 30 kg.
Tratamiento químico
Se utilizó una solución de H3PO4 (pureza 86%, densidad 1.88 g mL-1; Reasol®) (0.01, 0.1 y 1.0 mol L-1 o M) y tiempos de exposición de 1, 3, 5 y 7 días. Las unidades experimentales fueron 500 g de hojas de caña molida en bolsas de polietileno de 25×35 cm. El contenido de cada bolsa se asperjó con 250 mL de H3PO4 a 0.01, 0.1 o 1.0 M. Las bolsas se incubaron por 1, 3, 5 y 7 d. Transcurrido el tiempo de incubación correspondiente, las muestras se pasaron a bolsas de papel de estraza y se metieron a la estufa de aire forzado (Riossa®, modelo FOFD-71) a 60 °C por 3 días, para inhibir el tratamiento y secarlas.
Análisis químicos
La materia seca (MS) se determinó por secado a 105 °C, durante 24 h en estufa. Posteriormente, se determinaron fibra detergente neutro (FDN), fibra detergente ácido (FDA), lignina detergente ácido (LDA), hemicelulosa (Hem), celulosa (Cel) y sílice (S).
Degradabilidad ruminal y digestibilidad
Para la digestibilidad se usaron bolsas Ankom® (9.5×18 cm con porosidad de 50 µm) se pesaron 3 g en una balanza analítica (Ohaus Pioner®). La incubación de las muestras fue en un animal Holstein de 2 años, con fístula ruminal. Su alimentación fue con base en maíz (25%), melaza (5%), heno de alfalfa (20%), paja de avena (30%), pasta de soya (15%) y premezcla de vitaminas y minerales (5%). El animal se trató según las recomendaciones del Comité de Bienestar Animal del Colegio de Posgraduados (COLPOS 2016).
Todas las muestras se incubaron por triplicado al mismo tiempo en el rumen. Las bolsas ANKOM se colocaron dentro de una red de nylon, suspendida de la fístula con un hilo de nylon. Después de 72 h, las muestras fueron retiradas del rumen, se lavaron con agua corriente y agua destilada hasta quedar limpias, para secarse después a 60 °C por 48 h. La degradabilidad ruminal se determinó por diferencia entre el peso de la muestra menos el peso del residuo y se expresó como porcentaje de la muestra. Las muestras provenientes de la degradabilidad ruminal se digirieron con detergente neutro según el método propuesto por Van-Soest (1966), el residuo obtenido se pesó en balanza analítica (Ohaus Adventurer® modelo H-5276), se restó del peso inicial de aproximadamente 3 g, el resultado se expresó como porcentaje y fue considerado la digestibilidad.
Análisis estadísticos
El diseño experimental fue completamente al azar con arreglo factorial de tratamientos. Los factores fueron tiempo (niveles 1, 3, 5 y 7 días) y molaridad del H3PO4 (niveles 0.01, 0.1 y 1.0 M) más un testigo (molaridad 0, tiempo 0). Se obtuvieron las medias y las significancias (α = 0.05) de los efectos principales y de las interacciones. Se graficó el factor tiempo en el eje horizontal, las molaridades como líneas separadas y las variables de respuesta en el eje vertical. Las medias de los 13 tratamientos fueron separadas usando la prueba de Tukey (p < 0.05). Todos los análisis estadísticos se realizaron empleando el paquete estadístico SPSS®. El modelo fue Y = µ + αi + βj + (αβ)ij + τt + εijk, donde Y = variable respuesta, µ = promedio de todas las observaciones, αi = efecto del factor tiempo, βj = efecto del factor molaridad, (αβ)ij = efecto de la interacción de los factores tiempo y molaridad, τk = efecto del testigo, εijk = error experimental, i = 1, 3, 5 y 7 d, j = 0.01, 0.1 y 1 M y k = 1, 2, 3, 4 repeticiones.
Resultados
Interacciones significativas
Las variables FDN, LDA, S y CEL produjeron interacciones significativas (p < 0.05) de los factores tiempo y molaridad (Tabla 1). En forma gráfica estas interacciones se muestran en las figuras 1, 3, 4 y 6. En ellas se observa que los patrones de cambio o pendientes de las variables mencionadas difieren entre las molaridades bajas (0.01 y 0.1 M) y la molaridad mayor (1.0 M). Se observa que el ácido fosfórico (1.0 M), disminuyó (p < 0.01) el porcentaje de FDN en 14.27% al día 3, sin presentar cambios significativos en los siguientes días de tratamiento.
Tabla 1 Interacciones significativas entre los valores tiempo y molaridad (medias, errores estándar y valores de p).
| Variable de respuesta | Días de exposición al ácido | Error estándar | Valor de p | |||||
|---|---|---|---|---|---|---|---|---|
| Molaridad | 0 | 1 | 3 | 5 | 7 | |||
| FDN | 1 M | 67.18 | 61.12 | 60.81 | 57.68 | 1.530 | <0.01 | |
| 0.1 M | 80.98 | 85.51 | 79.93 | 78.62 | ||||
| 0.01 M | 82.80 | 86.03 | 80.32 | 78.09 | ||||
| 0 M | 75.40 | |||||||
| LDA | 1 M | 6.14 | 5.51 | 6.11 | 14.07 | 1.779 | <0.05 | |
| 0.1 M | 8..06 | 8.60 | 7.64 | 11.68 | ||||
| 0.01 M | 8.38 | 8.69 | 8.17 | 14.78 | ||||
| 0 M | 6.35 | |||||||
| S | 1 M | 5.27 | 4.30 | 5.14 | 4.95 | 0.142 | <0.05 | |
| 0.1 M | 6.92 | 6.20 | 5.66 | 6.31 | ||||
| 0.01 M | 6.72 | 6.44 | 6.14 | 6.82 | ||||
| 0 M | 4.55 | |||||||
| Cel | 1 M | 30.35 | 32.75 | 32.75 | 24.98 | 3.498 | <0.01 | |
| 0.1 M | 36.60 | 40.76 | 38.72 | 34.17 | ||||
| 0.01 M | 38.11 | 39.45 | 39.41 | 31.33 | ||||
| 0 M | 35.98 | |||||||
FDN: fibra detergente neutro, LDA: linina detergente ácido, S: sílice, Cel: celulosa.
Fibra detergente neutro o pared celular (FDN) y fibra detergente ácido (FDA)
Las Figuras 1 y 2 muestran a las variables FDN y FDA. Con H3PO4 1.0 M y en comparación con el testigo, los valores de FDN fueron 8.22 y 14.27% menores (p < 0.05) en los días 1 y 2, respectivamente.
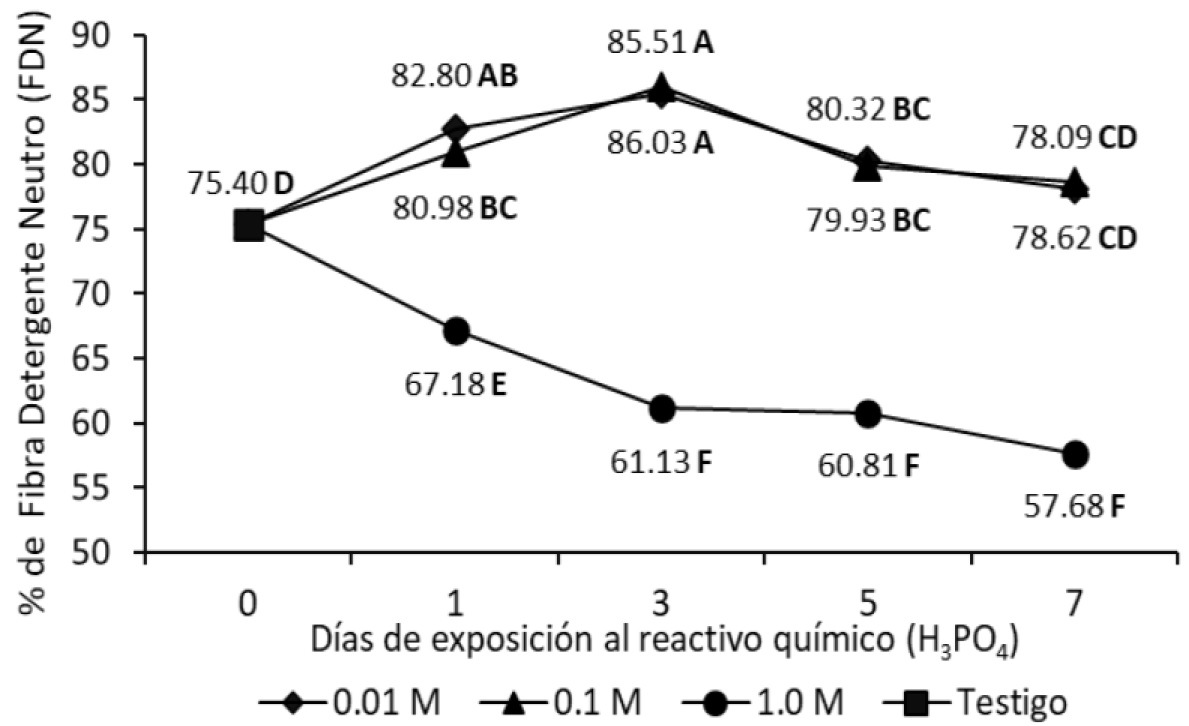
Figura 1 Efectos del tiempo y concentración (M) de H3PO4 (líneas separadas) del porcentaje de fibra detergente neutro, FDN o pared celular, en hojas de caña de azúcar. M: mol L-1. Letras distintas indican medias diferentes (Tukey, p < 0.05).
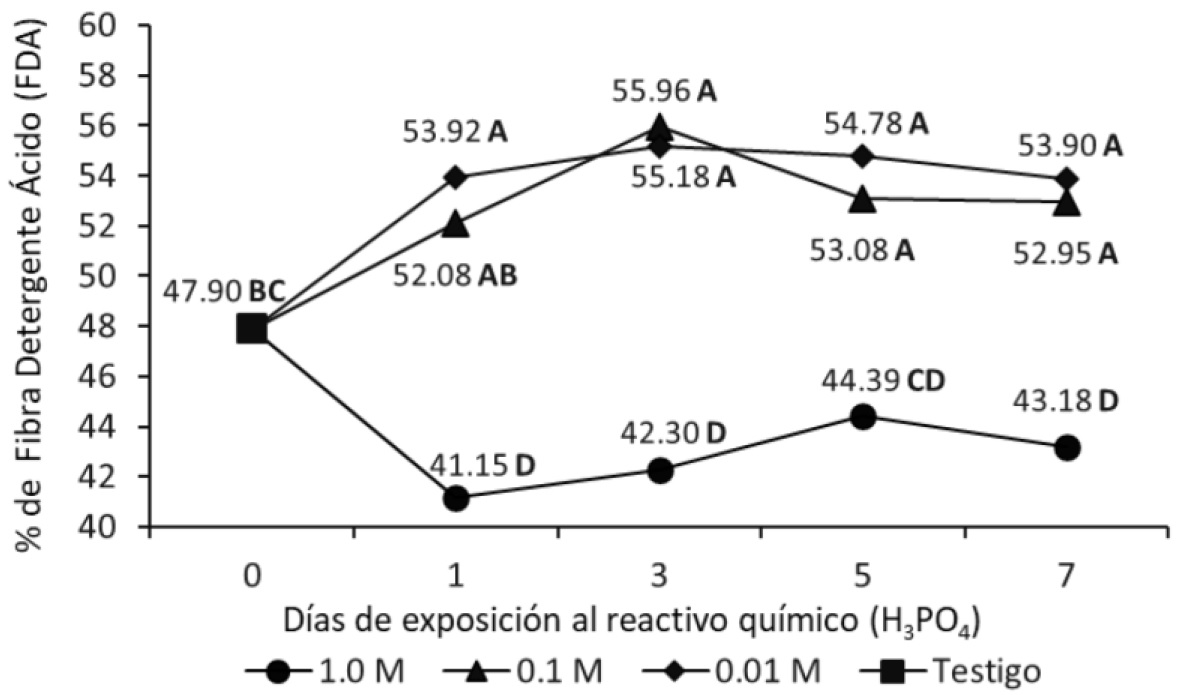
Figura 2 Efectos del tiempo y concentración (M) de H3PO4 (líneas separadas) del porcentaje de fibra detergente ácido FDA, en hojas de caña de azúcar. M: mol L-1. Letras distintas indican medias diferentes (Tukey, p < 0.05).
Al ser tratadas las muestras con H3PO4 a baja concentración (0.01 y 0.1 M), FDN y FDA aumentaron (p < 0.05) al día 1, con respecto al testigo. Contrariamente, cuando las muestras fueron tratadas con solución 1.0 M de H3PO4, ambas variables disminuyeron, por hidrólisis de hemicelulosa y celulosa. La concentración 1.0 M de H3PO4 disminuyó en 6.75% (p < 0.05) los valores de FDA al día 1 de tratamiento con respecto al testigo (Figura 2). Posteriormente no hubo cambios significativos de FDA (p > 0.05).
Lignina detergente ácido (LDA) y sílice (S)
La Figura 3 muestra la variable LDA, hasta el día 5 la LDA fue similar (p > 0.05) al valor del testigo, pero al día 7 su valor aumentó (p < 0.05) con las tres concentraciones de H3PO4 (Figura 3).
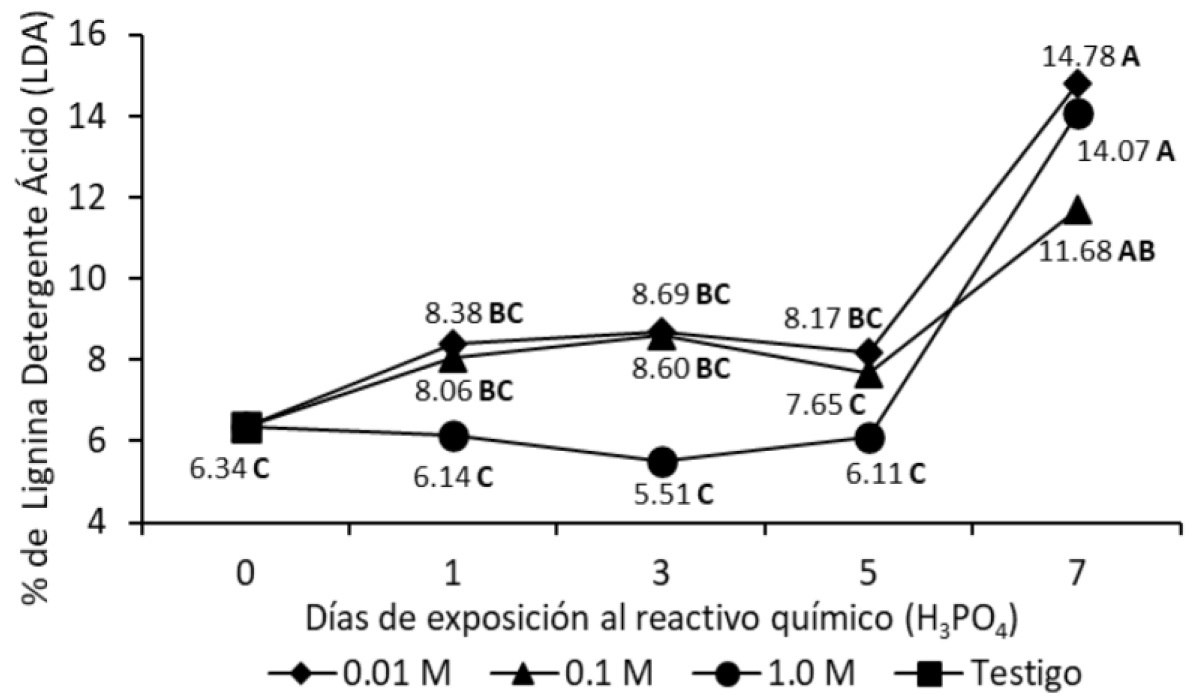
Figura 3 Efectos del tiempo y concentración (M) de H3PO4 (líneas separadas) del porcentaje de lignina detergente ácido LDA, de hojas en caña de azúcar. M: mol L-1. Letras distintas indican medias diferentes (Tukey, p < 0.05).
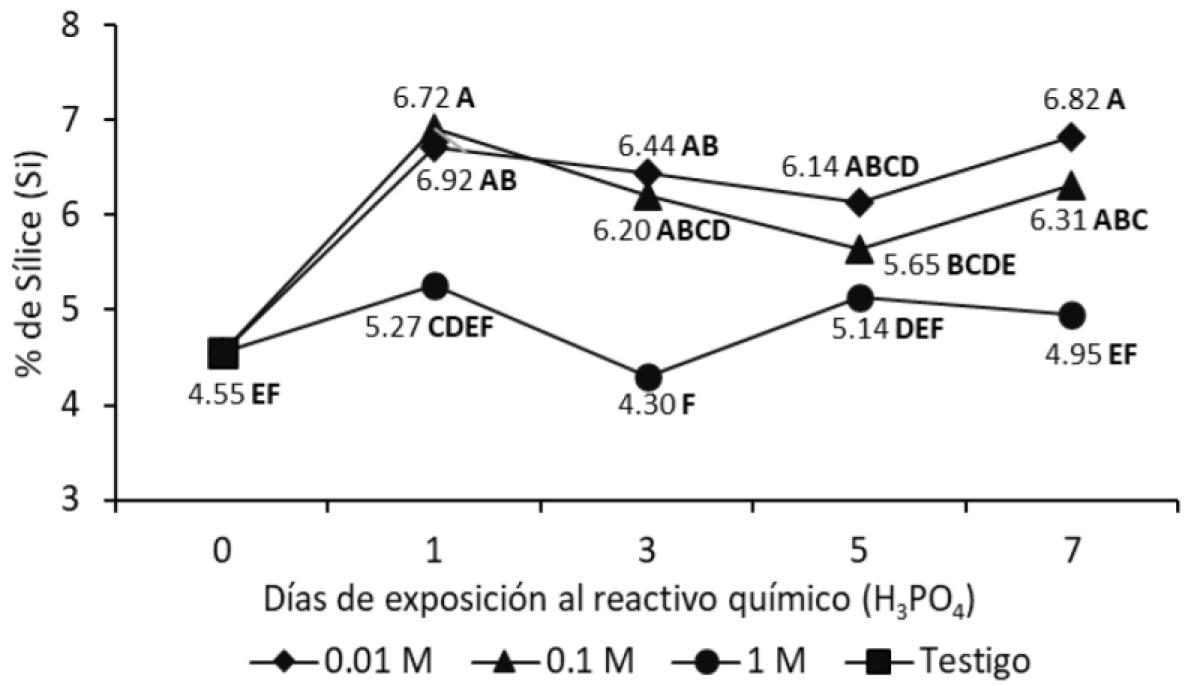
La figura 4 muestra la variable sílice (S), con la concentración 1.0 M, el valor del testigo no experimentó cambio alguno (p > 0.05), pero a concentraciones más bajas, S aumentó (p < 0.05) 2.37% a 0.1 M y 2.17% a 0.01 M respecto del testigo al día 1, y después permaneció constante hasta el día 7.
Hemicelulosa (Hem) y celulosa (Cel)
En las figuras 5 y 6 se muestran las variables hemicelulosa y celulosa. A concentración 1.0 molar de H3PO4 (Figura 5), la hemicelulosa disminuyó respecto al testigo, este cambio se observó al tercer día de exposición al tratamiento ácido (p < 0.05), 8.67% menos respecto al testigo, sin cambios posteriores. Las concentraciones bajas de H3PO4 (0.01 y 0.1 M) no afectaron los valores de Hem (p > 0.05).
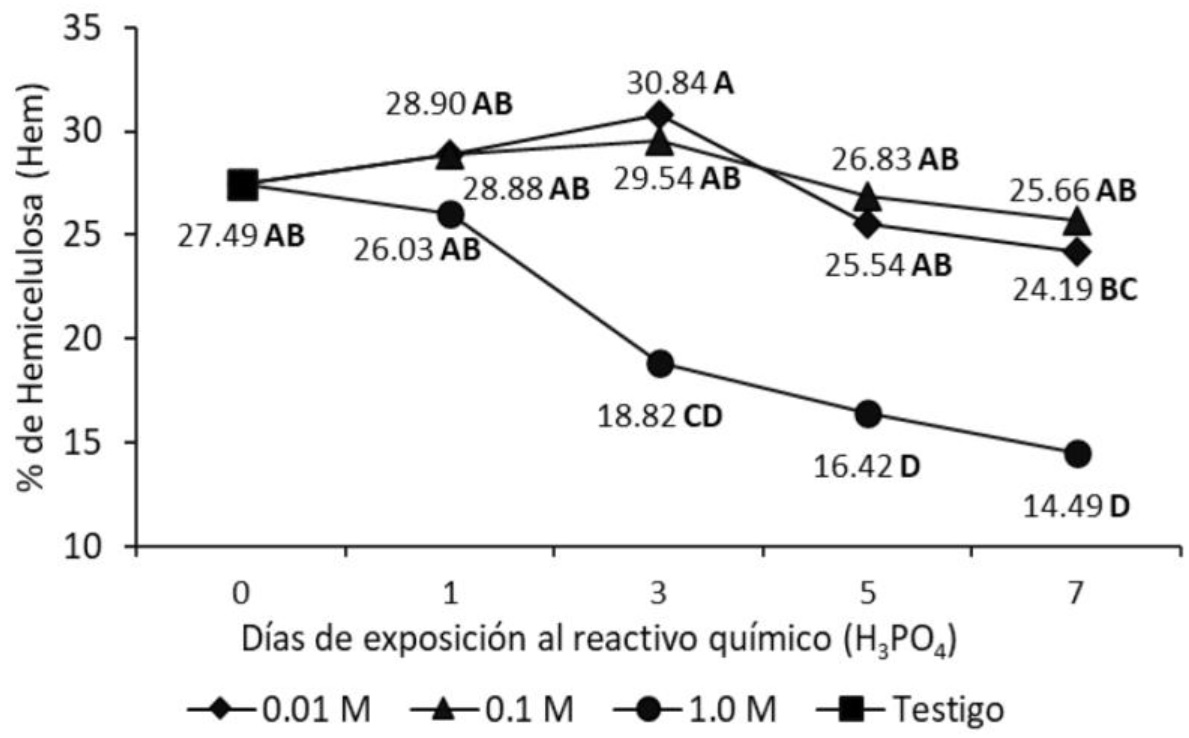
Figura 5 Efectos del tiempo y concentración (M) de H3PO4 (líneas separadas) del porcentaje de hemicelulosa (Hem), en hojas de caña de azúcar. M: mol/L. Letras distintas indican medias diferentes (Tukey, p < 0.05).
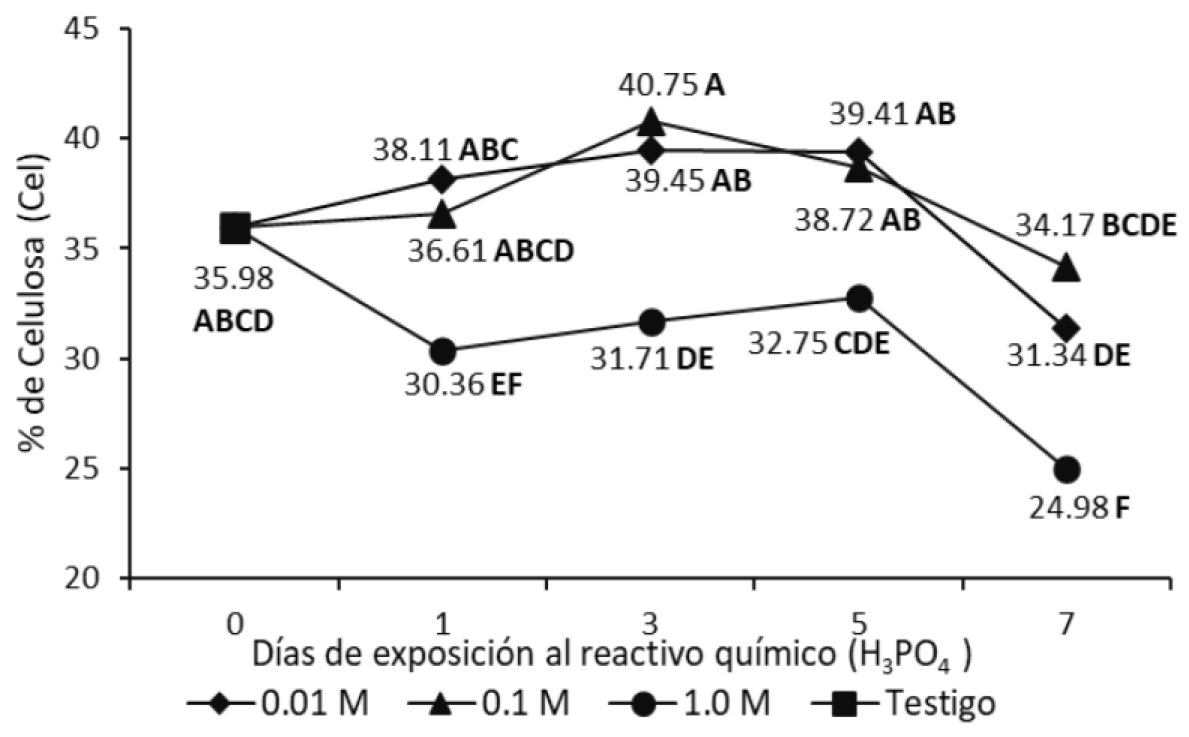
Figura 6 Efectos del tiempo y concentración (M) de H3PO4 (líneas separadas) del porcentaje de celulosa (Cel), en hojas de caña de azúcar. M: mol L-1. Letras distintas indican medias diferentes (Tukey, p < 0.05).
El día 1, la celulosa con el tratamiento 1.0 M fue 5.62% menor (p < 0.05) respecto al testigo (Figura 6); de 1 a 5 días no hubo diferencias en el contenido de celulosa. El efecto del día 1 se acentuó en el día 7 (11%). Los tratamientos a concentración (0.01 y 0.1 M) no cambiaron el contenido de celulosa en el transcurso del tiempo (p < 0.05).
Degradabilidad ruminal (Deg) y digestibilidad (Dig)
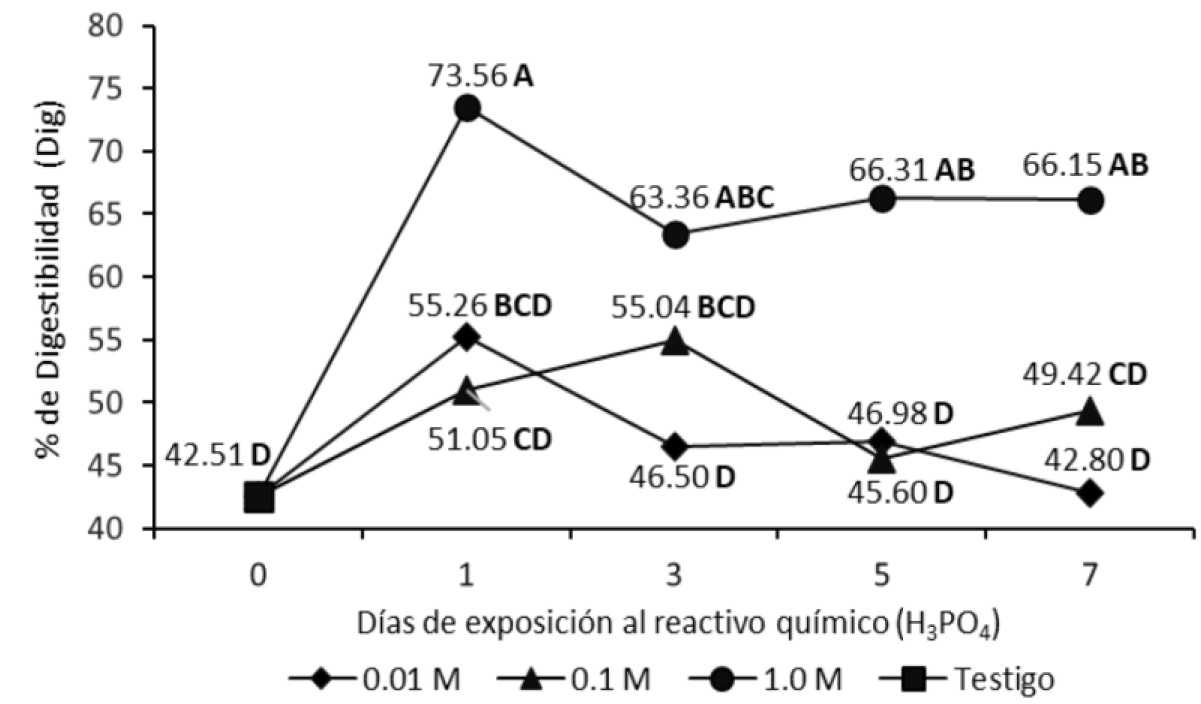
Del día 0 al día 1 con solución 1.0 M de H3PO4, la degradabilidad ruminal (Figura 7) aumentó, y también aumentó la digestibilidad (Figura 8). Los días posteriores no se observaron cambios en los valores de estas dos variables. Con las molaridades 0.01 y 0.1 M de H3PO4, no se observaron cambios en estas dos variables al transcurrir el tiempo.
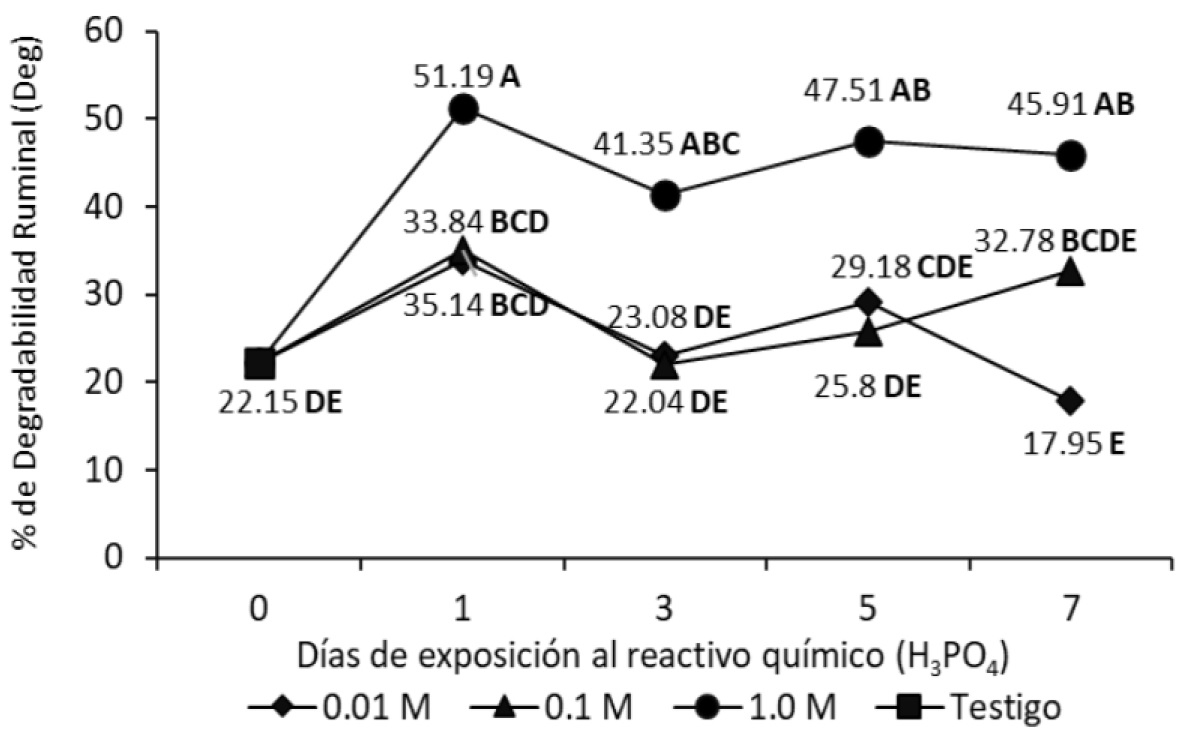
Figura 7 Efectos del tiempo y concentración (M) de H3PO4 (líneas separadas) del porcentaje de degradabilidad ruminal (Deg), en hojas de caña de azúcar. M: mol L-1. Letras distintas indican medias diferentes (Tukey, p < 0.05).
Discusión
De acuerdo Moodley y Kana (2018) la variación en composición estructural de hojas de caña de azúcar depende de la ubicación, crecimiento, periodo de cosecha y procedimiento analítico realizado. También Menandro et al. (2017) muestran que el contenido promedio de hemicelulosa, celulosa y lignina en hojas verdes de caña de azúcar es de 26, 32 y 18%, respectivamente; mientras que en hojas secas es de 29, 37 y 21%. Los correspondientes valores de FDN y FDA fueron 15 y 10% más bajos, que los reportados por Uppal y Kaur (2011) y Hermiati et al. (2022) reportan que para el bagazo de caña tratado con tres concentraciones: 1, 2 y 3 M de ácidos, reportan que los efectos del ácido fosfórico (H3PO4) a mayor concentración se observan debido a que se afectan significativamente los grupos funcionales y la morfología de la biomasa de las hojas de caña.
Existe evidencia de que el pH ácido, debilita a la pared celular (FDN) antes de romperse (Phyo et al. 2019). El H3PO4 en alta concentración afecta los grupos funcionales (Hermiati et al. 2022). Probablemente la disminución de FDN con H3PO4 1.0 M se debe a la hidrólisis de Hem, más no la disminución de FDA que no contiene Hem. Tal vez la disminución de FDA se debe a la hidrólisis de Cel o de los demás componentes de la fibra en condiciones ácidas. Por ejemplo, el ácido sulfúrico se usa para hidrolizar cristales de celulosa de bambú (Zhang et al. 2014). Al respecto, Siripong et al. (2016) reportaron que, en malezas, la acción del ácido fosfórico elimina la mayor parte de hemicelulosa de la pared celular, lo cual permite tener acceso a la celulosa, cuya remoción es menor.
El valor de LDA fue muy parecido al reportado por Aguirre et al. (2010) en hojas de caña de azúcar con puntas (6.3%). El valor calculado de S (sílice), en el residuo de caña de azúcar (4.45% de cenizas y 57.66% de S en las cenizas) fue 2.6% (Canilha et al. 2012, Gutierrez et al. 2018), que es 2% menor que el del presente estudio, debido a que contrariamente a lo sucedido con Hem y Cel, no se observó ningún efecto hidrolítico liberador de S, aun a esta alta concentración de H3PO4 1.0 M. El aumento de LDA observado el día 7, se debe probablemente a un efecto de reacción del H3PO4 con la lignina, como lo afirman Xie et al. (2019), ya que el ácido fosfórico es una molécula polar y puede penetrar en el polímero de lignina para actuar como plastificante. Mientras que Gao et al. (2020) concluyeron que los grupos fenólicos activos de la lignina kraft (obtenida por degradación alcanina de la madera), reaccionan con el grupo fosfato para obtener lignina fosforilada, en este estudio cuando los valores de Cel y Hem comenzaron a disminuir y el H3PO4 comenzó a unirse a la LDA en lugar de liberarla por hidrólisis. Contrariamente, Huang et al. (2019), mencionan que los catalizadores ácidos reducen la resistencia de la biomasa, al hidrolizar la hemicelulosa y una porción de lignina. Estos investigadores usaron H3PO4 entre 40 y 80%, mientras que en este estudio se usaron concentraciones de 0.1 a 10%.
Probablemente el aumento de S (sílice) al día 1, se debe a la adsorción de H3PO4 por S, de acuerdo con Hena et al. (2015), el bagazo de caña de azúcar modificado puede ser usado eficientemente para remover iones fosfato del agua, e incluso sin modificar, el bagazo de caña de azúcar posee sitios especiales de enlace para remover contaminantes, por ejemplo, el bagazo crudo adsorbe 90% de nitritos (Sarker et al. 2017). Probablemente, el S es responsable de esta adsorción ya que es componente de las zeolitas, usadas para adsorber fosfatos (Wan et al. 2018, Deng et al. 2022).
La disminución de hemicelulosa usando H3PO4 1.0 M (10%), fue reportada por otros investigadores. Mientras que Qiu et al. (2017), refieren que los contenidos de hemicelulosa y lignina disminuyeron con H3PO4 (85% p/p) en paja de trigo. En tanto que Wan et al. (2018), mencionan que el tratamiento ácido afecta principalmente a la hemicelulosa con un pequeño impacto en la lignina, el H3PO4 irrumpe los enlaces covalentes de hidrógeno, y solubiliza la hemicelulosa. La disminución de celulosa usando H3PO4 1.0 M (10%), fue reportada por otros investigadores. Por ejemplo, Hermiati et al. (2022), reportaron que los iones de hidrógeno de los ácidos sirven como catalizadores que hidrolizan los polisacáridos a monómeros de azúcar, degradando de forma ligera la fracción de celulosa. En tanto que Huang et al. (2019), refieren que el modo de acción del H3PO4, depende de su capacidad para interrumpir los enlaces de hidrógeno dentro de la celulosa, en su trabajo con tratamientos de H3PO4 a residuos de bambú encontraron que la cristalinidad de la celulosa disminuyó de 54.4 a 51.5% al aumentar la concentración de H3PO4 de 40 a 85%. Mientras que Qiu et al. (2017), reportaron que el contenido de celulosa de la paja de trigo disminuye cuando aumenta la concentración de H3PO4.
Dado que la degradabilidad es solamente ruminal, será menor que la digestibilidad (degradabilidad ruminal + digestión intestinal). Por tanto, todos los valores de la Figura 7 resultaron menores que sus correspondientes valores de la Figura 8. Al respecto, Araiza-Rosales et al. (2013) encontraron en ensilados de maíz, degradabilidades cercanas al 80% que aumentaron a cerca del 85% cuando se les agregó manzana de desecho. El aumento observado en la degradabilidad ruminal se debe a la degradación de FDN, FDA y celulosa que disminuyeron en el día 1. Mientras que Uppal et al. (2011) trabajando con H3PO4 a concentraciones 1.0, 2.0 y 3.0 M en bagazo de caña de azúcar, reportaron que los ácidos concentrados hidrolizan tanto los enlaces débiles de la hemicelulosa como los más fuertes de la celulosa β (1,4). Sobre lo mismo Xu et al. (2021) refieren que la lignina de distintos forrajes se puede degradar entre 7.22 y 15.04% en el rumen de búfalos, lo cual hace que la digestibilidad de los componentes lignocelulósicos sea mayor en búfalo que en ganado criollo. Sobre lo mismo De-Olivera et al. (2023) encontraron que, el tratamiento de caña de azúcar con óxido de calcio disminuye las fracciones de FDN, celulosa y lignina por lo que aumenta la digestibilidad in vitro. Estos resultados coinciden con los de la presente investigación en que la disminución de FDN, FDA y celulosa (Figuras 1, 2 y 6) hace que aumenten la degradabilidad ruminal (Figura 7) y la digestibilidad (Figura 8), probablemente por la hidrólisis de los carbohidratos estructurales de las hojas de caña de azúcar, que proporcionan energía (y adicionalmente fósforo) para el crecimiento de los microorganismos del rumen. En tanto que Palangi et al. (2023), reportaron que la adición de ácido fumárico aumenta la fracción “a” de rápida degradabilidad (59.71 a 64.96%) del forraje de alfalfa. Mientras que Contreras et al. (2019) estudiaron la degradabilidad ruminal de la fibra de los forrajes y residuos de cosecha, y encontraron una degradabilidad potencial de 70.25 % en paja de avena, valor muy alto comparado con la degradabilidad ruminal máxima del presente estudio.
El aumento de la concentración de H3PO4 mejora la digestibilidad enzimática, más que la temperatura y el tiempo (Qiu et al. 2017). Mientras que la digestibilidad enzimática de residuos de bambú pasó de 15.4 a 61.4% por tratamiento con ácido sulfúrico seguido por H3PO4 (Huang et al. 2019). En tanto que Phillip et al. (2023), el ácido acético a altas concentraciones penetra eficazmente la estructura de la celulosa y rompe los enlaces de hidrógeno, por lo que mejora la digestibilidad in vivo de la paja de arroz. Al respecto, Siripong et al. (2016) y Huang et al. (2019) reportan que el H3PO4 es de bajo costo, es poco corrosivo, puede disolver la celulosa, no es volátil, presenta estabilidad química, sus residuos son ambientalmente amigables y sus sales son fácilmente reciclables para ser usadas como fertilizantes, es un tampón de acidez efectivo en procesos bioquímicos y un nutriente para los microorganismos. El H3PO4 es menos peligroso en comparación con el ácido clorhídrico (HCl) y el ácido sulfúrico (H2SO4) que resultan corrosivos para el equipo y peligrosos para la manipulación humana (Wan et al. 2018).
Conclusiones
El ácido fosfórico 1.0 M (aproximadamente 10%), disminuye la fibra detergente neutro o paredes celulares y la fibra detergente ácido debido a la degradación de hemicelulosa y celulosa. Por lo que aumenta la biodisponibilidad de la materia seca para los microorganismos ruminales y, en consecuencia, aumenta la degradabilidad ruminal y la digestibilidad. La tecnología propuesta, es adecuada para los pequeños productores con la necesidad de tener alternativas de alimentos para el ganado, a partir del reciclado de biomasa, como las hojas del cultivo de caña de azúcar, desechos agrícolas, rastrojos y malezas.