Introducción
El cáncer de próstata (CaP) es la neoplasia maligna diagnosticada con mayor frecuencia a nivel mundial y la quinta causa de muerte por cáncer en los hombres; 375 000 muertes anuales en todo el mundo en 2020.1 La incidencia aumenta conforme avanza la edad, se considera que más del 80 % de los hombres desarrollarán CaP a los 80 años; en general, un 90 % de los casos se diagnostican en mayores de 65 años.1,2
El diagnóstico de CaP se basa principalmente en los niveles de antígeno prostático específico (PSA), exploraciones físicas para detectar la presencia del tumor y biopsias de tejido prostático.1,3 El PSA es el marcador bioquímico tumoral de mayor uso, sin embargo, su especificidad y sensibilidad son relativamente bajas, 45 % y 82 % respectivamente,4 siendo controvertido el valor de esta prueba.1
Se sabe que la fracción libre de PSA está más elevada en hombres con hiperplasia benigna prostática (HBP) que de hombres con CaP.5,6 También, los pacientes con CaP tienen un cociente PSA libre/PSA total más bajo que los pacientes con HBP, si el cociente es superior a 18 probablemente se trate de un adenoma y si el valor es inferior normalmente se indica una biopsia para descartar malignidad.6 Como consecuencia del uso generalizado de PSA en el procedimiento de detección del CaP es la exposición de los pacientes al sobrediagnóstico y sobretratamiento, siendo que no es específico del cáncer y no distingue entre cáncer indolente y agresivo.7 Para confirmar de manera confiable y concluyente un diagnóstico se utiliza la biopsia como estándar, tomando en cuenta dos criterios para que un paciente sea candidato a este procedimiento: un tacto rectal sospechoso y un resultado de PSA mayor a 4 ng/mL. Es importante informar al paciente sobre los riesgos asociados al procedimiento de la biopsia, tales como sangrado (sangrado rectal, hematospermia y hematuria) y fiebre (infecciones del tracto urinario y sepsis), presentes en un 2 % al 20 % en las intervenciones,3 siendo la sepsis un riesgo clínicamente significativo que ocurre hasta en un 5 % de los casos.8
En este contexto se han desarrollado biomarcadores circulantes y urinarios y, variables clínicas, o la combinación de éstos para minimizar el sobrediagnóstico sin perder la identificación de tumores agresivos. En este sentido, la puntuación del índice de salud prostática (PHI) para el diagnóstico de CaP como prueba no invasiva, consiste en una herramienta matemática multifactorial que combina los resultados del PSA libre (fPSA), PSA total (tPSA) y la isoforma [-2]proPSA (p2PSA); esta se sintetiza preferentemente en tejido canceroso por lo que su valor aumenta significativamente en el suero de hombres con CaP.1,7 De tal manera que PHI es un análisis de sangre simple que supera a cualquiera de sus componentes individuales para la identificación de cáncer, varios estudios de Europa y América han demostrado su eficacia,9 por lo que el objetivo de este estudio es determinar la sensibilidad y especificidad del índice de salud prostática (PHI) para el escrutinio de cáncer de próstata en población mexicana.
Método
El presente estudio es exploratorio, transversal analítico y retrospectivo, de tipo prueba diagnóstica. Se incluyeron datos de 84 sujetos mediante un muestreo no probabilístico por conveniencia, hombres de 50 a 70 años con probable cáncer de próstata (CaP) que fueron atendidos dentro del Hospital General Dr. Manuel Gea González en un periodo de tiempo de enero a noviembre del 2022 con tPSA mayor a 4 ng/mL.
Fueron sujetos de rechazo aquellos expedientes de pacientes que ya habían recibido tratamiento contra CaP o que no contaran con resultado de biopsia, valores de tPSA, fPSA o PHI.
Los valores de tPSA y fPSA fueron extraídos de la base de datos del laboratorio clínico del Hospital los cuales se determinaron por quimioluminiscencia en el equipo DXI 800. El valor del biomarcador PHI se calculó con la fórmula: PHI = (p2PSA/fPSA)x√tPSA. Por otra parte, se obtuvieron los resultados de las biopsias del área de patología, siendo éste el método estándar de oro para el diagnóstico de cáncer de próstata.
Para el análisis estadístico se consideró la normalidad de los datos con la prueba Kolmogorov-Smirnov, se utilizó la prueba t de student para los datos con distribución normal y la prueba U de Mann-Whitney para los datos no normales, se expresaron las variables cuantitativas con media y desviación estándar o mediana y rango intercuartílico. Por otra parte, para evaluar la eficacia del índice de salud prostática (PHI), de acuerdo con la curva ROC se eligió el mejor punto de corte, se calculó la sensibilidad y especificidad, valores predictivos positivo y negativo (VPP, VPN). También se analizó el índice de Youden (sensibilidad + especificidad - 1) a diferentes puntos de corte y se estimó la concordancia entre el PHI con la biopsia con el estadístico Kappa de Cohen (k). El análisis se llevó a cabo utilizando el programa estadístico SPSS versión 20.
Resultados
La población de estudio estuvo conformada por 84 hombres de 50 a 70 años, en el Cuadro 1 se describen las características. De acuerdo con la biopsia, se observa 28 hombres con cáncer de próstata (33 %). La edad promedio de la población fue de 63 ± 5 años. No se observan diferencias significativas en el PSA total y libre entre los individuos con y sin cáncer, pero si hay diferencia en las medianas del PHI 62.6 (46.9, 149.5) vs. 27.9 (18.9, 37.0), p = 0.001.
Cuadro 1 Características de la población de estudio
| Parámetro | Total (n=84) | Con CaP (n=28) | Sin CaP (n=56) | Valor de p |
|---|---|---|---|---|
| Edad (años) | 63 ± 5 | 62 ± 6 | 63 ± 5 | 0.902 |
| PSA total (ng/mL) | 10.3 (6.4, 15.8) | 11.9 (7.3, 24.3) | 9.9 (5.7, 14.8) | 0.219 |
| PSA libre (ng/mL) | 1.6 (0.9, 2.8) | 1.4 (0.9, 3.2) | 1.8 (1.0, 2.7) | 0.740 |
| PHI | 36 (26, 56) | 62.6 (46.9, 149.5) | 27.9 (18.9, 37.0) | 0.0001 |
CaP: cáncer de próstata, PSA: antígeno prostático específico, PHI: índice de salud prostática. Se presenta promedio ± desviación estándar y mediana (rango intercuartílico). Se comparan los grupos Con CaP vs Sin CaP, prueba t de student, prueba U de Mann-Whitney.
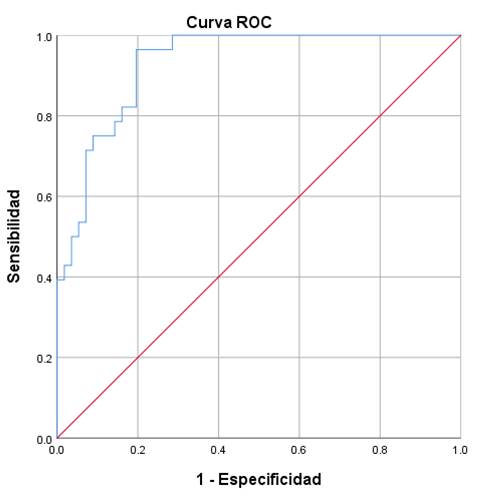
De acuerdo con la curva ROC, con un AUC de 0.930, el mejor punto de corte para considerar la práctica de biopsia utilizando el valor de PHI es de 43 puntos (Figura 1), obteniendo una sensibilidad para la prueba de PHI del 82 % (IC95%: 74-90 %) y especificidad del 84 % (IC95%: 76-92 %); así mismo su valor predictivo positivo fue de 72 % (IC95%: 62-81 %) y su valor predictivo negativo de 90 % (IC95%: 84-96 %).
En el Cuadro 2 se describe las sensibilidades a distintos puntos de corte, de acuerdo con la capacidad que tiene la prueba de detectar a los enfermos, el mejor punto de corte es a partir de los 40 puntos, con índice de Youden de 0.697. Por otra parte, se observó concordancia entre el PHI y la biopsia k = 0.65, (IC95%: 55-75 %).
Cuadro 2 Sensibilidad, 1- especificidad, valor predictivo positivo, valor predictivo negativo de la prueba de índice de salud prostática en diferentes puntos de corte
| Punto de corte | Sensibilidad | 1-Especificidad | VPP | VPN | Índice de Youden |
|---|---|---|---|---|---|
| 10 | 1.000 | 0.964 | 0.342 | 1.000 | 0.036 |
| 20 | 1.000 | 0.732 | 0.406 | 1.000 | 0.268 |
| 30 | 1.000 | 0.375 | 0.571 | 1.000 | 0.625 |
| 40 | 0.893 | 0.196 | 0.694 | 0.938 | 0.697 |
| 50 | 0.750 | 0.089 | 0.808 | 0.879 | 0.661 |
| 60 | 0.500 | 0.054 | 0.824 | 0.791 | 0.446 |
| 70 | 0.464 | 0.036 | 0.867 | 0.783 | 0.428 |
| 80 | 0.429 | 0.018 | 0.923 | 0.775 | 0.411 |
| 90 | 0.393 | 0.018 | 0.917 | 0.764 | 0.375 |
| 100 | 0.321 | 0.000 | 1.000 | 0.747 | 0.321 |
| 150 | 0.250 | 0.000 | 1.000 | 0.727 | 0.250 |
| 200 | 0.143 | 0.000 | 1.000 | 0.700 | 0.143 |
| 250 | 0.107 | 0.000 | 1.000 | 0.691 | 0.107 |
| 300 | 0.071 | 0.000 | 1.000 | 0.683 | 0.071 |
| 350 | 0.071 | 0.000 | 1.000 | 0.683 | 0.071 |
VPP: valor predictivo positivo, VPN: valor predictivo negativo
Discusión
Son múltiples las causas por las cuales el PSA puede elevarse, aproximadamente del 25-30 % de los casos con PSA elevados son identificados correctamente como cáncer.1 La biopsia de próstata es el único procedimiento para el diagnóstico del CaP, sin embargo, el sobrediagnóstico y complicaciones de “biopsias innecesarias” han llevado a desarrollar pruebas de detección alternativas previas a la biopsia. En este sentido, el PHI comparado con otros biomarcadores ha demostrado ser similar o mejor para la predicción del CaP,10,11 de tal manera que su uso se prefiere frente a otros biomarcadores.12 En la actualidad con la llegada de tecnologías genómicas y proteómicas avanzadas se han desarrollado otras pruebas de detección alternativas previas a la biopsia.13 Sin embargo, el PHI, además de ser la prueba menos costosa de los biomarcadores de CaP disponibles en Estados Unidos,14 muestra evidencia de su precisión para predecir el resultado de la biopsia de próstata y así evitar la biopsia innecesaria.15
El rendimiento de un biomarcador puede ser evaluado con distintas métricas tales como el área bajo la curva (AUC), la sensibilidad, la especificidad, además del valor predictivo positivo (VPP) y el valor predictivo negativo (VPN) que dependen de la prevalencia de la enfermedad en la población de interés.14 En este estudio, el análisis ROC mostró que PHI tiene mayor capacidad predictiva (AUC) respecto a otros reportados.16-20 Así mismo, los valores de corte reportados por otros estudios son menores a nuestros hallazgos.16,21,22 La sensibilidad de PHI obtenida en este estudio es similar a lo reportado en un metaanálisis, no así la especificidad la cual es más alta a lo reportado,23 un metaanálisis más reciente reporta una sensibilidad y especificidad de PHI para la detección de CaP de 0.791 (IC95%: 0.739 a 0.834) y 0,625 (IC95%: 0.560 a 0.686), respectivamente.24 Respecto al índice Youden, un estudio reporta que un valor de corte de 45.9 para PHI en biopsias reduciría el número de biopsias negativas en un 77.3%.25
Los resultados de este estudio retrospectivo deben interpretarse con sus limitaciones, como el pequeño tamaño de la muestra dado por conveniencia, la estrategia de reclutamiento, las características de la población, el método de biopsia de próstata y el grado de Gleason. Sin embargo, los hallazgos obtenidos son consistentes con la literatura, el PHI parece ser una buena herramienta con buena sensibilidad y especificidad para ser considerado como biomarcador para el escrutinio de CaP.
Conclusión
De acuerdo con los hallazgos obtenidos, se demuestra que el PHI tienen buena sensibilidad y especificidad para ser considerado como buen biomarcador para el escrutinio de CaP y así reducir la práctica de biopsias innecesarias y así mismos los riesgos que conlleva dicha práctica, sin embargo, no debe considerarse como un marcador aislado.