Introducción
A nivel mundial México destaca entre los principales países exportadores de miel, ocupando el séptimo lugar como productor con 58 mil 33 toneladas de miel al año (1) . La Península de Yucatán, que comprende los estados de Campeche, Quintana Roo y Yucatán, figura a nivel nacional como la principal región dedicada a la crianza de las abejas y la producción de miel2. Destaca por su exuberante vegetación y diversidad de especies vegetales, herbáceas, arbustivas y arbóreas tanto nativas como introducidas, las cuales florecen en las diferentes épocas del año, lo que permite a las abejas elaborar una miel de excelente calidad, sabor y aroma. Aproximadamente el 95 % a la producción de miel de la región se destina al mercado internacional, y que por sus características es una de las mieles más consumida en Europa y Estados Unidos3
La miel es un producto natural compuesto de azúcares monosacáridos, predominantemente fructosa y glucosa. También contiene en menor cantidad otras sustancias como son, ácidos orgánicos, enzimas y partículas sólidas derivadas de la recolección. El color de la miel puede variar de incoloro a pardo oscuro. Su consistencia es fluida, viscosa y total o parcialmente cristalizada4. El sabor, aroma y composición de la miel dependerá del origen floral y las condiciones climáticas donde se desarrollan las plantas5.
Existen normativas sanitarias diseñadas para controlar la presencia de residuos químicos en los alimentos como la miel, que ponen en riesgo la salud del consumidor, por tanto, todos los alimentos deben estar libres de cualquier tipo de residuos químicos o presentar niveles o Límites Máximos de Residuos (LMR) permitidos. La miel y otros productos de la colmena pueden contener sustancias catalogadas como nocivas para la salud humana como los plaguicidas, que también influyen en la salud de las colonias de abejas melíferas6. En los últimos años este tema ha sido de interés, ya que se ha identificado la presencia de residuos de plaguicidas de 173 compuestos diferentes en muestras de productos de las abejas (miel y cera)7. Los plaguicidas pueden llegar a los productos de la colmena como es el caso de la miel y cera a través de varias rutas, incluida la exposición de las abejas melíferas por medio del contacto con la deriva de fumigaciones o polvo contaminado, y por la ingestión de residuos en la vegetación y cuerpos de agua8.
Durante los vuelos en busca de recursos alimenticios, las abejas presentes en ecosistemas agrícolas e industriales tienden a estar en contacto con la mayor cantidad de residuos de plaguicidas en las flores de dichos cultivos, así como también, los plaguicidas pueden estar en la floración natural circundante y por lo tanto, ser llevados a la colmena, de manera que logran estar presentes en la miel, cera y demás productos de la colmena9.
En el último siglo, a nivel mundial se ha provocado una transformación en la superficie de la tierra debido a la actividad humana y a la agricultura intensiva10, en este sentido, en la última década debido a las actividades agropecuarias y al desarrollo humano en la Península de Yucatán, se han reducido los hábitats naturales y seminaturales generando una fragmentación y afectando significativamente la diversidad y abundancia floral de la selva tropical (11,12) , esto genera como resultado un impacto en la abundancia y salud de las abejas10.
Desde el 2016 a la fecha en los estados de la Península de Yucatán, los apicultores y el colectivo “Alianza Maya por las abejas de la Península de Yucatán” han reportado una pérdida masiva de colonias de abejas, debido al uso indiscriminado de plaguicidas aplicados en cultivos de soya, sorgo, sandía, melón y chile y a la deforestación, viéndose afectada la actividad apícola de la región13. Debido a la falta de estudios sobre la detección de plaguicidas en muestras de miel y cera, el objetivo de la presente investigación fue identificar y cuantificar la presencia de plaguicidas en miel y cera en colonias de abejas melíferas de municipios de la Península de Yucatán.
Material y métodos
Zonas de muestreo
El estudio se llevó a cabo en la Península de Yucatán, que abarca los estados de Campeche, Yucatán y Quintana Roo, en México. La selección de las zonas de muestreo se realizó mediante recorridos de reconocimiento en campo, con el objetivo de identificar dos tipos de vegetación: 1) vegetación primaria y acahual (VP): áreas que no han experimentado cambios significativos debido a actividades humanas o perturbaciones naturales; estas zonas presentan una cubierta vegetal con estructura y composición florística representativa del tipo de selva de la región. 2) vegetación secundaria o plantaciones frutícolas y cultivos agrícolas (VS): áreas donde la vegetación natural ha sido modificada o alterada por factores humanos o naturales, para el establecimiento de plantaciones frutícolas y cultivos agrícolas. Para la VP, se seleccionaron apiarios ubicados dentro de un radio de 5 km, asegurando la ausencia de cultivos agrícolas o frutales en la cercanía. En cuanto a la VS, se ubicaron apiarios a no más de 2 km de radio, manteniendo las características mencionadas. Este criterio se basó en estudios que demostraron que las abejas generalmente buscan alimento en un radio de hasta 2 km de su colmena14. Posterior a la selección del tipo de vegetación, se contactó a los apicultores para obtener su consentimiento para recolectar muestras de sus apiarios y que tuvieran un mínimo 10 colmenas.
Muestreo
Entre los meses de junio a octubre de 2023 se recolectaron 31 muestras de miel y 31 de cera en diversos apiarios de la Península de Yucatán. La distribución de las muestras por estado y tipo de vegetación fue la siguiente: 1) Campeche: cinco muestras de miel y cuatro de cera de VP; cinco muestras de miel y seis de cera de VS. 2) Yucatán: cinco muestras de miel y de cera en la VP; seis muestras de miel y cera de VS. 3) Quintana Roo: cinco muestras de miel y cuatro de cera de VP; cinco muestras de miel y seis de cera en VS.
Para la recolección de las muestras, se utilizó un cúter desechable para cortar una pieza de panal con miel y otro con cera de aproximadamente 12 cm2. La miel se depositó en tubos de centrifuga cónico de la marca eppenddorf con una capacidad de 14 ml y la cera en bolsas de plástico. Cada muestra se identificó según su procedencia y tipo de vegetación, así como cada apiario fue georreferenciado mediante GPS (Figura 1).
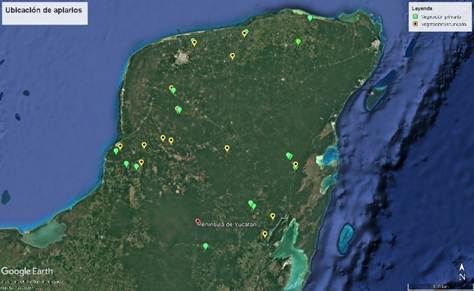
Color amarillo, apiarios cerca de vegetación secundaria. Color verde, apiarios cerca de vegetación primaria.
Figura 1 Ubicación de los sitios de muestreo de miel y cera de abejas
Una vez recolectadas las muestras de miel y cera del apiario, se almacenaron en congelación a -20 °C hasta su análisis por Cromatografía de gases con detección por espectrometría de masas con triple cuadrupolo (GC-MS/MS). Dichas muestras se analizaron en el laboratorio de servicios Analíticos del Centro de Investigación y Asistencia en Tecnología y Diseño del Estado de Jalisco, A. C. (CIATEJ) en su sede Noreste.
Análisis de residuos de plaguicidas en miel y cera
Productos químicos y soluciones
Se analizaron un total de 75 plaguicidas, los cuales disponía el laboratorio en su momento. Los siguientes estándares analíticos de los plaguicidas se obtuvieron de ChemService, Inc. (West Chester, PA, USA): 2,4'-DDT, éster 2-etilhexílico del 2,4'-D, éster isopropílico del 2,4'-D, isómero B del epóxido de hectacloro, bifentrina, cihalotrina gamma, cihalotrina lambda, ieldrina, difenoconazol, diflubenzurón, paclobutazol, pentacloroanilina, piridabeno, piriproxifeno, tebuconazol, alfa-HCH. De Sigma-Aldrich-Fluka (St. Louis, MO, USA): 2-fenilfenol, aldrín, carfentrazona-etilo, clorfenvinfos, clorpirifos-etilo, clorpirifos-metilo, cumafós, deltametrina, diazinón, diclofentión, dicofol, dimetoato, espiromesifen, etión, fenclorfos, fipronil-sulfona, fipronil-sulfuro, fipronil-desulfinil, fludioxonil, fluusilazol, fonofos, ftalimida, hexaclorobenceno, malatión, oxifluorfeno, pendimetalina, pentacloroanisol, pentaclorofenol, permetrina, pertán, fentoato, forato, fosmeta, profenofós, propetamfos, quinoxifén, piridafentión, pirimetanil, quinalfós, espirodiclofeno, tebutiurón, tecnazeno, terbufós, triclorfón, tetradifón, trifloxistrobina, triazofós. El cis-1,2,3,6- tetrahidroftalimida, endosulfán I, el endosulfán II, el fenitrotión, el paratión-etilo, el paratión-metilo y el fosfato de trifenilo (patrón interno) se adquirieron de Sigma-Aldrich-Supelco (Bellefonte, PA, USA). El fentión y el pirimifos-metilo se obtuvieron de Accustandard (New Haven, CT, USA), y ULTRA Scientific (N. Kingstown, RI, USA), respectivamente. El ácido fórmico (grado MS) y formiato de amonio (base de metal traza) se adquirieron en Sigma-Aldrich. El acetonitrilo grado HPLC y el agua grado HPLC fueron adquiridos en Tedia High Purity Solvents (Fairfield, OH). Las sales de extracción “Quick, Easy, Cheap, Effective, Rugged, and Safe” (QuEChERS) (Método AOAC) y los kits SPE de dispersión (Bond Elut), fueron adquiridos en Agilent Technologies (Santa Clara, CA, USA).
Preparación y extracción de muestras
De cada muestra se tomaron 7 g de miel y 3 g de cera. Se realizó la extracción de residuos de plaguicidas de acuerdo con una modificación del método analítico “QuEChERS”, previamente validado en el Laboratorio de Servicios Analíticos de la Sede Noreste del CIATEJ15,16.
Extracción de plaguicidas de la miel
En un tubo de plástico para centrífuga de 50 ml se pesaron 7 g de miel, a los cuales se agregaron 10 ml de agua desionizada y se agitaron manualmente durante un minuto. Se agregaron 15 ml de acetonitrilo acidificado al 1% con ácido acético (v/v) y se agitó manualmente nuevamente durante 1 min. Posteriormente se usaron 6 g de sulfato de magnesio (MgSO4) y 1.5 g de acetato de sodio (CH3COONa); todas las muestras se agitaron durante 1 min y se centrifugaron a 4,000 rpm por 5 min. Para hacer la limpieza del extracto se utilizaron 8 ml del sobrenadante y se transfirieron a un tubo de 15 ml con 400 mg de amina primaria-secundaria (PSA), 1,200 mg MgSO4 y 400 mg de octadecilsilano extra limpio (C18-EC); se agitaron durante 1 min y se centrifugaron a 4,000 rpm por 5 min.
Extracción de plaguicidas en la cera
Para su extracción se utilizó el método de Niell et al17. En un tubo de plástico para centrifuga de 50 ml se pesaron 3 g de cera, se agregaron 15 ml de acetonitrilo acidificado al 1% con ácido acético (v/v). Los tubos se mantuvieron en baño maría a 80 °C hasta la fundición de la cera; una vez fundida la cera se agitaron manualmente durante 20 seg y se colocaron nuevamente en el baño maría para que se fundieran, el proceso de fundición y agitación manual se repitió tres veces más, las muestras se mantuvieron en reposo hasta alcanzar la temperatura ambiente y se introdujeron a un congelador a -20 °C durante 2 h para que la cera se precipitara. Para la limpieza del extracto se extrajeron 8 ml del sobrenadante y se transfirieron a un tubo de 15 ml con 400 mg de amina primaria-secundaria (PSA), 1,200 mg MgSO4 y 400 mg de EC-C18, se agitaron durante 1 min y se centrifugaron a 4,000 rpm por 5 min.
Condiciones cromatografías y de detección
Para la cromatografía de gases (GC-MS/MS), se usó un cromatógrafo de gases 7890A acoplado a un espectrómetro de masas con cuadrupolo triple 7000B con ionización de impacto de electrones (EI), equipado con un automuestreador 7693A (Agilent Technologies). La separación cromatográfica se realizó utilizando dos columnas capilares DB-5 MS ultra inter (15 m × 0.250 mm × 0.25 μm de espesor de película; Agilent Technologies). Se utilizó una unión final purgada para conectar las dos columnas y se realizó un lavado después de cada ejecución. Se inyectaron 2 μl del extracto del sobrenadante en modo sin división (5 min a 21.1 psi), con un flujo constante de 1.0 ml/min (columna 1) y 1.2 ml/min (columna 2). El helio de alta pureza se utilizó como gas portador. La configuración del inyector fue de 65 ˚C (contener 0.2 min) a 310 ˚C a 600 ˚C/min. La temperatura del horno se programó de 60 ˚C (1 min) a 170 ˚C a 40 ˚C/min a 310 ˚C (4 min). El espectrómetro de masas se operó en el modo de ionización de impacto de electrones (energía de ionización 70 eV), mientras que la línea de trasferencia y las temperaturas de la fuente de iones se fijaron a 300 ˚C. Para la selección y cuantificación de análisis se utilizó el modo de monitoreo de iones (SIM) seleccionado con un mínimo de tres iones para cada análisis. La velocidad de escaneo para cada segmento se estableció aproximadamente en dos escaneos con el fin de obtener un mínimo de 10 puntos de datos por pico.
Resultados
Todas las muestras de miel del estado de Campeche, presentaron trazas de fipronil, tanto en vegetación primaria (VP) como en vegetación secundaria (VS). En las muestras de cera de la VP se detectaron dos plaguicidas desde trazas hasta 0.02 mg/kg y en las muestras de VS se presentó la mayor diversidad de plaguicidas (7), siendo el organofosforado coumafos el que presentó concentraciones de hasta 1.133 mg/kg (Cuadro 1).
Cuadro 1 Concentración de plaguicidas (mg/kg) encontrados en la miel y cera de colonias de abejas melíferas recolectados en diferentes tipos de vegetación de los estados de la Península de Yucatán
| Plaguicida | Grupo toxicológico | Clase | Muestras analizadas | Muestras positivas (%) | Concentración (mg/kg) | |||
|---|---|---|---|---|---|---|---|---|
| Min | Max | |||||||
| Campeche | VP: | |||||||
| Miel | fipronil | Fenilpirazol | Insecticida | 5 | 5 (100) | < o.oo5 | ||
| Cera | cis-1,2,3,6-tetrahidroftalimida | Metabolito del captan | Fungicida | 4 | 3 (75) | < o.oo5 | 0.010 | |
| coumafos | Organofosforado | Insecticida/acaricida | 4 | 2 (50) | < o.oo5 | 0.026 | ||
| VS: | ||||||||
| Miel | fipronil | Fenilpirazol | Insecticida | 5 | 5 (100) | < o.oo5 | ||
| Cera | coumafos | Organofosforado | Insecticida/acaricida | 6 | 3 (50) | < o.oo5 | 1.133 | |
| cis-1,2,3,6-tetrahidroftalimida | Ftalamida | Fungicida | 6 | 2 (33) | < o.oo5 | 0.081 | ||
| BHC alfa | Isomero del lindano | Insecticida | 6 | 1 (17) | < o.oo5 | |||
| dieldrin | Organoclorado | Insecticida | 6 | 1 (17) | < o.oo5 | |||
| boscalid | Clorado | Fungicida | 6 | 1 (17) | < o.oo5 | |||
| pentacloroanisol | Pentaclorofenol | Insecticida/fungicida | 6 | 2 (33) | < o.oo5 | |||
| acrinathrin | Piretroide | Insecticida/acaricida | 6 | 2 (33) | < o.oo5 | |||
| Yucatán | VP: | |||||||
| Miel | cis-1,2,3,6 tetrahidroftalimida | Metabolito del captan | Fungicida | 5 | 5 (100) | < o.oo5 | 0.026 | |
| Cera | cis-1,2,3,6-tetrahidroftalimida | Metabolito del captan | Fungicida | 5 | 5 (100) | < o.oo5 | 0.022 | |
| coumafos | Organofosforado | Insecticida/acaricida | 5 | 3 (60) | < o.oo5 | 0.067 | ||
| pentacloroanisol | Pentaclorofenol | Insecticida/fungicida | 5 | 3 (60) | < o.oo5 | |||
| dicofol | Organoclorado | Insecticida/acaricida | 5 | 1 (20) | < o.oo5 | |||
| VS: | ||||||||
| Miel | cis-1,2,3,6-tetrahidroftalimida | Metabolito del captan | Fungicida | 6 | 6 (100) | < o.oo5 | 0.014 | |
| Cera | cis-1,2,3,6-tetrahidroftalimida | Metabolito del captan | Fungicida | 6 | 4 (67) | < o.oo5 | 0.022 | |
| coumafos | Organofosforado | Insecticida/acaricida | 6 | 3 (50) | < o.oo5 | 0.051 | ||
| pirimifós-metil | Organofosforado | Insecticida/acaricida | 6 | 1 (17) | < o.oo5 | |||
| Quintana Roo | VP: | |||||||
| Miel | fipronil sulfide | Metabolito del fipronil | Insecticida | 5 | 5 (100) | < o.oo5 | ||
| Cera | cis-1,2,3,6-tetrahidroftalimida | Metabolito del captan | Fungicida | 4 | 3 (75) | < o.oo5 | 0.00 | |
| coumafos | Organofosforado | Insecticida/acaricida | 4 | 4 (100) | < o.oo5 | 0.023 | ||
| VS: | ||||||||
| Miel | fipronil | Fenilpirazol | Insecticida | 5 | 5 (100) | < o.oo5 | ||
| fipronil sulfona | Metabolito del fipronil | Insecticida | 5 | 1 (20) | < o.oo5 | |||
| Cera | coumafos | Organofosforado | Insecticida/acaricida | 6 | 3 (50) | < o.oo5 | 0.010 | |
| trans-permetrina | Piretroide | Insecticida | 6 | 1 (17) | < o.oo5 | 0.006 | ||
| cis-1,2,3,6-tetrahidroftalimida | Metabolito del captan | Fungicida | 6 | 6 (100) | < o.oo5 | 0.011 | ||
| fipronil-sulfona | Metabolito del fipronil | Insecticida | 6 | 1 (17) | < o.oo5 | |||
VP= vegetación primaria; VS= vegetación secundaria.
En Yucatán, de todas las muestras analizadas de miel presentaron concentraciones de 0.026 y 0.0014 mg/kg de cis-1,2,3,6- tetrahidroftalimida en la VP y VS respectivamente. En la cera de la VP se presentó la mayor diversidad de plaguicidas (cuatro), seguido por la VS con tres plaguicidas (Cuadro 1).
Para el estado de Quintana Roo en la miel de la VP y VS se detectaron trazas de fipronil. Para la cera en la VP se detectaron dos plaguicidas y cuatro en la VS (Cuadro 1).
Discusión
Los resultados obtenidos indican que la presencia de los plaguicidas encontrados en la miel y cera de abejas están relacionados con la región y tipo de vegetación donde fueron recolectadas las muestras; estos hallazgos podrían indicar un factor de riesgo significativo para la salud de las abejas6, además es probable que la contaminación de la miel y cera por plaguicidas ocurriera a través de dos vías principales: vía indirecta, se refiere al transporte de sustancias tóxicas por parte de las abejas pecoreadoras al recolectar néctar, polen, agua y resinas. Vía directa, considerada la más importante, implica la contaminación de los productos apícolas con acaricidas, antibióticos y plaguicidas volátiles, principalmente como resultado de las prácticas apícolas18. En este estudio la detección de los plaguicidas agrícolas como el fipronil y cis-1,2,3,6-tetrahidroftalimida, junto con el acaricida coumafos (aplicado directamente a la colmena19 respaldan estas vías.
Se observó una mayor diversidad y cantidad de plaguicidas en la cera, en primer lugar, se encontraron ocho insecticidas, seguido por dos fungicidas y un acaricida. En comparación con la miel, donde se encontró un insecticida y un fungicida. Estos resultados coinciden con los reportados por Vargas-Valero et al20 en la región centro-norte de México, reportando una mayor cantidad y diversidad de plaguicidas en la cera. Esta diferencia podría atribuirse a la naturaleza hidrofóbica de la mayoría de los plaguicidas, que les confiere alta estabilidad y facilita su transferencia a la cera21; adicionalmente, prácticas de manejo inadecuadas, como el reciclaje de cera y la permanencia prolongada de panales en las colmenas, podrían contribuir a la acumulación de estos compuestos.
Vegetación primaria
En las muestras de miel y cera recolectadas en las áreas de VP en los tres estados de la Península de Yucatán, se detectaron trazas y bajos niveles de plaguicidas. Los compuestos más frecuentes fueron: fipronil, presente en el 63 % de las muestras de miel, Cis-1,2,3,6-tetrahidroftalimida, el cual es un metabolito derivado del fungicida captan y fue detectado en el 32 % de las muestras de miel y el 93 % de las muestras de cera y coumafos encontrado en el 53 % del total de las muestras de cera de la VP (Cuadro 1). Al comparar estos resultados con los LMR establecidos por la Unión Europea22, se observó que ninguno superó los límites máximos en miel: fipronil 0.005 mg/kg, cis-1,2,3,6-tetrahidroftalimida 0.05 mg/kg, y coumafos 0.1 mg/kg. Estos resultados son similares a los publicados por Fluton et al23, que encontraron una interacción entre diferentes tipos del paisaje (agrícola, urbano, bosque y pastizales) y la exposición a plaguicidas. En el contexto de la presente investigación, donde los apiarios en VP se seleccionaron específicamente por ausencia de cultivos agrícolas/frutales, la presencia de trazas de fipronil y el metabolito de captan, podría atribuirse a la contaminación de cera estampada adquirida comercialmente y utilizada para la construcción de nuevos panales.
En el caso del coumafos, su presencia podría deberse al uso de este acaricida por parte de los apicultores para controlar el ácaro Varroa o el escarabajo de la colmena. Asimismo, factores como el bajo reemplazo de panales y el reciclaje de cera podrían contribuir a la acumulación de este compuesto. Además, no se descarta la posibilidad de que hayan recolectado estos plaguicidas durante el pecoreo, considerando su capacidad para volar hasta 14 km en busca de alimento24. Dado que aún no se ha establecido una explicación definitiva para la presencia de residuos de plaguicidas en muestras de VP, se recomienda continuar con muestreos y análisis a largo plazo.
Vegetación secundaria
En las muestras de miel procedentes de VS de los estados de Campeche y Quintana Roo se detectaron trazas de fipronil y en las mieles de Yucatán se detectó el metabolito del derivado del fungicida captan (cis-1,2,3,6 tetrahidroftalimida) (Cuadro 1). En cuanto a la cera procedente de los tres estados, los plaguicidas más frecuentes en el total de las muestras fueron el metabolito del captan (67 %), seguido por el organofosforado coumafos (50 %). El coumafos es un insecticida y acaricida sintético lipofílico y altamente persistente. Se distribuye a través de la trofolaxis y el contacto entre ellas, y actúa tanto por contacto como de forma sistémica (25) . A pesar de no estar autorizado en México para el tratamiento de Varroa en abejas, algunos apicultores en la Península de Yucatán utilizan un producto no registrado llamado “polvo mágico”, que contiene coumafos en concentraciones de 639.55 y 900 mg/kg19. Este polvo se aplica para controlar el pequeño escarabajo de la colmena y el ácaro Varroa. Los LMR para el coumafos varían según la legislación, para los Estados Unidos es de 0.15 mg/kg en miel y 45 mg/kg en cera26; para la Unión Europea 0.1 mg/kg en miel22 y para Canadá 0.02 mg/kg en miel y 0.1 mg/kg en cera27. Los resultados de este estudio mostraron que el 63 % de las muestras de cera de VS contenían concentraciones de coumafos por debajo del LMR de Estados Unidos, excepto una muestra que alcanzó 1.133 mg/kg. Esta concentración difiere con lo encontrado por Valdovinos-Flores et al (2016) y Fulton et al (2019) los cuales reportaron valores de 0.155 a 2.220 y 15.5 mg/kg respectivamente19,23. Se sospecha que el uso del "polvo mágico" continúa en la región, contribuyendo a la presencia de coumafos.
La reutilización de cera y la medicación de colonias con coumafos también pueden contribuir a la acumulación de este plaguicida en la cera, incluso contaminando la cera virgen (28) . La acumulación de residuos de coumafos en la cera de los panales podría tener implicaciones en la fortaleza y supervivencia de las colonias. Por lo tanto, se requieren estudios para determinar la concentración de plaguicidas en la cera comercial en la región.
La menor cantidad y diversidad de plaguicidas en la VP en comparación con la VS, posiblemente se debe a la menor superficie agrícola cerca de los apiarios de VP. Las superficies sembradas varían entre los estados: Campeche (334,905.29 ha), Yucatán (706,130.06 ha) y Quintana Roo (127,604.11 ha) (29) . Campeche, es el principal productor de soya en México (29) , utiliza grandes cantidades de plaguicidas, lo que posiblemente influyó en los resultados, especialmente en la presencia de cis-1,2,3,6-tetrahidroftalimida, la cual se encontró en altas frecuencias en la cera de VS. El captan se utiliza en cultivos de soya, tomate, chile y frutales en la región.
El fipronil se detectó en trazas en la miel de VS de Campeche y Quintana Roo, es un insecticida sistémico altamente tóxico para las abejas, incluso en dosis subletales30. Su capacidad de bioacumulación y toxicidad reforzada con el tiempo representa un riesgo significativo (31) . Debido a lo anterior, no se descarta encontrar niveles cuantificables, por tanto, se requiere continuar con el monitoreo. Finalmente, la diversidad y cantidad de plaguicidas detectados en la miel y cera de la Península de Yucatán, comparado con el norte y centro de México19,20 probablemente se debe a una menor superficie de áreas de cultivos agrícolas, además que aún predominan áreas de vegetación nativa, sin embargo, se requiere seguir el monitoreo a lo largo de los años para observar el comportamiento.
Conclusiones e implicaciones
La mayor concentración y diversidad de plaguicidas se detectaron en la cera de abejas recolectada en apiarios cercanos a cultivos agrícolas y frutales. Además, se identificó el posible uso de productos químicos no autorizados en México para el control del ácaro Varroa destructor y el escarabajo de la colmena. En cuanto a la miel, la detección de trazas de plaguicidas sugiere la necesidad de realizar estudios adicionales para monitorear su presencia en cantidades cuantificables. De acuerdo a los resultados, estos fueron menores en comparación con el norte del país; posiblemente se debe a la menor densidad de cultivos agrícolas y a pesar de la deforestación, aún existen grandes áreas con presencia de vegetación nativa en la región donde se realizó el estudio. Es crucial continuar el monitoreo de la presencia de plaguicidas en los productos de la colmena, ampliando el área de estudio y el número de muestras en la región y a nivel nacional. Se recomienda realizar muestreos en diferentes épocas del año para determinar si la cantidad y diversidad de plaguicidas encontradas están relacionadas con las actividades agrícolas en cada región del país.















