Introducción
El polimetilmetacrilato (PMMA) es un material termoplástico transparente, tradicionalmente utilizado en la confección de prótesis dentales1. Es un material maleable, liviano, fuerte, inerte radiolúcido, no ferromagnético y estable2. Además de estas, posee características mecánicas, físicas y estéticas que se diferencian de otros materiales plásticos, puesto que tiene una mayor translucidez, excelente resistencia, fácil moldeo, preserva las piezas dentales antagónicas y puede repararse si su superficie se raya; no obstante, su baja resistencia al desgaste es la principal deficiencia1. También se ha demostrado que el PMMA tiene cierta tendencia a acumular biopelícula dental en superficies de aparatología, al igual que sucede en tejidos duros y blandos3. Por ello en las últimas décadas la nanotecnología se ha relacionado con la odontología para mejorar la variedad de materiales a base de resina, entre ellos el PMMA; es así como surgen nanocompuestos que conjuntan una matriz polimérica y un relleno a nanoescala, que proporcionan nuevas propiedades, tanto mecánicas como físicas, que dependen del tamaño y morfología de las Nps4. El proceso para la obtención de nanocompuestos se lleva a cabo encapsulando partículas nanométricas, ya sean metálicas u óxido-metálicas, en una capa de polímeros, dando lugar a nanocompositos5. Así ambos materiales producen una sinergia provocando que los nanocompuestos posean mejores características en conjunto que de manera individual6.
Por otro lado, se sabe que la cavidad bucal cuenta con muchas superficies, desde tejidos blandos hasta tejidos mineralizados superficiales, cada una de ellas recubierta por una gran cantidad de bacterias generando biopelícula en su superficie. Algunas de estas bacterias han sido consideradas como cariogénicas y periodontopatógenas, que son las patologías bacterianas más comunes en la cavidad estomatológica en los seres humanos7.
Debido a la amplia variedad de microorganismos que se detectan en la boca, ya que se ven reflejados en materiales de prótesis removibles, aparatos ortodónticos, resinas o cualquier material de restauración que se encuentra expuesto a bacterias, ya sean Gram-positivas o Gram-negativas como estreptococos, lactobacilos, enterococos, e incluso hongos y virus entre otra gran variedad de microorganismos, ya que en la boca encontramos aproximadamente 600 especies distintas, pero solo el 1% de las mismas son patógenas, las cuales son etiología de la caries dental, gingivitis, periodontitis, estomatitis, infecciones odontogénicas, osteítis alveolar y amigdalitis8. Entre las enfermedades micóticas podemos encontrar la candidiasis bucal9. Por otro lado, podemos mencionar el herpes labial, varicela zóster y la infección por el virus Epstein-Barr como enfermedades de origen viral10. Por lo anterior, es importante el estudio de nuevos materiales que inhiban el crecimiento de bacterias, virus y hongos que puedan causar disbiosis en cavidad oral.
Candida albicans es un hongo muy común en la boca, sobre todo en adultos de la tercera edad. Es por ello que se destina tiempo, esfuerzo y recursos en la búsqueda de materiales eficientes para inhibir su crecimiento, y, dado que este sector de la población tiende al uso de distintas prótesis dentales elaboradas a partir de PMMA, la comunidad científica desarrolla distintos materiales compuestos que buscan implementar al polimetilmetacrilato propiedades antimicrobianas y antifúngicas, una alternativa es la adición de Nps.
En esta revisión se propone el análisis de las propiedades antimicrobianas de las Nps que son adicionadas al PMMA y así evitar la proliferación de microorganismos relacionados con la cavidad bucal. Las Nps que se incluyeron en esta revisión sistemática son: NpsTiO2, NpsAg y: Nps de platino (Pt), así como Nps biogénicas con Bacillus amyloliquefaciens (NpsMAg) y con rizoma de Curcuma aromatica (NpsCAg), debido a las propiedades antimicrobianas que confieren al PMMA. Es por ello que se realizará una comparación entre ellas, para conocer cuál tiene un mayor efecto antimicrobiano al ser adicionadas al PMMA, en el campo odontológico y de esta manera ayudar a la prevención de las patologías estomatológicas.
Debido al efecto antimicrobiano que confiere la adición de Nps al PMMA, se ha comprobado que existe una reducción significativa de microorganismos como hongos, bacterias y virus; causantes de infecciones o patologías presentes en la práctica diaria odontológica. Lo anterior para ayudar a mejorar la calidad del PMMA en las determinadas condiciones del ambiente oral. Es por ello que el objetivo general de la revisión sistemática es comparar las propiedades antimicrobianas de los compositos de PMMA/Nps, en el campo odontológico y así ayudar a la prevención de las patologías estomatológicas.
Material y métodos
Para la investigación se desarrolló un protocolo basado en los lineamientos PRISMA11,12, para la realización de revisiones sistemáticas que incluyó los siguientes enunciados:
Problema: la población de interés incluyó las principales problemáticas en el uso de materiales dentales, que es la formación de microorganismos que se adhieren al PMMA, debido a la falta de higiene oral o la composición de los mismos.
Intervención: realizar un estudio comparativo del efecto antimicrobiano que confieren los distintos tipos de Nps adicionados al PMMA.
Comparación: la reproducción y desarrollo de microorganismos en la cavidad oral se reduce con la presencia de Nps con propiedades antimicrobianas en comparación con los materiales dentales carentes de ellas.
Resultados: en la revisión sistemática se espera obtener resultados significativos en la reducción de microorganismos, esto gracias a las Nps añadidas al PMMA para las diversas aplicaciones en odontología, además de comparar las distintas Nps empleadas con este fin.
Se utilizaron las palabras clave: nanopartículas, polimetilmetacrilato, compositos, antimicrobiano, odontología y propiedades, para realizar la búsqueda bibliográfica, los componentes PICO de la revisión sistemática son los siguientes:
Componentes PICO de la búsqueda bibliográfica
Problema: proliferación bacteriana en las prótesis de PMMA, que conducen a patologías estomatológicas.
Intervención: revisión bibliográfica sobre compositos con diferentes tipos de Nps al PMMA.
Comparación: realizar un estudio comparativo de las diferentes Nps, dosis y Concentración Mínima Inhibitoria (CMI).
Outcome (resultados): reducción de la proliferación bacteriana con cierto tipo de Nps y a cierta concentración.
Se incluyeron los artículos de antigüedad no mayor a seis años hasta la fecha, textos completos, artículos que incluyan en el título: PMMA adicionado con alguna Nps; estar aplicado a la odontología; sólo se incluirán estudios in vitro (en los que se muestre el número de muestras realizadas por cada estudio, tipo de partícula, tamaño de partículas, organismos a los que inhibe y CMI. Se excluyeron los artículos publicados antes de 2014; aquellos aplicados a otra área que no sea a odontología y artículos que no se relacionen con “PMMA adicionado con Nps”.
Se llevó a cabo una primera búsqueda de manera electrónica en enero de 2020, por cinco miembros, una persona en la base de datos PubMed (U.S. National Library of Medicine, National Institutes of Health). De igual manera dos individuos en Medline (National Library of Medicine of the United States). Por último, una quinta persona en CONRICyT (Consorcio Nacional de Recursos de Información Científica y Tecnológica). Los resultados posteriormente se excluyeron siguiendo los criterios, que serán descritos tras la segunda búsqueda.
La segunda estrategia de búsqueda se llevó a cabo nuevamente en las mismas bases de datos electrónicas, en octubre del 2020. En esta ocasión no se agregaron artículos a la revisión debido a que no cumplieron con los criterios de inclusión que serán mencionados.
La estrategia de búsqueda elegida fue: {Subject AND Adjective} {Subject: (Title) AND Adjective: (Title)}. Asimismo, se acotó por idioma y fecha. Los artículos resultantes fueron examinados por cinco observadores para poder discernir cuáles cumplían los criterios de inclusión a partir de la lectura del resumen y del título.
Resultados
La búsqueda inicial mostró 341 estudios cuyo título se relacionaba con los patrones de búsqueda, de los cuales, al eliminar los duplicados, el resultado fue de 247 artículos, de estos fueron excluidos 111 por el filtro de fecha, ya que no son revisiones sistemáticas, lo que arrojó 136 artículos incluidos. Por otro lado, al aplicar un tercer filtro de texto completo se obtuvieron 108 artículos. Posterior a la lectura rápida de títulos y resúmenes se eliminaron 89 debido a la falta de relación con el tema de estudio, por ello únicamente se incluyeron diecinueve, que aportan información importante acerca de los nanocompositos, por consiguiente, con propiedades antimicrobianas y con aplicación en la odontología. Específicamente de esos diecinueve artículos, se excluyeron once que no cumplían con los criterios de inclusión: dos no reportaban Nps antimicrobianas, únicamente lo mencionaban en el título, uno tenía un enfoque claro en citotoxicidad más que en el efecto antimicrobiano, dos más se enfocaban en materiales no aplicables en la cavidad oral, por lo que fueron descartados, tres mas no mencionan PMMA, y por lo tanto cumplían con un criterio de exclusión, y tres de ellos eran revisiones literarias o sistemáticas. De esta manera, se seleccionaron finalmente ocho artículos (Figura 1).
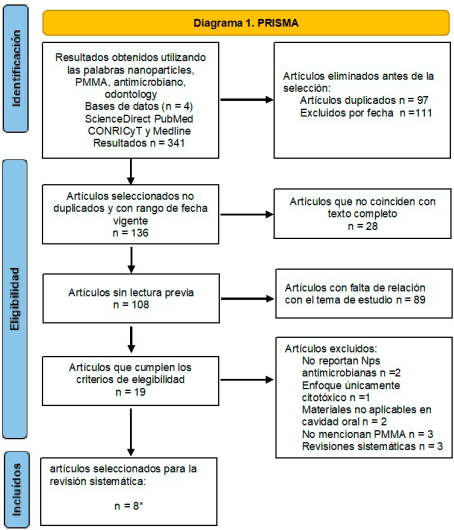
*Se incluyeron aquellos artículos relacionados con el tema: “Compositos de PMMA/NPs con propiedades antimicrobianas aplicados a la odontología.
Fig. 1 Diagrama PRISMA
En la segunda búsqueda se obtuvieron 341 artículos, de los cuales al eliminar duplicados se obtuvieron 247. Al aplicar los filtros el resultado se redujo a 136, de igual manera al ser evaluados a texto completo y al ser leídos se obtuvieron ocho nuevamente, por tanto, la presente revisión sistemática únicamente se basa en los encontrados inicialmente.
En los ocho artículos seleccionados se estudiaron las propiedades de compositos de PMMA/Nps de distintos óxidos metálicos, tales como dióxido de titanio (TiO₂), plata (Ag), dióxido de silicio (SiO₂) y platino (Pt)13-20. Incluso un artículo de la literatura emplea Nps de grafeno para potencializar y mejorar las propiedades deseadas en el composito sintetizado18. Un artículo más estudia la posibilidad de sintetizar Nps de plata biogénicas (NpsAg) a partir de B. amyloliquefaciens (NpsMAg) y rizoma de C. aromatica (NpsCAg), para disminuir la toxicidad de las Nps sintetizadas químicamente, este último se enfocó en analizar el efecto que tenían las Nps de plata biogénicas en presencia de Streptococcus mutans19.
De los artículos presentados solo cuatro de ellos se analizaron mediante análisis unidireccional de varianza (ANOVA), en el que la investigación se apoya para realizar pruebas a dos o más microorganismos15-20. También dos de ellos fueron evaluados estadísticamente por medio de la prueba T-student14-20. Uno de ellos fue estudiado por medio de ANOVA y el análisis post hoc de Tukey utilizando el software SPSS15.
Por el contrario, la bibliografía presenta distintos métodos de estudio de la CMI, ya sea por el método de Miles y Misra, el de microdilución en placa de 96 pocillos a base de resazurina, prueba Kirby-Bauer (método de difusión en disco), clasificación de células activadas por fluorescencia (FACS por sus siglas en inglés) y ensayo de crecimiento planctónico 14,19-20.
Todos los artículos manejaron distintos tamaños de partícula, de amplia diferencia entre ellos, desde 3 a 5 nanómetros hasta 170 nm. Existe gran variedad de microorganismos a los que inhibe, como C. albicans, C. scotti, S. mutans, Lactobacillus acidophilus, Enterococcus faecalis, Pseudomona aeruginosa, S. sobrinus, Staphylococcus aureus y Escherichia coli (Tabla 1).
Tabla 1 Propiedades antimicrobianas de los compuestos con nanopartículas
| Art. | Tipo de nanopartículas | Número de muestras | Tamaño de partícula (nm) | Microrganismos | Concentración mínima inhibitoria (CMI) | Resultados |
|---|---|---|---|---|---|---|
| 13 | Dióxido de titanio (TiO2) | 5 | 56-170 | C. scotti | 0.4% | No especificado |
| 14 | Plata (Ag) | 3 | 20 | C. albicans | 3.5% | 94% ± 99% del área |
| 15 | Dióxido de titanio (TiO2) y dióxido de silicio (SiO2) | 6 | TiO2= 21; SiO2=20 | S. mutans y L. acidophilus | 1% para ambos microorganismos | 93% L. acidophilus 92% S. mutans |
| 16 | Dióxido de titanio (TiO2) | 24 | 80-100 | E. faecalis y P. aeruginosa | 3% para ambos microorganismos | 92% P. aeruginosa |
| 17 | Platino (Pt) | 2 | 3-5 | S. mutans y S. sobrinus | 0.1% para ambos microorganismos | 88.9% S. mutans y 88.2% S. sobrinus |
| 18 | Plata (Ag) y grafeno (G-Ag) | 3 | NA | S. aureus, S. mutans y E. coli | 2% para todos los microorganismos | S. aureus 90.5* mutans 89.0* y E. coli 91.67* |
| 19 | Plata Biogénicas con Bacillus amyloliquefaciens (MAg), y rizoma de Curcuma aromatica (CAg) | 3 | 20-40 | S. mutans | MAgNPs = 3.9µ/mL; CAgNPs = 50µ/mL | MAgNPs=99%; CAgNPs=94% |
| 20. | Dióxido de titanio (TiO2) | 18 | 10-30 | L. acidophilus, S. mutans y C. albicans | 2.5% para todos los microorganismos | No especificado |
*Los datos presentan como media ± 0.05; se utilizó la prueba T para calcular la significancia estadística
Los artículos fueron evaluados por los criterios de escala de calidad metodológica, empleando los siguientes lineamientos (Tabla 2)21: a) número de muestras mayor a la media de 9.6; b) realiza comparación entre concentraciones de inhibición; c) los criterios de elección fueron específicos; d) describe una medida de la severidad de la condición tratada y al menos una medida diferente del resultado clave al inicio; e) especifica el o los organismos sobre los que actúa; f) menciona la concentración óptima inhibitoria antimicrobiana, y g) inhibe tres o más microorganismos.
Tabla 2 Escala PEDro empleada para la evaluación de la calidad metodológica de los artículos21
| Artículo | A | B | C | D | E | F | G |
|---|---|---|---|---|---|---|---|
| 17 | No | Sí | Sí | Sí | Sí | Sí | No |
| 16 | No | Sí | Sí | Sí | Sí | Sí | No |
| 14 | No | Sí | Sí | Sí | Sí | No | Sí |
| 12 | No | Sí | Sí | Sí | Sí | Sí | No |
| 18 | Sí | No | Sí | Sí | Sí | Sí | No |
| 13 | No | No | Sí | Sí | Sí | Sí | No |
| 11 | Sí | Sí | Sí | Sí | Sí | Sí | No |
| 15 | No | Sí | Sí | Sí | Sí | Sí | Sí |
A) Número de muestras mayor a la media de 9.6.
B) Realiza comparación entre concentraciones de inhibición.
C) Los criterios de elección fueron específicos.
D) Describe una medida de la severidad de la condición tratada y al menos una medida diferente del resultado clave al inicio.
E) Especifica el o los organismos sobre los que actúa.
F) Menciona la concentración óptima inhibitoria antimicrobiana.
G) Inhibe tres o más microorganismos.
Sin embargo, no todos manejan un número de muestras promedio que demuestren sustento suficiente para proporcionar fiabilidad, únicamente lo cumplen dos de los seleccionados. Por el contrario, sí realizan un análisis y comparación entre las concentraciones empleadas para llegar a una CMI, a excepción de dos artículos, uno de ellos no especifica una CMI en sus resultados, inclusive entre los artículos se emplearon distintas técnicas para evaluar la CMI. De igual manera pocos son los artículos que comparan la capacidad antimicrobiana de más de tres microorganismos, son solo dos que así lo muestran en sus resultados, el resto maneja de uno a dos (Tabla 2).
Discusión
En las distintas ramas de la odontología, las propiedades antimicrobianas, en los diferentes materiales empleados, resulta muy relevante y por ello, se ha investigado durante años, con el fin de desarrollar materiales con mejores propiedades. Una herramienta empleada para ello es la adición variada de Nps; sin embargo, existe una extensa discusión acerca de cuál es la mejor.
Los autores Totu et al.13, Alrahlah et al.16 y Abdulrazzaq et al.20 fabricaron nanocompositos de PMMA/NpsTiO2 a diferentes CMI de dióxido de titanio (TiO2), con el objetivo de utilizar como base de dentadura, en sus estudios se realiza una evaluación de la actividad antibacteriana de estos compositos (tabla 1). Totu et al. evaluaron estos compositos contra C. scotti, los tres compositos preparados a 0.4%, 1% y 2.5% de NpsTiO2 inhiben el crecimiento bacteriano, aunque al finalizar no cuantifica el nivel de inhibición13. Por el contrario, Alrahlah et al. evaluaron compositos de PMMA/NpsTiO2 con concentraciones de 1% y 3% de NpsTiO2 contra E. faecalis y P. aeruginosa, resultando una inhibición del 92%16. Los autores anteriores además de evaluar la actividad antibacteriana, también realizaron estudios de caracterización fisicoquímica y pruebas de resistencia en dentaduras moldeadas de estos materiales, donde determinaron que con buena distribución en PMMA y en pequeñas concentraciones las NpsTiO2 pueden ayudar a mejorar las características mecánicas de los compositos de PMMA/NpsTiO2, además ambos autores coinciden en que el efecto antibacteriano se potencializa al irradiar bajo luz ultravioleta.
Sodagar et al.15 y Abdulrazzaq et. al.20, de igual forma, sintetizaron compositos de PMMA/NpsTiO2, ambos evaluaron contra bacterias criogénicas. Sodagar et. al. emplearon tanto NpsTiO2 como NpsSiO2 a 1% contra L. acidophilus y S. mutans, mostrando resultados de 93% y 92%15. Por su lado, Abdulrazzaq et al.20 sintetizaron dos compositos de PMMA/NpsTiO2 a 2.5% y 5% de nanotubos de dióxido de titanio mediante síntesis hidrotermal y los evaluó contra tres cepas microbianas que incluyen C. albicans, L. acidophilus y S. mutans y de igual forma lo realizó bajo la presencia de radiación ultravioleta Se presenta una disminución de biofilm bacteriano en la resina acrílica del composito PMMA/NpsTiO2, comportamiento que, de igual forma que los autores anteriores concluyen, se intensifica al irradiar bajo luz ultravioleta.
Lo anterior nos sugiere que las NpsTiO2 a concentraciones menores del 3%, tienen buena actividad antimicrobiana contra L. acidophilus, S. mutans, C. albicans, E. faecalis, P. aeruginosa y C. scotti, y que esta actividad antimicrobiana se potencializa al utilizar radiación UV, además de que los compositos de PMMA/NpsTiO2 a concentraciones debajo del 3% conservan, e incluso mejoran, sus propiedades mecánicas y de resistencia, y se observa sobre estos materiales una reducción de película criogénica.
Con respecto a los compositos de PMMA/NpsAg, las Nps de plata fueron probadas en una concentración de 3.5% contra C. albicans y mostraron un intervalo de inhibición en superficie de 94% ± 99%14. Cabe señalar que la preparación de compositos ternarios por ejemplo PMMA/NpsAg/GO (con grafeno), es una alternativa viable para conducir a materiales cuyas propiedades puedan ser mejoradas o incrementadas, en este caso dichos compositos se evaluaron contra S. aureus, S. mutans y E. coli, al evaluarse al 2% se observó mejor actividad antibacteriana contra S. aureus y S. mutans que contra E. coli, con respecto a los halos de inhibición mostrados18. En cambio, al evaluar las NpsMAg a 3.9µ/Ml, estas mostraron 99% de efectividad contra S. mutans19.
Las distintas concentraciones y composición nos muestran que las Nps de plata solas son capaces de decrecer significativamente los niveles presentes de C.albicans en la superficie del PMMA. Pero al combinarse con otros materiales (compositos), se incrementan considerablemente las propiedades antimicrobianas de estos nuevos materiales.
Por otra parte, encontramos que el uso de Nps de platino en discos de acrílico al 0.1% sobre S. mutans y S. sobrinus redujo considerablemente la adhesión microbiana, a 88.9% y 88.2% respectivamente17. La bacteria Gram-positiva S. mutans es objeto de estudio en numerosas investigaciones, pero no en todas es tratada con los mismos agentes, por lo que se llega a distintas conclusiones.
Los compositos de PMMA/NpsPt en general muestran un buen porcentaje de inhibición: 88.9%; pero, en comparación con NpsMAg, estas últimas muestran una diferencia significativa de inhibición del 99%17,19. En comparación con los compositos de PMMA/NpsTiO2 y SiO2, la inhibición es del 92%, por lo que el uso de las NpsPt no deja de ser relevante.
Conclusiones
Los compositos de PMMA/Nps y PMMA/NpsAg/GO demostraron poseer un efecto antimicrobiano con uno o más microorganismos. Las diferentes Nps son incorporadas al PMMA, un material dental imprescindible para la fabricación de prótesis dentales. Las Nps están siendo investigadas ampliamente en los últimos años debido a las ventajas que han sido comprobadas con el fin de desarrollar biomateriales compuestos con propiedades mejoradas, para su aplicación odontológica.
En general la concentración de Nps en la fabricación de compositos de PMMA, juega un papel importante en las características del material; a bajas concentraciones (3%) de NpsAg PMMA/NpsTiO2 o PMMA/NpsPt, los compositos tienden a conservar las propiedades mecánicas y de resistencia necesarias para su utilización en prótesis dentales. A concentraciones menores al 3% los compositos muestran inhibición en la actividad antimicrobiana, principalmente los que contienen PMMA/NpsAg, y más aún cuando estas son biogénicas. Posteriormente las PMMA/NpsTiO2 mostraron un porcentaje de inhibición en la actividad microbiana muy parecida a las NpsAg. Las NpsTiO2 son de las que se tienen más reportes y en las que se ha observado un rango más amplio de inhibición de bacterias, y por último se encuentran las de platino que, aunque muestran un menor el porcentaje de inhibición, no deja de ser relevante, pues esto se consigue con la concentración mínima inhibitoria más baja. Cabe señalar que la radiación de luz ultravioleta beneficia el efecto antimicrobiano en los compositos PMMA/Nps. No en todos los artículos presentados se muestra el porcentaje de inhibición, pero si se presenta el de concentración mínima inhibitoria para la reducción de estos microorganismos.
Es por ello que, al comparar las propiedades antimicrobianas de los compositos PMMA/Nps, las Nps que presentan mejores propiedades antimicrobianas son las de plata, más aún cuando son biogénicas; sin embargo, aún no se investiga su efectividad con un número más amplio de microorganismos. En general los compositos de PMMA/NpsAg, PMMA/NpsTiO2 o PMMA/NpsPt aseguran una disminución efectiva de biofilm en prótesis dentales hechas de PMMA, y con ello estos biomateriales ayudarían a la prevención de patologías estomatológicas, sin efectos citotóxicos, siempre y cuando sean utilizados a concentraciones bajas para conservar o mejorar las propiedades mecánicas del PMMA.















