Introducción
En México el plátano ”Macho” (Musa balbisiana ABB) se cultiva en una superficie de 19,834.34 ha, distribuidas en las regiones tropicales del país. En dicha superficie se producen 380,902.69 Ton de fruto. Los estados de Chiapas, Veracruz, Oaxaca, Tabasco y Guerrero producen el 89 % de este frutal, siendo Chiapas el principal productor (34 % del total) (SIAP, 2022).
Como cualquier otro cultivo, el plátano “Macho” se ve afectado por una serie de problemas fitosanitarios causados por bacterias como el Moko del plátano (Ralstonia solanacearum), virus estriado del plátano (Banana streak virus), nematodo barrenador (Radopholus similis) y hongos como la Sigatoka Negra (Mycosphaerella fijiensis Morelet), que afectan la producción (Javer et al., 2009; Manzo-Sánchez et al., 2017; Susan et al., 2017).
La Sigatoka Negra (SN) es una enfermedad que ataca a todas las especies del género Musa y representa el mayor riesgo para la producción debido a que disminuye la capacidad fotosintética de las plantas. El hongo de la SN se reproduce tanto de forma sexual como asexual (Guzmán et al., 2013), por lo que su diseminación se realiza por tres vías: 1. Material vegetal infectado (hojas enfermas, retoños infectados); 2. Dispersión de ascosporas (reproducción sexual); 3. Dispersión de conidios (reproducción asexual). Los conidios se propagan a cortas distancias en la misma planta o en plantas vecinas; las ascosporas pueden recorrer con el viento cientos de kilómetros (Rodríguez y Cayón, 2008).
El control convencional de la SN alterna el uso de fungicidas protectantes (Mancozeb, que pertenece al grupo de los ditiocarbamatos), como sistémicos (benzimidazoles, que son un grupo de compuestos químicos orgánicos aromáticos heterocíclicos), aplicados en aceite o en emulsión de agua. Sin embargo, la constante presión a la que ha sido sometida la población de M. fijiensis, por la aplicación de los fungicidas químicos, ha derivado en la selección de cepas resistentes a dichas moléculas motivando, con ello, al aumento de la frecuencia de su aplicación (Adriano-Anaya et al., 2018) con el consecuente impacto negativo en la salud del ecosistema y de los humanos (Mena-Espino y Couoh-Uicab, 2015). El impacto económico de la SN es tal que se han llegado a reportar pérdidas entre el 50 y el 100 % de la producción si no se hace un adecuado control de la enfermedad, rubro que puede representar entre el 35 y 48 % de los costos totales de producción de banano y que en México ha significado una inversión anual entre 40 y 50 millones de dólares para controlar la enfermedad (Orozco-Santos et al., 2013). Desde luego que esto ha implicado además un impacto ambiental importante, pues se realizan anualmente en promedio 52 aspersiones aéreas semanales de fungicidas químicos sobre las plantaciones, las cuales han generado contaminación de suelo y cuerpos de agua con los subproductos zinc y metilentioureas provenientes de la degradación del mancozeb (Geissen et al., 2010).
El interés por conservar el ambiente ha llevado a la búsqueda de alternativas biológicas para el control de la SN. Las bacterias del género Bacillus han mostrado potencial para el control de la SN ya que posee capacidad tanto para colonizar la superficie foliar y formar estructuras de resistencia (esporas) que ayudan a sobrevivir a condiciones ambientales adversas, como para producir diversos antibióticos y enzimas, que hidrolizan los componentes de la pared de las ascosporas de M. fijiensis (Patiño et al., 2007; Sánchez, 2016; García et al., 2022; Cruz-Martín et al., 2023). La eficiencia de control de la SN con diferentes cepas de Bacillus, se encuentra entre 25 % - 33.6 % (Castillo-Arévalo, 2022; Cruz-Martín et al., 2018; Gutiérrez-Monsalve et al., 2015). Alternativamente extractos de diversas plantas han mostrado potencial para el control de la SN. En este sentido, los extractos de Cinnamomum zeylanicum (canela), Capsicum annuum (chile) y Azadirachta indica (neem) controlaron la SN en 67.5 % (Kumakech et al., 2022). Por su parte Morales et al. (2011) obtuvieron un promedio de 48 % de control de la SN con extractos de cundeamor (Momordica charantia L.), salvia (Salvia officinalis L.) y caña santa (Cymbopogon citratus (DC.), mientras que Ewané et al. (2020) reportaron 44 % con extracto de girasol mexicano (Tithonia diversifolia) y Adriano-Anaya et al. (2023) 35 % con la mezcla de extractos de clavo (Sysygium aromaticum) y ajo (Allium sativum).
El control biológico de la SN ha sido realizado con aplicaciones independientes de microorganismos o de extractos de plantas asperjados sobre las hojas de las Musa y escaso es el trabajo reportado donde el control de la enfermedad se realice con la aplicación del microorganismo biocontrolador en el sistema vascular de la planta. Por lo anterior el objetivo de este trabajo fue determinar el efecto de aplicar Bacillus subtilis ANT01 en el sistema vascular de plantas de plátano “Macho” sobre la severidad de la Sigatoka Negra.
Materiales y métodos
Sitio de trabajo
El trabajo fue realizado en la Estancia Agroecológica “Ayol” del Municipio de Tapachula Chiapas; México (14°49’46” N; 92°17’42” O; 69 msnm; precipitación pluvial promedio 2,600 mm; humedad relativa 80 %; temperatura promedio anual de 26°C).
Material vegetal y sistema de siembra
Como material vegetal fueron utilizados hijuelos de plátano “Macho” de 1.0 m de altura y sin síntomas de SN, sembrados con distanciamiento entre planta y entre surco de 3.0 m (1100 plantas ha-1).
Tamaño del tratamiento
Cada uno de los tratamientos empleados (Tabla 1) estuvo constituido por 20 plantas distribuidas en dos surcos de 30 m de longitud.
Tabla 1 Diseño de tratamientos para determinar el efecto de la aplicación de Bacillus subtilis ANT01 en el sistema vascular del plátano “Macho” para el control de la Sigatoka Negra.
Table 1: Treatments design to assess the effect of the injection of Bacillus subtilis ANT01 into the vascular system of plantain “Macho” to control the Black Sigatoka.
| Tratamiento | Frecuencia de aplicación (días) |
| 1 (Control) | Aspersión foliar de extracto de clavo y ajo cada 14 días |
| 2 | Aspersión foliar de extracto de clavo y ajo cada 14 días + aplicación de B. subtilis ANT01 cada 7días |
| 3 | Aspersión foliar de extracto de clavo y ajo cada 14 días + aplicación de B. subtilis ANT01 cada 14 días |
Biocontroladores, concentración y forma de aplicación
Como biocontroladores de la SN fueron utilizados extracto alcohólico de ajo (Allium sativum; 150 µg sólidos disueltos mL-1), extracto alcohólico de clavo (Zysygium aromaticum; 72 µg sólidos disueltos mL-1) (Adriano-Anaya et al., 2018) y Bacillus subtilis ANT01 con 108 UFC mL-1. Los extractos de ajo y clavo fueron mezclados en una aspersora manual de 20 L y fueron asperjados sobre el haz y el envés de las hojas hasta punto de goteo. B. subtilis ANT01 fue inoculado, 10 - 20 mL dependiendo de la fase de desarrollo de la planta, directamente en el sistema vascular de la planta, a distancia de 20 cm del nivel del suelo.
Variables determinadas
Severidad de la Sigatoka Negra (SSN). La SSN en cada una de las hojas de todas las plantas, fue determinada cada 14 días mediante la escala de Stover modificado por Gauhl (Stover, 1971; Gauhl, 1990), la cual esta constituía por siete grados, donde; 0 = hojas sanas o libres de síntomas de SN, 1 = hojas con < 10 manchas, 2 = hojas con < 5 % de área enferma, 3 = hojas con enfermedad en 6 % - 15 % del área, 4 = hojas con enfermedad en 16 % - 33 % del área, 5 = hojas con enfermedad en 34 % - 50 % del área y 6 = hojas con enfermedad en > 50 % del área. La SSN en cada planta o tratamiento fue determinada mediante la fórmula (1) usada por Gutiérrez-Monsalve et al. (2015):
SN = ∑ (Número de hojas enfermas por cada grado de la escala) [ (Número total de hojas observadas)-1 (grado mayor de la escala) ]-1
La determinación de la SSN inició a partir de la 4ª semana después de la siembra de las plantas.
Cantidad de hojas sanas y hoja más joven con síntomas de Sigatoka Negra. La cantidad de hojas sanas y la hoja más joven con síntomas de SN fueron cuantificadas cada 14 d, durante la etapa vegetativa de todas las plantas a partir de la 4ª semana después de la siembra de las plantas.
Parámetros de producción. Los parámetros de producción fueron: peso del racimo (kg), número de “manos” por racimo y tiempo de maduración del fruto (semanas), dichos parámetros fueron cuantificados en 10 plantas de cada uno de los tratamientos.
Resultados y discusion
La etapa vegetativa de las plantas de plátano “Macho” tuvo una duración promedio de 266 días después de iniciado los tratamientos. En dicha etapa la dinámica de la SSN, en los diferentes tratamientos de este trabajo mostró tres fases (Figura 1): la primera fase de incremento en el valor de la SSN con duración promedio observada de 42 d posterior a la siembra; la segunda fase de disminución de la SSN con duración de 70 días y la tercera fase de estabilización de la SSN con duración de 154 d.
Figura 1 Dinámica de la severidad de la Sigatoka Negra en plantas de plátano “Macho” sometidos a diversos tratamientos de biocontrol. STn = Severidad en las plantas del Tratamiento n como fueron descritos en el Cuadro 1. Las barras indican el error estándar.
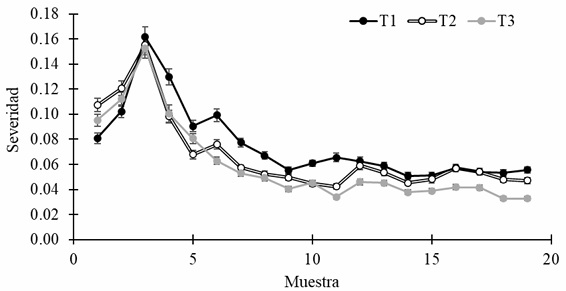
Figure 1: Black Sigatoka severity dynamics in plantain “Macho” subjected to several treatments of biocontrol. STn = severity in plants from treatment n as previously described in Table 1. Bars indicate standard errors.
Al inicio del trabajo la SSN en las plantas de todos los tratamientos tuvo un valor promedio de 0.0945 ± 0.0133 alcanzando, en el muestreo tres, un valor promedio de 0.1564 ± 0.0047 (+ 65.5 %). Después de alcanzar el mayor valor, la SSN descendió en todos los tratamientos hasta un valor promedio de 0.0562 ± 0.0096 en la muestra ocho. A partir del muestreo ocho y hasta el muestreo 19 el promedio de la SSN en las plantas de los Tratamientos 1, 2 y 3 fue, respectivamente, de 0.0568 ± 0.0047, 0.0498 ± 0.0053 y 0.0396 ± 0.049, lo que representó reducción del 39.9 %, 47.3 % y 58.1 % respecto a la SSN inicial y de 61.7 %, 68.1 % y 74.7 % respecto al valor máximo. El análisis estadístico de los datos de la tercera fase mostró diferencias significativas entre los tratamientos (Fc = 32.88, FT = 3.32, error = 0.000752, gl = 30) y la prueba de Tukey mostró que los tratamientos fueron diferentes [alfa= 0.05 (DMS = 0.0053, Error = 0.0000251, GL = 39), T1 = 0.0567 a, T2 = 0.0498 b, T3 = 0.0396 c].
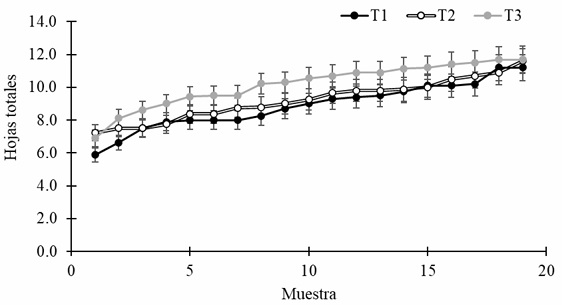
La dinámica de la generación de hojas, durante el periodo de estudio, se muestra en la Figura 2. En dicha figura se observa que al inicio las plantas tuvieron un promedio de 6.7 hojas y que esa cantidad siempre fue en aumento durante toda la fase vegetativa. Al llegar a la etapa reproductiva las plantas de todos los tratamientos presentaron, en promedio, un total de 11.4±0.55 hojas, sin diferencia estadística significativa entre ellas (Fc = 2.70; Ft = 3.35; Error = 43.4; gl = 27).
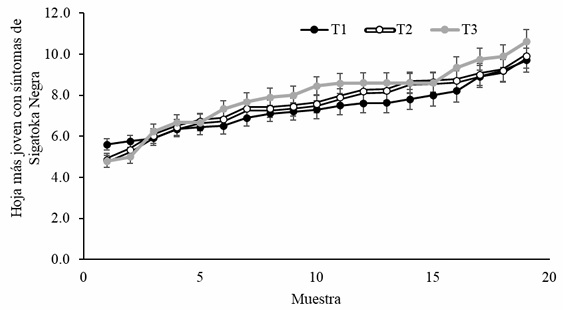
Por otro lado, la dinámica de la hoja más joven con presencia de SSN mostró (Figura 3) un comportamiento paralelo al observado al de hojas totales, es decir, aumentó conforme las plantas alcanzaron la etapa reproductiva. Inicialmente la 5ª hoja fue la más joven con presencia de SSN (promedio de 5.1 ± 0.46) y al final de la etapa vegetativa fue la 10ª hoja (promedio 10.1 ± 0.47) sin diferencia estadística significativa entre los tratamientos (Fc = 2.05, FT = 3.35, gl = 27).
Los parámetros productivos de las plantas de los tratamientos empleados en este trabajo se muestran en la Tabla 2. En el citado cuadro se observa que el plátano “Macho” produce racimos con peso entre 10.1 - 11.9 kg, con número de “manos” entre 4.9-5.9 y con 11.4-11.8 semanas a cosecha. Las diferencias entre los tratamientos no fueron estadísticamente significativas (Peso de racimo: Fc = 2.50, Número de manos: Fc = 3.12, Semanas a cosecha: Fc = 0.10, Ft alfa = 0.05, 2, 27 = 3.35).
Tabla 2 Parámetros productivos de plátano “Macho” sometidos a diferentes tratamientos (Tn) de control de Sigatoka Negra. Tratamientos con la misma letra no son estadísticamente diferentes.
Table 2: Yield parameters of the plantain “Macho” subjected to different treatments (Tn) to control the Black Sigatoka. Treatments with the same letter are not statistically different.
| Tratamiento | Peso del racimo (kg) | Número de "manos" | Semanas a cosecha |
| T 1 | 10.1 ± 1.47 a | 4.9 ± 0.32 a | 10.7 ± 2.00 a |
| T 2 | 10.5 ± 2.26 a | 5.3 ± 0.67 a | 11.7 ± 2.70 a |
| T 3 | 11.9 ± 1.85 a | 5.9 ± 1.37 a | 11.4 ± 1.90 a |
| Promedio | 10.8 ± 0.95 a | 5.4 ± 0.51 a | 11.4 ± 0.50 a |
El control de la SN, con agroquímicos o biológicos, en plátanos y bananos cultivados, generalmente se realiza con la aplicación de una única sustancia o ingrediente activo. Considerando lo previo, en este trabajo se hipotetizó que la adición de otro biocontrolador al programa existente en la Estancia Agroecológica “Ayol”, mejoraría el control de la enfermedad. La reducción de la SSN observada en los tratamientos donde se aplicó B. subtilis ANT01 (Figura 1), además de la aplicación de los extractos de ajo y clavo, puede estar relacionada con la capacidad de producción de moléculas antagónicas producidas por el microorganismo efector (Cruz-Martin et al., 2022) o por la inducción de mayor respuesta defensiva de las plantas derivada de la interacción entre los componentes del sistema sea este microorganismo-planta, metabolito secundario-planta o microorganismo-metabolito secundario-planta (Torres et al., 2009; Pieterse et al., 2014;). En este sentido, el incremento en la SSN observada al inicio de todos los tratamientos (Figura 1), similar a lo reportado por Casas et al. (2021), puede relacionarse con las dos líneas de defensa de la respuesta inmune de la planta: la primera de ellas derivada de la acción de algún metabolito presente en el extracto o el fermento que activaron los genes de virulencia del patógeno haciéndolo más agresivo, o inhibieron los genes de resistencia de la planta, haciendo a la planta más susceptible, ambos componentes de la inmunidad activada por los Patrones Moleculares Asociados a Patógenos (PAMPs), o PTI (Göhre y Robatzek, 2008; Zipfel, 2008, 2009; Castro et al., 2012); y la segunda, derivada de la respuesta de hipersensibilidad de la planta en la cual la muerte celular alrededor del tejido infectado se acelera (el síntoma de la SN es el área foliar necrosada) por la liberación de especies reactivas de oxígeno (ROS), aunado a la activación de las rutas del ácido salicílico, ácido jasmónico y etileno, conocida como Inmunidad Activada por Efectores o ETI. Inicialmente la ETI es una respuesta defensiva local, la cual se transforma en respuesta defensiva sistémicas (Tsuda y Katagiri, 2010).
La disminución en la SSN observada durante la segunda fase de los tratamientos (Figura 1) puede estar relacionada al aumento de capacidad defensiva de las plantas desencadenada por el estímulo de inductores químicos (extractos de plantas) y biológicos (fermentos de B. subtilis) tipificada como Resistencia Sistémica Inducida o SAR (Choudhary et al., 2007; Choudhary y Johri, 2009; Pieterse et al., 2014), la cual puede prever la presencia de nuevos sitios de infección, lo que aunado a la emergencia de nuevas hojas tiene como resulta una menor proporción de tejido infectado y por consecuencia menor grado de SSN.
La actividad antifúngica del fermentado de B. subtilis ANT01 puede observarse tanto en el nivel de disminución de la SSN durante la segunda fase, como en nivel de control alcanzado en la etapa de cuasi-estabilización (Figura 1). Sin embargo, la aparente contradictorio de esta última fase, es decir alcanzar mayor reducción de la SSN en el tratamiento con menor frecuencia de aplicación de B. subtilis ANT01 (T3), pudiera ser explicado como un efecto de “toxicidad” derivado de la acumulación de metabolitos cuando la aplicación se realiza cada siete días, un efecto observado también cuando los extractos de plantas son aplicados con esa misma frecuencia (datos no mostrados).
Aunque la estimación de la SSN es realizada mediante la escala propuesta por Stover modificado por Gauhl (Stover, 1971; Gauhl, 1990), el reporte del valor de severidad es resultado de la aplicación de diversas fórmulas propuestas para tal caso. En este sentido los valores de SSN calculados en este trabajo para el mejor tratamiento (T3) fue, en promedio, 12.20 veces menor que lo reportado por Sierra et al. (2014) para el clon AAB Enano Guantanamero cultivado con diferentes estrategias de control de SN, 8.49 veces menor que lo reportado por Castillo-Arévalo (2022) quien empleó Trichoderma sp y Bacillus subtilis y 3.62 veces menor que lo reportado por Barrera et al. (2016) para el plátano Hartón cultivado bajo diferentes niveles de sombreado, Así mismo empleando el Promedio Ponderado de Infección (PPI) calculado en este trabajo (0.345) fue 5.86 veces menor que el reportado por Quevedo et al. (2018) el cual fue de 2.02 empleando diferentes fungicidas protectantes y sistémicos. La mayor eficacia para el control de la SN observada en este trabajo puede ser resultado de la frecuencia de aplicación de los biocontroladores combinada con los distintos abonos empleados para fertilizar el suelo, los cuales probablemente mejoraron el sistema inmune de las plantas.
Por otro lado, el promedio de hojas totales (Figura 2) observado en las plantas de todos los tratamientos de este trabajo, se encontró dentro del rango reportado por distintos autores: 12.7 (Quevedo et al., 2018), 11.7 (Barrera et al., 2016), 10.0-12.0 (Grajales, 2016), 8.8-12.1 (Sierra et al., 2014), 12.0 (Castellanos et al., 2009), 11.4 (Hernández et al., 2007), los cuales generalmente emplean fertilización química del suelo, por lo cual se puede sugerir que la cantidad y frecuencia de los distintos abonos empleados en el presente trabajo fue adecuado para nutrir las plantas.
Por su parte la HMJE, promedio, observada en este trabajo (Figura 3) fue similar a lo reportado por Barrera et al. (2016) y, ambos casos, mejor que lo reportado por Sierra et al. (2014) y Castellanos et al. (2009) quienes reportaron a las hojas 5.1 y 1.8, respectivamente. Aunque el reporte de Barrera et al. (2016) no indica el empleo de algún fungicida químico o biológico la presencia de SN en las hojas más avanzadas pudiera ser resultado de una probable función de “escudo protector“ de la malla sombra empleada que evitó que las esporas del patógeno arribaran a la superficie de las hojas; o que en realidad si se empleó fungicida en el proceso y no se reportó. El encontrar síntomas de SN en hojas jóvenes en los trabajos de Sierra et al. (2014) y Castellanos et al. (2009) quienes utilizaron fungicidas químicos y biológicos en diversas combinaciones, puede ser un indicativo de que las moléculas contenidas en extractos y fermentados empleados en este trabajo tienen alta potencia para controlar al patógeno, o que la variante de M. fijiensis circulante en la región donde se realizó el trabajo es altamente susceptible a dichas moléculas.
El peso de los racimos cosechados de las plantas empleadas en este trabajo (Cuadro 2) está dentro del rango (6.6 - 14.9 kg) reportado por Cedeño et al. (2020), Barrera et al. (2016), Grajales (2016) y Hernández et al. (2007). Sin embargo, el número de manos por racimo fue 26.8 % menor a lo reportado por Hernández et al. (2007), dicha diferencia puede ser resultado de la variedad de plátano empleada.
Finalmente, desde la perspectiva del tiempo desde la siembra hasta la cosecha de las plantas de plátano “Macho” de este trabajo, pasando por la etapa de florecimiento, se pude decir que la duración de dichas etapas fenológicas estuvo dentro de los parámetros reportados para otras variedades de plátanos (Marcelino et al., 2010; Grajales, 2016; Cedeño et al., 2020).
Conclusiones
Al aplicar cada 14 días Bacillus subtilis ANT01 (108 UFC mL-1) en el sistema vascular de plantas de plátano “Macho” se disminuye 58.1 % la severidad de la Sigatoka Negra, con respecto a solamente asperjar vía foliar los extractos de clavo y ajo. Sin embargo, la inyección de la bacteria no afectó el número total de hojas por planta, la hoja mas joven con síntomas, el peso del racimo, número de manos ni las semanas a cosecha.
Este resultado podría ofrecer una alternativa práctica para su implementación a escala comercial, sin embargo más investigación es requerida principalmente en plantaciones comerciales para validar esta posible recomendación, además de hacer un análisis de costo-beneficio ad-hoc.