Introducción
En las últimas décadas, el avance de las técnicas percutáneas ha permitido ofrecer estrategias de tratamiento menos invasivas para disminuir la morbilidad en los pacientes con cardiopatías congénitas. En enfermos con cardiopatías con flujo pulmonar dependiente del conducto, la angioplastia con stent del conducto arterioso en el periodo neonatal se utiliza como puente a la cirugía reparadora definitiva. Por otro lado, en los pacientes con fisiología univentricular que requieren una fuente de flujo pulmonar estable y controlado, a los que clásicamente se les realizaba una anastomosis sistémico-pulmonar, la angioplastia ductal con stent es una alternativa como primer estadio de tratamiento hasta el segundo estadio de paliación con una anastomosis cavo-pulmonar (cirugía de Glenn).
Desde una perspectiva histórica, en la década de 1990 surgieron los primeros reportes en animales y neonatos de colocación de un stent en el conducto arterioso como tratamiento de la cianosis en pacientes con flujo pulmonar dependiente del conducto, en los primeros a modo de experimentación y en los segundos en pacientes críticamente enfermos que no reunían condiciones para soportar un procedimiento quirúrgico. A pesar de que los resultados iniciales no fueron del todo satisfactorios, el surgimiento de una alternativa de tratamiento menos invasivo para paliación de la cianosis resultó alentador1,2.
El paso de los años y las mejoras tanto técnicas como de equipamiento permitieron que el procedimiento adquiriera mayor lugar en estos pacientes. El desarrollo de stents coronarios con mayor flexibilidad y menor trombogenicidad fue un factor que contribuyó de manera significativa al avance de esta estrategia. En 2011, la American Heart Association publicó sus guías de indicaciones de cateterismo cardiaco en pacientes pediátricos. En las mismas, la indicación de implante de stent ductal en pacientes con cardiopatías congénitas con una única fuente de flujo pulmonar que requieren de una fuente extra de flujo pulmonar por un periodo corto es de clase IIa con nivel de evidencia B3.
Se han reportado escasas experiencias procedentes de Latinoamérica en la última década. Dos de estos trabajos coinciden en que, si bien la morbilidad fue baja, la mortalidad global fue aproximadamente del 20%4,5.
En países con mayor experiencia con esta estrategia, se comparó con la anastomosis sistémico-pulmonar y se reportaron tasas de mortalidad a corto plazo similares con ambos procedimientos, pero menos complicaciones y estadías en cuidados intensivos en favor de la angioplastia con stent en el conducto arterioso6.
Presentamos el siguiente estudio con el fin de revisar y analizar nuestra experiencia, proyectando trabajos prospectivos.
Método
Se realizó un estudio descriptivo, retrospectivo, de corte transversal, en el cual se incluyeron pacientes menores de 3 meses tratados en el Hospital Garrahan, entre octubre de 2016 y diciembre de 2022, con angioplastia con stent ductal como tratamiento paliativo inicial en cardiopatías congénitas con flujo pulmonar dependiente del conducto. En la base de datos REDCap se volcaron datos demográficos, clínicos, anatómicos y funcionales previos y posteriores a la intervención.
Los resultados del procedimiento se evaluaron describiendo las complicaciones intra- y posprocedimiento. Se consideró exitoso en aquellos casos que no requirieron reintervención por disfunción del stent previo a la cirugía. Se registraron los días de internación tras el procedimiento, los requerimientos de inotrópicos y de asistencia respiratoria mecánica, el requerimiento de diuréticos al alta y la mortalidad previa al procedimiento quirúrgico definitivo (entendido este como segundo estadio de paliación univentricular o cirugía reparadora biventricular). Para evaluar los efectos anatómicos de la implantación del stent ductal se usó el índice de Nakata (a nivel hiliar) al momento de la intervención y previo al procedimiento quirúrgico definitivo. El primero fue medido por angiografía y para el segundo se utilizó la mejor imagen disponible en el siguiente orden: angiografía, angiografía por tomografía computada (angio-TC), resonancia magnética y ecocardiograma.
Se incluyeron variables clínicas previas al procedimiento quirúrgico definitivo. También se revisó si en el acto quirúrgico se realizó plástica de ramas pulmonares.
Las variables discretas se presentan con porcentajes y las variables continuas con sus medianas y sus respectivos intervalos intercuartílicos.
Resultados
Los procedimientos fueron llevados a cabo en el servicio de hemodinamia del Hospital Garrahan, formado por cuatro hemodinamistas con años de experiencia en el tratamiento de cardiopatías congénitas de pacientes recién nacidos. La distribución de los casos fue similar entre estos. Todos los pacientes fueron planteados para el procedimiento luego de realizar el diagnóstico inicial con ecocardiograma. En algunos casos fue necesario realizar angio-TC con contraste para definir adecuadamente la morfología del conducto, y en unos pocos casos el cateterismo diagnóstico inicial se utilizó para plantear la posibilidad de implantar un stent ductal. En la actualidad se encuentra protocolizada la realización de angio-TC en aquellos pacientes en quienes se plantee la colocación de un stent en el conducto arterioso para definir con mayor certeza la morfología ductal. En los casos que correspondía se suspendió el goteo de prostaglandinas 12 horas antes para favorecer la constricción pulmonar. Para el procedimiento, todos los pacientes requirieron anestesia general con asistencia respiratoria mecánica. En la mayoría de los casos el acceso vascular utilizado fue tanto arterial como venoso, y los introductores oscilaron entre 3 y 5 Fr. En cuatro pacientes el acceso arterial fue carotídeo por el origen del conducto arterioso desde el tronco braquiocefálico. Se utilizaron stents coronarios no farmacológicos con diámetros entre 3.5 y 4.5 mm y de longitud variable. En siete casos fue necesario el implante de dos stents para mantener la permeabilidad del conducto arterioso (Figs. 1 y 2). Al finalizar el procedimiento se efectuó angiografía de control para certificar el buen funcionamiento del stent y su permeabilidad, y luego, con una saturación acorde al modelo hemodinámico, se finalizó el procedimiento y los pacientes pasaron a la unidad de cuidados intensivos (Fig. 3). Posterior al procedimiento se encuentra protocolizado mantener anticoagulación con heparina por 48 horas y luego iniciar antiagregación con ácido acetilsalicílico.
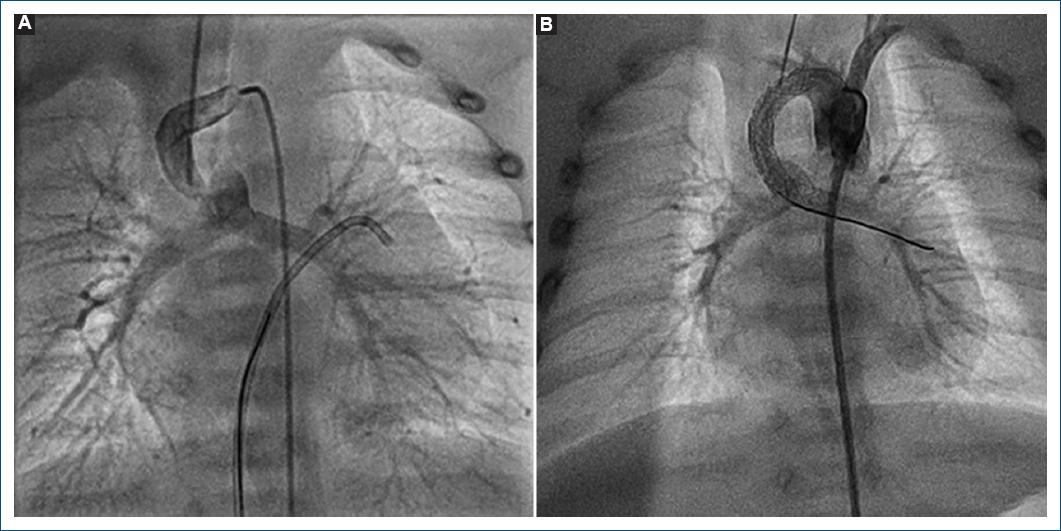
Figura 1 A: angiografía que evidencia el origen del conducto arterioso en el tronco braquiocefálico derecho en un paciente con ventrículo único con atresia pulmonar con arco aórtico izquierdo. B: angiografía tras la angioplastia con colocación de dos stents.
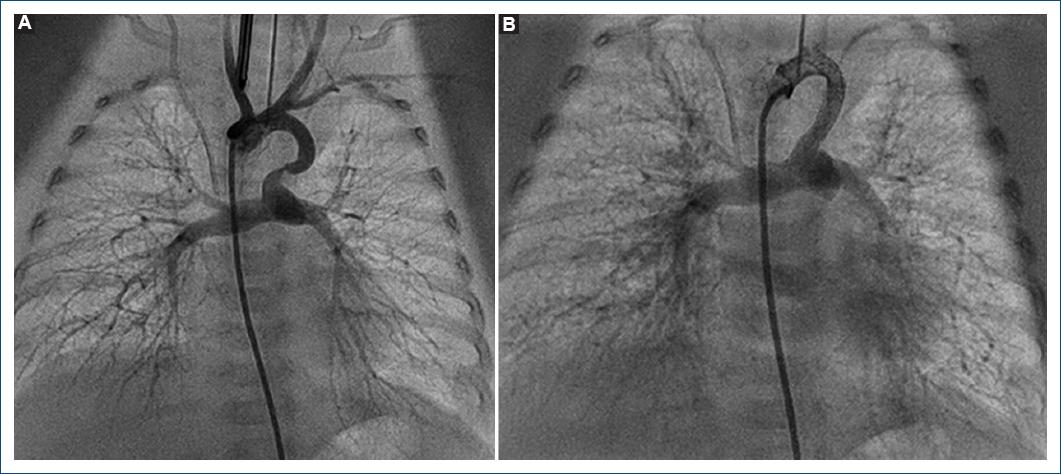
Figura 2 A: angiografía que evidencia origen del conducto arterioso en el tronco braquiocefálico izquierdo en un paciente con tetralogía de Fallot y arco aórtico derecho. Se evidencia algo de tortuosidad y constricción en el tercio proximal a la arteria pulmonar. B: angiografía tras la angioplastia con colocación de dos stents.
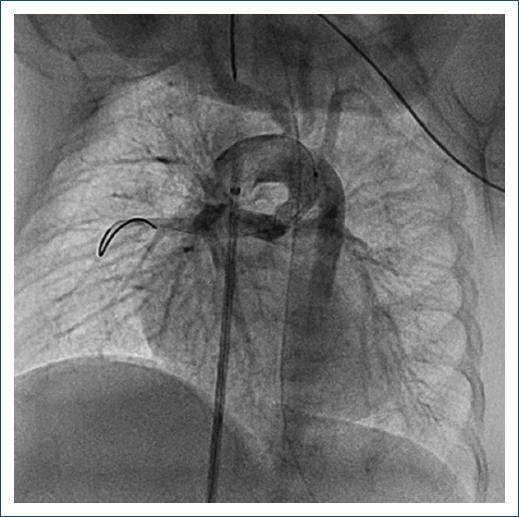
Figura 3 Angiografía tras la angioplastia con un stent en un conducto arterioso originado en el arco transverso en un paciente con atresia pulmonar con comunicación interventricular.
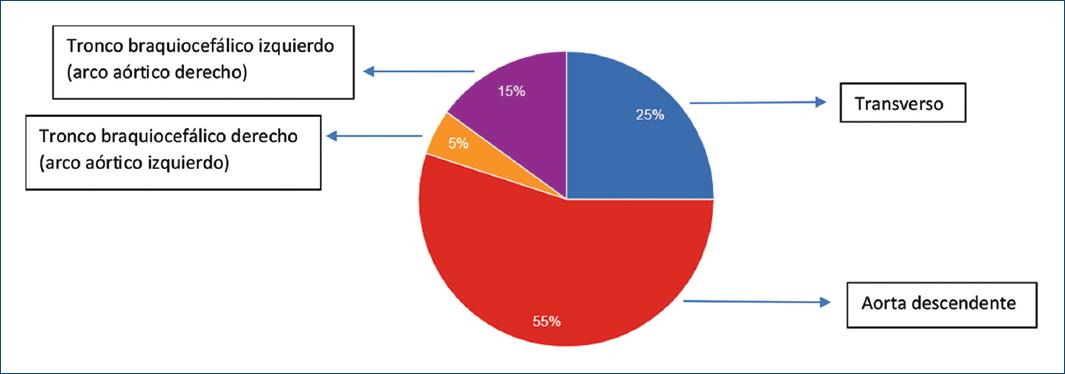
Se incluyeron en el estudio 20 pacientes. Las características basales previas al procedimiento, tanto clínicas como anatómicas, se describen en la tabla 1. En cuanto a la morfología ductal, el 35% correspondían a morfología tortuosa y el 65% a conductos rectos. En la figura 5 se describen los distintos orígenes del conducto arterioso, que se ejemplifican en las figuras 1 a 4. En la tabla 2 se destacan las características de los pacientes al momento del procedimiento.
Tabla 1 Características basales del grupo analizado
| n | Porcentaje o mediana (IC 25-75) | |
|---|---|---|
| Pacientes con angioplastia con stent ductal | 20 | |
| Diagnóstico prenatal de cardiopatía | 10 | 50% |
| Cardiopatía congénita | ||
| APSI | 7 | 35% |
| AP con CIV | 6 | 30% |
| VU + EP o AP | 4 | 20% |
| Tetralogía de Fallot | 2 | 10% |
| Anomalía de Ebstein con AP | 1 | 5% |
| Edad gestacional, semanas | 20 | 38 (37.7-39.2) |
| Peso al nacimiento, kg | 20 | 3.15 (2.48-3.36) |
| Síndrome genético | 4 | 20% |
| Comorbilidad (shock, arritmia, dificultad respiratoria) | 9 | 47.4% |
| Flujo pulmonar dependiente exclusivamente del conducto arterioso | 13 | 65% |
| PG previo al procedimiento | 18 | 90% |
| Días de PG | 18 | 14.5 (9.2-19) |
| Asistencia respiratoria mecánica previo al procedimiento | 10 | 50% |
| Inotrópicos previo al procedimiento | 6 | 30% |
| Función ventricular conservada | 19 | 95% |
| Función de válvula AV sistémica conservada | 18 | 90% |
AP: atresia pulmonar; APSI: atresia pulmonar con septum íntegro; AV: aurículo ventricular; CIV: comunicación interventricular; EP: estenosis pulmonar; IC: rango intercuartílico; PG: prostaglandinas; VU: ventrículo único.
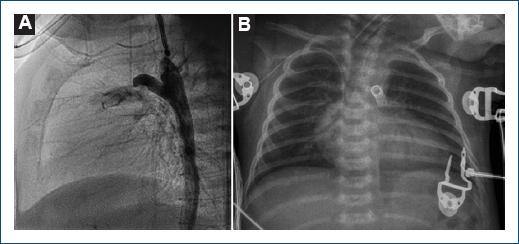
Figura 4 A: angiografía en un paciente con anomalía de Ebstein con atresia pulmonar que evidencia un conducto arterioso con origen en la aorta descendente. B: radiografía de tórax de control que evidencia cardiomegalia a expensas de la aurícula derecha, arco pulmonar excavado y punta elevada con normal posicionamiento del stents ductal.
Tabla 2 Características de los pacientes al momento de la intervención
| n | Porcentaje o mediana (IC 25-75) | |
|---|---|---|
| Días de vida | 20 | 20 (13-32) |
| Peso, kg | 20 | 3 (2.1-4)* |
| Saturación | 20 | 80 (72-85) |
| Índice de Nakata inicial | 20 | 167 (140-193) |
| Complicaciones intraprocedimiento | 2 | 10% |
*Se muestra el rango, y no el IC 25-75, para informar que el procedimiento se llevó a cabo en pacientes de bajo peso. IC: rango intercuartílico.
Durante el procedimiento se registraron dos complicaciones, una migración y una trombosis, que se resolvieron satisfactoriamente, con egreso de la sala de hemodinamia de la totalidad de los pacientes.
Posterior al procedimiento, dos pacientes presentaron disfunción del stent (uno por migración y otro por trombosis), que fue resuelta por cirugía a los 6 y 8 días, realizándose en un caso la colocación de un tubo del ventrículo derecho a la arteria pulmonar y en el segundo caso cirugía reparadora, ya que se revaloró al paciente con condiciones para la misma.
Egresaron 19 pacientes (95%) de la institución, la mayoría (79%) con requerimiento de diuréticos. Fallecieron luego del procedimiento tres pacientes, todos con diagnóstico de atresia pulmonar con tabique íntegro, en ningún caso en relación directa con el procedimiento. En la tabla 3 se presentan todas las variables analizadas luego del procedimiento.
Tabla 3 Variables analizadas luego del procedimiento
| n | Porcentaje o mediana (IC 25-75) | |
|---|---|---|
| Asistencia respiratoria mecánica, días | 16 | 4 (1-12.8) |
| Inotrópicos, días | 11 | 5 (1.5-11) |
| Días desde la intervención hasta el alta | 19 | 22 (12.5-43.5) |
| Edad al egreso hospitalario, días de vida | 19 | 41 (29.5-93) |
| Requerimiento de diuréticos | 15 | 79% |
| Reintervención por disfunción del stent | 2 | 10% |
| Días desde la intervención hasta la reintervención | 2 | 7 (6-8) |
| Muertes | 3 | 15% |
| Edad al momento de la muerte, días | 3 | 66 (26-142) |
IC: rango intercuartílico.
Se analizaron 17 pacientes con posibilidades de una cirugía definitiva. En seis se realizó anastomosis cavo-pulmonar (cirugía de Glenn) y en nueve cirugía reparadora biventricular. En dos pacientes, la cirugía se encuentra planificada. En cinco pacientes se realizó plástica de ramas pulmonares. En la tabla 4 se detallan las características de los pacientes al momento de la cirugía definitiva.
Tabla 4 Características al momento de la cirugía definitiva
| n | Porcentaje o mediana (IC 25-75) | |
|---|---|---|
| Cirugía definitiva | 17 | 85% |
| Cirugía planificada | 2 | 10% |
| Peso al momento de la cirugía definitiva, kg | 17 | 6.3 (5.6-7.6) |
| Saturación al aire ambiente | 17 | 80 (78.5-85.2) |
| Índice de Nakata, mm/m² | 15 | 180 (153-226.5) |
| Días desde la angioplastia con stent hasta la cirugía definitiva | 16 | 172 (95.7-288.7) |
| Edad al momento de la cirugía definitiva, meses | 16 | 6.8 (3.8-10.2) |
IC: rango intercuartílico.
Discusión
La experiencia en la angioplastia con stent ductal se ha expandido durante las últimas dos décadas y se evidencia en las publicaciones que han aparecido en dicho periodo en la literatura internacional. Los tiempos de intervención y las complicaciones en el procedimiento han ido descendiendo. Por otro lado, la complejidad de los casos, tanto por la morfología ductal como por el tipo de cardiopatías de los pacientes seleccionados, ha aumentado. Esto refleja las mejoras tecnológicas y la adquisición de mayor experiencia de los médicos hemodinamistas en esta técnica7,8.
Tanto en los registros internacionales como en nuestra presentación, la mayoría de los pacientes tenían diagnóstico de atresia pulmonar con septum íntegro (APSI) o de atresia pulmonar con comunicación interventricular. Dentro de las características iniciales destacamos que un gran porcentaje de nuestra población presentó alguna comorbilidad previa al procedimiento, como se pone de manifiesto por los requerimientos de inotrópicos y de asistencia respiratoria mecánica. El resto de las características iniciales son comparables a las de una experiencia multicéntrica de referencia de los Estados Unidos de América9.
Todos los pacientes intervenidos egresaron de la sala de hemodinamia. Solo dos pacientes (10%) requirieron reintervención posterior por disfunción del stent, resultado que consideramos muy favorable para esta estrategia teniendo en cuenta que en centros con mayor experiencia se reporta una necesidad de reintervención de aproximadamente el 25% de los pacientes. Consideramos al procedimiento exitoso en un 75% de los pacientes que lograron arribar al segundo estadio sin requerimiento de reintervención o sin muerte. Esta tasa de éxito se acerca a las presentadas por los equipos de hemodinamia de centros de referencia. Dos factores que consideramos que aumentaron la complejidad técnica para el grupo analizado son el peso al momento del procedimiento y la morfología del conducto arterioso. En el primer caso destaca que seis pacientes tenían un peso ≤ 2.5 kg. El segundo factor a considerar es la tortuosidad del conducto arterioso, que se evidenció en aproximadamente un tercio de los pacientes; si bien en los primeros reportes fue considerado como un factor limitante para ofrecer el tratamiento, en la actualidad se toleran mayores grados de tortuosidad, ya que en manos experimentadas se puede lograr una adecuada alineación del conducto con la colocación del stent. No se registraron complicaciones mayores ni muertes durante el procedimiento. De acuerdo con los resultados presentados en relación al procedimiento en sí, consideramos que la experiencia inicial es satisfactoria6.
El egreso de casi la totalidad de los pacientes y los periodos cortos de requerimientos de inotrópicos y de asistencia respiratoria mecánica son similares a los reflejados en los trabajos con mayor número de pacientes. Si bien esta recuperación y el requerimiento de terapia son alentadores, la estadía institucional fue ligeramente mayor que en las experiencias mencionadas9-11.
La mortalidad global en nuestra población fue del 15% y todos los pacientes fallecidos tenían diagnóstico de APSI. Uno de los casos se presentó con miocardiopatía irreversible del ventrículo izquierdo, otro desarrolló taquiarritmias antes del procedimiento y posteriormente presentó una muerte súbita, y el tercero tenía inestabilidad hemodinámica previa con un cuadro de sepsis de foco enteral y posterior al procedimiento falleció por shock séptico.
Al considerar la saturación de oxígeno al aire ambiente evidenciamos que todos los pacientes, excepto uno que requirió reintervención precoz por trombosis en el interior del stent con consecuentemente caída de la misma, presentaron una saturación acorde a cada caso a corto y mediano plazo. Al momento de la cirugía definitiva observamos que todos los pacientes que se encontraban en condiciones de recibirla presentaban una saturación de oxígeno al aire ambiente dentro de parámetros aceptables para los distintos modelos hemodinámicos.
Otro resultado marcadamente favorable del procedimiento fue el aumento del índice de Nakata. Si bien ya se encuentra demostrado que tanto la angioplastia con stent en el conducto arterioso como la anastomosis sistémico-pulmonar no presentan diferencias en el crecimiento de las ramas cuando se comparan ambas estrategias6, en esta serie vemos que con la implantación del stent en el conducto arterioso las ramas pulmonares crecen adecuadamente a pesar de que un pequeño número de pacientes requirieron plástica en las ramas al momento de la cirugía definitiva. En una proporción mayor de pacientes se logró arribar a una cirugía reparadora biventricular, pero consideramos que esto podría estar condicionado por el hecho de que un mayor número de pacientes con atresia pulmonar con comunicación interventricular llegaron a dicha instancia.
Comparando nuestra serie de casos con las experiencias publicadas de centros de los Estados Unidos de América y de Europa, se evidencian diferencias en la cantidad de pacientes incluidos, pues la mayoría de los trabajos internacionales son multicéntricos. En los dos estudios que incluyeron más pacientes, el centro que realizó la mayor cantidad de implantes de stent ductal reportó resultados de 36 casos10,11.
Conclusiones
En vistas de la expansión de este procedimiento en las últimas décadas y de que la experiencia local que presentamos muestra resultados similares a los de otros hospitales de ámbito internacional, se sostiene en nuestro país esta estrategia como alternativa a la anastomosis quirúrgica buscando disminuir la morbimortalidad en este grupo complejo de pacientes. Por otro lado, se requieren estudios prospectivos que comparen ambas estrategias para poder brindar la mejor opción de tratamiento a nuestra población.