Introducción
El orden Asparagales, dentro de las monocotiledoneas, incluye 14 familias (Amaryllidaceae, Asparagaceae, Asphodelaceae, Asteliaceae, Blandfordiaceae, Boryaceae, Doryanthaceae, Hypoxidaceae, Iridaceae, Ixioliriaceae, Lanariaceae, Orchidaceae, Tecophilaeaceae y Xeronemataceae), 1122 géneros y más de 36,000 especies (APG). Este orden representa la mayor tasa de diversificación de las monocotiledóneas (Magallón and Castillo 2009), con una edad estimada del grupo corona de aproximadamente 125.3 millones de años (Tank et al., 2015) y una gran diversidad en tamaños de genoma desde 0,3 -82,2 pg (Leitch and Leitch 2013). En este orden existen reportes de diversos géneros que presentan un cariotipo bimodal como Aloe, Agave, Camasia, Yucca, Chologalum, Hastingsiana, Hesperocallis, entre otros (Halpin and Fishbein 2013; Robert et al., 2008; McKain et al., 2016).
Aloe L. pertenece a la familia Asphodelaceae que contiene alrededor de 940 especies y una edad aproximada de 45 a 63 millones de años. Aloe L. es conocida como una Lili del desierto, con gran aplicación como planta medicinal (Carter and Royal Botanic Gardens 1994), de la cual se conocen alrededor de 500 especies distribuidas alrededor del mundo, principalmente en zonas tropicales (Carter and Royal Botanic Gardens 1994; Gunjan and Roy 2010). El género presenta una gran diversidad en tamaño y morfología desde árboles que crecen 15 m de altura hasta pequeñas plantas con una roseta de 30 mm y aunque en su mayoría son diploides (2n=14), se han identificado algunas especies tetraploides y una especie hexaploide (Brandham and Doherty 1998).
Las especies analizadas del género Aloe L. en general muestran una estabilidad en el cariotipo bimodal con una estructura básica haploide de un cromosoma grande, submetacéntrico (un brazo del cromosoma es ligeramente mayor que otro), tres cromosomas grandes acrocéntricos (se refiere a cromosomas con el centrómero cercano a un extremo) y tres cromosomas pequeños acrocéntricos (Brandham and Doherty 1998), sin embargo existen reportes de asimetría cariotípica en algunas especies del género (Gunjan and Roy 2010). En contraste con la uniformidad de la estructura básica cromosómica, este género presenta una gran variación en el contenido de ADN 1C desde 10.5 pg en A. tenuori hasta 23.9 pg en A. peckii, (Brandham and Doherty 1998).
Al evaluar la distribución de la posición de los loci 5S y 45S en 13 especies de Aloe, se evidenció una conservación en localización intersticial en cromosomas grandes para 5S, en comparación con diferencias en el número, localización y tamaño de loci encontrado entre las especies analizadas en 45S (Adams et al., 2000) posiblemente originados durante la especiación de Aloe.
Por su parte, los agaves, pertenece a la familia Asparagaceae que incluye aproximadamente 2900 especies distribuidas alrededor del mundo y se estima que la divergencia del grupo corona comenzó hace unos 89 millones de años (Eguiarte 1994).
El género Agave L. es un género joven dentro de Asparagales con una edad estimada entre 7.8 y 10.1 millones que incluye más de 290 especies Good-Avila et al. (2006), todas ellas con cariotipo bimodal conservado de 30 cromosomas en genoma haploide que consiste en 5 cromosomas grandes y 25 cromosomas pequeños. En este género se aprecia una serie de ploidías naturales desde diploides hasta octoploides, con una conservación en los sitios y distribución de las regiones 5S y 45S, independientemente del nivel de ploidía y un incremento proporcional del contenido de ADN con relación al nivel de ploidía (Robert et al., 2008).
El Agave híbrido H11648 fue desarrollado en Tanzania a principios del siglo pasado, originado de la cruza de las especies A. angustifolia x A. amaniensis y retrocruzado con A. amaniensis. Es un híbrido con gran capacidad para generar fibra larga con un alto rendimiento, por lo que ha sido la base productiva de fibra natural en Tanzania y el único híbrido comercial de agaves.
El clado agavoide descrito por Bogler and Simpson (1996) incluye 15 géneros y 10 de ellos presentan un cariotipo bimodal constante de 5 cromosomas grandes y 25 cromosomas pequeños mientras que los 5 géneros restantes muestran números variables de cromosomas grandes y pequeños. A este grupo se le denominó como ABK (Agavoid Bimodal Karyotype), por sus siglas en inglés (McKain et al., 2012).
En diversas referencias se propone la hipótesis de que el cariotipo bimodal en Agave se establece como la integración de dos genomas ancestrales, con diversos eventos posteriores de rearreglos internos, duplicaciones, poliploidía y diversos cambios evolutivos (Ramos et al., 2023; McKain et al., 2012). Por su parte, la filogenia basada en genomas completos de cloroplasto agrupa a los géneros Agave, Manfreda, Polianthes y Bescornia, dentro del clado ABK de cloroplasto, sugiriendo diversidad evolutiva con relación a otros géneros de cariotipo bimodal (McKain et al., 2016).
La hibridación in situ (ISH) ha sido una herramienta clave para identificar rearreglos, inserciones, patrones de distribución y numero de sitios de hibridación, así como componentes parentales de cariotipos en diversas especies como fresa, trigo, cebada, algodón, entre otros (Humphreys et al., 1995; Rey et al., 2018; Yu-xiang et al., 2013). En particular, la hibridación genómica in situ (GISH) se ha empleado ampliamente para la identificación de componentes genómicos tanto en híbridos como en alopoliploides como Nicotiana tabacum (Shibata et al., 2013).
Derivado de lo anterior, en esta investigación hibridamos el genoma de Aloe vera en las células en interfase y cromosomas en metafase de Agave híbrido H11648 con el objetivo de determinar la representatividad de Aloe vera, especie con cariotipo bimodal y alejada evolutivamente por varios millones de años, en el genoma del Agave, empleando GISH.
Métodos
Preparación de células en interfase
La colecta de raíces se realizó de plantas de A. híbrido H11648 mantenidas en maceta. Los cromosomas en metafase se obtuvieron a partir de ápices de la raíz incubados en una solución saturada de paradiclorobenceno (PDB) durante 3 horas a temperatura ambiente y posteriormente fijadas en una solución de alcohol absoluto y ácido acético glacial (3:1) durante 24 horas.
Las puntas de raíz fueron incubadas con viscozyma (SIGMA cat. V2010) a 37°C por 25 minutos y posteriormente, se realizaron dos lavados con agua. Bajo estereoscopio se retiró la cofia de la raíz y se preparó una suspensión celular con ácido acético al 60% y se colocaron 10 ml de la suspensión celular en el portaobjetos y se colocó un cubreobjetos para realizar la homogenización mediante “squash”. El análisis de preparaciones se realizó en un microscopio de contraste de fases. A las preparaciones que presentaban cromosomas en metafase y núcleos en interfase, se les retiró el cubreobjetos para su uso en la técnica de GISH.
Marcaje de la sonda
Por su parte el marcaje de ADN genómico de Aloe se realizó por Nick Translation para la incorporación de DIG-11dUTP empleando el kit para marcaje con digoxigenina 'DIG DNA Labeling Kit', (RocheTM). La incorporación se verificó mediante dot-blot de acuerdo con lo reportado por Robert et al., (2008).
GISH de ADN genómico de Aloe
Las preparaciones seleccionadas que contenían núcleos en interfase y cromosomas en metafase de Agave híbrido fueron tratadas con 100 μg/ml de RNasa A, incubando durante 1 hora a 37°C con dos lavados posteriores con 2X SSC, durante 5 min. Transcurrido el tiempo, las preparaciones se incubaron en 10 mM de HCL por 5 min y posteriormente se incubaron con pepsina (10 μl/ml) (SIGMA cat. P6887) a 37 °C por 15 min. Posteriormente fueron lavadas dos veces en 2X SSC por 5 min. Se fijaron en paraformalehído 4% (p/v) (SIGMA cat. P6148), durante 10 min. Transcurrido el tiempo las preparaciones se lavaron dos veces en 2X SSC por 5 min y se deshidrataron con etanol a diferentes concentraciones 70%, 90% y 96%, por 3 min cada una, secando a temperatura ambiente. La desnaturalización de éstas se realizó incubando 2 minutos con 70% de formamida (v/v) (SIGMA cat. F5786) a 75°C. Inmediatamente a la desnaturalización, fueron deshidratadas en etanol al 70%, 90% y 96%, en hielo durante 5 min en cada paso.
A cada preparación se le aplicaron 40μl de la mezcla de hibridación compuesta de formamida 50% (v/v) (SIGMA cat. F5786), 2X SSC, 10% de Sulfato de Dextrano (p/v) (SIGMA cat. D8906), 0.17% de SDS y 100 ng del ADN genómico de Aloe con marcaje) previamente desnaturalizada a 75 °C durante 10 min y mantenida en hielo hasta su aplicación. Las preparaciones con la mezcla de hibridación se incubaron a 42 °C en cámara húmeda durante toda la noche. Posterior a la hibridación, se procedió a la detección de la sonda en donde las preparaciones fueron lavadas dos veces en 2X SSC por 5 min. Después de los lavados fueron colocadas por 5 min (una preparación a la vez) en una serie de 20% de formamida (v/v) y 2X SSC atemperadas a 42 °C a baño húmedo. Enseguida, las preparaciones se lavaron dos veces en 4X SSC y 0.2% (v/v) de tween 20 (SIGMA cat. P1379) durante 5 min.
Transcurrido el tiempo de lavados astringentes, a las preparaciones se les adicionó BSA 5% (p/v) (SIGMA cat. A2153) y se incubaron a 37 °C durante 20 min para posteriormente aplicar 5 μl (0.75U/μl) de estreptavidina acoplada con CY3 para la detección del ADN genómico de Aloe vera, y se incubó a 37°C durante una hora. Pasado el tiempo de detección, las preparaciones se lavaron dos veces en 4x SSC y 0.2% de tween 20 (v/v) (SIGMA cat. P1379). Las preparaciones se escurrieron y se aplicaron 30 μl (1.5 μg/ml) del medio de montaje Vectashield con DAPI (VECTOR cat. H-1200), un cubreobjetos fue colocado sobre la preparación y por último se mantuvo en oscuridad por 10 min. Las preparaciones fueron a analizadas en un microscopio de epifluorescencia Carl Zeiss Axioplan y las imágenes se capturan mediante una cámara Axiocam MRm y el software AxioVision de Carl Zeiss.
Las imágenes fueron procesadas en los parámetros de curvas de nivel, brillo y contraste en el programa Photoshop versión 25.3.1.
Resultados
En este trabajo, a partir de puntas de raíz colectadas a primeras horas de la mañana se obtuvieron tanto núcleos en interfase como cromosomas en metafase de Agave híbrido H11648 y en los cuales se analizó, mediante GISH el perfil de hibridación del genoma Aloe.
Para determinar la representatividad del genoma de otra especie con cariotipo bimodal en el genoma de agaves, se realizó la hibridación genómica in situ de Aloe tanto en núcleos en interfase (Figura 1 panel a-c), como en cromosomas en metafase (Figura 1 panel d-f) de Agave híbrido H11648. A partir de la localización genómica de Aloe se observó una hibridación (señales en color rojo) de éste en todas las regiones del genoma de Agave híbrido, observando una cobertura casi completa, aunque con ligeras diferencias en intensidad para algunas pequeñas regiones del genoma de Agave descondensado, en interfase (Figura 1c). Por su parte en cromosomas en metafase se aprecian sitios de hibridación (señales en rojo) a lo largo de los cromosomas tanto en el componente de cromosomas pequeños, como en el componente de cromosomas grandes, pero con hibridación en todos los cromosomas (Figura 1f) aunque con cobertura diferencial.
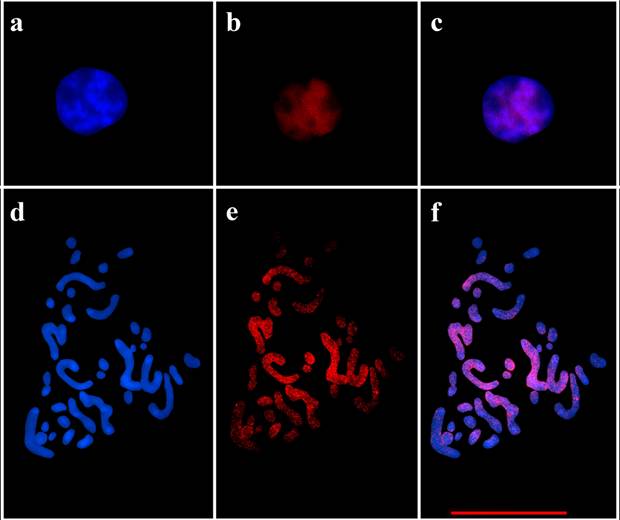
Figura 1 Hibridación genómica in situ de Aloe vera en Agave híbrido H11648. Paneles (a-c) hibridación genómica en células en interfase de Agave híbrido H11648 teñidas con DAPI (a), genoma de Aloe vera marcado con Cy3-rhodamina (b) e imágenes acopladas (c). Los paneles (d-f) muestran la hibridación genómica in situ de Aloe vera en cromosomas en metafase de Agave híbrido H11648: DAPI(d), genoma de Aloe-Cy3 (e), imágenes acopladas (f). La barra de escala representa 10 mm.
El perfil específico de hibridación se presenta en una muestra de los cromosomas, seleccionando 5 grandes y 25 pequeños (Figura 2a), se observó perfiles de hibridación en los 30 cromosomas. En los cromosomas grandes se observó cobertura casi completa a lo largo de cada cromosoma, aunque con menor incidencia en las regiones teloméricas, en 3 de los 5 cromosomas y parcial en los dos restantes, mientras que en de los 25 cromosomas pequeños se observó una cobertura casi completa en 12 de ellos y parcial en los 13 cromosomas restantes.
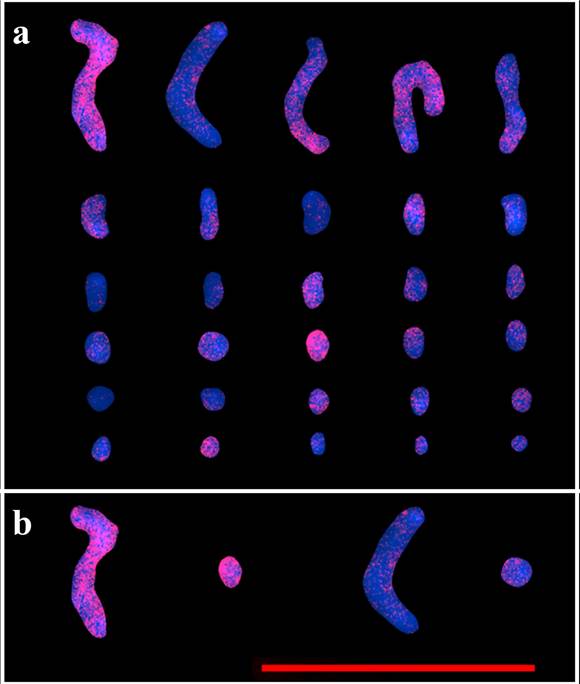
Figura 2 Perfil de hibridación genómica in situ del genoma de Aloe vera en el componente bimodal de Agave híbrido H11648. a) cromosomas en metafase de Agave teñidos con DAPI (azul) con hibridación genómica de Aloe vera marcado con Cy3 (Rosado). b) Comparativo de cobertura en cromosomas contrastantes seleccionados con relación al perfil de hibridación del genoma de Aloe vera. La barra de escala representa 10 mm.
La comparación de cobertura del genoma de Aloe vera en cromosomas de Agave híbrido H11648, de manera contrastante se presenta en la Figura 2b, en la cual se comparan dos cromosomas grandes y dos pequeños con perfiles de hibridación diferencial, mientras que en uno grande y uno pequeño la cobertura es cercana al 90% del cromosoma total, el otro es cercano al 10%. El patrón de hibridación se aprecia distribuido a lo largo de los cromosomas, sin un perfil de hibridación específico aparente.
La presencia de hibridación en cromosomas en metafase o núcleos en interfase, evidencia de manera global la conservación de regiones comunes a ambos genomas, ello a pesar de la diferencia evolutiva de varios millones de años.
En otras especies, empleando GISH se ha podido identificar la parte del componente genómico de especies parentales donde claramente uno de los parentales hibrida en una parte de los cromosomas en metafase (Lee et al., 2016). El perfil de hibridación observado en el presente trabajo, sugiere una gran conservación de los genomas evaluados y aporta evidencia que descarta, al menos parcialmente, la hipótesis de la hibridación de genomas como origen del cariotipo bimodal en agaves.
Discusión
Mientras que las diferencias en el tamaño del genoma pueden surgir de duplicaciones o deleción de ADN redundante o de la duplicación del genoma completo, hay casos de una forma especial de asimetría caracterizada por la presencia de dos conjuntos distintos de cromosomas de tamaño contrastante en un complemento cromosómico, es decir, un "cariotipo bimodal". Tales cariotipos bimodales pueden originarse ya sea por fusión que resulta en la formación de un gran conjunto de cromosomas a partir de diversos cromosomas pequeños o regiones de cromosomas específicos o por fisión que resulta del fraccionamiento de un cromosoma en nuevos cromosomas más pequeños o acumulación diferencial de cromosomas, secuencias repetitivas o por combinaciones alopoliploides de especies con diferentes tamaños cromosómicos (Baez et al., 2019). Los cariotipos bimodales son comunes en familias de monocotiledóneas como Asphodelaceae (Aloe, Haworthia y Gasteria) y Agavaceae (Agave, Yucca y Camassia) (Weiss-Schneeweiss and Schneeweiss 2013).
Los resultados obtenidos en este trabajo con relación a la representatividad del genoma de Aloe en el genoma de Agave, tanto en cromosomas grandes como pequeños sugiere, de manera preliminar que el cariotipo bimodal no se obtuvo por la integración de dos genomas, tal como se ha reportado para los cariotipos bimodales de especies de espárragos, donde se plantea la hipótesis de un reordenamiento cromosómico que involucra eventos de fusión-fisión (Schubert and Lysak 2011).
El orden Asparagales, que incluye 14 familias tiene una edad estimada del grupo corona de aproximadamente 125.3 millones de años (Tank et al., 2015) y una gran diversidad en tamaños de genoma en valor C que varían entre 0,3 y 82,2 pg (Leitch and Leitch 2013). El género Aloe L. pertenece a la familia Asphodelaceae que contiene alrededor de 940 especies y una edad aproximada de 45 a 63 millones de años y presenta una gran diversidad en tamaño y morfología de planta, aunque en su mayoría son diploides se (2n=2x=14). Sus especies muestran en general estabilidad en el cariotipo bimodal con una estructura básica haploide de un cromosoma grande, submetacéntrico tres cromosomas grandes acrocéntricos y tres cromosomas pequeños acrocéntricos (Brandham and Doherty 1998). El contenido de ADN reportado en valor C es cercano a los 20 pg por genoma haploide (Steele et al., 2012), pero existen reportes de asimetría cariotípica en algunas especies del género (Gunjan and Roy, 2010). En el estudio reportado por Jahan y colaboradores en (2014), se establece que los cromosomas de Aloe vera mostraron una longitud promedio de una población analizada en Pakistán que varió de 2.36 hasta 7.95 µm.
Por su parte, el género Agave, de acuerdo a lo reportado por (Good-Avila et al., 2006) , es un género joven dentro de Asparagales con una edad estimada entre 7.8 y 10.1 millones de años con una constancia en su tamaño de genoma en valor C cercano a 4.2 pg de ADN por genoma haploide, que incrementa de manera casi proporcional con el nivel de ploidía (Gomez-Rodriguez et al., 2013; Robert et al., 2008) y todas sus especies presentan el cariotipo bimodal típico con número básico de 30 cromosomas, de los cuales 5 cromosomas son grandes y 25 cromosomas son pequeños (Castorena-Sánchez et al., 1991; Robert et al., 2008). Este género presenta una serie de ploidía desde diploide hasta octoploide manteniendo siempre la proporción del número básico y del cariotipo bimodal.
El perfil de hibridación presentado aquí muestra que el genoma de Aloe, una especie ancestral, está presente en los cromosomas de Agave tanto en el componente de cromosomas grandes como en los pequeños, observando algunos con hibridación casi completa de los cromosomas, a pesar de la distancia evolutiva de ambas familias. Este hecho es relevante y sugiere un mecanismo de conservación de una gran cantidad de información genética a lo largo de la evolución de ambas especies, lo cual contrasta con las diferencias observadas entre las especies de Agave y de Aloe al evaluar mediante hibridación fluorescente in situ la distribución de la región 5S y 45S en 13 especies de Aloe, se evidenció una conservación en localización intersticial en cromosomas grandes de la región 5S, en comparación con diferencias en el número, localización y tamaño de loci encontrado entre las especies analizadas en la región 45S (Adams et al., 2000), posiblemente originados durante la especiación de Aloe. En contraste, a lo observado en Agave muestra que cada genoma haploide presenta un sitio 18S en cromosoma grande y un sitio 5S en cromosoma pequeño y su número aumenta de manera proporcional con el nivel de ploidía, en todas las especies de Agave analizadas (Robert et al., 2008; Gomez-Rodriguez et al., 2013).
Los géneros de Agave y Aloe están evolutivamente alejados con una divergencia superior a 27 millones de años (Bogler and Simpson 1996; Steele et al., 2012), por lo cual es de suma importancia lo observado en el presente trabajo, toda vez que el perfil de hibridación del genoma de Aloe en el de Agave híbrido muestra presencia de sitios distribuidos a lo largo del genoma de Agave, sugiriendo conservación de regiones genómicas conservadas presentes en especies ancestrales anteriores a la divergencia evolutiva de éstas.
La divergencia estimada en géneros relacionadas a los agaves como Yucca se estimó en 20 millones de años, mientras que con Camassia o Hesperaloe se estimó en 25 millones de años y con Hosta en aproximadamente 27 millones de años (McKain et al., 2016) y todas ellas presentan un cariotipo bimodal. Basado en análisis de filogenia, se ha reportado que Aloe vera compartió el ancestro reciente más común con las especies de Poales y Zingiberales, también dentro del orden Asparagales; siendo más cercano a los otros géneros suculentos como Haworthia, Gasteria y Astroloba (Chase et al., 2016; Qian and Jin 2016) que con los agaves.
Lee et al. (2016) demostraron mediante GISH en un híbrido de Aloe con cariotipo bimodal, que la especie A. arborescens es el donador del genoma materno y el complemento proviene de A. vera, lo cual se observó mediante el patrón de hibridación genómica en solamente algunos de los cromosomas del cariotipo. En contraste con este reporte, nuestros resultados mostraron presencia del componente genómico de Aloe vera en todos los cromosomas de Agave híbrido a lo largo del cariotipo bimodal.
Se ha reportado en angiospermas, que la hibridación ancestral es una fuerza evolutiva importante que desempeña un papel destacado en los mecanismos de especiación (Stull et al., 2023). Por su parte la diversidad cromosómica puede surgir de alteraciones a través de translocaciones intragenómicas, inversiones pericéntricas y fusión/fisión, que pueden afectar o no el tamaño del genoma (Vimala et al., 2021). La diferencia en el tamaño del genoma haploide entre Agave (4.2 pg) y Aloe (19 pg) es de casi 4 veces, posiblemente derivado de la contribución de las regiones repetidas como satélites y retroelementos que provocan el incremento del genoma.
El mayor impacto en la variación del tamaño del genoma en las plantas, así como en todos los eucariotas, parece haber sido la amplificación/eliminación de secuencias repetitivas, especialmente elementos móviles (Wang et al., 2021a). El número de secuencias repetitivas difiere significativamente entre las especies, y el contenido promedio de secuencias repetitivas en las plantas oscila entre el 14% y el 90%. La mayoría (más del 75%) de este contenido repetitivo se identificó como elementos móviles (Elliott and Gregory, 2015; Vondrak et al., 2020). Se ha reportado que las regiones repetidas en especies como Allium (Pearce et al., 1996) y Agave (Ramos et al., 2023), Zea (Sharma and Presting, 2008), entre otros, puede rondar del 60 al 90% del genoma total. Como complemento a este trabajo sería importante el aislamiento de familias de retroelementos presentes en especies ancestrales para determinar su contribución al tamaño del genoma de los agaves.
GISH ha sido ampliamente utilizado para determinar el componente ancestral/parentales de híbridos o especies alopoliploides (Markova and Vyskot, 2009), como Arabidopsis (Ali et al,. 2004), Brassica (Hasterok et al., 2005), Trifolium (Ullah et al., 2022), Coffea (Herrera et al., 2012), Gossypium (Wu et al., 2013), Nicotiana (Shibata et al., 2013), Tragopogon (Chester et al., 2015), y Triticum (Wang et al., 2021b), entre otros. La diferenciación exitosa de los subgenomas en los cromosomas y los núcleos de interfase de los poliploides a través de GISH depende en gran medida de la presencia de secuencias repetitivas específicas del genoma (Kato et al., 2005).
Conclusiones
La presencia y cobertura de hibridación del ADN de una especie ancestral como Aloe vera en cromosomas en metafase o núcleos en interfase de agave, evidencia de manera global la conservación de regiones comunes a ambos genomas, descartando la teoría de la hibridación genómica como origen del cariotipo bimodal. Lo anterior es relevante ya que el género Agave L. es un género joven dentro de asparagales con una edad estimada entre 7.8 y 10.1 millones que incluye más de 290 especies (Good-Avila et al., 2006), todas ellas con cariotipo bimodal conservado de 30 cromosomas en genoma haploide que consiste en 5 cromosomas grandes y 25 cromosomas pequeños. Por su parte Aloe L. pertenece a la familia asphodelaceae que contiene alrededor de 940 especies y una edad aproximada de 45 a 63 millones de años y hasta el momento se desconoce el origen del cariotipo bimodal en los agaves. La información generada en esta investigación de manera directa sugiere que el cariotipo bimodal en agaves puede ser originado por fusiones y fisiones más que por aloplopliploidía de especies ancestrales. Hasta nuestro conocimiento, este es el primer reporte empleando GISH para estudiar el origen del cariotipo bimodal en agaves.





![Prácticas de manejo para la producción de (Vigna unguiculata [L.] Walp) en productores del Municipio de Pungarabato, Guerrero, México](/img/s/next.gif)










