Introducción
La restauración de los ecosistemas se ha convertido en una necesidad fundamental para los retos ambientales y socio económicos que enfrentan los ecosistemas a nivel mundial (Fremout et al., 2022) debido a que una de las principales metas de la restauración es que las acciones implementadas lleven al incremento o recuperación de las funciones y servicios de estos (Derhé et al., 2016; Bhutia et al., 2019; Staples et al., 2020). La restauración tiene impactos positivos en la biodiversidad (Huang et al., 2019; Mestre et al., 2017) y, por tanto, en el suministro de servicios ecosistémicos (Huang et al., 2019; Deng et al., 2023), ya que el número e identidad de las especies presentes influyen en una o varias de las funciones del ecosistema, como la producción y descomposición de hojarasca, almacén de carbono, retención de humedad, entre otros (Ma et al., 2024; Ou et al., 2020).
El sotobosque es un componente vital en los ecosistemas forestales (Su et al., 2021) debido a que es un estrato de vegetación distinguible de un estrato superior -generalmente compuesto de árboles. En el sotobosque se encuentran plántulas de especies arbóreas con alturas menores a 1.5 m, además de arbustos, herbáceas líquenes y briofitas (hepáticas, antoceros y musgos), rosetas y trepadoras, entre otras. Por tanto, el sotobosque contribuye significativamente a la complejidad, estructura y función de los ecosistemas forestales restaurados (Balandier et al., 2022; Deng et al., 2023; Landuyt et al., 2019; Mejía-Canales et al., 2018). No obstante, dicha influencia requiere de un proceso de cambio continuo, de tal manera que conforme se incrementa el tiempo de la restauración, la composición y estructura vegetal cambia (Rodríguez-Calcerrada et al., 2010; Ma et al., 2024). De acuerdo con Ma et al. (2024) la diversidad de arbustos y herbáceas en bosques secundarios es significativamente afectada por la edad de la restauración (1, 10, 30, 60 y 90 años), donde las áreas de 10 y 90 años se registraron los mayores valores, lo cual está asociado a diversos factores tanto bióticos como abióticos de los sitios.
De acuerdo con la Sociedad de Restauración Ecológica (Gann et al., 2016) existen atributos que deben tomarse en consideración para determinar si un sitio restaurado contiene suficientes recursos bióticos y abióticos para continuar su desarrollo sin la intervención del hombre. Entre dichos atributos se encuentran: 1. estructura: donde se observen las diferentes edades, especies, tamaño de los individuos que forman una la comunidad, bosque o ecosistema; 2. presencia de especies nativas hasta donde sea posible; 3. presencia de grupos funcionales; y 4. presencia de poblaciones con capacidad reproductiva. Estos atributos pueden ser evaluados en cualquier ecosistema, mediante tres características principales: 1. estructura 2. diversidad (taxonómica y funcional) y 3. procesos ecológicos (Ruiz-Jaén & Aide, 2005). Aunado a lo anterior, se encuentra el uso de un ecosistema o bosque de referencia con el que se puedan comparar los atributos de la zona restaurada que se está evaluando (Gann et al., 2016). Bajo este contexto, la diversidad del sotobosque ha sido utilizada como un indicador de la integridad de los ecosistemas (Zhang et al., 2021), por lo que las metas en los trabajos de restauración deben incluir también la restauración de las especies del sotobosque, particularmente con especies nativas (Chen et al., 2018).
En México como en otros lugares del mundo, una de las prácticas ampliamente utilizadas para la recuperación de los ecosistemas forestales han sido las reforestaciones (Derhé et al., 2016) las cuales tratan de acelerar los procesos de sucesión natural a través de la modificación del microclima, además de otros beneficios. Lo anterior ha resultado en el reconocimiento de la importancia de las reforestaciones en la recuperación de zonas deforestadas y degradadas, por lo que la Comisión Nacional Forestal (CONAFOR) llevó a cabo la restauración forestal a gran escala mediante la operación del Programa Nacional Forestal (PRONAFOR) durante el periodo 2013-2018 (Méndez-Toribio et al., 2018). Sin embargo, la gran mayoría de las investigaciones han estado enfocadas a evaluar el “éxito” de las reforestaciones de las especies arbóreas, mientras que la dinámica de las comunidades vegetales del sotobosque ha recibido muy poca atención (Duan et al., 2019; Deng et al., 2013). En México las reforestaciones se han considerado exitosas por el hecho de presentar una alta supervivencia de las especies plantadas. Sin embargo, la información es insuficiente cuando se pretende considerar que un ecosistema ha recuperado sus procesos y funciones, dado que es importante considerar la composición, riqueza, abundancia y diversidad, entre otros parámetros de las especies presentes en el sotobosque de los ecosistemas restaurados. Por tanto, la hipótesis de este trabajo fue que, a mayor edad de la reforestación, esta presentará menor diversidad vegetal en el sotobosque, dado que se asemejaría cada vez más a un Bosque de Referencia (BR). Para probar lo anterior, el objetivo del presente estudio fue comparar la riqueza, la diversidad, y composición de especies del sotobosque (arbustos y herbáceas) en dos zonas reforestadas con Pinus montezumae Lamb. de diferentes edades, una zona sin reforestar referida posteriormente como zona degradada y un bosque de referencia en el noreste del estado de Puebla. Lo anterior, bajo la expectativa de que este trabajo sirva para demostrar la importancia de considerar al sotobosque en los programas, evaluaciones e iniciativas de recuperación de áreas degradadas y deforestadas.
Materiales y métodos
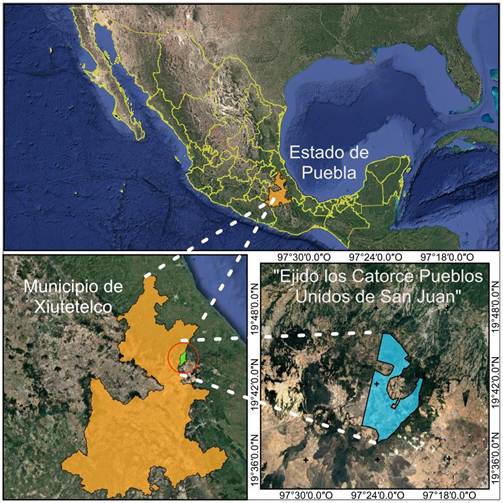
Este estudio se realizó en el ejido Los Catorce Pueblos Unidos de San Juan, municipio de Xiutetelco, al noreste del estado de Puebla (19°38’19.40” N -97°24’8.71” O y 19°45’12.72” N -97°22’3.77” O) (INEGI, 2021), con una elevación entre 2,500 y 3,000 m (Figura 1).
El clima predominante es templado-subhúmedo, la temperatura media anual entre 12-18 °C y la precipitación promedio de 650-850 mm por año (García, 2004). Los suelos dominantes son Regosol éutrico y Andosol ócrico (INEGI, 2020). La vegetación original predominante es bosques mixtos de coníferas y latifoliadas, como Pinus teocote Schiede ex Schltdl., P. montezumae Lamb., P. patula Schiede ex Schltdl. et Cham. y Alnus jorullensis Kunth.
También existen diversas zonas de transición de matorral xerófilo, con diversas especies de pastos y especies arbóreas de bajo porte, típicas de clima semiárido (Comisión Nacional para el Conocimiento y Uso de la Biodiversidad (CONABIO), 2023).
Para llevar a cabo este estudio, se seleccionaron cuatro zonas con condiciones abióticas y fisiográficas similares (exposición, pendiente y altitud). Dos zonas reforestadas con P. montezumae de 5 y 9 años (ZR5 y ZR9), un bosque de referencia de P. montezumae Lamb. y P. teocote Schiede ex Schltdl. (BR), área arbolada (remanente del bosque natural con cierto grado de perturbación) y una zona degradada (ZD), considerada como el testigo (t0), previa a la reforestación (Figura 2).
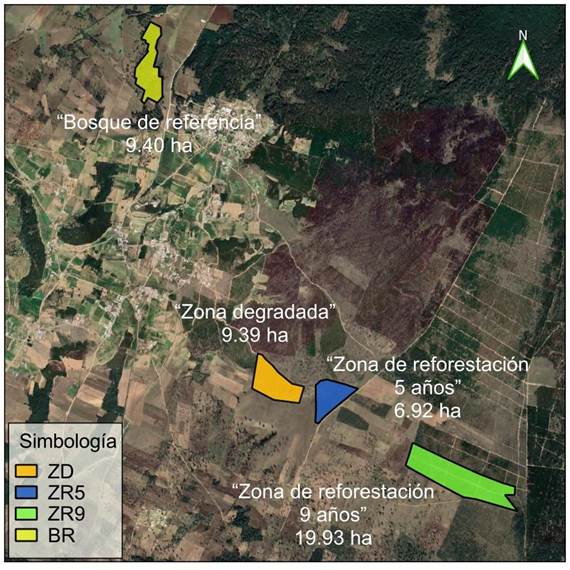
Figure 2 Location of the four study areas in the ejido Los Catorce Pueblos Unidos de San Juan, Puebla: degraded (ZD), two reforestations with Pinus montezumae (RZ5 and RZ9) and a reference forest (BR).
Diversidad del sotobosque
Mediante un muestreo aleatorio se seleccionaron cinco sitios circulares de 100 m2 por zona (Figura 3) utilizando una malla de puntos (cada 100 m). Dentro de los sitios de 100 m2 se establecieron cuatro sub-sitios de 1 m2, con la finalidad de evaluar las especies herbáceas del sotobosque.
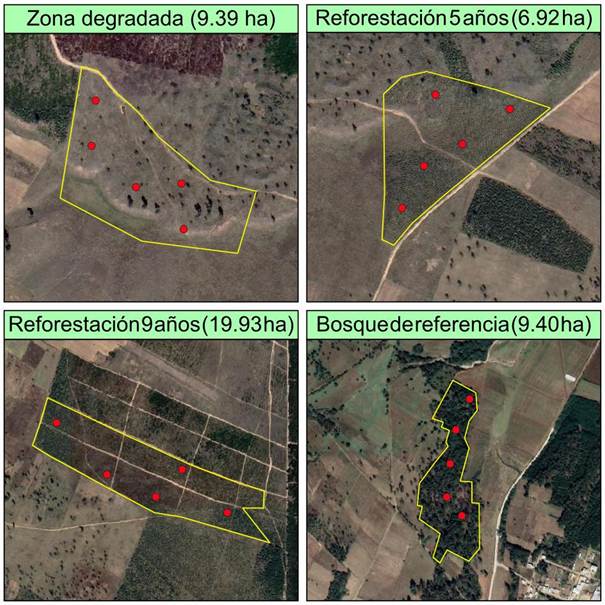
Figura 3 Distribución de los sitios de muestreo dentro de las zonas de estudio; zona degradada (ZD), dos reforestaciones con Pinus montezumae de 5 y 9 años (ZR5 y ZR9) y un bosque de referencia (BR), en el ejido Los Catorce Pueblos Unidos de San Juan, Puebla.
En los sitios de 100 m2 se identificaron in situ las especies arbustivas (plantas con crecimiento secundario leñoso y sin una definición del tallo principal) y se registró el número de individuos por especie (densidad) y diámetro de copa (cm), a partir de la cual se calculó la superficie de la copa (Rodríguez-Laguna et al., 2008) para posteriormente transformarla en cobertura. En los cuatro subsitios de un m2, se estimó la cobertura (%) de cada una de las especies herbáceas. Las especies no reconocidas en campo fueron llevadas al herbario (CHAP) de la División de Ciencias Forestales, de la Universidad Autónoma Chapingo para su identificación.
Por otra parte, se generaron curvas área-especie utilizando el software EstimateS 9.1 (Moreno, 2001; Magurran, 2004; Ventura-Ríos et al., 2017), para determinar la intensidad de muestreo del área total del estudio. Lo anterior indicó que en el área muestreada se capturó el 70% de la riqueza total del área de estudio. La diversidad alfa se determinó como el número de especies (riqueza total) dentro de cada zona estudiada, además de determinar la diversidad utilizando los índices de Margalef, de Simpson y el de equidad (Moreno, 2021).
Para determinar la diversidad beta (β; es decir la similitud florística entre las zonas de estudio), se utilizó el índice de Jaccard (Moreno, 2001; Koleff, 2005). Este se calculó mediante la siguiente ecuación:
Donde:
Ij = Índice de semejanza florística de Jaccard
a = Número de especies que se encuentran en la comunidad a
b = Número de especies que se encuentran en la comunidad b
c= Número de especies presentes en ambas comunidades a y b
El Índice de Valor de Importancia Relativo (IVIR) se calculó para las especies del sotobosque (herbáceas y arbustivas) a partir de la dominancia (cobertura) y frecuencia relativa (Mostacedo & Fredericksen, 2000)(Alday et al., 2012).
Donde:
La frecuencia relativa se estimó de la siguiente manera:
Donde:
Análisis estadístico
Para determinar la existencia de diferencias estadísticamente significativas entre las zonas de estudio en las variables de la diversidad vegetal, se verificó la normalidad de los datos con la prueba de Shapiro-Wilk. Dado que en todos los casos se cumplió con los supuestos de normalidad y homogeneidad de varianzas, se realizó un análisis de varianza (ANOVA) de un factor, con un nivel de confianza del 95%, seguido de una prueba de comparación de medias de Tukey (α=0.05), utilizando el software R en la plataforma R Studio (The R Core Team, 2022).
Resultados y discusión
Riqueza y composición vegetal
La riqueza específica total en el área muestreada arrojó 41 especies en el sotobosque entre arbustos y herbáceas, las cuales se distribuyeron en 17 familias. El 80% de las especies encontradas (33) fueron nativas y un 20% (8) exóticas (CONABIO, 2023) (Apéndice 1). Respecto a la riqueza total dentro de las zonas de estudio, se presentó el siguiente orden decreciente: ZR5>ZD>ZR9>BR (Tabla 1). No obstante, entre ZR5 y ZD la riqueza total no fue significativamente diferente), pero sí de estas al compararlas con ZR9 y BR (α≤0.05) (Tabla 1), así como entre estas dos últimas.
Tabla 1 Número de especies y comparación de medias (entre paréntesis) por forma de vida entre las cuatro zonas de estudio: una zona degradada (ZD), en dos reforestaciones (ZR5 y ZR9) y un bosque de referencia (BR), en el ejido Los Catorce Pueblos Unidos de San Juan, Puebla.Table 1. Number of species and comparison of means (in parentheses) by life form between the four study areas: a degraded zone (ZD), in two reforestations (ZR5 and ZR9) and a reference forest (BR), in the ejido Los Catorce Pueblos Unidos de San Juan, Puebla
| Forma de vida | ZD | ZR5 | ZR9 | BR | ||||
|---|---|---|---|---|---|---|---|---|
| Herbáceas | 32 | (21.8)a | 31 | (22.0)a | 24 | (14.4)b | 17 | (9.0)c |
| Arbustos | 0 | (0)b | 2 | (2.0)a | 2 | (2.0)a | 2 | (2.0)a |
| Riqueza Total | 32 | (21.8)a | 33 | (24)a | 26 | (16.4)b | 19 | (11.0)c |
ZD: zona degradada, ZR5: zona con 5 años de haber sido reforestada, ZR9: zona con 9 año de haber sido reforestada, y BR: bosque de referencia. Comparación entre zonas de estudio para una misma forma de vida. Letras diferentes indican diferencias estadísticas significativas entre zonas para cada forma de vida (α= 0.05).
ZD: degraded zone, RZ5: zone that has been reforested for 5 years, RZ9: zone that has been reforested for 9 years, and BR: reference forest. Comparison between study zones for the same life form. Different letters indicate significant statistical differences (α≤0.05), between zones for the life form.
En el sotobosque las especies herbáceas fueron las más abundantes en todas las zonas estudiadas (Tabla 1), con un mayor número de especies. No obstante, destaca que el BR fue el que presentó una menor riqueza total de especies herbáceas (17 especies). Respecto a los arbustos, estos presentaron 0 especies en la ZD, significativamente menor a ZR5=ZR9=BR. Si bien no hay un patrón en cuanto al incremento de la riqueza de especies conforme se incrementa la edad de los rodales analizados en este estudio, resalta el hecho de que ZD y ZR5 no presentan diferencias estadísticas significativas en riqueza, mientras que ZR9 se diferencia de dichas zonas, así como de BR.
De acuerdo con Ma et al. (2024) la disponibilidad de luz afecta directamente a las especies herbáceas, particularmente a las perennes, por lo que tanto la diversidad de arbustos perennes y herbáceas fue significativamente afectada por la edad de la restauración. Dichos autores señalaron que los valores mayores en diversidad específica se presentaron en las áreas de 10 y 90 años, comparado con los menores valores encontrados a los 60 años. Así en nuestro estudio, el BR como se esperaba, presentó la menor riqueza de especies en el sotobosque, posiblemente por la entrada menor de luz por efecto de la cobertura del dosel arbóreo. En varios estudios se ha demostrado que el dosel superior tiene un efecto sobre la composición del sotobosque (Chen et al., 2018), debido a que este modifica el ambiente lumínico en el interior del bosque por la reducción en la trasmisión de hacia la parte baja. Este se considerada una de las principales fuerzas que determinan la abundancia de especies en el sotobosque, ya que la menor entrada de luz modifica las condiciones ambientales, disminuye la temperatura y aumenta la humedad en el piso forestal, lo que a su vez modifica la química del matillo y suelo superficial (Ou et al., 2020; Shen et al., 2020).
La similitud entre ZR5 y ZD en cuanto a la mayor riqueza de especies herbáceas es apoyado por los resultados de Poudel et al. (2019), quienes encontraron que en los rodales más jóvenes se presenta una mayor diversidad de especies herbáceas y que la edad del rodal tiene un efecto en la composición, la diversidad y la abundancia de las especies en el sotobosque. Por otro lado, la presión antrópica (e.g., fuego, pastoreo, tala no regulada) puede modificar drásticamente la compleja relación entre los factores abióticos y bióticos. Por ejemplo, el microclima se ve modificado al aumentar la radiación solar y disminuir la disponibilidad de agua en el suelo (Kutnar et al., 2019; Ou et al., 2020; Shen et al., 2020) lo que se puede observar en ZD y ZR5. Bajo estas condiciones las especies pioneras contribuyen al aumento de la riqueza específica (Gotelli, 2008; Ares et al., 2010), aunque estas especies no persisten de manera indefinida. La presencia de las especies pioneras tiene efectos positivos tanto en la estabilización del suelo (e.g., gramíneas amacolladas) como en la aportación de sombra. Adicionalmente, cuando estas especies mueren y se incorporan al mantillo, durante el proceso de descomposición aportan nutrimentos al suelo a una mayor velocidad que otro tipo de especies, favoreciendo la presencia de nuevas especies en el proceso de sucesión. Las especies pioneras son remplazadas por especies tolerantes a la sombra a medida que el dosel superior se va cerrando (Poudel et al., 2019). Bajo este contexto, en el área de estudio, la perturbación por actividades humanas (principalmente pastoreo) de poblados aledaños puede explicar parcialmente la menor riqueza encontrada en el BR (Kutnar et al., 2019; Granados-Victorino et al., 2015; Luna-Bautista et al., 2015).
La riqueza y diversidad del sotobosque, son los componentes más importantes de la diversidad vegetal en los estratos de un bosque, contribuyendo a diferentes funciones en el ecosistema (Quijada et al., 2020; Mejía-Canales et al., 2018; Chen et al., 2018). A pesar de que las especies herbáceas representan únicamente el 1% de la biomasa de los bosques, estas contribuyen en más de un 20% al matillo foliar del piso forestal, el cual destaca por su importancia en la incorporación de nutrimentos que puede ser mucho más alta que la que proporcionan los árboles (Gillam, 2007). En este estudio, ZD y ZR5 presentan condiciones y características similares en relación con la cantidad de luz, suelos pobres en nutrimentos y poca humedad, pudiendo generar ambientes que promueven la dominancia de especies pioneras (Cabrera-Luna & Gómez-Sánchez, 2005).
En cuanto a las familias registradas en todo el sotobosque se encontró que las de mayor número de especies fueron la Asteraceae (13), Poaceae (5), Fabaceae (3) y Lamiaceae (3), las cuales son características de regiones montañosas, áridas y semiáridas de México, concordando con lo reportado por Pompa-Castillo et al. (2021), en una zona montañosa similar a la del presente estudio. Por tanto, conocer con mayor detalle las interacciones entre los diferentes factores bióticos y abióticos de un sitio, permitirá tomar mejores decisiones para su recuperación.
Diversidad alfa y beta del sotobosque
El índice de diversidad de Margalef mostró diferencias estadísticas significativas (α= 0.05) entre las zonas de estudio, donde el valor mayor se encontró en ZD (4.67) y ZR5 (4.26), es decir en la zona degradada y la plantación más joven y, el menor valor en el BR (2.42) (Tabla 2). La diversidad calculada con el índice de Simpson mostró diferencias estadísticas entre condiciones evaluadas, observándose mayor diversidad en ZR5 (0.90) y ZD (0.88) que coincide con el resultado observado con el índice de Margalef. La zona del BR (0.80) presentó un valor intermedio y ZR9, la condición que presentó la menor diversidad (0.78 (Tabla 2). Por tanto, se observó un patrón de disminución de la diversidad con el aumento de la edad del rodal. Al respecto, Morales-Salazar et al. (2012) sostienen que el aumento en la diversidad de especies está en función de la edad del bosque y de su estadio sucesional, además que la diversidad del sotobosque presenta una variación significativa a lo largo de gradientes bióticos y abióticos (Deng et al., 2023). Lo anterior, puede explicar parcialmente. lo observado en el presente estudio, donde el BR mostró la menor riqueza y diversidad de especies en el sotobosque (Tabla 1, 2).
Tabla 2 Índice de Margalef, índice de Simpson y equidad del sotobosque en las cuatro zonas de estudio en el ejido Los Catorce Pueblos Unidos de San Juan, Puebla.Table 2. Margalef richness index, Simpson index, and understory equity, in the four study zones in the ejido Los Catorce Pueblos Unidos de San Juan, Puebla.
| Zonas | Índice de Margalef | Índice de Simpson (1-D) | Equidad (1/D)/S |
|---|---|---|---|
| ZD | 4.67 a | 0.88 ab | 0.39 ab |
| ZR5 | 4.26 a | 0.90 a | 0.45 ab |
| ZR9 | 3.16 b | 0.78 c | 0.30 b |
| BR | 2.42 b | 0.80 bc | 0.47 a |
Letras diferentes indican diferencias estadísticas significativas entre zonas para los índices de Margalef y Simpson y la equidad (α≤ 0.05). ZD: zona degradada, ZR5: zona reforestada de 5 años, ZR9: zona reforestada de 9años y BR: bosque de referencia.
Different letters indicate statistically significant differences between zones for the Margalef and Simpson indices and equity (α≤ 0.05). ZD: degraded area, RZ5: 5-year reforested area, RZ9: 9-year reforested area and RF: reference forest.
El índice de Simpson está influenciado por la abundancia de las especies dominantes (Magurran, 2004), lo cual es evidente en RZ9 por los valores de diversidad y equidad, atribuido principalmente a la especie dominante Muhlenbergia macroura (Kunth) Hitchc. (Tabla 2). La presencia, abundancia y dominancia de dicha especie en el área de estudio es destacable, y puede verse favorecida por los incendios, tala no regulada y pastoreo que se registran ahí. Sus atributos de ser una gramínea perenne y pionera que forma grandes macollos, además de su raíz fibrosa, le confieren resistencia y capacidad para permanecer en sitios expuestos a perturbaciones tanto naturales como antrópicas (Mejía-Saules, 1993). Baccharis conferta Kunth y Senecio salignus D.C. también registradas en la zona de estudio, son especies pioneras que aparecen y se desarrollan después de una perturbación (incendio, agricultura, tala no regulada y pastoreo) por lo que estas especies son importantes en la incorporación de materia orgánica al suelo y reciclaje de nutrimentos, así como provisión de refugios y alimento para fauna (Rendón-Pérez et al., 2021).
En cuanto a la diversidad beta, ZR5 y ZR9 compartieron un 64% de especies y SD-ZR5 un 63%. Por el contrario, el BR presentó el menor porcentaje de especies compartidas con las demás zonas (Tabla 3). Chust et al. (2006) señalan que la diversidad beta se correlaciona con la distancia geográfica entre condiciones evaluadas, el clima (especialmente la precipitación) y la elevación; mientras que la pendiente y la geología del lugar registraron una correlación baja en un bosque tropical en Panamá. Si bien en este estudio no se analizó la correlación con variables ambientales, las observaciones en campo indican una mayor disponibilidad de luz en ZD, ZR5 y ZR9, que en BR. Para tener mayores evidencias es conveniente medir otros factores abióticos como podrían ser variables físico-químicas del suelo (textura, disponibilidad de nutrimentos, saturación de bases del suelo, CIC, etc.) con la finalidad de entender con mayor claridad el porqué de la similitud especifica de las zonas estudiadas como lo señalan Chust et al. (2006).
Tabla 3 Diversidad beta para el sotobosque de cuatro zonas de estudio: zona degradada (ZD), dos zonas reforestadas de 5 y 9 años (ZR5 y ZR9), y un bosque de referencia (BR), en el ejido Los Catorce Pueblos Unidos de San Juan, Puebla.Table 3. Beta diversity of four study zones: degraded zone (ZD), two reforested zones of 5 and 9 years (ZR5 and ZR9), and a reference forest (BR), in the ejido Los Catorce Pueblos Unidos de San Juan, Puebla.
| Zonas | ZD | ZR5 | ZR9 | BR |
|---|---|---|---|---|
| ZD | 1.00 | 0.63 | 0.52 | 0.25 |
| ZR5 | 0.63 | 1.00 | 0.64 | 0.24 |
| ZR9 | 0.52 | 0.64 | 1.00 | 0.35 |
| BR | 0.25 | 0.24 | 0.35 | 1.00 |
Índice de valor de importancia relativa
Los resultados del IVIR mostraron que, en todo el sotobosque M. macroura fue la especie más importante ecológicamente, con 13.34, 7.68 y 21.39% en las zonas, ZD, ZR5 y ZR9, respectivamente. El BR se diferenció por ser P. virescens la especie que registró el mayor valor de IVIR (14.40%). En todas las condiciones M. macroura estuvo presente, aunque en el BR pasó a un tercer lugar, con un IVIR de 10.75%. El resto de las especies presentes por zona tiene valores de IVIR relativamente bajos si se comparan con los valores de M. macroura y P. virescens (Tabla 4).
Tabla 4 Índice de valor de importancia relativa (IVIR) del sotobosque, en una zona degradada (ZD), en reforestaciones con P. montezumae de 5 y 9 años (ZR5 y ZR9), y un bosque de referencia (BR) en el ejido Los Catorce Pueblos Unidos de San Juan, Puebla.Table 4. Relative Importance Value Index (IVIR) of the understory, in a degraded zone (ZD), in reforestations of 5 and 9 years with P. montezumae (ZR5 and ZR9), and a reference forest (BR) in the ejido Los Catorce Pueblos Unidos de San Juan, Puebla.
| Especies | Dominancia absoluta (%) |
Dominancia relativa |
Frecuencia absoluta |
Frecuencia relativa |
IVI al 100 % |
|---|---|---|---|---|---|
| ZD | |||||
| Muhlenbergia macroura (Kunth) Hitchc | 147 | 22.10 | 5 | 4.59 | 13.34 |
| Piptochaetium virescens (Kunth) Parod | 76 | 11.39 | 4 | 3.67 | 7.53 |
| Eryngium carlinae F. Delaroche | 63 | 9.54 | 5 | 4.59 | 7.06 |
| Plantago nivea Kunth | 61 | 9.20 | 5 | 4.59 | 6.89 |
| Arenaria lycopodioides Willd. ex Schltdl. | 54 | 8.14 | 5 | 4.59 | 6.37 |
| Trifolium repens L. | 31 | 4.60 | 5 | 4.59 | 4.59 |
| Rumex acetosella L. | 29 | 4.30 | 5 | 4.59 | 4.44 |
| Viola hookeriana H.B.K | 25 | 3.70 | 5 | 4.59 | 4.14 |
| Pseudognaphalium roseum (Kunth) Anderb. | 24 | 3.58 | 5 | 4.59 | 4.08 |
| Euphorbia terracina L. | 18 | 2.68 | 5 | 4.59 | 3.63 |
| Geranium lilacium Kunth | 14 | 2.11 | 5 | 4.59 | 3.35 |
| Bidens triplinervia Kunth | 13 | 2.00 | 5 | 4.59 | 3.29 |
| Erigeron longipes DC. | 23 | 3.39 | 3 | 2.75 | 3.07 |
| Salvia lavanduloides Kunth | 10 | 1.43 | 5 | 4.59 | 3.01 |
| Oxalis corniculata L. | 9 | 1.28 | 5 | 4.59 | 2.93 |
| Arenaria reptans Hemsl. | 8 | 1.21 | 5 | 4.59 | 2.90 |
| Hypericum silenoides Juss. | 7 | 1.02 | 5 | 4.59 | 2.80 |
| Ammi majus L. | 9 | 1.32 | 4 | 3.67 | 2.49 |
| Sibthorpia repens (Mutis ex L.) Kuntze | 14 | 2.07 | 2 | 1.83 | 1.95 |
| Taraxacum officinale G. H. Weber ex Wigg. | 5 | 0.75 | 3 | 2.75 | 1.75 |
| Festuca elatior L. | 5 | 0.75 | 2 | 1.83 | 1.29 |
| Oxalis alpina (Rose) Rose ex R. Knuth | 5 | 0.75 | 2 | 1.83 | 1.29 |
| Erigeron sp. | 4 | 0.57 | 2 | 1.83 | 1.20 |
| Fragaria vesca L. | 2 | 0.23 | 2 | 1.83 | 1.03 |
| Conyza schiedeana (Less) Cronquist | 1 | 0.19 | 2 | 1.83 | 1.01 |
| Halenia brevicornis (Kunth) G. Don | 1 | 0.08 | 2 | 1.83 | 0.96 |
| Circium rhaphilepis (Hemsl.) Petrak | 4 | 0.57 | 1 | 0.92 | 0.74 |
| Erigeron karvinskianus DC. | 4 | 0.57 | 1 | 0.92 | 0.74 |
| Bromus catharticus Vahl | 1 | 0.19 | 1 | 0.92 | 0.55 |
| Galium praetermissum Greenm | 1 | 0.11 | 1 | 0.92 | 0.52 |
| Potentilla candicans Bonpl | 1 | 0.11 | 1 | 0.92 | 0.52 |
| Astragalus coccineus (Parry) Brandegee | 1 | 0.08 | 1 | 0.92 | 0.50 |
| 663 | 100 | 109 | 100 | 100 | |
| ZR5 | |||||
| Muhlenbergia macroura (Kunth) Hitchc | 84 | 12.03 | 4 | 3.33 | 7.68 |
| Astragalus lyonnetii Barneby | 78 | 11.16 | 4 | 3.33 | 7.25 |
| Bidens triplinervia Kunth | 66 | 9.44 | 5 | 4.17 | 6.80 |
| Piptochaetium virescens (Kunth) Parod | 62 | 8.83 | 5 | 4.17 | 6.50 |
| Arenaria lycopodioides Willd. ex Schltdl. | 43 | 6.17 | 5 | 4.17 | 5.17 |
| Heterotheca inuloides Cass. | 40 | 5.74 | 5 | 4.17 | 4.96 |
| Eryngium carlinae F. Delaroche | 36 | 5.10 | 5 | 4.17 | 4.63 |
| Erigeron karvinskianus DC. | 28 | 3.98 | 5 | 4.17 | 4.08 |
| Rumex acetosella L. | 21 | 3.02 | 5 | 4.17 | 3.59 |
| Erigeron sp. | 24 | 3.37 | 4 | 3.33 | 3.35 |
| Baccharis conferta Kunth | 16 | 2.29 | 5 | 4.17 | 3.23 |
| Erigeron longipes DC. | 28 | 3.95 | 3 | 2.50 | 3.22 |
| Senecio salignus DC. | 14 | 2.08 | 5 | 4.17 | 3.12 |
| Geranium lilacium Kunth | 14 | 1.97 | 5 | 4.17 | 3.07 |
| Astragalus coccineus (Parry) Brandegee | 24 | 3.41 | 3 | 2.50 | 2.96 |
| Hypericum silenoides Juss. | 11 | 1.58 | 5 | 4.17 | 2.87 |
| Trifolium repens L. | 10 | 1.36 | 5 | 4.17 | 2.77 |
| Viola hookeriana H.B.K | 17 | 2.48 | 3 | 2.50 | 2.49 |
| Pseudognaphalium roseum (Kunth) Anderb. | 5 | 0.72 | 5 | 4.17 | 2.44 |
| Plantago nivea Kunth | 17 | 2.37 | 3 | 2.50 | 2.43 |
| Potentilla candicans Bonpl | 16 | 2.33 | 3 | 2.50 | 2.42 |
| Euphorbia terracina L. | 8 | 1.15 | 4 | 3.33 | 2.24 |
| Oxalis corniculata L. | 8 | 1.15 | 4 | 3.33 | 2.24 |
| Festuca elatior L. | 3 | 0.43 | 4 | 3.33 | 1.88 |
| Ammi majus L. | 5 | 0.65 | 3 | 2.50 | 1.57 |
| Conyza schiedeana (Less) Cronquist | 2 | 0.32 | 3 | 2.50 | 1.41 |
| Salvia prunelloides Kunth | 6 | 0.83 | 2 | 1.67 | 1.25 |
| Oxalis alpina (Rose) Rose ex R. Knuth | 4 | 0.54 | 2 | 1.67 | 1.10 |
| Halenia brevicornis (Kunth) G. Don | 2 | 0.25 | 2 | 1.67 | 0.96 |
| Lepechinia schiedeana (Schltdl.) Vatke | 8 | 1.08 | 1 | 0.83 | 0.96 |
| Taraxacum officinale G. H. Weber ex Wigg. | 1 | 0.11 | 1 | 0.83 | 0.47 |
| Circium rhaphilepis (Hemsl.) Petrak | 1 | 0.07 | 1 | 0.83 | 0.45 |
| Arenaria reptans Hemsl. | 0 | 0.04 | 1 | 0.83 | 0.43 |
| 696 | 100 | 120 | 100 | 100 | |
| ZR9 | |||||
| Muhlenbergia macroura (Kunth) Hitchc | 253 | 36.68 | 5 | 6.10 | 21.39 |
| Arenaria lycopodioides Willd. ex Schltdl. | 76 | 11.08 | 5 | 6.10 | 8.59 |
| Rumex acetosella L. | 67 | 9.73 | 5 | 6.10 | 7.92 |
| Piptochaetium virescens (Kunth) Parod | 39 | 5.67 | 5 | 6.10 | 5.88 |
| Oxalis corniculata L. | 37 | 5.30 | 5 | 6.10 | 5.70 |
| Astragalus lyonnetii Barneby | 43 | 6.21 | 4 | 4.88 | 5.54 |
| Potentilla candicans Bonpl | 46 | 6.72 | 2 | 2.44 | 4.58 |
| Oxalis alpina (Rose) Rose ex R. Knuth | 26 | 3.78 | 4 | 4.88 | 4.33 |
| Baccharis conferta Kunth | 8 | 1.18 | 5 | 6.10 | 3.64 |
| Senecio salignus DC. | 8 | 1.18 | 5 | 6.10 | 3.64 |
| Erigeron karvinskianus DC. | 15 | 2.11 | 4 | 4.88 | 3.49 |
| Bidens triplinervia Kunth | 13 | 1.85 | 4 | 4.88 | 3.37 |
| Heterotheca inuloides Cass. | 11 | 1.60 | 4 | 4.88 | 3.24 |
| Astragalus coccineus (Parry) Brandegee | 17 | 2.40 | 3 | 3.66 | 3.03 |
| Trifolium repens L. | 5 | 0.65 | 4 | 4.88 | 2.77 |
| Ammi majus L. | 4 | 0.51 | 3 | 3.66 | 2.08 |
| Festuca elatior L. | 2 | 0.22 | 3 | 3.66 | 1.94 |
| Erigeron sp. | 7 | 0.94 | 2 | 2.44 | 1.69 |
| Geranium lilacium Kunth | 3 | 0.44 | 2 | 2.44 | 1.44 |
| Eryngium carlinae F. Delaroche | 2 | 0.22 | 2 | 2.44 | 1.33 |
| Fragaria vesca L. | 4 | 0.54 | 1 | 1.22 | 0.88 |
| Galium praetermissum Greenm | 3 | 0.36 | 1 | 1.22 | 0.79 |
| Plantago nivea Kunth | 3 | 0.36 | 1 | 1.22 | 0.79 |
| Circium rhaphilepis (Hemsl.) Petrak | 1 | 0.18 | 1 | 1.22 | 0.70 |
| Bromus catharticus Vahl | 0 | 0.04 | 1 | 1.22 | 0.63 |
| Hypericum silenoides Juss. | 0 | 0.04 | 1 | 1.22 | 0.63 |
| 688 | 100 | 82 | 100 | 100 | |
| BR | |||||
| Piptochaetium virescens (Kunth) Parod | 64 | 19.70 | 5 | 9.09 | 14.40 |
| Geranium lilacium Kunth | 61 | 18.85 | 3 | 5.45 | 12.15 |
| Muhlenbergia macroura (Kunth) Hitchc | 46 | 14.24 | 4 | 7.27 | 10.75 |
| Fleischmannia pycnocephala (Less.) R.M. King & Rob. | 32 | 9.93 | 5 | 9.09 | 9.51 |
| Baccharis conferta Kunth | 20 | 6.18 | 5 | 9.09 | 7.64 |
| Lepechinia schiedeanaa (Schltdl.) Vatke | 20 | 6.16 | 4 | 7.27 | 6.71 |
| Aegopogon cenchroides Humb. & Bonpl. ex Willd | 29 | 8.93 | 2 | 3.64 | 6.28 |
| Senecio salignus DC. | 8 | 2.55 | 5 | 9.09 | 5.82 |
| Fragaria vesca L. | 9 | 2.77 | 4 | 7.27 | 5.02 |
| Bidens triplinervia Kunth | 13 | 3.85 | 2 | 3.64 | 3.74 |
| Bromus catharticus Vahl | 2 | 0.46 | 3 | 5.45 | 2.96 |
| Roldana lineolata (DC.) H. Rob & Brettell | 7 | 2.08 | 2 | 3.64 | 2.86 |
| Galium praetermissum Greenm | 3 | 1.00 | 2 | 3.64 | 2.32 |
| Oxalis alpina Rose ex R. Knuth | 1 | 0.31 | 2 | 3.64 | 1.97 |
| Rumex acetosella L. | 6 | 1.69 | 1 | 1.82 | 1.76 |
| Ammi majus L. | 0 | 0.08 | 1 | 1.82 | 0.95 |
| Trifolium repens L. | 0 | 0.08 | 1 | 1.82 | 0.95 |
| Viola hookeriana H.B.K | 0 | 0.08 | 1 | 1.82 | 0.95 |
| 325 | 100 | 55 | 100 | 100 |
La composición de especies del sotobosque está regulada por la presencia de un dosel superior que determina la entrada de luz (cantidad y calidad) y por tanto su disponibilidad para favorecer a las especies demandantes de luz en el proceso de germinación y ocupación del sitio (Rendón-Pérez et al., 2021). Lo anterior, parece ser el caso de M. macroura que estuvo presente en las cuatro zonas de estudio, notándose los mayores valores en SD, ZR5, y ZR9 (Tabla 4), donde no existe un dosel cerrado que impida la entrada de luz. En cambio, en el BR la cobertura del dosel es mayor comparado con el dosel de las reforestaciones, por lo que el ingreso de luz es menor, a su vez puede haber mayor humedad y nutrimentos en el suelo, lo que favorece la presencia de otras especies en el sotobosque y que se ve reflejado en los menores valores del índice de Jaccard al compararse con las demás zonas (Tabla 3). Muhlenbergia macroura tiene una distribución natural en ecosistemas de praderas alpinas y subalpinas (zacatonales) en el Eje Neovolcánico Transversal en bosques de pino, encino, encino-pino y oyamel y en altitudes que van de los 1800 a 4000 m (Mejía-Saules, 1993), condiciones que concuerdan con el área del presente estudio.
Conclusiones
El sotobosque es un componente importante en la riqueza y diversidad en las reforestaciones, particularmente las especies herbáceas. Los resultados, en general, corroboran la hipótesis planteada, ya que el sotobosque fue menos diverso a medida que la edad de las reforestaciones aumentó; aunque en términos de composición esto no sucedió, ya que el BR fue el que menos similitud presentó con las demás condiciones (ZD, ZR5 y ZR9). La especie Muhlenbergia macroura representó el mayor IVIR dentro del sotobosque, lo que la cataloga con un valor de importancia estructural alto en las reforestaciones evaluadas.
Es importante dar seguimiento a estas reforestaciones, llevando a cabo evaluaciones a corto, mediano y largo plazo para obtener un panorama más amplio sobre los cambios de distintos atributos, funciones y procesos. Los resultados indican que el identificar los cambios que ocurren en la composición y diversidad del sotobosque a medida que la estructura horizontal de las reforestaciones cambia, puede ser un referente para determinar si las prácticas implementadas están contribuyendo a la recuperación de una zona o ecosistema degradado. La reforestación como estrategia para la recuperación del ecosistema parece estar funcionando en el área de estudio, sin embargo, se necesita continuar con las observaciones tanto de la composición de especies del sotobosque como de otros procesos ecológicos.