Introducción
El acto quirúrgico es un evento complejo1, la fluidoterapia tiene como objetivo mantener al paciente en un estado de euvolemia, evitando la hipovolemia e hipervolemia, ambas relacionadas a complicaciones perioperatorios2. El monitoreo básico: presión arterial media (PAM), frecuencia cardiaca (FC), gasto urinario (GU), por sí solos no pueden tomarse como guía para la reposición de volumen intravascular3. La cinética de fluidos ha sugerido de manera experimental que el GU se ve disminuido durante el acto anestésico independientemente de la técnica, pudiendo ser normal un GU 0.3-0.5 mL/kg/hr durante este periodo4, pero por el momento no hay evidencia clínica que avale esto. Shoemaker en los 705 propone el concepto de «indices hemodinámicos supranormales» para guiar la reanimación en pacientes críticos. Después Rivers6 publica sus resultados con la «terapia guiada por metas» en pacientes sépticos, sin embargo, estos resultados nunca se han vuelto a reproducir 7-9. En perioperatorio se ha introducido el término de fluidoterapia guiada por metas (GDFT por sus siglas en inglés), desde 2012 con los trabajos de Brandstrup10. El advenimiento del monitoreo dinámico, basado en las interacciones cardiopulmonares (variabilidad del volumen sistólico [VVS], variabilidad de la presión de pulso [DPP], variabilidad pletismográfica [PVi]), trata de predecir una respuesta a volumen, también se ha introducido como una herramienta más para tratar de guiar la fluidoterapia en el periodo perioperatorio. Un metanálisis publicado en 202211 sugirió ventajas modestas con el uso de este abordaje, en términos económicos y términos de recuperación en los pacientes. El daño renal por congestión se ha descrito en el perioperatorio12,13. Por último, el término «tolerante al volumen» hace referencia al impacto que pueda causar la congestión de volumen en los pacientes14. Hasta el momento, ningún trabajo ha explorado la correlación existente entre este abordaje con el GU durante el acto anestésico, por lo tanto, no estamos seguros de la verdadera utilidad del GU como herramienta para complementar una guía en términos de fluidoterapia. El presente trabajo tiene la hipótesis de que el tipo de régimen para guiar la fluidoterapia no se correlaciona con el GU durante el periodo transanestésico.
Material y métodos
Se realizó una cohorte prospectiva durante el periodo comprendido de enero 2022 a enero 2023, en el Hospital de Especialidades del Centro Médico La Raza del Instituto Mexicano del Seguro Social (IMSS). El trabajo cuenta con aprobación por los comités de Ética e Investigación R-2022-3501-177. Se siguieron las pautas dictadas por las guías ESTROBE (Strengthening the Reporting of Observational studies in Epidemiology)15. Para la protección de datos personales a cada paciente se le asignó una codificación alfanumérica y se firmó un consentimiento informado. En la población de estudio, los pacientes fueron mayores de edad programados de forma electiva para cirugía abdominal bajo anestesia, sin enfermedad hepática, renal, cardiaca o enfermedad de Raynaud. Se excluyeron los pacientes que fueron egresados a la unidad de cuidados intensivos (UCI). Las variables recolectadas se clasificaron en demográficas (edad, sexo), variables de estudio (GU [total de uresis producida durante la cirugía entre el peso del paciente por unidad de tiempo-hora], tipo de fluidoterapia [convencional, GFDT], tipo de solución [solución Hartmann o NaCl 0.9%], total de ingresos).
Protocolo de anestesia
Todos los pacientes se manejaron con anestesia general balanceada, se les monitorizó de forma convencional: presión arterial no invasiva (PANI), pulsioximetría, electrocardiógrafo, temperatura y train of four, para la inducción se utilizó: fentanilo 3-5 μg/kg, lidocaína 1 mg/kg, propofol 1-1.5 mg/kg, rocuronio 0.06 mg/kg o cisatracurio 0.1 mg/kg, para el mantenimiento sevoflorano a 0.8-1 concentración alveolar mínima (CAM). El régimen de terapia convencional consistió en guiar la fluidoterapia con base en la hoja de balance de líquidos, mientras que GDFT (PVi) se basó en mantener un valor < 14, con ayuda de la administración de minirretos (250 mL) con solución cristaloide (Hartmann / NaCl 0.9%) según lo reportado por Mühlbacher16; en caso de presentar hipotensión arterial (PAM < 65 mmHg o PAM > 20% con respecto a la basal) se administró efedrina a dosis convencionales. A todos los pacientes se les colocó sonda Foley para monitorizar GU.
Objetivo principal
Explorar la correlación existente entre el tipo de régimen de fluidoterapia con el GU durante el periodo transanestésico. El objetivo secundario es explorar la correlación entre el tipo de solución con el GU.
Estadística y cálculo de muestra
Para el cálculo de tamaño de muestra se utilizó casuística reportada por Virág11 con un poder estadístico de 80% (1-β = 0.80) y una significancia de 95% (α = 0.05) de dos colas, dando el resultado de 26 pacientes (13 pacientes por grupo). Los datos cuantitativos se presentaron como mediana (rango intercuartil), mientras que los cualitativos con frecuencia (porcentaje). Los resultados se presentan en forma de risk ratio (RR) junto al IC95% y valor de p. Se tomó como significancia estadística p < 0.05. Para el análisis estadístico se utilizará el programa Rstudio (versión 25).
Resultados
De los 35 pacientes incluidos, sólo uno fue excluido, 50% fueron mujeres con mediana de edad de 16 años (rango intercuartil [RIQ] 42.5-61.5 años), uresis 0.60 mL/kg/hr (0.30-0.86 mL/kg/hr) e ingresos 1,625 mL (1,138-2,290 mL), en términos de soluciones, hubo un mayor uso de Hartmann (59.4%). El resto de la descripción de las variables se muestra en la Tabla 1.
Tabla 1: Descripción general de todas las variables del estudio (N = 32).
| Variables | n (%) |
|---|---|
| Edad (años)* | 50 [42.5-61.5] |
| Sexo (femenino) | 16 (50) |
| Solución | |
| Salina | 13 (40.6) |
| Hartmann | 19 (59.4) |
| Terapia | |
| Guiada por metas | 16 (50) |
| Convencional | 16 (50) |
| Uresis (mL/kg/hr)* | 0.60 [0.30-0.86] |
| Ingresos (mL)* | 1,625 [1,138-2,290] |
* Datos presentados como mediana [RIQ].
Al momento de comparar grupos, se observó una mayor edad en el grupo GDFT, 52 vs 48 años, p = 0.38, mientras que en el grupo convencional mayores ingresos 1,675 mL (1,162.5-2,447.5 vs 1,086-2,037.5), p = 0.46 y uresis 0.69 (0.35-0.89 vs 0.30-0.80), p = 0.42; sin embargo, sin significancia estadística (Figura 1).
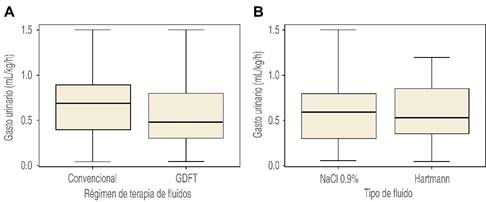
Figura 1: Comparación del gasto urinario con el tipo de régimen utilizado (A), y con el tipo de fluido utilizado (B).
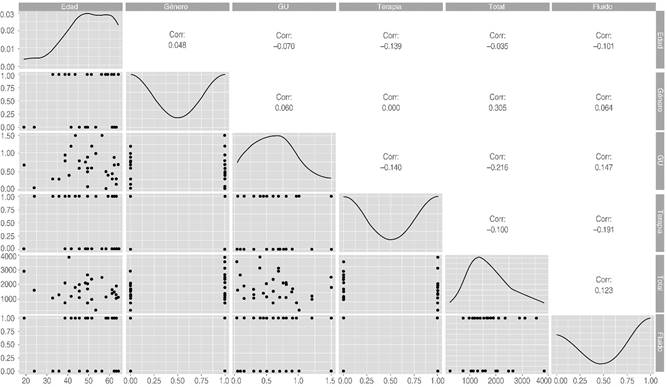
En términos de comparación con base en el tipo de solución, el grupo de Hartmann presentó mayor uresis, 0.68 vs 0.5 mL/kg/hr respectivamente, sin ser tampoco estadísticamente significativo, p = 0.40. El resto de las comparaciones se muestra en las Tablas 2 y 3. El análisis de matriz de correlación no mostró ninguna correlación significativa (Figura 2).
Tabla 2: Comparación de datos demográficos y de estudio entre pacientes con régimen convencional y guiados por metas de fluidoterapia (N =32).
| Variables | Metas N = 16 n (%) |
Convencional N = 16 n (%) |
p |
|---|---|---|---|
| Edad (años)* | 48 [39.5-61.5] | 52 [46.7-61.2] | 0.38 |
| Sexo (femenino) | 10 (62.5) | 6 (37.5) | 0.34 |
| Uresis (mL/kg/hr)* | 0.47 [0.30-0.80] | 0.69 [0.35-0.89] | 0.42 |
| Ingresos (mL)* | 1,500 [1,086-2,037.5] | 1,675 [1,162.5-2,447.5] | 0.46 |
| Solución | |||
| Hartmann | 11 (68.8) | 8 (50) | |
| NaCl 0.9% | 5 (31.3) | 8 (50) |
* Datos presentados como mediana [RIQ].
Las comparaciones se realizaron por la prueba U de Mann-Whitney o por la prueba de χ2.
Tabla 3: Comparación de datos demográficos y de estudio entre pacientes con solución Hartmann y NaCl 0.9% (N = 32).
| Variables | Hartmann N = 19 n (%) |
NaCl 0.9% N = 13 n (%) |
p |
|---|---|---|---|
| Edad (años)* | 51 [44-62] | 50 [38.5 - 60] | 0.70 |
| Sexo (femenino) | 9 (47.4) | 7 (53.8) | 0.71 |
| Uresis (mL/kg/hr)* | 0.68 [0.40 - 0.90] | 0.5 [0.22 - 0.84] | 0.40 |
| Ingresos (mL)* | 1,700 [1,200 - 2,350] | 1,500 [1,064 - 2,265] | 0.40 |
| Régimen | |||
| Convencional | 11 (57.9) | 5 (38.5) | |
| GDFT | 8 (42.1) | 8 (61.5) |
GDFT = fluidoterapia guiada por metas.
* Datos presentados como mediana [RIQ].
Las comparaciones se realizaron por la prueba U de Mann-Whitney o por la prueba de χ2.
El modelo GLM no mostró ninguna relación estadísticamente significativa en el análisis univariado para el GU, estos resultados se mantuvieron incluso después del ajuste del modelo por edad, sexo y total de ingresos (R2 0.14). Los resultados del modelo se muestran en la Tabla 4.
Tabla 4: Modelo lineal generalizado para determinar las variaciones del gasto urinario con base en las variables del estudio.
| Modelo | Modelo univariado | Modelo multivariado | ||||
|---|---|---|---|---|---|---|
| β | RR (IC95%) | p | β | β (IC95%) | p | |
| Edad (años) | –0.002 | –0.38 (–0.01-0.009) | 0.70 | –0.004 | –0.67 (–0.01-0.007) | 0.50 |
| Sexo (femenino) | 0.04 | 0.33 (–0.22-0.32) | 0.74 | 0.01 | 0.76 (–0.17-0.04) | 0.44 |
| Ingresos (mL) | 0.0009 | –1.21 (–0.0002-0.00006) | 0.23 | –0.0001 | –1.54 (–0.0003-0.00003) | 0.13 |
| Tipo de régimen | –0.10 | –0.77 (–0.37-0.16) | 0.44 | –0.012 | –0.83 (–0.40-0.01) | 0.41 |
| Tipo de solución | 0.11 | 0.81 (–0.16-0.39) | 0.42 | 0.012 | 0.83 (–0.16-0.04) | 0.41 |
Datos presentados como Coeficiente de regresión (β), Risk ratio (RR) e intervalo de confianza al 95% (IC95%). R2 = 0.14
Discusión
Hasta donde sabemos, este es el primer trabajo en explorar la correlación entre el tipo de fluidoterapia utilizada y el GU durante el transanestésico. El GU por sí solo tiene poca especificidad como marcador de daño renal17. Oliguria es un GU < 0.5 mL/kg/hr, durante el transanestésico la uresis podría verse disminuida por vasodilatación, redistribución de volumen más lento del compartimiento central al periférico4, aumento de los patrones moleculares asociados a daño (DAMPs) y aumento de la presión intraabdominal (cirugía laparoscópica)18. Sin embargo, el verdadero papel del GU durante el transanestésico aún no queda claro, el trabajo de Quan19 reporta que la medición del GU en el periodo postoperatorio junto a los niveles séricos de creatinina (Cr) mejoran la sensibilidad del diagnóstico de lesión renal aguda (LRA). De manera similar, Jin20 también sugiere que el monitoreo del GU mejora el diagnóstico de LRA en el contexto de paciente crítico. Por último, el trabajo de Gameiro21 también refiere la disminución del GU en el contexto del diagnóstico de LRA. En resumen, la LRA asociada a un GU bajo es común, pero también menos severa cuando se compara con LRA acompañada de alteraciones asiladas de Cr19-21. Los pacientes guiados de forma convencional recibieron más volumen sin ser estadísticamente significativo, resultados congruentes con lo reportado en otros trabajos. Lui22 en cirugía colorrectal laparoscópica reportó que no existe significancia estadística en el total de cristaloides utilizados, pero al igual que nosotros, al grupo control se le administraron más fluidos, 2,001.4 vs 1,979 mL, p = 0.63 grupo GDFT; este mismo estudio reportó una uresis más elevada en el grupo GDFT en comparación con el grupo control, 515.4 mL vs 547.6 mL, al contrario de nuestros resultados, en los cuales, pacientes con régimen convencional presentaron más GU, hay que tomar en cuenta que en el estudio se reportó como uresis total. Mühlbacher16 al igual que nosotros no reporta diferencia estadística en términos de total de fluidos administrados entre grupos: GDFT vs control 1,357 mL (393) vs 1363 mL (434). Por último, Tang23 en gastrectomía laparoscópica sí reporta diferencia significativa entre grupos GDFT vs rutina 786.71 (305.9) vs 1,182.5 (341.8), p ≤ 0.001; en este trabajo, sí se reporta la uresis total, siendo menor en el grupo GDFT 245.4 mL vs 367.6 mL, p = 0.009, otra vez. Un metaanálisis11 reportó que la GDFT se relaciona con menos administración de líquidos durante transanestésico, lo que llama la atención es que sólo realizaron un modelo de efectos fijos a pesar de presentar alta heterogeneidad entre estudios incluidos (I2 96.9%). Limitaciones. Primero, no se estandarizó el control de una de las principales variables fuertemente asociadas a LRA postoperatoria, la PAM18,24; segundo, no se midió ningún tipo de desenlaces en términos de función renal con algún tipo de biomarcador (Cr); tercero, no existe dicotomización entre los casos laparoscópicos y los casos abiertos, por ende, no pudimos correlacionar el tiempo de pneumoperitoneo el cual ha sido sugerido en los últimos años como un posible factor de riesgo para LRA.
Conclusión
A pesar de no existir significancia estadística entre grupos, guiar fluidoterapia con un abordaje GDFT disminuye el total de fluidos administrados a los pacientes. Sin embargo, no queda clara la asociación existente entre el GU y los diferentes regímenes de fluidoterapia, porque, la anestesia general parece disminuir el GU, por este motivo, no debe de sugerirse guiar la fluidoterapia basándose exclusivamente en el GU como meta. Hacen falta ensayos clínicos para corroborar la existencia de una posible asociación entre estas variables, además para determinar el verdadero impacto clínico que esta pudiese causar.