INTRODUCCIÓN
Las actividades mineras en México comenzaron a inicios de la época Colonial en el año 1600, principalmente en los estados de Zacatecas, San Luis Potosí, Chihuahua y Guanajuato (Gaytán-Alfaro y Benita 2014), gracias a ello actualmente el país tiene relevancia a nivel internacional (SE 2022). La explotación minera fue y sigue siendo una actividad relacionada con la contaminación ambiental, principalmente de los suelos, limitándolos física, química y biológicamente para el establecimiento de vegetación, así como la contaminación visual generada por el alto volumen de desechos que se han correlacionado con problemas de salud y destrucción de hábitats (Covarrubias y Cabriales 2017). Tal es el caso del Distrito Minero de Cerro de San Pedro que se localiza en la porción centro sur del estado de San Luis Potosí, a 19.5 km al noreste de la ciudad de San Luis Potosí, capital del mismo estado. Se tiene documentado que en estas minas se explotaron sulfuros minerales, entre los que se encontró galena, esfalerita, calcopirita, tetraedrita y arsenopirita, que pueden ser las fuentes principales de plomo, zinc, cobre y arsénico (Monroy 2010). Asímismo, los jales mineros con alto contenido de polisulfuros metálicos, al estar expuestos al aire y agua se oxidan y generan drenaje ácido de minas (DAM), que propicia acidez del suelo y migración de compuestos que pueden liberar elementos potencialmente tóxicos (EPT), como el arsénico y los metales pesados (Burillo et al. 2017). La movilización de los EPT está relacionada con las condiciones del suelo como el pH (condiciones de acidez) y de Eh (condiciones óxido-reductoras) las cuales, además, determinan el estado de oxidación del As y consecuentemente su especiación en solución. Asímismo, la variación de estos parámetros puede aumentar la movilización de los EPT así como su biodisponibilidad, llevando en consecuencia a su absorción desde el suelo hacia las plantas (USEPA 1992). El arsénico se encuentra presente en la corteza terrestre en una concentración promedio de 0.0005 % (OMS 2012). Su enriquecimiento natural en la superficie terrestre se debe principalmente a las erupciones volcánicas y al hidrotermalismo; mientras que las actividades antrópicas que contribuyen a su aumento en la superficie terrestre son la minería de yacimientos polimetálicos y del carbón, así como el uso de recursos geotérmicos para la generación de electricidad. La posterior dispersión del arsénico se efectúa por mal manejo de los residuos, o la aplicación de plaguicidas o herbicidas que lo contienen, que han distribuido el As en amplias zonas geográficas (Huang et al. 2020). Por otro lado, los efectos de la exposición crónica al arsénico en humanos ocasionan cáncer, enfermedades cardiovasculares y problemas neurológicos, entre otros (Quansah et al. 2015). Se han correlacionado las concentraciones de arsénico y su especiación con la fracción fitodisponible, que es aquella capaz de ser bioacumulada por una planta (Vazquez Rodríguez 2007). En el sitio de estudio, se estima que existen altas concentraciones de arsénico que puedan superar los límites máximos permisibles en suelos, definidos en la NOM 147 SEMARNAT 2004 (DOF 2005).
El área geográfica de interes es representativa de otros sitios con clima semiárido donde la extracción minera ha sido una actividad que ha generado pasivos ambientales con EPT. De acuerdo con Tessier et al. (1979), la movilidad relativa permite diferenciar siete fracciones geoquímicas: soluble, intercambiable (cationes y aniones), ligada a carbonatos, ligada a óxidos de hierro y manganeso, ligada a materia orgánica y sulfuros así como la fracción residual. Con estas se puede determinar el potencial de movilización, mediante otros protocolos realizados para evaluar fitoaccesibilidad y la acumulación de arsénico en la planta (Covarrubias et al. 2017). El objetivo de este estudio fue evaluar la concentración de arsénico en sedimentos y suelos rizosféricos, así como, mediante un protocolo de extracción secuencial, diferenciar en qué fracciones geoquímicas se encuentra preferentemente ligado.
MATERIALES Y MÉTODOS
Zona de estudio
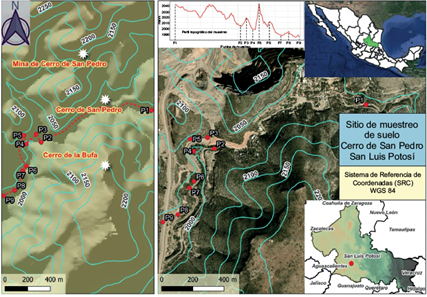
El presente estudio se desarrolló en la localidad del Cerro de San Pedro, San Luis Potosí, México ubicado a una altitud de 2089 msnm con coordenadas de 100º 47’ 49’’ de longitud oeste y 22º12’48’’ de latitud norte (Fig. 1).
Muestreo
Los puntos de muestreo se ubicaron abarcando un gradiente longitudinal de 2.9 km, iniciando en una zona no impacatada por el drenaje acído de mina y continuando sobre el arroyo San Pedro, pasando por la zona impactada con un desnivel de aproximadamente 50 m al punto final de muestreo (Fig. 1). El tipo de muestreo fue dirigido, considerando que en cada punto seleccionado se encontró la especie vegetal Asphodelus fistolusus, seleccionada como un bioindicador de contaminación de arsénico. Se recoletaron tres diferentes tipos de muestras: especies vegetales (A. fistulosus), sedimentos del arroyo (S) y suelos rizosféricos (SR) circundantes a las raíces de las plantas de A. fistulosus. Se obtuvieron cinco puntos de muestreo considerando la presencia de A. fistulosus. Los puntos de muestreo de suelos se identificaron como: 1S, 1SR al 5S, 5SR, con dos repeticiones. Los sedimentos se colectaron de 0 a 10 cm de profundidad, de acuerdo con la NOM-021-RECNAT-2000 (SEMARNAT 2002), mientras que los suelos rizosféricos se tomaron circundantes a las especies vegetales colectadas. Todas las muestras se coletaron con dos repeticiones y se realizaron medias estadísticas (Fig. 2).
Preparación de las muestras
Los tres tipos de muestras, sedimentos, suelos rizosféricos y plantas de A. fistulosus, se depositaron en bolsas de plástico herméticas etiquetadas para posteriormente ser transportadas al laboratorio del Instituto de Metalurgia de la Universidad Autónoma de San Luis Potosí.
Muestras de suelos rizosféricos y sedimentos
Las muestras de suelos rizosféricos (SR) y sedimentos (S) se secaron en un horno a una temperatura de 50º C hasta peso constante, posteriormente se tamizaron a tamaño de partícula menor a 600 micras, se almacenaron en frascos de plástico previamente lavados con HNO3 al 10 %. Se guardaron en un lugar libre de humedad hasta su análisis (Vázquez Rodríguez 2007).
Procesamiento de las muestras de A. fistulosus
Las plantas se seccionaron en hojas y raíces. Se tomaron dos plantas por sitio de muestreo y se determinó la concentración de arsénico en hojas y raíces. El lavado de las plantas se realizó de la siguiente manera: 1) se enjuagaron las plantas con agua desionizada hasta cubrir la totalidad de la muestra; 2) se realizaron tres lavados en una sonda de ultrasonido, el primero fue con una solución de EDTA a 50 mM durante 30 min, la segunda solución se preparó con HNO3 a 0.1 N durante 10 min y por último con la solución de hexametafosfato de sodio (NaSPO3)6 1M durante 15 min; 3) finalmente se volvieron a enjuagar las muestras con agua desionizada hasta cubrir la totalidad de las muestras. Una vez lavadas las secciones de las plantas se secaron en una estufa a una temperatura de 50 ºC hasta peso constante (Ortega Morales 2012).
Determinación de la concentración total de As
A todas las muestras (plantas, sedimento y suelo rizosférico) se les cuantificó la concentración de arsénico mediante digestión con horno de microondas (CEM, MARSX3100), utilizando 0.5 g de muestra a la que se le agregó una solución ácida de HNO3/HCl en una relación 3:2 v/v, con una presión de 0 a 300 psi por 10 min y una rampa de temperatura hasta 150 ºC, con un enfriamiento de 5 min. Posteriormente, las muestras obtenidas fueron filtradas con papel Whatman No. 5 (poro de 2.5 μm) y analizadas por horno de grafito con espectrometría de absorción atómica (EAA-HG, Analyst 200 PinAAcle 900T, Perkin Elmer). El procedimiento se realizó por duplicado para cada análisis y se empleó como material de referencia el NIST 2711, obteniendo un 87 % de recuperación para arsénico.
Determinación de pH y carbonatos
La medición del pH se hizo de acuerdo con el métodos EPA 9045C para los sedimentos y suelos rizosféricos, que consiste en mezclar suelo con agua destilada (relación 1:5) durante 10 min, después se usó un electrodo combinado de Ross conectado a un potenciómetro con compensador de temperatura y calibrado con sustancias amortiguadoras patrón 4, 7 y 10.
La evaluación por difracción de rayos X mostró la presencia principalmente de calcita, por lo que se realizó la determinación de carbonatos por titulación volumétrica de la desgasificación de CO2 por ácidificación de la muestra sólida (Ortega Morales 2012).
Extracción secuencial sucesiva
La extracción secuencial sucesiva incluyó siete fracciones: fracción soluble (SOL), medida en agua meteórica, que corresponde a CO2 en equilibrio con agua desionizada para simular el agua de lluvia; fracción intercambiable cationicamente (INTC); fracción de arsénico asociado a carbonatos (CAR); fracción de arsénico intercambiable aniónicamente (INTA); fracción ligada a oxihidróxidos de hierro y manganeso (OFM), fracción asociada a materia orgánica (MO), y la fracción residual (RES), siendo aquella prácticamente no lábil (Tessier 1979).
A 1 g de muestra sólida (i.e. sedimento o suelos rizosféricos) se le agregó 16 mL de agua, se ajustó el pH a 5.5, se agitó por 20 min, se centrifugó a 3000 rpm y se filtró con papel PTFE a 0.20 µm en un matraz de 25 mL. La solución filtrada se acidificó con tres gotas de HNO3 para su posterior análisis químico. Asimismo por cada fracción se agregó sucesivamente solución del suelo remanente contenido en el vial, tal como se describe en el cuadro I.
CUADRO I PROCEDIMIENTO DE EXTRACCIÓN SECUENCIAL (VÁZQUEZ RODRÍGUEZ 2007).
| Fracción | Condiciones |
| SOL | *H2O desionizada a un pH 5.5,agitación 20 min a 3000 rpm |
| INT | *(Mg NO3)2 ̵ 6 H2O (0.5M), agitación 20 min a 3000 rpm |
| CAR | *CH3COONa (1M) pH 5.5, agitación 5 h a 3000 rpm |
| INTA | *NaH2PO4 Agitación por 2 periodos de 24 h. Periodo 1 (1M), Periodo 2 (1.5 M) a 3000 rpm. |
| OFM | *NH4OH.HCl (1 M) a 25 %v/v con CH3COOH, 96 ºC por 3 h, agitación 20 min a 3000 rpm |
| MO | *H2O2 al 30% a pH 2 ajustado con HNO3, segunda etapa al 37% *CH3COONH4 (3.2M) v/v, con HNO3 96 ºC por 5 h, agitación 20 min a 3000 rpm |
| RES | *Digestión en horno de microondas, HNO3:HCl 3:2 v/v, 0-300psi, 150 ºC |
Soluble a agua meteórica (SOL), Intercambiable catiónico (INT), Carbonatos (CAR),Intercambiable anicónico (INTA), Oxihidroxidos de Fe y Mn (OFM), Materia orgánica y Sulfuros (MO), Residual (RES)
Fitoaccesibilidad
El procedimiento utilizado consta de poner el suelo rizosférico en contacto con una solución sintética que simula la composición de ácidos carboxílicos de los exudados de las raíces de las plantas, tal como fue propuesto por Cieslinski y Van-Res (1998). De acuerdo con Vázquez Rodríguez (2007) el método se prepara con una solución sintética de ácidos orgánicos de bajo peso, que incluye compuesto y concentración de la composición de la solución sintética de ácidos orgánicos (Cuadro II).
CUADRO II SOLUCIÓN SINTÉTICA DE ÁCIDOS CARBOXÍLICOS DE BAJO PESO MOLECULAR (MODIFICADO DE CIESLINSKI Y VAN-RESS 1998).
| Compuesto | Concentración |
| Ácido Acético | 2.898 M |
| Ácido Succínico | 1.940 M |
| Ácido Oxálico | 0.043 M |
| Ácido Málico | 0.0398 M |
| Ácido Tartárico | 0.0263 mM |
| Ácido Fumárico | 0.012 mM |
| Ácido Cítrico | 0.0006 mM |
Bioacumulación
La concentración de As en raíces y hojas determina la bioacumulación y la movilidad del arsénico en la planta. La capacidad de acumulación de metales pesados y metaloides que tienen las diferentes especies de vegetales se calculaó por medio de la siguiente ecuación
En donde, FBC es el factor de bioacumulación de la planta, CfP es la concentración del metal en el tejido de la planta (mg/kg peso seco) al final del tratamiento y CiS es la concentración del metal en el medio.
Análisis estadístico
Se realizó estadística descriptiva para todas las variables y análisis de varianza o Kruskal Wallis, dependiendo de las variables de concentración de arsénico y fitoaccesibiidad. Se utilizó el paquete informático Infostat (Di Rienzo et al. 2017).
Todas las muestras se analizaron por duplicado y se reporta el valor promedio y su desviación estándar. Se calculó el porcentaje de error de cada muestra considerando la desviación estándar y en todos los casos este fue menor a 15 %. Se realizaron correlaciones de Spearman (rs) entre el pH y las concentraciones totales y las concentraciones fitoaccesibles en sedimentos y suelos rizosféricos, así como con la concentración bioacumulada en A. Fistulosus por medio del programa Statistica v.8.
RESULTADOS
Concentración total de arsénico
El cuadro III muestra la concentración de As (mg/kg) en los sedimentos (S) y suelos rizosféricos (SR). Los resultados evidencian que todas las muestras analizadas superan las concentraciones de referencia establecidas para la remediación de sitios contaminados según la NOM 147 SEMARNAT 2004 que establece 22 mg/kg para suelos de uso agrícola/residencial. Los datos obtenidos fueron de 9.1 a 46.2 veces más de lo marcado en la norma.
CUADRO III CONCENTRACIONES TOTALES DE As (mg/kg) MEDIA ± (n = 2) EN SEDIMENTO (S) Y SUELO RIZOSFÉRICO (SR) DE A. fistulosus.
| Puntos de muestreo | Concentración total de As (mg/kg) (media±DE) | CRT1 | CRT2 |
| 1S | 199. 8 ± 17 | 9. 1 | *pdn |
| 1SR | 216. 9 ± 15 | 9. 9 | *pdn |
| 2S | 641. 8 ± 90 | 29. 2 | 2. 5 |
| 2SR | 568. 5 ± 24 | 25. 8 | 2. 2 |
| 3S | 554. 8 ±12 | 25. 2 | 2. 1 |
| 3SR | 583 ± 5 | 26. 5 | 2. 2 |
| 4S | 1004. 3 ±11 | 45. 7 | 3. 9 |
| 4SR | 1013 ± 16 | 46. 1 | 3. 9 |
| 5S | 923. 3 ± 10 | 42. 0 | 3. 6 |
| 5SR | 1017 ± 98 | 46. 2 | 3. 9 |
*pdn = Por debajo del límite máximo permisible. CRT1 = Número de veces que supera el límite máximo permisible para As en suelos de uso agrícola/residencial 22mg/kg. CRT2 = Número de veces que supera el límite máximo permisible para As en suelos de uso industrial 260 mg/kg. Los reultados se As muestran en media ± desviación estándar (DE).
Asimismo, el cuadro III muestra que la concentración en los puntos S y SR va aumentando conforme se avanza aguas abajo, pasando de 199.8 ± 17 en S1 y 216.9± 15 en SR1, hasta una concentración máxima en 5S y 5SR de 923.3± 103 y 1017± 9.8, respectivamente. También se observó una influencia de la altitud en el gradiente longitudinal (aproximadamente 50 m snm) descendiendo conforme se avanza en los puntos de muestreo (Cuadro IV).
pH y contenido de carbonatos
En el cuadro IV se observan los resultados de pH, contenido de carbonatos y la altitud (msnm) para cada punto de muestreo. Se puede observar que los suelos al estar situados en una región con clima árido suelen ser mayormente alcalinos y calcáreos, por contar con altas temperaturas y bajas precipitaciones, magnificando la concentración de las sales en el suelo.
Los contenidos de carbonatos presentes en suelos sedimentarios y suelos rizosféricos oscilan de 4.4 hasta 30.5 %. El punto con menor contenido de carbonatos fue el sedimento 4S, siendo el porcentaje más bajo con 4.4 % posiblemente por estar situado cerca de un sumidero donde se evidencia la presencia de drenaje ácido de mina (Fig. 6). Lo anterior confirma que el pH ácido consumió los carbonatos de los suelos expuestos a los lixiviados ácidos producidos por la intemperización de los polisulfuros metálicos presentes de los residuos mineros.
Extracción secuencial aniónica (ESA) para As
El cuadro III muestra la concentración de As (mg/kg) en los sedimentos (S) y suelos rizosféricos (SR). Los resultados evidencian que todas las muestras analizadas superan las concentraciones de referencia establecidas para la remediación de sitios contaminados según la NOM 147 SEMARNAT 2004 que establece 22 mg/kg para suelos de uso agrícola/residencial. Los datos obtenidos fueron de 9.1 a 46.2 veces más de lo marcado en la norma.
Asimismo, el cuadro III muestra que la concentración en los puntos S y SR va aumentando conforme se avanza aguas abajo, pasando de 199.8 ± 17 en S1 y 216.9± 15 en SR1, hasta una concentración máxima en 5S y 5SR de 923.3± 103 y 1017± 9.8, respectivamente. También se observó una influencia de la altitud en el gradiente longitudinal (aproximadamente 50 m snm) descendiendo conforme se avanza en los puntos de muestreo (Cuadro IV).
La figura 3 muestra un mayor porcentaje del arsénico en la forma residual representando un 58.37 % ± 10.85 desde S1 hasta S5, siendo esta fracción del arsénico la menos disponible. El porcentaje de arsénico fitoaccesible puede ser definido por la sumatoria de las contribuciones de cada una de las etapas de las extracciones INTC, INTA y OFM, y que corresponieron a 8.9 % ± 7.3, 9.5 % ± 7.6, 19.2% ± 5.6 respectivamente (datos no reportados en cuadros). Cabe mencionar que en suelos con pH < a 7 y potencial redox reducido, el As podría encontrarse en su forma trivalente, como un ácido arsenioso soluble. Por otro lado, en condiciones de potenciales redox oxidantes, el As se presenta en forma pentavalente como anión con carga negativa a pH > 3, el cual puede ser adsorbido, precipitado o coprecipitado con otros metales tales como el Ca, Pb y Zn.
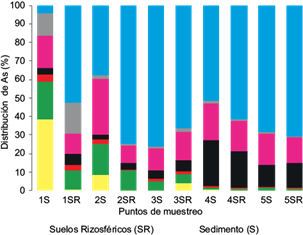
Fig. 3 Distribución porcentual de As en extracción secuencial aniónica en sedimentos (S) y en suelos rizosféricos (SR) de A. fistulosus; ■ Fracción soluble, ■ Intercambiable catiónico, ■ Asociado a carbonatos, ■ Intercambiable aniónicamente, ■ Asociado a oxihidróxidos de hierro y manganeso, ■ asociada a materia orgánica y sulfuros y ■ fracción residual.
Fitoaccesibilidad de As en suelos rizosféricos de A. fistulosus
El análisis de fitoaccesibilidad para suelos rizosféricos simuló las condiciones de la rizósfera por medio de una solución de ácidos orgánicos de bajo peso molecular. La concentración de arsénico total versus el porcentaje de fitodisponibilidad, calculado con base en esta concentración total, indica el porcentaje que podría ser absorbido por la planta a través de la rizosfera (Fig. 4 ).
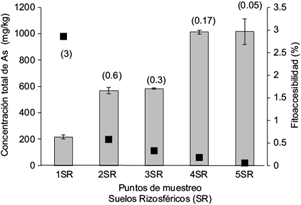
Fig. 4 Porcentaje de fitoaccesibilidad ■ con respecto a la concentración total de [As]T ■ en suelos rizosféricos (SR) de A. fistulosus. Media ± desviación estándar.
Los valores promedio de la fitoaccesibilidad fueron 6.2, 2.2, 1.9, 1.8 y 0.6 mg/kg para cada uno de los puntos de muestreo que corresponde a porcentajes de fitoaccesibilidad de 2.86, 0.58, 0.33, 0.17 y 0.05 % respectivamente con relación a la concentración total de arsénico ([As]T).
Bioacumulación de arsénico en A. fistulosus
Considerando los resultados de la sección anterior, se determinaron las concentraciones bioacumuladas de As en hojas y raíces de A. fistulosus (Fig. 5). Se encontró que la especie A. fistulosus retiene el arsénico principalmente en las raíces.
Drenaje ácido de mina
Los jales mineros con alto contenido de polisulfuros metálicos, al estar expuestos al aire y el agua se oxidan y generan drenaje ácido de minas (DAM), que propicia acidez al medio y la migración de compuestos que pueden liberar elementos potencialmente tóxicos (EPT), como el arsénico y metales pesados aumentando su labilidad (Burillo et al. 2017).
En época de lluvia hay evidencia de drenaje ácido de mina en Cerro de San Pedro tal como se observa en la figura 6, en el sitio de estudio, existe presencia de DAM, sin embargo, es importante señalar que para en este trabajo no se realizaron análisis o pruebas de DAM.
DISCUSIÓN
Concentración de Arsénico
El arsénico rebasa los valores de concentración de referencia totales (CRT) para suelos de uso agrícola/residencial (CRT1: 22 mg/kg), y también para los suelos de uso industrial (CRT2: 260 mg/kg) de acuerdo con los criterios establecidos por la norma mexicana NOM-147-SEMARNAT/SSA1-2004 (SEMARNAT 2007), excepto por los puntos 1S y 1SR, los cuales están situados antes de la fuente de contaminación. Los suelos con mayor concentración de As fueron 5S-5SR colectados aguas abajo. Existe una correlación de 0.96 con un intervalo de confianza de p < 0. 05 entre los valores de S y SR por lo que las concentraciones totales de As no varían mucho entre ambos tipos de muestras de suelos. lo cual se debe a que fueron tomados en el mismo punto, sin embargo la concentración total de As es ligeramente mayor en los SR que en los S (p < 0.05), esto ocurre porque los sedimentos son aquellas partículas que al estar expuestas a las rutas de arrastre de partículas por vía eólica e hídricas se van movilizando hacia aguas abajo en comparación con los SR donde actúan fijadores como son la materia orgánica y sus compuestos orgánicos, e inclusive las raíces de las plantas, debido al intercambio catiónico y aniónico entre suelo y raíz (Wang et al. 2017). También interviene la pendiente, considerando que el estudio es in situ. Este comportamiento muestra que conforme se desciende aguas abajo la concentración total del As aumenta.
pH y carbonatos
Se encontró que los suelos son calcáreos, de acuerdo con el contenido de carbonatos. Con los datos obtenidos de pH y porcentaje de carbonatos, se obtuvo que el pH es dependiente del contenido de carbonatos presente en los suelos, ya que los carbonatos neutralizan a los ácidos. En los suelos rizosféricos esta correlación puede ser menor por que intervienen otros factores como la acción de los ácidos orgánicos (Vázquez Rodríguez 2007).
Extracción secuencial aniónica (ESA) para As
Con los resultados obtenidos de la ESA se observa la posibilidad de transporte coloidal, ya que conforme se avanza aguas abajo del gradiente longitudinal, el porcentaje de As asociado a la fracción soluble en agua meteórica disminuye, para observarse que el As soluble se encuentra predominantemente asociado a la fracción ligada a los oxihidróxidos de hierro y manganeso (OFM) en sedimentos, seguido de las fases intecambiables catiónica y aniónica (INTA e INTC). Lo anterior podría se consecuencia del tiempo que ha ocurrido para llevar a cabo mayor estabilización (Corrales et al. 2018). Se realizó una correlación entre la concentración de As asociado a la fracción carbonatada contra el porcentaje de carbonatos en los suelos y se encontró una correlación de 0.5 (p < 0.05). A partir del punto AS5 no se observó de manera significativa As asociado a la fracción carbonatada como en los iniciales, este hecho puede atribuirse a que los carbonatos fueron consumidos para amortiguar el drenaje ácido de mina en el cauce donde se observó presencia de DAM (Fig. 6).
Conforme se avanza aguas abajo, se observa la transición del As hacia fracciones asociadas a fases de oxihidroxidos de hierro, prevaleciendo en primer lugar la fracción intercambiable aniónicamente y en segundo lugar la asociada a la fracción de OFM amorfa. Lo cual indica un proceso de intemperización y estabilización sobre estas nuevas fases de OFM, las cuales debido a su menor tamaño de partícula pueden ser arrastradas a mayores distancias por el cauce del arroyo aguas abajo. Las concentraciones de As en la fracción OFM mostraron una correlación de 0.9 entre la concentración total de Fe y As en solución, lo que implica que el 90 % del arsénico liberado en esta etapa podría estar relacionada con el proceso reductivo de disolución de las fases de oxihidróxidos de hierro. Es importante resaltar que la mayoría del arsénico está en fracción residual poco lábil.
Fitoaccesibilidad de As en suelos rizosféricos de A. fistulosus
Los resultados de este ensayo muestran que existe una fracción disponible asociado a la actividad biológica de la planta (Fig. 4) y que podría ser traslocada al interior de A. fistulosus y bioacumulada en alguna de sus partes (raíz o tallo). La correlación entre el pH y la fitoaccesibilidad es negativa, al disminuir el pH, la fitoaccesibilidad en los suelos aumenta (rs= 0.9) lo cual está relacionado con una mayor concentración de As lábil y disponible para ser traslocada, evidenciando un potencial impacto negativo sobre la biota circundante asociada a la dispersión de este elemento desde la fuente de los residuos mineros. En los suelos rizosféricos la concentración total de As aumenta conforme se avanza en dirección aguas abajo del arroyo de San Pedro. Sin embargo, el porcentaje de fitoaccesibilidad va disminuyendo en el mismo sentido (Fig. 4) lo cual podría atribuirse a que el As aguas abajo se encuentra en fases más estables ligadas a oxihidróxidos de hierro más critalinos asociados a ciclos de disolución y reprecipitación que conllevan a una mayor cristalinidad y mayor estabilidad química (Hernández et al. 2013, Sánchez Cuadros 2019). La figura 3, muestra que el As en el primer punto de muestreo resulta ser más soluble de acuerdo con los resultados de la extracción secuencial, por eso este punto es el más fitoaccesible en comparación con la figura 4, El As en la fracción residual pueden ser más estable químicamente con el paso del tiempo y se ubican a mayor distancia de la fuente, el As en los primeros puntos es más soluble, encontrándose inclusive en forma intercambiable, debido a que los procesos de intemperización no han sido los suficientemente largos para permitir la estabilización natural de las nuevas fases minerales formadas (Tec-Caamal 2021). La variación en la altitud conlleva una inclinación en el terreno que reduce los tiempos de retención de los contaminantes, lo cual sugiere una mayor cristalización de este elemento con los oxihidróxidos de hierro de formación reciente (Fresno-García 2017). Lo anterior explica que a mayor solubilidad mayor es la fitoaccesibilidad y en consecuencia su posible bioacumulación (Fu et al. 2019a, Fu et al. 2019b, Gavilán et al. 2020). Por otra parte, se correlacionó la fitoaccesibilidad contra la sumatoria de algunas fracciones mineralógicas definidas en la extracción secuencial (soluble en agua meteórica, carbonatos, intercambiable catiónico e intercambiable aniónicamente) y se obtuvo una correlación de 0.8 ± 0.08 asociado a las fracciones solubles y carbonatos; es decir, que hay una relación de hasta un 80 % de arsénico que puede ser fitoaccesible asociadas a dichas fracciones mineralógicas solubles. Se observó además que el arsénico asociado a la fracción intercambiable no influye significativamente a la fitoaccesibilidad en los suelos rizosféricos de A. fistulosus (Fig. 4). Los valores promedio de la fitoaccesibilidad fueron 6.2 (3 %), 2.2 (0.6 %), 1.9 (0.3 %), 1.8 (0.17 %) y 0.6 mg/kg (0.05 %) para cada uno de los puntos de muestreo (Fig. 4), respectivamente con las concentraciones totales de As.
Bioacumulación de As en A. fistulosus
Se observa en la figura 5 una mayor acumulación en las raíces que en las hojas sugiriendo que, lo que ocurre con A. fistulosus es un proceso de estabilización que retiene el As en la zona rizosférica principalmente, esto posiblemente ocurre porque la planta incorpora el arsénico de manera similar a la del fósforo, el cual es un elemento esencial para el metabolismo vegetal (Huaranga et al. 2022). En nuestro estudio, se observaron rangos de bioacumulación en raíz de 9.4 a 14 mg/kg y de 1.5 a 3.1 mg/kg en hoja, otros estudios realizados en otras áreas mineras en México mostraron una bioacuulación más elevada de As en raíz en esta misma planta (Salas Luevano et al. 2021). Sin embargo, en este estudio no se consideró la posibilidad de que se realicen procesos de oclusión en la planta.
CONCLUSIONES
Los suelos del arroyo de San Pedro, San Luis Potosí, México contienen arsénico en cantidades que superan las concentraciones de referencia totales de acuerdo con la NOM-147-SEMARNAT/SSA1-2004 (SEMARNAT 2007) El arsénico rebasa desde nueve hasta más 46 veces las concentraciones de referencia totales del suelo para uso agrícola/residencial. La concentración de arsénico varía de acuerdo con las propiedades fisicoquímicas de los puntos de muestreo como son el relieve, pendiente, tiempos de retención del material, erosión, pH, Eh carbonatos, etc. Las concentraciones de As son similares en los sedimentos y suelos rizosféricos. El pH es dependiente del contenido de carbonatos presente en los suelos, ya que los carbonatos actúan como un factor de amortiguamiento del pH, al disminuir el pH, se consumen los carbonatos. La correlación del pH y la fitoaccesibilidad del As en suelos rizosféricos es negativa por lo que al disminuir el pH la fitoaccesibilidad en los suelos aumenta. El As se encuentra en forma soluble e intercambiable en el inicio de la fuente de contaminación donde inicia la deposición de los residuos mineros en el arroyo, posteriormente ocurren procesos de intemperización y/o estabilización. Se observa que existe una atenuación natural del As, ya que en los puntos lejanos a la fuente de contaminación (aguas abajo), existe una mayor asociación en la fracción residual categorizándose como la menos lábil. Para evaluar el riesgo ambiental, además de considerar las concentraciones totales de los EPT, es de mayor importancia considerar la solubilidad y la especiación química de los elementos, lo cual influye directamente en la biodisponibilidad y fitoaccesibilidad, aun y cuando estas concentraciones superen los CRT establecidos. Se demostró que la fracción fitoaccesible está asociada a las fracciones minerales solubles en agua meteórica, intercambiable e incluso asociada a carbonatos en una alta proporción.