INTRODUCCIÓN
El tomate Solanum lycopersicum (L.) es uno de los cultivos hortícolas más importantes en México por los elevados beneficios económicos que genera (Reyes-Cortés et al. 2017). Durante 2023, el estado de Sinaloa aportó 561 124.58 t de la producción de tomate con una superficie sembrada de 11 655.4 ha y un rendimiento de 55.05 t ha (SIAP 2023); sin embargo, los cultivos son afectados por plagas que ocasionan una disminución en su producción, como la del gusano del fruto Heliothis virescens (F.), que es una plaga polífaga, capaz de sobrevivir y desarrollarse en plantas que pertenecen a más de 37 familias diferentes (Blanco et al. 2007). El control de este patógeno se realiza con insecticidas convencionales sintéticos (Viteri et al. 2019), aunque el uso de insecticidas biológicos es cada vez más común debido a que son eficientes y amigables con el medio ambiente (Anjos et al. 2022).
Los hongos y nemátodos entomopatógenos son agentes que causan enfermedades letales a varias especies de plagas, por lo que son usados en su manejo integrado (Půža y Tarasco 2023). Dentro de los principales hongos destacan Beauveria bassiana (Vuill) y Metarhizium anisopliae (Metschnikoff), los cuales pueden matar a gusanos de plagas en un lapso de cuatro a siete días debido a las esporas y toxinas fúngicas, además de formar nuevas esporas que se dispersan en el ambiente (Quesada-Moraga et al. 2020). La mayoría de los micoinsecticidas producidos comercialmente están elaborados a base de hongos entomopatógenos como Beauveria spp., Metarhizium spp., Lecanicillium spp. (anteriormente Verticillium) e Isaria spp. (antes Paecilomyces) (Espinel et al. 2018). Específicamente, M. anisopliae ha demostrado ser efectivo en el control de langostas, termitas y saltamontes en EUA, Australia y Brasil (van Lenteren et al. 2017). Asimismo, los nematodos entomopatógenos son utilizados comúnmente como agentes de control biológico de plagas. Las especies Steinernema riobrave Poinar y Raulston (1994) y Rhabditis blumi (Sudhaus) son parásitos obligados de insectos (Poinar 1979). Los estados juveniles son infecciosos, penetran por la boca o el ano de los insectos, los invaden y liberan a las bacterias para causar su muerte en 24 a 48 h, reproduciéndose en el cadáver (Gaugler 2002). Steinernema carpocapsae ataca a Agrotis ipsilon; Phyllotreta striolata, S. longicaudum y H. bacteriophora a larvas de escarabeidos (Guo et al. 2015, 2016). Estos organismos pueden producirse en masa utilizando diferentes métodos (Shapiro-Ilan et al. 2016, 2023), por lo que requieren ser formulados para su uso en campo.
Se ha demostrado que los hongos y nematodos son efectivos como controladores de plagas en campo, por lo que es muy importante que en su formulación se consideren las condiciones ambientales, las especies de plagas objetivo y el momento justo de aplicación para lograr resultados óptimos (Půža y Tarasco 2023). Estos dependen también de otros factores como los portadores adecuados, la temperatura, el contenido de agua, las concentraciones del estadio infectante y la aireación del organismo (Kim y Jaffuel 2015, Peters 2016, Cruz-Martínez et al. 2017).
En este trabajo se evaluó la efectividad de un formulado en emulsión del hongo Metarhizium anisopliae y la de un formulado de los nematodos Steinernema riobrave y Rhabditis blumi en cápsulas de alginato contra larvas de H. virescens en laboratorio y en campo.
MATERIALES Y MÉTODOS
El trabajo se llevó a cabo en el Centro Interdisciplinario de Investigación para el Desarrollo Integral Regional del Instituto Politécnico Nacional (CIIDIR-IPN), unidad Sinaloa. Durante 2017 se realizaron recolecciones de larvas de H. virescens en cultivos de tomate, tomatillo y garbanzo por utilizarlos como hospederos del insecto. Las larvas fueron alimentadas con dieta artificial a base de harina de maíz y trigo, levadura, vitaminas y bacteriostáticos hasta la formación de pupas y adultos.
En la evaluación en laboratorio se usó la cepa Metarhizium anisopliae (CIDSM01) con número de acceso (KR998522). Las especies de nematodos utilizadas en la prueba de virulencia fueron Steinernema riobrave y Rhabditis blumi. En la prueba de campo se utilizó únicamente S. riobrave. En campo se establecieron cinco tratamientos: testigo (agua), Abatec (testigo químico), formulación en emulsión de M. anisopliae, M. anisopliae Metasin y la formulación de S. riobrave en cápsulas de alginato.
Producción, formulación y evaluación del hongo entomopatógeno
La propagación del hongo M. anisopliae (CIDSM01) se realizó siguiendo el método bifásico estandarizado por García et al. (2006). En la fase líquida se preparó un medio de cultivo a base de melaza de caña de azúcar y sales minerales. Para propagar el hongo se tomaron 25 mL del inóculo de la fase líquida y se agregaron a 300 g de arroz previamente precocido en bolsas de plástico y esterilizado en autoclave a 1.5 psi y 121 ºC por 15 min. La viabilidad de las esporas se midió utilizando la técnica de Inglis et al. (2012). En el bioensayo de patogenicidad del hongo M. anisopliae (CIDSM01) se utilizaron larvas de tercer instar de H. virescens con tres réplicas de diez larvas cada una, aplicándose 1 × 108 esporas/mL sobre el insecto.
La formulación de M. anisopliae en emulsión se realizó siguiendo la metodología de Batta et al. (2011). Los compuestos se mezclaron previamente por separado y luego las dos fases se combinaron en proporciones de 1:1. La fase acuosa consistió en la mezcla de agua destilada estéril (45 %), dispersante no iónico InexA (2 %) y emulsionante soluble en agua Tween 80 (3 %), mientras que en la fase oleosa se mezclaron aceite de soya (47 %) y lecitina (3 %). Posteriormente fueron agitadas durante 30 min a 200 rpm con un agitador magnético, para finalmente agregar la suspensión de esporas del hongo y obtener la formulación en emulsión que contenía 1 × 108 esporas/mL.
Evaluación de la efectividad de los formulados en laboratorio
La evaluación de la efectividad del formulado se realizó mediante un bioensayo usando larvas de H. virescens de tercer instar criados en laboratorio; se usaron diez larvas por tratamiento con tres repeticiones. Se aplicó 1 mL de la emulsión conteniendo 1 × 108 esporas/mL sobre el cuerpo de las larvas durante 10 s. Después las larvas se individualizaron en una caja Petri, adicionando una porción de dieta artificial y se incubaron a 27 ± 1 ºC por 72 h. Cada 24 h se observó el número de larvas muertas (Céspedes et al. 2008).
Producción y formulación de los nematodos entomopatógenos
Los nematodos S. riobrave y R. blumi se propagaron en una caja Petri de 60 mm de diámetro invertida dentro de otra caja Petri de 100 × 15 mm en las cuales se les colocaron larvas de G. mellonella y S. frugiperda. Estas se pusieron en papel filtro Whatman núm. 1 situadas dentro de la caja Petri de 60 mm. Después se agregaron 5 mL de agua destilada estéril a la primera caja. Los insectos infectados permanecieron en la trampa durante una semana, para lograr la emergencia y migración de los juveniles infectivos (JI) hacia el agua. El procedimiento se repitió varias veces para obtener una mayor cantidad de cada especie (Matha y Áček 1984).
Para la cuantificación de los nematodos se tomó 1 mL de la solución inicial para formar una dilución 1:100 en agua destilada estéril, homogenizándola manualmente durante 30 s. Luego se tomó 1 mL y se colocó en una caja de Petri con cuadrícula. Se contaron los JI vivos bajo el estereoscopio, repitiendo esto en cinco ocasiones. Para determinar la concentración de nematodos en la solución se utilizó la siguiente fórmula:
A = D *C/B (1)
donde A representa los mililitros de suspensión de la concentración conocida y de la suspensión a ser diluida, B el número de nematodos/mL de solución a ser diluida, C el volumen final de la nueva dilución en mililitros, y D la concentración deseada de la nueva dilución. C - A representan los mililitros de agua que deben agregarse para hacer la nueva dilución (Woodring y Kaya 1988).
Para realizar la prueba de virulencia de los nema todos entomopatógenos se utilizaron cajas Petri de 60 × 15 mm con un círculo de papel filtro Whatman núm. 1 de 5 cm de diámetro. Después se agregó la dieta artificial y posteriormente se colocó una larva de tercer instar de H. virescens por caja con tres réplicas. Los tratamientos fueron S. riobrave y R. blumi a dosis de 100, 250 y 500 JI/mL, con diez unidades experimentales por réplica y agua destilada como control. Las larvas fueron inoculadas y colocadas en una caja de Petri e incubadas a 23 ± 3 ºC durante siete días, registrando la mortalidad de larvas cada 24 h (Caccia et al. 2014).
Análisis estadístico
La mortalidad de las larvas se analizó con el paquete estadístico SAS v. 9.0. Se realizó un análisis de varianza (ANDEVA) y después una prueba de comparación de medias Tukey (α ≤ 0.05). Como los datos no presentaban normalidad se tuvieron que transformar al arco seno para cumplir los supuestos para el ANDEVA.
Formulación de los nematodos entomopatógenos
Para la formulación de los nematodos entomopatógenos S. riobrave y R. blumi se partió de larvas de G. mellonella, S. frugiperda y H. virescens, las cuales fueron almacenadas en frascos ámbar de 50 mL. Para la encapsulación se utilizaron alginato de sodio y cloruro de calcio. Las cápsulas se formaron mezclando 10 mL de una suspensión de nematodos a una concentración de 500 JI/mL y 10 mL de alginato de sodio al 3 %, con lo cual se obtuvo una mezcla de alginato al 1.5 % y una concentración de nematodos de 250 JI/mL. La mezcla se goteó sobre una solución de cloruro de calcio al 4 % (Leyva-Hernández et al. 2018). Las cápsulas formadas se almacenaron en refrigeración a 15 ºC para prolongar así la vida útil de los nematodos, facilitando además el transporte de estos agentes de control biológico a la evaluación de campo.
Evaluación de la efectividad de los formulados en campo
La evaluación de la efectividad del hongo y los nematodos se realizó en una parcela de tomate variedad saladette en un lote experimental de 0.5 ha en el CIIDIR-Sinaloa. El terreno se preparó considerando la metodología regional (comunicación personal) con una distancia entre surcos de 1.6 × 10 m de largo y una distancia de 25 cm entre plantas. El trasplante de las plántulas a campo se realizó 30 días después de la siembra, y se utilizó un sistema de riego por goteo. Los tratamientos evaluados fueron: testigo (agua), Abatec (testigo químico), formulación de M. anisopliae en emulsión, M. anisopliae Metasin y la formulación de S. riobrave en alginato, por haber resultado esta especie más virulenta que R. blumi. Los tratamientos se aplicaron una sola vez cuando el cultivo se encontraba en floración y en la formación de frutos a los 45 días, utilizando una bomba de mochila marca Truper de 3.8 L.
Evaluación del rendimiento de los frutos
La cosecha de frutos se realizó a los 60 días, recolectando frutos maduros de la parcela útil. Después se pesaron en una báscula digital marca Torrey y se clasificaron de acuerdo con la calidad comercial y/o daños producidos por la plaga. Los resultados de rendimiento se extrapolaron a toneladas/hectárea. La evaluación de los frutos con daños de H. virescens se realizó después de obtener el rendimiento del tomate (García-Gutiérrez et al. 2020).
RESULTADOS Y DISCUSIÓN
Evaluación de patogenicidad de la cepa M. anisopliae sin formular y en emulsión
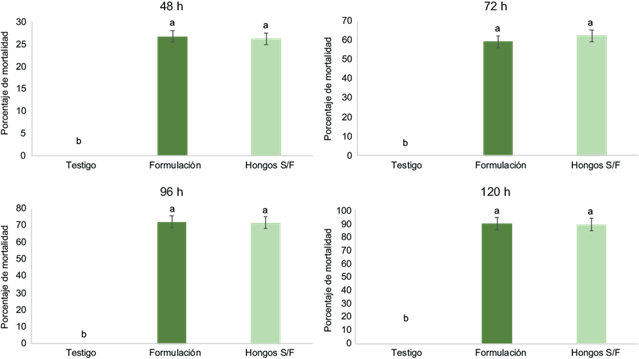
La cepa de M. anisopliae (CIDSM01) sin formular y la cepa de M. anisopliae en emulsión fueron patogénicas contra larvas del tercer instar de H. virescens a 1 × 108 esporas/mL, alcanzando la máxima mortalidad de larvas a las 120 h sin diferencia estadística significativa (Tukey p ≤ 0.05). Este ensayo indicó la efectividad de ambas cepas desde las 48, 72, 96 y 120 h después de su aplicación y mostró la efectividad del hongo en emulsión (Fig. 1).
Evaluación de la virulencia de S. riobrave y R. blumi en cápsulas de alginato contra H. virescens en laboratorio
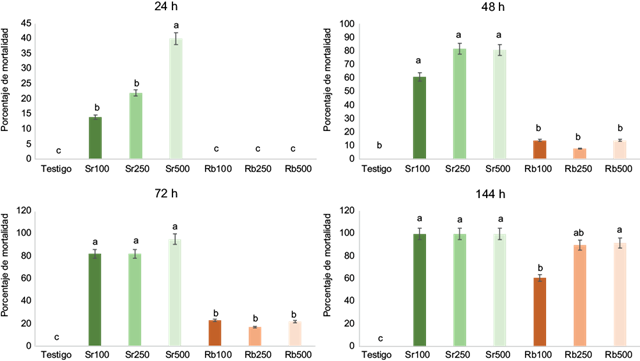
En laboratorio, los nematodos S. riobrave y R. blumi fueron virulentos para larvas del tercer instar de H. virescens. R. blumi presentó mortalidad desde las 48 h y a las 144 h alcanzó los mayores porcentajes de larvas muertas en las tres concentraciones (100, 250 y 500 JI/mL), mientras que para S. riobrave, la mortalidad de las larvas se presentó desde las 24 h (pi), alcanzándose el 90 % de mortalidad las 48 h, con diferencia estadística en la prueba de Tukey (p ≤ 0.05) (Fig. 2). Por esta razón se eligió a S. riobrave para elaborar la formulación en cápsulas de alginato a una concentración de 250 JI/mL, además de que la mortalidad de larvas fue estadísticamente igual a la del tratamiento con 500 JI/mL (Fig. 2).
Evaluación de la efectividad de nematodos y hongos entomopatógenos en campo
Los datos de producción de tomate y daños en fruto en cada tratamiento aparecen en el Cuadro I. La menor cantidad de frutos dañados por H. virescens se obtuvo con Abatec, con diferencias estadísticas significativas respecto al testigo. Los tratamientos con nematodos y hongos no presentaron diferencias entre sí ni con Abatec®, aun cuando este último, en promedio, tuvo mayor número de frutos dañados. En cuanto a la producción comercial de tomate, las formulaciones del hongo en emulsión y el nematodo en cápsulas de alginato fue estadísticamente igual a los del hongo comercial. En lo que respecta a la producción total, estos mismos productos y el control fueron estadísticamente iguales (Tukey p≤ 0.05).
CUADRO I PRODUCCIÓN COMERCIAL DE TOMATE, PRODUCCIÓN DE FRUTOS DAÑADOS POR H. virescens Y PRODUCCIÓN TOTAL DE TOMATE EN LA EVALUACIÓN DE CAMPO DE TRATAMIENTOS APLICADOS.
| Núm. de tratamiento | Tratamiento | Producción comercial* (ha) | Producción de Frutos dañados* (t/ha) | Producción total* (t/ha) |
| 1 | Abatec | 35.86a | 2.31c | 38.17a |
| 2 | S. riobrave (encapsulado) | 27.88ab | 2.70bc | 30.59ª |
| 3 | M. anisopliae | 30.10ab | 3.50ab | 33.60ª |
| 4 | M. anisopliae (emulsión) | 29.34ab | 2.85bc | 32.19ª |
| 5 | Testigo (agua) | 23.66b | 3.99a | 27.66a |
*Comparación de medias.
Medias con letras iguales dentro de cada columna son iguales (Tukey p ≤ 0.05).
La formulación en emulsión de M. anisopliae fue patogénica a dosis de 1 × 108, alcanzando 90 % de mortalidad de larvas a las 120 h. Al respecto, Fite et al. (2020) usaron una concentración de 1 × 109 esporas/mL, obteniendo 71% de mortalidad de larvas de Helicoverpa armigera (Hubner) a los 11 días. Por su parte, Shanker et al. (2023) aplicaron una concentración de 1 × 1010 esporas/mL, obteniendo 87.7 % de mortalidad a las 120 h en este mismo insecto. Según Yasin et al. (2019), entre más elevada sea la concentración utilizada del hongo, más eficiente será el control del insecto.
Por otro lado, se observó que la formulación del hongo en emulsión mejoró la adhesión de las esporas al follaje, a la vez que protegió al hongo de la radiación solar, reduciendo el efecto hidrofóbico de las esporas. De esta manera se obtuvo una mayor dispersión del ingrediente activo y una mayor cobertura en el follaje de la planta, resultado que ha sido mencionado por Batta et al. (2012).
El nematodo S. riobrave provocó una mortalidad de 90 % a las 48 h en larvas de tercer instar de H. virescens, y fue más virulento que R. blumi a 100, 250 y 500 JI/mL a los siete días. Al respecto, Leyva-Hernández et al. (2018) usaron 500 JI de S. riobrave, causando 90 % de mortalidad a larvas de S. frugiperda a las 96 h. Sin embargo, con R. blumi no se registró mortalidad de larvas de este insecto. Por su parte, Fallet et al. (2022) reportaron mortalidad de 58 % de larvas de S. frugiperda con S. riobrave (10 JI). Lo anterior indica la importancia de la concentración de JI en la formulación y la especie de insecto a controlar.
En este trabajo, la infectividad de R. blumi encapsulados inició a las 48 h. Al respecto, Lalitha et al. (2023) obtuvieron 96 % de sobrevivencia de S. carpocapsae, S. monticolum y R. blumi después de tres semanas de haber sido encapsulados con goma arábiga y perlas de gel de alginato de sodio. Este retraso, en comparación con la acción de S. riobrave de 24 h, se puede deber al tiempo que tarda el nematodo en salir de la cápsula. Bogantes et al. (2018) utilizaron 10 y 20 cápsulas con 40 Jl por cápsula, obteniendo 4 y 12 % de infección, respectivamente, a las 48 h. En este estudio, los tratamientos de nematodos en cápsulas y nematodos sin formular presentaron una mortalidad acumulada superior al 30 % a las 48 h, lo cual indica que las concentraciones de los nematodos utilizados fueron efectivos para infectar a H. virescens. Esto resultados confirman que para el control de una plaga es importante la especie y la concentración de nematodos para utilizar (Yasin et al. 2019; Acharya et al. 2020).
El mejor tratamiento para el control del gusano del fruto del tomate fue Abatec, con el cual se obtuvo el menor número de frutos dañados por larvas y la mayor producción de tomate comercial. Las formulaciones de nematodos y hongos no mostraron diferencia estadística con el insecticida Abatec. Estos datos son similares a los reportados por García et al. (2020), quienes no encontraron diferencias estadísticas entre los tratamientos de hongos entomopatógenos sin formular y el insecticida Abatec.
CONCLUSIONES
En laboratorio, el hongo M. anisopliae en emulsión causó 90 % de mortalidad de larvas del fruto del tomate a las 120 h con 1 × 108 esporas/mL, mientras que S. riobrave causó mortalidad del 100 % y R. blumi de 85 % a las 144 h con 100 y 500 JI/mL (pi). En condiciones de campo, el insecticida Abatec mostró la menor cantidad de frutos dañados por el gusano (2.310 t/ha), seguido de S. riobrave en cápsulas de alginato (2.700 t/ha) y M. anisopliae en emulsión (2.850 t/ha), entre las cuales se presentaron diferencias estadísticas; sin embargo, no hubo diferencias en la producción total, mientras que entre los frutos de calidad comercial sí hubo diferencias estadísticamente significativas, siendo el mejor tratamiento Abatec seguido del hongo en emulsión S. riobrave encapsulado y M. anisopliae R , por lo que las formulaciones elaboradas del hongo en emulsión y los nematodos encapsulados fueron efectivas contra el gusano del fruto a las dosis evaluadas.