INTRODUCCIÓN
Uno de los impactos antrópicos más generalizados en el planeta es sin duda el cambio climático, el cual afecta a una gran variedad de factores físicos que rigen las condiciones para la vida. Los parásitos metazoarios son organismos que permiten monitorear el estado de salud de los ecosistemas, debido a que son sensibles a las variaciones ambientales que afectan también a las comunidades de sus hospederos. Algunos cambios ambientales expresados como incrementos de temperatura pueden favorecer a algunos grupos de parásitos de ciclos de vida directos, facilitando su transmisión; a su vez, pueden reducir los niveles de infección de otros parásitos de ciclos indirectos (Marcogliese 2001).
Se considera que fenómenos naturales como El Niño Oscilación del Sur (ENOS), que ocurre de manera periódica en el Océano Pacífico pero con repercusiones en el clima a nivel mundial, pueden intensificarse debido al cambio climático (Lluch-Cota et al. 2010, Lamb et al. 2018). Debido a esto, en los últimos años se ha presentado un incremento en el número de estudios enfocados a explorar los vínculos entre enfermedades parasitarias y el cambio climático en ambientes acuáticos (Goedknegt et al. 2015, Marcogliese 2016, Lamb et al. 2018). En los últimos años, los cambios generados en el medio ambiente y sus efectos sobre las interacciones hospedero-parásito han sido implicados en la aparición o reemergencia de varias enfermedades parasitarias en poblaciones de animales silvestres (Marcogliese 2016, Lamb et al. 2018). Por ejemplo, incrementos en la temperatura superficial del mar registrados durante un evento de ENOS se asociaron con la aparición de una enfermedad ulcerativa cutánea que afectó a 18 especies de peces marinos en las Islas Galápagos (Lamb et al. 2018). Las especies de parásitos de peces marinos generalmente exhiben cambios temporales en su estructura y composición debido a variaciones ambientales (bióticas y abióticas) a nivel local (Balboa y George-Nascimento 1998, Garcías et al. 2001, Villalba-Vásquez et al. 2018); sin embargo, estas variaciones pueden ser más intensas cuando ocurren al mismo tiempo eventos climáticos anómalos como ENOS (Alvitres et al. 1999, Oliva et al. 2008, Miranda-Delgado et al. 2019). En México existe un conocimiento limitado sobre los efectos de fenómenos climáticos como ENOS en la dinámica de las comunidades de parásitos marinos, a pesar de que muchas especies que infectan a peces de importancia comercial pueden representar algún riesgo para la salud humana, como es el caso de algunas larvas de helmintos (Castellanos-Garzón et al. 2020).
Scomberomorus sierra, conocido localmente como sierra del Pacífico, es un pez marino de gran importancia comercial que se distribuye desde el sur de California hasta Chile (Collette y Nauen 1983, Aguirre-Villaseñor et al. 2006). Es considerado un depredador oportunista que se alimenta principalmente de peces pequeños, por lo que sus hábitos alimenticios lo exponen a ser infectado por parásitos en estadios larvarios que utilizan a sus presas como hospederos intermediarios. La parasitofauna de este pez ha sido reportada en dos localidades del Pacifico mexicano (Pérez-Ponce de León et al. 1999, Bárcenas 2021), así como en la misma localidad del presente estudio (Santos-Bustos et al. 2020); sin embargo, no se han realizado hasta la fecha estudios enfocados a determinar la posible influencia de algunos eventos climáticos anómalos como ENOS sobre la variación temporal de sus comunidades de parásitos. Por lo tanto, el objetivo del presente estudio fue determinar los posibles efectos de las fluctuaciones climáticas a gran escala (ENOS) en la variación de los niveles de infección de los parásitos de S. sierra en la bahía de Acapulco.
MATERIALES Y MÉTODOS
Durante un periodo discontinuo de nueve años (marzo de 2011 y 2012, diciembre de 2018 y mayo de 2019) se examinó a un total de 391 especímenes de S. sierra. Los peces se obtuvieron a partir de las capturas comerciales que se realizan de manera regular en la bahía de Acapulco (16º 51’ N; 99º 52’ O), Guerrero. Los datos de temperatura superficial se obtuvieron de otros estudios realizados durante el mismo periodo de estudio en dicha localidad. Durante el periodo que abarcó el estudio se registraron dos eventos climáticos anómalos: una fase de enfriamiento de ENOS (La Niña, 2010-2011) y una fase cálida (El Niño, 2018-2019). Por lo tanto, se obtuvieron datos del índice multimétrico de El Niño (MEI) para cada fecha de muestreo, de la base de datos de la Administración Nacional Oceánica y Atmosférica de EUA (NOAA, por su sigla en inglés). Durante los muestreos se determinó la longitud total, peso y sexo de cada uno de los peces, siendo posteriormente disectados para la recolección e identificación de parásitos. Cada uno de los parásitos fue identificado hasta el nivel taxonómico más bajo posible, con base en la literatura existente.
Durante la recolección de parásitos se identificaron y cuantificaron las presas consumidas (ítems) por cada uno de los ejemplares examinados. Se utilizó el factor de condición de Fulton (Kn) para evaluar el estado de salud de los peces mediante la fórmula Kn = W t /L t 3 , donde W t es el peso total y L t la longitud total.
Para caracterizar los niveles de infección de cada especie de parásito se emplearon los parámetros de prevalencia y abundancia promedio, los cuales fueron calculados de acuerdo con Bush et al. (1997). Se utilizó el estadístico no paramétrico G (Sokal y Rohlf 1998) para determinar posibles diferencias significativas entre los porcentajes de infección de las especies de parásitos y los años de muestreo, en tanto que para determinar diferencias entre las abundancias promedio de las especies de parásitos se empleó el modelo lineal general (MLG). Se utilizó el coeficiente de correlación de Spearman (rs) para determinar posibles relaciones entre la longitud total de los peces y la abundancia de cada especie de parásito.
El concepto del rango del hospedero (Rohde 2015) fue utilizado para clasificar a las especies de parásitos como especialistas o generalistas. Un parásito especialista es aquel con una marcada afinidad por una familia, género o especie, mientras que una especie generalista es la que parasita a varias familias. En el presente estudio las especies especialistas fueron aquellas reportadas en peces escómbridos (Scombridae) y las generalistas fueron aquellas reportadas en especies de peces de diferentes familias (Aguirre-Macedo et al. 2007).
El índice de dispersión (ID) varianza/media fue utilizado para describir patrones de dispersión de las especies de parásitos. Si ID = 1, la dispersión es al azar; si ID > 1 es agregada, y si ID < 1 es regular o uniforme. Los análisis se efectuaron a los niveles de comunidad componente (a nivel de muestra de hospederos) e infracomunidad (a nivel de hospedero). Los parámetros evaluados a nivel componente incluyeron la riqueza total de especies, el número total de individuos, el índice de Shannon-Wiener (H) como medida de diversidad y el índice Berger-Parker (IBP) como medida de dominancia numérica (Magurran 2004). Se emplearon además los índices de Sorensen y de porcentaje de similitud (PS) para determinar diferencias o semejanzas en la composición de especies durante el periodo de estudio. En los casos de los años en que se efectuaron dos muestreos (2012 y 2018), los datos fueron agrupados en algunos análisis para reducir el posible efecto de la variación estacional. Se utilizaron pruebas t de Student para establecer diferencias entre los parámetros a nivel componente.
Se construyeron curvas de rango-abundancia de especies para describir los cambios ocurridos en la estructura de las comunidades a lo largo del tiempo, a partir de la observación de la dominancia o uniformidad de las abundancias relativas de especies (Magurran 2004). Las curvas obtenidas fueron ajustadas a las descritas por varios modelos teóricos (serie geométrica, logarítmica, log-normal y de la barra rota). Se utilizó como criterio de mejor ajuste el valor más alto obtenido para el coeficiente de determinación (R2) de cada modelo. Se aplicó un segundo análisis para evaluar cambios en la estructura de las comunidades, a partir de la evidencia de anidamiento en las infracomunidades de parásitos de cada una de las muestras. Para determinar la presencia de anidamiento se utilizó el calculador de temperatura (Tº) propuesto por Atmar y Patterson (1995). De acuerdo con los criterios del calculador de temperatura de anidamiento, 0º representa una entropía mínima (es decir, un anidamiento perfecto), en tanto que 100º representa una entropía máxima (aleatoriedad).
Las infracomunidades se describieron en términos del número promedio de especies de parásitos por hospedero, el número promedio de individuos de cada especie y el valor promedio del índice de diversidad de Brillouin (H’). Se utilizó el modelo lineal general multivariado (MLG), para establecer diferencias entre los parámetros infracomunitarios entre los años de muestreo. La longitud total de los peces se utilizó como covariable para controlar la influencia de la longitud total del hospedero. Se aplicó además un análisis de componentes principales (ACP), para identificar los factores bióticos y abióticos responsables de generar cambios temporales en la estructura de las comunidades de parásitos durante el periodo de estudio. Para todos los análisis estadísticos se utilizaron los programas SPSS v. 20 y Rstudy (3.6.2) v. 2019.
RESULTADOS
Composición de las especies
Se registraron un total de 20 especies de parásitos metazoarios (15 helmintos y cinco crustáceos) en una muestra global de 391 peces S. sierra recolectados en la bahía de Acapulco, Guerrero. El grupo de parásitos mejor representado fue el de los digéneos (30 % del total de las especies), seguido por los nemátodos (20 %) y copépodos (20 %). De acuerdo con el sitio de infección, 11 especies fueron clasificadas como ectoparásitas y 9 como endoparásitas. Los ectoparásitos dominaron numéricamente en ambas fases climáticas examinadas (77.45 y 89.23 %, respectivamente). Del total de especies, nueve fueron clasificadas como especialistas (tres monogéneos, cuatro digéneos y dos copépodos), en tanto que las 11 restantes como generalistas (Cuadro I).
CUADRO I PARÁMETROS DE INFECCIÓN DE LOS PARÁSITOS METAZOARIOS DE LA SIERRA Scomberomorus sierra EN LA BAHÍA DE ACAPULCO, GUERRERO, MÉXICO.
| Parásitos | Sitio de infección | Año | |||
| 2011 (n = 76) | 2012 (n = 95) | 2018 (n = 161) | 2019 (n = 59) | ||
| Digenea | P% (A, RI) | P% (A, RI) | P% (A, RI) | P% (A, RI) | |
| Anacetabulum (larva) E | Branquias | 0.66 (0.01, 0-2) | 0.60 (0.07, 0-11) | 15.25 (0.32, 1-4) | |
| Didymocilindrus sp.E | Branquias | 67.11 (13.49, 5-101) | 57.24 (4.66, 2-43) | 15.58 (0.61, 1-17) | 55. 93 (2.61, 1-22) |
| Didymocystis sp.E | Intestino, estómago | 67.11 (7.78, 1-48) | 40.79 (3.96, 1-47) | 16.95 (0.83, 2-12) | |
| Glomeritrema sp.E | Branquias | 10.53 (0.72, 1-30) | 1.79 (0.03, 1-3) | 15.25 (0.31, 1-3) | |
| Lecithochirium microstomum G Chandler, 1935 | Intestino | 1.32 (0.01, 0-1) | 0.66 (0.22, 1-3) | 6.22 (0.09, 1-2) | 8.47 (0.20, 1-6) |
| Prosorhynchoides cybii G Park,1939 | Intestino | 21.05 (0.66, 1-14) | 21.71 (1.31, 1-19) | 1.84 (0.08, 1-11) | 3.39 (0.05, 1-2) |
| Monogenea | |||||
| Mexicotyle mexicana E (Meserve, 1938) Lebede, 1984 | Branquias | 27.63 (0.50, 1-8) | 65.79 (2.77, 1-26) | 18.72 (0.46, 1-13) | 38.98 (0.80, 1-6) |
| Scomberocotyle scomberomori E (Koratha, 1955) Hargis, 1956 | Branquias | 1.32 (0.03, 0-2) | 1.69 (0.02, 0-1) | ||
| Thoracocotyle crocea E MacCallum, 1913 | Branquias | 61.84 (3.16, 1-30) | 75 (7.51, 1-55) | 19.43 (0.46, 1-26) | 25.42 (2.63, 1-73) |
| Cestoda | |||||
| Tetraphyllidea (larva) G | Intestino | 1.32 (0.13, 2-10) | |||
| Acanthocephala | |||||
| Rhadinorhynchus cf . pristis G | Intestino | 1.19 (0.02, 1-2) | 5.08 (0.08, 1-3) | ||
| Nematoda | |||||
| Anisakis sp. (larva) G | Intestino | 14.47 (0.54, 1-21) | 12.50 (0.91, 1-27) | 2.49 (0.02, 0-1) | - |
| Hysterothylacium sp. G | Intestino | 6.58 (0.11, 1-11) | 11.18 (0.27, 1-5) | 11.86 (0.31, 1-6) | |
| Philometra sp. G | Gónada | 1.32 (0.08, 0-6) | 13.82 (0.38, 1-6) | ||
| Procamallanus sp. G | Intestino | 5.26 (0.26, 4-6) | 0.60 (0.01, 0-1) | ||
| Copepoda | |||||
| Caligus omissus E | Branquias | 26.32 (0.39, 1-3) | 73.03 (1.37, 1-8) | 41.02 (0.62, 1-4) | 37.29 (0.53, 1-3) |
| Lernanthrophus cf. giganteus G | Branquias | 2.63 (0.03, 0-1) | |||
| Orbitacolax cf. aculeatus G | Branquias | 1.32 (0.02, 1-2) | 1.24 (0.01, 0-1) | ||
| Cybicola buccatus EWilson 1922 | Branquias | 0.65 (0.01, 0-1) | 11.86 (0.12, 1-2) | ||
| Isopoda | |||||
| Livoneca redmanii G Leach 1818 | Branquias | 1.19 (0.01, 0-1) | |||
n: número de peces examinados; (P%): prevalencia; A: abundancia promedio; RI: rango de intensidad. Los superíndices a la derecha de la especie indican la clasificación del parásito: E: especialista, G: generalista.
Variación en los niveles de infección
La prevalencia de ocho de las especies más ampliamente distribuidas entre los hospederos examinados (excepto Lecithochirium microstomum) varió significativamente entre los años de muestreo. La prevalencia de infección de Didymocilindrus sp. fue más alta en marzo de 2011 (G = 106.56, p < 0.05), en tanto que Mexicotyle mexicana (G = 176.32 p < 0.05), Thoracocotyle crocea (G = 158.6, p < 0.05), Hysterothylacium sp. (G = 74.87, p < 0.05) y Caligus (G = 128.78, p < 0.05), registraron valores altos de prevalencia en 2012. Por su parte, Prosorhynchoides cybii (G = 136.05, p < 0.05), Didymocystis sp. (G = 142.08, p < 0.05) y Anisakis sp. (G = 32.32, p < 0.05) registraron valores altos de prevalencia durante dos años consecutivos (2011-2012; Cuadro I). En contraste con los porcentajes de infección, sólo dos especies de parásitos (Hysterothylacium sp. [MLG, F5,390 = 7.75, p < 0.01] y C. omissus [MLG, F5,390 = 3.79, p < 0.05]), presentaron una variación significativa en su abundancia durante el periodo de muestreo (Cuadro I). La abundancia de tres especies de parásitos se correlacionó positiva o negativa con la longitud total de los peces. Se registraron correlaciones positivas entre la longitud total y la abundancia del monogéneo T. crocea (rs = 0.257, p < 0.05) y del digéneo P. cybii (rs = 0.574, 0.836, p < 0.05) en muestreos de marzo de 2011 y 2012, mientras que la abundancia del copépodo C. omissus registró una correlación negativa (rs = -0.648, p < 0.05) durante el muestreo de marzo de 2012. De manera general, los valores de prevalencia se correlacionaron de forma positiva con los valores de abundancia de cada especie de parásito, lo cual indica que las especies más prevalentes fueron también las más abundantes (rs = 0.928, p < 0.01).
Distribución espacial
Los valores del ID indicaron que 12 especies de parásitos (65 % del total) presentaron un patrón de dispersión agregado, en todos o la mayoría de los muestreos. Los valores de agregación más altos (ID > 5) los presentaron el monogéneo T. crocea, los digéneos (didimozoideos) Anacetabulum sp., Didymocilindrus sp., Didymocystis sp. y Glomeritrema sp., y el nemátodo Anisakis sp.
Composición de la dieta de S. sierra
El análisis de la dieta de S. sierra indicó que su espectro alimenticio estuvo constituido por cinco tipos (ítems) de alimento, destacando los peces, los cuales representaron el mayor porcentaje en la muestra global (94 %). No obstante, la dieta de S. sierra fue más variada durante el muestreo de marzo de 2011 (H = 0.87, Cuadro II).
CUADRO II CARACTERÍSTICAS DE LAS COMUNIDADES COMPONENTES DE PARÁSITOS DE LA SIERRA Scomberomorus sierra EN LA BAHÍA DE ACAPULCO, GUERRERO, MÉXICO.
| Fecha | T ºC | MEI | Hosp. | Long. (cm) | Dieta | Riqueza | No. de parásitos | IBP | Especie dominante | H | Tº |
| Mar. 2011d | 26.2 | -1.8 | 76 | 44.9 ± 3.42* | 0.87* | 14* | 2099* | 0.488 | Dici | 1.15* | 16.82º |
| Mar. 2012d | 27.6 | -0.6 | 19 | 47.2 ± 4.3* | 0.53 | 10 | 621 | 0.320 | Thor | 1.00 | 29.36º |
| Ago. 2012r | 29.8 | -0.1 | 76 | 40.2 ± 4.6 | 0.63 | 12 | 1080* | 0.333 | Dici | 1.08 | 18.84º |
| Ene. 2018d | 27.1 | -0.8 | 84 | 28.5 ± 2.9 | 0.79 | 13 | 330 | 0.303 | Dici | 1.11 | 9.95º |
| Dic. 2018d | 27.4 | 0.1 | 77 | 24.1 ± 3.3 | 0.42 | 9 | 85 | 0.365 | Cali | 0.95 | 18.26º |
| May. 2019d | 29.6 | 0.3 | 59 | 35.7 ± 6.7 | 0.78 | 13 | 519 | 0.299 | Thor | 1.11 | 16.31º |
T ºC: temperatura superficial del mar; MEI: valores de anomalías climáticas; Hosp.: número de hospederos examinados; Long.: longitud total; Dieta: variedad de la dieta; IBP: índice de Berger-Parker; H: Índice de diversidad de Shannon-Wiener; Dici: Didymocilindrus sp., Thor: Thoracocotyle crocea, Cali: Caligus omissus.
*Significante a p < 0.05. Los superíndices representan códigos de las estaciones climáticas (d: secas, r: lluvias) utilizados en el análisis multivariado. Valores negativos del MEI representan la fase de enfriamiento del ENOS (La Niña), en tanto que valores positivos la fase cálida (El Niño).
Comunidad componente
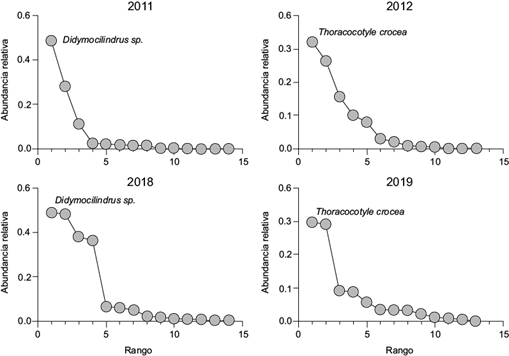
A nivel de comunidad componente, la riqueza de especies de parásitos varió significativamente de nueve en diciembre de 2018 a 14 en marzo de 2011 (t = 6.62, p < 0.01). El número total de parásitos varió de 85 en diciembre de 2018 a 2099 en marzo de 2011 (t = 7.59, p < 0.01). Los valores de diversidad variaron también de manera significativa (de 0.95 a 1.15, Cuadro II) a lo largo del periodo de estudio. El digéneo Didymocilindrus sp., el monogéneo T. crocea y el copépodo C. omissus fueron las especies que dominaron numéricamente en las comunidades de parásitos de S. sierra. La similitud entre las comunidades a este nivel varió de 13.73 a 65.78 % (Fig. 1) y fue mayor a nivel cualitativo (media = 69.10 %) que a nivel cuantitativo (media = 38.4 %). Las curvas de rango-abundancia (Fig. 2) construidas para observar posibles cambios en la estructura de las comunidades de parásitos, indicaron que la distribución de las abundancias relativas de las especies cambió notablemente entre los años de muestreo. Por ejemplo, durante 2011 y 2012 las abundancias se ajustaron a una distribución de tipo logarítmico (R2 = 0.794 y 0.994, respectivamente), mientras que en los muestreos de 2018 y 2019 una distribución de tipo log-normal presentó un mejor ajuste de las abundancias (R2 = 0.897, 0.864). Además, se registró una alternancia en la especie dominante entre los años de muestreo (Cuadro II). Por otra parte, en todos los muestreos se observó anidamiento significativo; sin embargo, el anidamiento fue más alto durante el de enero de 2018 (Tº = 9.95, Cuadro II).
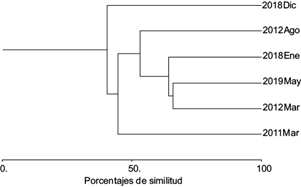
Fig. 1 Porcentajes de similitud (índice de Bray-Curtis) de las comunidades de parásitos de la sierra Scomberomorus sierra en la bahía de Acapulco, Guerrero, México.
Infracomunidades
Los tres parámetros evaluados a nivel de infracomunidad (número promedio de especies, número promedio de parásitos y diversidad promedio) presentaron el mismo patrón de variación temporal; es decir, registraron valores más altos durante el muestreo de marzo de 2012 (MLG, p < 0.01) para disminuir en los siguientes, e incrementarse nuevamente al final durante mayo de 2019 (Fig. 3). La longitud total de los hospederos se correlacionó positivamente (p < 0.01) con cada uno de los parámetros infracomunitarios cuando todos los muestreos fueron agrupados.
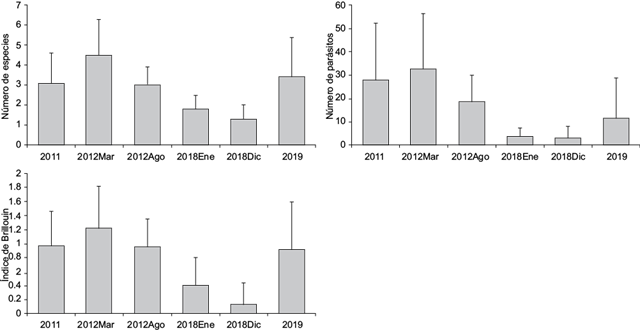
Fig. 3 Valores promedio de los parámetros de infracomunidad (± desviación estándar) de la sierra Scomberomorus sierra en la bahía de Acapulco, Guerrero, México.
En el ACP aplicado para identificar la posible influencia de los factores bióticos y abióticos sobre la estructura de las infracomunidades de parásitos (Fig. 4), las dos primeras variables componentes del modelo explicaron el 62.4 % de la varianza total. Estas variables contribuyeron con el 42.5 % (autovalor = 4.73) y el 20 % (autovalor = 2.13), respectivamente. La primera variable indicó que durante la fase de enfriamiento del ENOS, las infracomunidades de parásitos de S. sierra se caracterizaron por presentar una mayor diversidad y riqueza de especies, así como una mayor carga total de parásitos. La condición física de los peces fue más baja (Kn = -0.373) durante esta fase. Por su parte, la segunda variable sugirió que la fase cálida del ENOS se caracterizó por temperaturas ligeramente más altas, las cuales fueron relacionadas con una dieta menos variada (H = 0.481) por parte de los hospederos, así como con una menor riqueza y carga parasitaria.

Fig. 4 Dispersión del análisis de componentes principales de los factores bióticos y abióticos que influyen en la riqueza y diversidad de especies de las infracomunidades de parásitos de Scomberomorus sierra. Variables “predictoras”: Enso: valores del índice multivariado (MEI); Temperatura: valores de temperatura superficial; Estación: estación climática (secas/lluvias); Dieta: variedad de la dieta del hospedero; Kn: factor de condición de Fulton; Talla: longitud total. Parámetros de infracomunidad: Riqueza: número de especies de parásitos; H: valores del índice de diversidad de Brillouin; Equidad: uniformidad de las abundancias; Total: número total de parásitos; RDidy: número de especies de didimozoideos.
DISCUSIÓN
En los ecosistemas marinos, el aumento de los gases de efecto invernadero alteran tanto la química como la circulación oceánica, ocasionado cambios abruptos y persistentes en la temperatura superficial del mar, al igual que en la productividad de las redes alimenticias (Goedknegt et al. 2015, Marcogliese 2016, Lamb et al. 2018). El calentamiento global puede también hacer más intensos y cada vez más impredecibles algunos fenómenos naturales como El Niño o La Niña. En el presente estudio, variaciones atípicas en la temperatura superficial del mar ocasionadas por estos fenómenos generaron variaciones significativas en los niveles de infección de algunas especies de parásitos de S. sierra, ocasionando cambios importantes en la estructura de sus comunidades.
Composición de especies
El patrón general de riqueza de las especies de parásitos registradas en S. sierra durante el periodo de estudio fue el siguiente: Digenea > Copepoda > Nematoda > Monogenea > Cestoda = Acanthocephala = Isopoda. No existió diferencia entre la riqueza de especies en los dos eventos climáticos comparados (17 especies en ambos casos, Cuadro I); sin embargo, la composición de especies presentó algunas variaciones. Por ejemplo, larvas del céstodo tetrafilideo, así como el copépodo Lernanthrophus cf. giganteus sólo se registraron durante la fase fría del ENOS, en tanto que el acantocéfalo Rhadinorhynchus cf. pristis y el isópodo Livoneca redmanii sólo ocurrieron durante la fase cálida (2018-2019). Los ectoparásitos (tres monogéneos, tres digéneos didymozoideos, cuatro copépodos y un isópodo) dominaron numéricamente las comunidades de parásitos en ambas fases climáticas, representando el 80 % del total de parásitos recuperados.
Los monogéneos tienen un ciclo de vida directo y se transmiten a sus hospederos por medio del contacto; exhiben además alta especificidad hospedatoria y pueden reproducirse dentro de un amplio rango de temperaturas (Sasal y Morand 1998, Mendlová y Šimková 2014). No obstante, los niveles de infección de M. mexicana y T. crocea fueron más altos durante 2012 (fase fría del ENOS). El monogéneo T. crocea es considerado un parásito especialista del género Scomberomorus en las costas del Pacífico y el Atlántico del continente americano (Hayward y Rohde 1999). Su amplio rango de distribución geográfica sugiere que puede infectar peces a muy diferentes temperaturas; sin embargo, nuestros resultados indicaron que puede ser más infectivo cuando la temperatura se encuentra algunos grados por debajo de la temperatura promedio local (p. ej., 2011 y 2012; Cuadro II).
Los didimozoideos son considerados también altamente específicos para ciertos hospederos. Este grupo parasita principalmente peces escómbridos tropicales y subtropicales y rara vez se encuentra en especies de peces de agua dulce (Mele et al. 2012, Nascimento-Justo y Kohn 2012). Didymocilindrus sp. fue clasificada como una especie ectoparásita, ya que sólo fue recolectada de las branquias de S. sierra. Este helminto presentó sus niveles de infección más bajos durante el muestreo de 2018 (fase cálida), no observándose diferencias en su prevalencia respecto a los otros años de muestreo (Cuadro I).
Variación en los niveles de infección parasitaria entre las dos fases climáticas
Las variaciones interanuales registradas en los niveles de infección de ocho especies de parásitos (M. mexicana, T. crocea, Prosorhynchoides cybii, Didymocystis sp., Didymocilindrus sp., Anisakis sp., Hysterothylacium sp. y C. omissus) recolectados en S. sierra, pueden considerarse como un aspecto común de éstas y otras comunidades de parásitos marinos (Poulin 2006, Villalba-Vásquez et al. 2018, Miranda-Delgado et al. 2019, Violante-González et al. 2019, 2020). Los cambios registrados en cuatro especies de parásitos intestinales (P. cybii, Didymocystis sp., Anisakis sp. e Hysterothylacium sp.) pueden atribuirse a cambios en el comportamiento alimenticio del hospedero a lo largo del tiempo, así como a la disponibilidad de presas infectadas con estadios infectivos (Luque at al. 2004, Alves y Luque 2006, Oliva et al. 2008).
A pesar de que S. sierra tiene una dieta especializada, ya que se alimenta principalmente de peces pequeños (Collette y Nauen 1983), se comporta como un depredador oportunista, alimentándose de presas que abundan durante alguna temporada específica (Moreno-Sánchez et al. 2011). El análisis de la dieta de este pez indicó que su alimentación fue más variada durante algunos años (Cuadro II), cuando la temperatura del agua fue ligeramente más baja. Los descensos en la temperatura superficial del mar en la bahía de Acapulco, aunque ligeros, pueden influir en la productividad de las redes alimenticias (Miranda-Delgado et al. 2019), por lo que los parásitos que utilizan rutas tróficas (especies intestinales) para infectar a sus hospederos pueden ser más abundantes y diversos durante algunas temporadas en que sus hospederos se alimentan de una mayor variedad de presas.
Sin embargo, la densidad poblacional y el comportamiento gregario de S. sierra pueden ser una mejor explicación de la variación temporal y espacial registrada en los niveles de infección de tres especies de ectoparásitos (M. mexicana, T. crocea y C. omissus). La formación de grandes cardúmenes por parte de S. sierra puede facilitar la transmisión de algunas especies de parásitos, principalmente de aquellos que presentan un ciclo de transmisión directo como los monogéneos y copépodos (Sasal y Morand 1998, Luque et al. 2004).
Patrón de dispersión de las especies de parásitos
Los parásitos de peces marinos tienden a presentar un tipo de dispersión agregada (Rohde 2005, Poulin 2013). Este patrón de agregación origina que la mayoría de los hospederos no tenga o albergue pocos individuos, en tanto que unos pocos presenten muchos parásitos (Poulin y Morand 2000). El 65 % de las especies de parásitos que infectaron a S. sierra, presentaron una dispersión agregada en la mayoría de los años de muestreo; no obstante, el nivel de agregación varió a lo largo del tiempo. Estos resultados sugieren por lo tanto la existencia de diferencias en las tasas de exposición a ectoparásitos (monogéneos o copépodos) por parte del hospedero, debido posiblemente al efecto de los factores ambientales (Poulin 2013) o bien a diferencias en el comportamiento alimenticio a lo largo de los años de S. sierra, el cual influyó en el nivel de agregación de algunas especies de endoparásitos.
Comunidad componente
La riqueza de especies de parásitos a nivel componente en S. sierra (nueve a 14 especies, Cuadro II) fue muy similar a la reportada para este hospedero tanto en la misma como en otras localidades (Santos-Bustos et al. 2020, Bárcenas 2021). Sin embargo, la similitud en la composición de especies a nivel cuantitativo fue ligeramente más baja entre fases climáticas (38.4 %) que durante la misma fase (45.13 y 43.90 %, respectivamente); esto sugiere que la estructura y composición de especies de la comunidad de parásitos puede ser más variable entre estos dos eventos climáticos anómalos (La Niña y El Niño). Por ejemplo, la riqueza más baja de especies, así como la menor carga parasitaria, se registraron durante el muestreo de diciembre de 2018 (fase cálida del ENOS, Cuadro II). La especie dominante durante este muestreo fue C. omissus, un copépodo considerado como especialista de S. sierra. La temperatura tiene gran influencia en el ciclo de vida de muchas especies de ectoparásitos, y varios estudios indican que los niveles de infección pueden alcanzar un pico durante los periodos más cálidos (Brazenor et al. 2020). En la bahía de Acapulco, las temperaturas más cálidas se registran generalmente entre abril y junio; por ello, no es común observar temperaturas cálidas durante diciembre. Por lo tanto, la dominancia de C. omissus durante este mes de muestreo podría atribuirse al incremento atípico de la temperatura generado por el fenómeno de El Niño.
La presencia de anidamiento en las comunidades de parásitos también se ha considerado como evidencia de estructuración en estas comunidades (Poulin y Valtonen 2001, Norton et al. 2004). Un patrón de especies anidadas sugiere que las especies de parásitos con altas prevalencias (especies comunes) pueden encontrarse en infracomunidades ricas o pobres en especies, en tanto que las especies raras sólo están presentes en las infracomunidades de mayor riqueza en especies (Poulin y Valtonen 2001). A pesar de que este patrón de estructuración no se ha detectado en todas las comunidades de parásitos examinadas hasta la fecha en México (Vidal-Martínez y Poulin 2003, Violante-González et al. 2008), todas las comunidades de S. sierra presentaron anidamiento, aunque no con la misma intensidad (Cuadro II). Existen varios procesos que pueden generar anidamiento en las infracomunidades de parásitos, incluidos el muestreo pasivo y la colonización secuencial de parásitos (Violante-González et al. 2008). Debido a que diferentes especies de parásitos dominaron las comunidades de parásitos a lo largo del periodo de estudio, así como a los cambios registrados en la distribución de las abundancias de especies (Fig. 2), es posible considerar que un proceso de colonización secuencial de las distintas especies de parásitos pueda explicar la variación en la intensidad del anidamiento observado en las comunidades de parásitos de S. sierra.
Infracomunidades
Las fluctuaciones climáticas a gran escala como el Niño y La Niña afectan muchos procesos ecológicos, incluidos los de transmisión de gran variedad de especies de parásitos (Alvitres et al. 1999, Oliva et al. 2008). Por ejemplo, los parásitos de transmisión trófica presentan estadios larvarios de vida libre, los cuales son afectados por las mismas condiciones físicas oceanográficas (temperatura, salinidad, corrientes), que a su vez impactan a los estadios larvarios de otros organismos marinos, incluidos aquellos que actúan como sus hospederos intermediarios o definitivos (Marcogliese 2005, Jacobson et al. 2012, Miranda-Delgado et al. 2019).
Los resultados del ACP (Fig. 4) aplicado para identificar la posible influencia de los factores bióticos y abióticos sobre la estructura de las infracomunidades de parásitos confirmaron los resultados obtenidos. Las dos fases climáticas del ENOS ejercieron efectos distintos sobre las comunidades de parásitos de S. sierra. Por ejemplo, la fase de enfriamiento (La Niña) tuvo un efecto indirecto (en cascada) sobre la estructura de las infracomunidades de parásitos. Las temperaturas superficiales más frías registradas durante este evento posiblemente incrementaron la productividad y la biomasa de las redes alimenticias dentro de la localidad (Marcogliese 2005, Oliva et al. 2008), dando como resultado una mayor disponibilidad de presas para S. sierra. Esta mayor disponibilidad y variedad de presas se vio reflejada a su vez en una mayor diversidad y riqueza de especies de endoparásitos que infectan al hospedero a partir del consumo de presas infectadas. Es muy común que cuando ingresan corrientes de aguas frías a la bahía de Acapulco ingresen también grandes cardúmenes de peces forrajeros (sardinas y anchovetas), por lo que grandes predadores como S. sierra son capturados con mayor frecuencia dentro de la Bahía durante estos episodios. Por otra parte, la fase cálida (El Niño) pareció tener un efecto directo sobre algunas especies de ectoparásitos como los copépodos C. omissus y Cybicola buccatus, los cuales presentaron niveles de infección más altos durante esta fase (Cuadro I).
CONCLUSIONES
De manera general, los resultados sugieren que las especies de parásitos de S. sierra responden de manera diferente a los cambios ambientales que ocurren durante eventos climáticos anómalos como la Niña y El Niño. Temperaturas superficiales más frías pueden incrementar la productividad marina, ocasionando mayores infecciones de algunos parásitos intestinales, los cuales son adquiridos por el hospedero a partir de la ingestión de una mayor cantidad y variedad de presas, muchas de ellas infectadas con estadios larvarios. Por su parte, las temperaturas más cálidas pueden generar mayores infecciones de algunas especies de ectoparásitos. Por lo tanto, las variaciones en los niveles de infección de estas especies de parásitos pueden ocasionar cambios importantes en la estructura de las comunidades de parásitos de S. sierra en la bahía de Acapulco durante estos eventos climáticos atípicos.