INTRODUCCIÓN
El rendimiento y la calidad de los cultivos agrícolas dependen en gran medida de las condiciones del suelo. Diferentes campos de la actividad humana pueden contaminar este recurso por el uso de productos químicos contenidos en el agua residual doméstica y en efluentes industriales (Biczak et al. 2018). Estos productos están asociados con residuos agrícolas y fertilizantes, así como actividades industriales, mineras y de refinación del petróleo (Chopra et al. 2009). Además, estas actividades pueden contaminar el suelo con metales como Pb y Cd, metaloides como As, hidrocarburos aromáticos policíclicos y bifenilos policlorados, entre otros. Estos contaminantes en el suelo pueden transferirse a los humanos por medio de las plantas y animales (Kopittke et al. 2019).
Entre los contaminantes químicos se distinguen los surfactantes que se utilizan en la agricultura para la producción de biocidas (Gerba 2015), acondicionadores del suelo (Abu-Zreig et al. 2003), plaguicidas (Appah et al. 2020), materiales con nanotecnología (Biczak et al. 2018) como la fabricación de nanoformulaciones con arcillas (Kumar et al. 2019, Romero-Méndez et al. 2019, 2021). Los surfactantes son compuestos de moléculas anfipáticas o anfifílicas que contienen restos hidrofóbicos (repelentes al agua) o lipofílicos (afines a los lípidos) e hidrofílicos o polares (Massinon et al. 2014). El grupo hidrófobo suele ser un hidrocarburo de cadena larga y el grupo hidrófilo es un grupo iónico (Fernández-Cirreli et al. 2008), como es el caso de los surfactantes catiónicos que contienen iones de amonio cuaternario como partes hidrófilas (Castro et al. 2014). Esta estructura les permite adsorberse fácilmente a las partículas que tienen carga negativa (Ying 2006).
Los niveles elevados de surfactantes en el ambiente pueden afectar en gran medida el ecosistema, al generar toxicidad para los organismos, desde mamíferos (Ivanković y Hrenović 2010) y peces hasta microorganismos como bacterias, algas y protozoos (Kreuzinger et al. 2007, Jing et al. 2012, Chen et al. 2014).
La fitotoxicidad se define como un efecto negativo en el crecimiento o desarrollo de las plantas y se puede relacionar con anomalías celulares (Werrie et al. 2020). Algunos productos fitoquímicos influyen en los procesos fisiológicos de crecimiento y desarrollo en la división de células vegetales y el alargamiento de raíces (Yan et al. 2015). La fitotoxicidad puede deberse a sustancias como hidrocarburos, surfactantes, metales pesados, fitotoxinas, pesticidas y antibióticos que se encuentran mezclados en el ambiente (Pan y Chu 2016, Majeed et al. 2019, An-Nori et al. 2020, Gupta et al. 2020).
Se ha investigado el uso de sustancias surfactantes en diferentes plantas cultivadas en suelo al utilizar agua de riego. En los resultados se encontraron diversos síntomas de fitotoxicidad provocados por surfactantes catiónicos como cloruro de tetraetil amonio y bromuro de tetraetil amonio en Hordeum vulgare y Raphanus sativus L. (Pawłowska y Biczak 2016, Biczak et al. 2018), y cloruro de bencil dimetil dodecil amonio en Lemna minor y Brassica napus (Richter et al. 2016); así como por surfactantes aniónicos como sulfonato de aquil benceno lineal en Lactuca sativa y Abelmoschus esculentus (Sawadogo et al. 2014), y alquil benceno sulfonato de sodio en Lycopersicon esculentum Mill. (Misra et al. 2010).
El contacto directo y constante con contaminantes presentes en el suelo provoca daño a las membranas de las células de la raíz y los compuestos tóxicos podrían ingresar en el interior del organismo vegetal (Liu et al. 2013). Algunos estudios se enfocan a la aplicación de surfactantes en sistemas hidropónicos con el objetivo de evaluar el impacto del uso de aguas contaminadas; al respecto, se tienen estudios en trigo con Igepon TC-42, lauril éter sulfato sódico y cloruro de dodecil trimetil amonio (Garland et al. 2000, 2004, Li et al. 2019); y en lechuga y berro contaminados con cloruro de dimetil dodecil amonio (Khan et al. 2018). La razón para utilizar un sistema hidropónico es que las raíces tienen contacto directo con la solución nutritiva y las plantas pueden crecer más rápido que en el cultivo convencional en suelo (Janiak et al. 2020).
La mayoría de las investigaciones se han realizado en cultivos hidropónicos con plantas de lechuga (Wang et al. 2011, Heidari 2013, Song y Kim 2016). En particular, las pruebas de fitotoxicidad con plantas como L. sativa presentan varias ventajas. Primero, son simples, rápidas y confiables. En segundo lugar, son económicas y no requieren equipos importantes. En tercer lugar, las plantas pueden ser más sensibles al estrés ambiental que otros organismos (Valerio et al. 2007).
Los resultados de toxicidad permiten cuantificar los cambios fisiológicos en las plantas y estimar la evaluación del riesgo de contaminación ambiental sobre el posible uso de surfactantes. Por lo tanto, el objetivo de este estudio fue evaluar la fitotoxicidad de cuatro surfactantes catiónicos en el crecimiento de plantas de lechuga (Lactuca sativa L.) cultivadas con hidroponía.
MATERIALES Y MÉTODOS
Surfactantes
Para los experimentos se utilizaron cuatro surfactantes catiónicos: bromuro de hexadecil trimetil amonio (C19H42BrN), cloruro de trimetil octadecil amonio (CH3(CH2)17N(Cl)(CH3)3), dodecil amina (CH3(CH2)11NH2) y hexadecil amina (CH3(CH2)15 NH2) (Sigma Aldrich Chemical).
Materia prima
Se usaron plantas de lechuga (var. Montemar) con 30 días de crecimiento, seis hojas y una altura de 12 cm en recipientes de plástico oscuros de 1 L. Se colocó una planta en un recipiente con solución nutritiva (Steiner 1961) compuesta de la siguiente manera (en meq/L): 12 NO3 -, 1 H2PO4 -, 7 SO4 2-, 7 K+, 2 Mg2+ y 9 Ca2+. Se utilizó agua destilada con la siguiente composición química: pH 6.0, conductividad eléctrica (CE) de 0.2 dS/m, cloruros 0.004 %, sulfatos 0.0004 %, Fe negativo, CO2 negativo, alcalinidad 10.0 mg/L max. El pH se ajustó a 5.5 con H3PO4 y la CE final fue de 0.5 dS/m los primeros 10 días, 1.0 dS/m a los 20 días y 1.5 dS/m a los 30 días. Los fertilizantes utilizados fueron Ca(NO3)2·4H2O, KNO3, MgSO4·7H2O, K2SO4 y H3PO4. Los micronutrientes se añadieron con Kelatex-Multi, que proporciona Fe 6.25 %, Mn 2 %, B 0.40 %, Zn 2 %, Cu 0.15 % y Mo 0.05 % a manera de quelato EDTA. Las plantas tuvieron un periodo de adaptación de cinco días antes de la aplicación de los tratamientos.
Cultivo hidropónico de la lechuga con el sistema de raíz flotante
Se estableció un sistema hidropónico de raíz flotante en los invernaderos del Centro de Hidroponía de la Facultad de Agronomía y Veterinaria, Universidad Autónoma de San Luis Potosí, el cual constó de cuatro experimentos (junio y agosto de 2019 y enero y marzo de 2020), en un invernadero tipo túnel de 9 × 5 m. Las temperaturas medias (ºC) fueron las siguientes: junio: 20.36, agosto: 19.62, enero: 14.06 y marzo: 21.19). En el sistema hidropónico se utilizó una solución nutritiva (Steiner 1961) al 25 %. Se aplicaron 11 tratamientos con 0, 1, 2, 3, 4, 5, 6, 7, 8, 9 y 10 mg/L de los surfactantes catiónicos bromuro de hexadecil trimetil amonio (HDTMA), cloruro de octadecil trimetil amonio (OTAC), dodecil amina (DDA) y hexadecil amina (HDA). Durante la evaluación, se agregó agua destilada (correspondiente a la traspiración de las plantas) diariamente y la solución nutritiva se reemplazó cada 10 días aumentado un 25 % la concentración de la solución Steiner hasta llegar al 75 %. El diseño experimental fue completamente al azar. Cada tratamiento tuvo seis repeticiones (66 unidades experimentales) y una planta como unidad experimental. Las variables medidas cada 24 h fueron CE (Orion Meter 155, EUA.) en la solución nutritiva, consumo diario de agua (bureta de 50 mL) y contenido de NO3 -, K+ y Ca+2 en la solución nutritiva (Ionómetro Laqua Twin, Horiba, Japón). Al final del ciclo se estableció el consumo de estos nutrientes por la planta: se obtuvo una diferencia de concentraciones de cada nutriente y se comparó con el contenido inicial, estableciéndose una relación entre la concentración medida y la aplicada. Al final del experimento se midieron las siguientes variables: biomasa seca de raíz y hoja, para lo cual se utilizó un horno de secado de aire forzado (Omron, Japón) a 72 ºC, hasta obtener un peso constante que se midió en una balanza digital (serie Ohaus PAJ4102N Gold, EUA); anchura y longitud de las hojas, que se registraron con una regla de 20 cm; número de hojas y área foliar (CID 202 Portable Leaf Area Meter, EUA).
RESULTADOS Y DISCUSIÓN
El surfactante DDA no indujo diferencias significativas en el consumo de agua (Fig. 1); el HDA lo redujo de 34 hasta 82 % a partir de 2 mg/L, el OTAC de 19.9 a 59 % a partir de 1 mg/L y el HDTMA de 27 a 78.4 % a partir de 1 mg/L. En un cultivo de lechuga en hidroponía con aplicación de HDTMA en una concentración de 0.5 mg/L, el consumo de agua disminuyó en un 17.5 % debido a que el surfactante afectó el sistema radical y esto limitó la absorción de agua (Romero-Méndez et al. 2019). En este sentido, Pawloska y Biczak (2016) mencionan que los surfactantes catiónicos presentes en la rizosfera inducen a una limitación en el crecimiento de raíces al estar en contacto directo con la raíz. Esto se debe a que el surfactante provoca un daño en las membranas de las células y los compuestos tóxicos ingresan en las células de la planta (Liu et al. 2013). La disminución en el consumo de agua por las plantas de lechuga en este experimento se atribuye al efecto negativo de los surfactantes en las raíces (Fig. 2). De acuerdo con lo mencionado por Yan et al. (2015), algunos productos fitoquímicos impactan el crecimiento y desarrollo de células vegetales y el alargamiento de raíces. Werrie et al. 2020 mencionan que cuando se presentan anomalías celulares y se afecta negativamente el crecimiento puede decirse que hay fitotoxicidad.
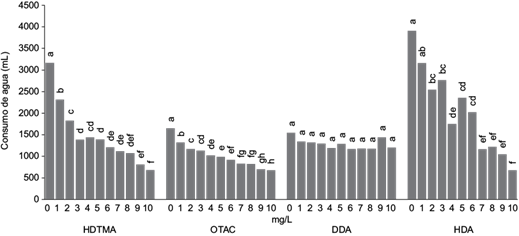
Fig. 1 Consumo de agua durante el periodo de contacto con los surfactantes HDTMA, OTAC, DDA y HDA en el crecimiento de lechuga hidropónica. Letras distintas en los tratamientos indican diferencias significativas (Tukey, p ≤ 0.05). (HDTMA: bromuro de hexadecil trimetil amonio, OTAC: cloruro de octadecil trimetil amonio, DDA: dodecil amina y HDA: hexadecil amina.)

Fig. 2 Efecto de cuatro surfactantes catiónicos sobre las raíces de lechugas cultivadas en hidroponía. (HDTMA: bromuro de hexadecil trimetil amonio, OTAC: cloruro de octadecil trimetil amonio, DDA: dodecil amina y HDA: hexadecil amina.)
La CE inicial (Fig. 3a) de la solución al 25 % fue de 0.62 dS/m. Después de 10 días de exposición a la aplicación con surfactantes se encontró que el DDA disminuyó la CE en un 35 % en comparación con la concentración inicial. Los otros surfactantes indujeron una menor CE a partir de 2 mg/L: el HDTMA la redujo en 43 % y el OTAC en 27.4 %, en tanto que tratamiento de 3 mg/L con HDA la disminuyó en 42 %. Las plantas modifican la CE a medida que absorben nutrientes y agua de la solución nutritiva (Trejo-Téllez y Gómez 2012). En este caso, al aumentar la dosis de surfactante la disminución de CE en las plantas de lechuga fue menor debido a que absorbieron menos nutrientes debido al daño radical provocado por los surfactantes.

Fig. 3 Conductividad eléctrica durante el desarrollo de lechuga cultivada en hidroponía expuesta a cuatro surfactantes (HDTMA, OTAC, DDA y HDA). (a) 10 días, 25 % de solución Steiner; (b) 20 días, 50 % de solución Steiner; (c) 30 días, 75 % de solución Steiner. Letras distintas en los tratamientos indican diferencias significativas (Tukey, p ≤0.05). (HDTMA: bromuro de hexadecil trimetil amonio, OTAC: cloruro de octadecil trimetil amonio, DDA: dodecil amina y HDA: hexadecil amina.)
La solución al 50 % (Fig. 3b) generó una CE inicial de 1.05 dS/m, la cual disminuyó al aplicarse los tratamientos con surfactantes. La disminución de DDA fue del 31 % respecto al valor inicial, sin diferencias significativas entre los tratamientos. En el caso del HDTMA, al aplicar 3 mg/L, se observó una reducción del 22 %. Con OTAC, el tratamiento con 1 mg/L produjo una disminución del 28 %. Finalmente, el surfactante HDA mostró una reducción del 54 % al aplicar 4 mg/L en comparación con la CE inicial. Lo anterior puede compararse con los resultados obtenidos por Janiak et al. (2020), quienes midieron la CE para estimar la presión osmótica de la solución durante el ciclo de crecimiento de la lechuga. La CE en los cultivos con surfactantes fue 1.2-1.5 veces mayor que en el cultivo de referencia con agua limpia. Domingues et al. (2012) mencionan que la CE es proporcional al contenido total de iones, por lo que una reducción de la CE va acompañada de una menor cantidad total de iones disponibles para la absorción por las raíces.
Al utilizar una solución al 75 %, la CE inicial (Fig. 3c) fue de 1.5 dS/m y después de 10 días mostró diferencias significativas. Al utilizar el tratamiento de 2 mg/L, la CE se redujo en 20 y 52 % con los surfactantes HDTMA y HDA, respectivamente. Los resultados con el tratamiento de 3 mg/L fueron similares: la CE disminuyó en 53 y 30 % con OTAC y DDA, respectivamente. Romero-Méndez et al. (2019) mencionan que la absorción de nutrientes disminuye debido a que el daño radicular del surfactante limita estas funciones. Domingues et al. (2012) afirman que cada uno de los macro y micronutrientes tienen al menos una función dentro de la planta y su exceso o deficiencia conduce a síntomas de deficiencia o toxicidad.
La variable biomasa seca (Fig. 4) no mostró diferencias significativas con el surfactante DDA en ningún tratamiento aplicado. Con el OTAC, la biomasa seca disminuyó en 46 a 67 % conforme se aumentó la dosis a partir de 4 mg/L; de igual manera, con el HDA se redujo de 60 a 88 % a partir del tratamiento con 4 mg/L, y con el HDTMA de 27 a 81 % a partir de 1 mg/L. Janiak et al. (2020) reportan que la materia seca de lechuga cultivada con un sistema aeropónico por 42 días se reduce 50 % con una dosis de 1.7 g/L del surfactante aniónico SLES. De igual manera, la materia seca de lechuga cultivada durante cuatro meses con agua de riego y detergente aniónico (sulfonato de alquilbenceno lineal) disminuye un 30 % con una concentración de 13 mg/L y un 75 % con una concentración de 135 mg/L (Sawadogo et al. 2014). La presencia de surfactantes catiónicos en el cultivo de lechuga durante 12 días reduce la materia seca en un 66 % con BDTH y un 75 % con BDDA a una concentración de 0.25 mg/L (Khan et al. 2018).
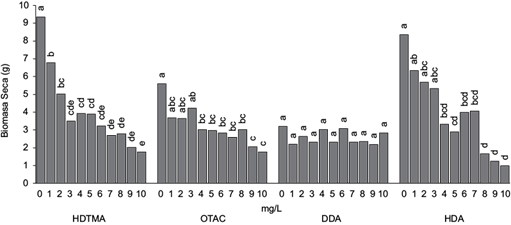
Fig. 4 Biomasa seca de tejido vegetal de lechuga expuesta a los surfactantes HDTMA, OTAC, DDA y HDA en el crecimiento de lechuga hidropónica. Letras distintas en los tratamientos indican diferencias significativas (Tukey, p < 0.05). (HDTMA: bromuro de hexadecil trimetil amonio, OTAC: cloruro de octadecil trimetil amonio, DDA: dodecil amina y HDA: hexadecil amina.)
Los resultados del cuadro I muestran que la aplicación de surfactantes en la solución nutritiva afectó las variables número de hojas, longitud y ancho de hoja. El número de hojas se redujo 23 y 31 % con el tratamiento de 1 mg/L de HDTMA y OTAC, respectivamente; 18 % con 4 mg/L de HDA, y 22 % con 3 y 8 mg de LDDA. El tratamiento con HDTMA a 2 mg/L y concentraciones mayores a 4 mg/L redujo la longitud de la hoja en 16-21 %. En el caso del OTAC, concentraciones a partir de 4 mg/L redujeron la longitud de la hoja en un 21 %. Con HDA, el tratamiento con 4 mg/L y concentraciones mayores a 7 mg/L provocaron una disminución del 30 al 40 %. En cuanto al DDA, no se observaron diferencias entre los tratamientos.
CUADRO I CARACTERÍSTICAS DE LAS HOJAS DE LECHUGA EXPUESTA A LOS SURFACTANTES HDTMA, OTAC, DDA Y HDA DURANTE EL CRECIMIENTO DE LECHUGA HIDROPÓNICA.
| Tratamientos | Número de hojas | Longitud de hojas (cm) | Ancho de hojas (cm) | |||||||||
| HDTMA | OTAC | DDA | HDA | HDTMA | OTAC | DDA | HDA | HDTMA | OTAC | DDA | HDA | |
| 0 mg/L | 20 a | 21.3 a | 14.0 ab | 15.0 a | 14.3 a | 13.5 a | 13.0 a | 14.8 a | 11.5 a | 13.7 a | 10.6 a | 14.7 a |
| 1 mg/L | 15 b | 14.5 b | 12.3 ab | 15.2 a | 12.7 ab | 12.5 a | 11.7 a | 14.2 a | 10.2 ab | 9.7 bcd | 9.0 a | 13.5 ab |
| 2 mg/L | 13 bc | 15.7 b | 11.3 ab | 12.8 ab | 12.0 bc | 13.2 a | 11.4 a | 12.2 ab | 9.7 abc | 10.8 b | 9.2 a | 11.7 bc |
| 3 mg/L | 13 bc | 15.7 b | 10.8b | 13.5 ab | 12.3 ab | 13.0 a | 10.5 a | 13.5 a | 9.5 abc | 11.0 b | 8.8 a | 13.2 ab |
| 4 mg/L | 14 bc | 14.0 b | 15.2 a | 12.2 b | 11.2 bcd | 10.7 b | 11.0 a | 10.3 bc | 9.7 abc | 10.5 bc | 8.2 a | 12.2 bc |
| 5 mg/L | 13 bc | 11.5 c | 12.7 ab | 13.0 ab | 10.0 cde | 9.5 bc | 12.0 a | 12.8 ab | 8.0 c | 8.8 cde | 9.5 a | 13.2 ab |
| 6 mg/L | 12 cd | 11.2 c | 12.2 ab | 13.7 ab | 9.7 de | 7.2 d | 10.7 a | 13.7 a | 8.7 bc | 8.2 de | 8.5 a | 13.2 ab |
| 7 mg/L | 11cd | 10.7 c | 12.7 ab | 9.7 c | 9.3 de | 8.0 cd | 10.8 a | 8.8 cd | 7.8 c | 7.8 e | 8.3 a | 9.5 cd |
| 8 mg/L | 11 cd | 11.5 c | 11.0 b | 9.7 c | 8.5 e | 8.2 cd | 11.0 a | 9.0 cd | 4.7 d | 8.0 de | 9.0 a | 9.3 cd |
| 9 mg/L | 11 cd | 10.8 c | 11.8 ab | 8.7 c | 8.5 e | 8.2 cd | 11.7 a | 7.8 cd | 4.7 d | 8.0 de | 9.5 a | 8.3 d |
| 10 mg/L | 9 d | 10.2 c | 11.5 ab | 8.0 c | 8.5 e | 8.0 cd | 12.0 a | 7.3 d | 5.5 d | 7.3 e | 9.7 a | 7.8 d |
| DMS | 2.85 | 2.09 | 4.01 | 2.38 | 2.24 | 1.5 | 2.52 | 2.69 | 2.1 | 1.78 | 2.92 | 2.48 |
| CV | 11.51 | 8.09 | 16.82 | 10.3 | 10.9 | 7.63 | 11.4 | 12.29 | 13.29 | 9.77 | 16.58 | 11.15 |
Letras distintas en los tratamientos por columna indican diferencias significativas (Tukey, p < 0.05). HDTMA: bromuro de hexadecil trimetil amonio, OTAC: cloruro de octadecil trimetil amonio, DDA: dodecil amina y HDA: hexadecil amina.
En cuanto al ancho de la hoja, el efecto negativo se presentó con diferentes tratamientos. El HDTMA, a partir de 5 mg/L, redujo el ancho en un 30 %. El OTAC, a partir de 2 mg/L, provocó una disminución del 21 %. En el caso del DDA, los tratamientos con concentraciones superiores a 1 mg/L redujeron el ancho en un 15 %. Para el HDA se observó una disminución del 20 % con 2 mg/L, del 17 % con 4 mg/L, y a partir de 7 mg/L la reducción fue del 35 %. De acuerdo con lo mencionado por Richter et al. (2016), en Lemna minor la fitotoxicidad del surfactante catiónico BDDA mostró efectos visuales de hojas ligeramente cloróticas y reducción general del tamaño y número de hojas, en tanto que Trinchera y Baratella (2018) mencionan que la adición del surfactante no iónico metiloxirano (MOS) en la modalidad de fertirriego no afectó el número hojas en el cultivo de lechuga. El grado de fitotoxicidad depende de la concentración del surfactante, la duración de exposición y las especies de las plantas (Biczak et al. 2018).
La aplicación del surfactante DDA no mostró ninguna diferencia estadística en el área foliar con los tratamientos aplicados (Fig. 5). En los demás tratamientos el área foliar se redujo a partir de 2 mg/L conforme aumentó la dosis. Con el OTAC se redujo de 40 a 55 %, con el HDA de 41 hasta 89 % y con el HDTMA de 37 a 83 %. En contraste, Trinchera y Baratella (2018) encontraron que el uso de surfactantes con fertirrigación en suelo induce hojas de lechuga más expandidas y delgadas, lo cual aumenta el área foliar de 5 a 13 % al utilizar una concentración de 0.2-1.0 mL de metiloxirano (MOS) en la solución Hoagland.
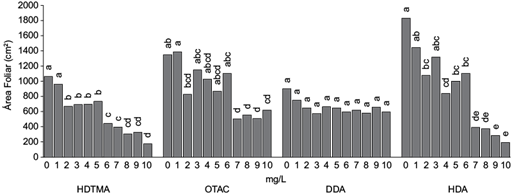
Fig. 5 Área foliar de lechuga expuesta a los surfactantes HDTMA, OTAC, DDA y HDA en el crecimiento de lechuga hidropónica. Letras distintas en los tratamientos indican diferencias significativas (Tukey, p < 0.05). (HDTMA: bromuro de hexadecil trimetil amonio, OTAC: cloruro de octadecil trimetil amonio, DDA: dodecil amina y HDA: hexadecil amina.)
El consumo de nitrato en la solución nutritiva (Fig. 6a) de HDTMA y OTAC no se modificó por el tratamiento de 1 mg/L, ya que éste fue igual al testigo. Se observó un efecto negativo en el consumo a partir de los siguientes tratamientos: con HDTMA, desde 2 mg/L, la reducción fue del 45 al 82 %; con OTAC, entre el 10 y el 28 %; con DDA, a partir de 1 mg/L, la disminución fue del 14 al 49 %, y con HDA, la reducción fluctuó entre el 11 y el 57 %. Reichman y Wightwick (2013) observaron una reducción del 50 % en el contenido de nitrato al usar surfactantes catiónicos (cloruro de bencil dimetil dodecil amonio y cloruro de bencil dimetil tetradecil amonio) en dosis de 0.025-0.25 mg/L. Por otro lado, Trinchera y Baratella (2018) evaluaron el surfactante no iónico MOS mediante la aplicación de una dosis de 0.2 a 1.0 mL/L en un sistema de fertirrigación; los resultados para el nitrógeno total indicaron una disminución del 5 % al utilizar 0.2 mL/L, y un aumento del 12 % al utilizar 1.0 mL/L. Naseem y Arif (2018) observaron que las plantas pueden absorber los contaminantes químicos acumulados en ambientes acuáticos o terrestres a través de sus raíces, lo que puede causar fitotoxicidad.
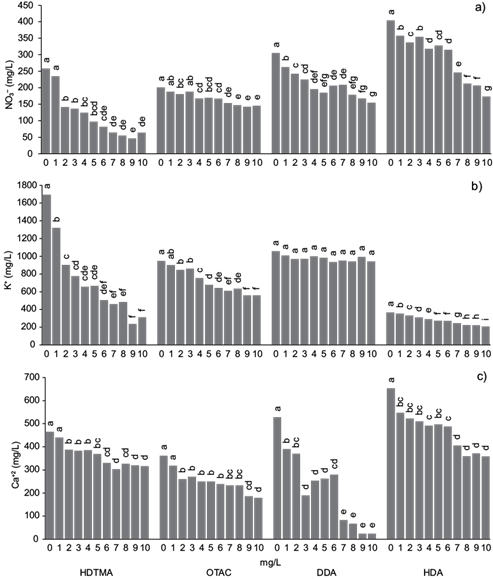
Fig. 6 Consumo de nutrientes en la solución nutritiva expuesta a los surfactantes HDTMA, OTAC, DDA y HDA en el crecimiento de lechuga hidropónica. (a) Nitrato, (b) potasio, (c) calcio. Letras distintas en los tratamientos indican diferencias significativas (Tukey, p < 0.05). (HDTMA: bromuro de hexadecil trimetil amonio, OTAC: cloruro de octadecil trimetil amonio, DDA: dodecil amina y HDA: hexadecil amina.)
El tratamiento con 1 mg/L del surfactante HDTMA disminuyó de 22 a 81 % el consumo de potasio en la solución nutritiva (Fig. 6b). En el caso del OTAC, el tratamiento con 2 mg/L redujo la cantidad consumida de potasio en la solución nutritiva de 11 a 41 %. Con el DDA no se observaron diferencias significativas, mientras que con el tratamiento del surfactante HDA el consumo disminuyó de potasio en 38 a 43 % a partir de 1 mg/L. Janiak et al. (2020) y Reichman y Wightwick (2013) también reporatron un efecto similar de los surfactantes en el nivel de potasio en el rango de 27-10 % con una dosis de 1.7-0.07 g/L del surfactante aniónico lauril éter sulfato de sodio (SLES) y de 52-63 % al usar un detergente ecológico y aguas grises de lavandería. En contraste, Trinchera y Baratella (2018) observaron una reducción de K+ de 8 % al administrar el surfactante tensioactivo no iónico MOS por fertirrigación en dosis de 0.2-1.0 mL/L, lo cual indicó una menor disponibilidad de nutrientes que puede comprometer el rendimiento de la lechuga.
El consumo del calcio en la solución nutritiva (Fig. 6c) con el surfactante HDTMA a partir del tratamiento con 2 mg/L presentó una reducción del 17 al 32 %. De la misma forma, con el tratamiento de 2 mg/L del surfactante OTAC disminuyó la cantidad consumida de Ca en 18 a 43 %. A partir del tratamiento de 1 mg/L de DDA se presentó una reducción en el consumo de Ca del 26 al 95 % y con dosis similar de HDA éste disminuyó de 17 a 45 %. Por el contrario, Janiak et al. (2020) detectaron un incremento del 18 % al usar el surfactante aniónico lauril éter sulfato de sodio (SLES) y de 11 % con la dosis de 0.08 g/L del surfactante dodecil benceno sulfonato (SDBS). Trinchera y Baratella (2018) mencionan que el surfactante aniónico no es un factor limitante para el crecimiento de la lechuga, ya que sus tratamientos tienen resultados similares en la concentración de calcio.
Estos experimentos con surfactantes catiónicos como HDA, DDA, HDTMA y OTAC comprueban que los tensioactivos producen efectos tóxicos por los compuestos que integran las formulaciones, los cuales pueden influir en los efectos biológicos. La longitud de la cadena de carbonos y del ion acompañante del surfactante podría estar implicada en la toxicidad sobre las plantas de lechuga; los de cadena corta (HDA 16, DDA 12) causan menor daño que los de cadena larga (OTAC 21, HDTMA 19). Además, el ion acompañante puede incrementar la toxicidad (cloro en OTAC y bromo en HDTMA). De acuerdo con lo mencionado por Rosen y Kunjap (2012), la toxicidad es muy dependiente de la longitud de la cadena hidrocarbonada, así como de la pureza de los compuestos químicos utilizados. La toxicidad de los tensioactivos aumenta con la longitud de la cadena etoxilada y disminuye con la ramificación. Los mecanismos que intervienen son principalmente la alteración de la permeabilidad, el transporte de membranas y la unión a macromoléculas, que provocan un mal funcionamiento (Cserháti 2002). La unión de tensioactivos a proteínas que alteran el plegamiento de la cadena polipeptídica y la carga superficial de la molécula causa una modificación de su actividad biológica (Cserháti 2002). Las moléculas tensioactivas con porciones polares y no polares penetran las cadenas de alquilo y modifican la bicapa de fosfolípidos de las membranas celulares (Pérez et al. 2009). Esta interacción cambia la orientación de la membrana, la solubiliza, la daña (Wong et al. 2012) y provoca la fuga del constituyente intracelular (Pérez et al. 2009); además, aumenta la permeabilidad de otros contaminantes presentes en el medio.
CONCLUSIONES
Los surfactantes catiónicos presentes en la solución nutritiva afectan negativamente el consumo de agua y nutrientes (NO3 -, K+ y Ca2+), lo cual disminuye el crecimiento de la lechuga, además de presentar fitotoxicidad en el sistema radicular conforme se aumenta la concentración del compuesto químico en la solución. Con el surfactante DDA no se observó daño en la mayoría de las variables, pero a partir de 7 mg/L generó fitotoxicidad en la raíz. Asimismo, el surfactante HDA causó menor daño a las plantas en dosis menores que 4 mg/L. La longitud de la cadena de carbonos y el ion acompañante del surfactante podría estar implicada en la toxicidad de plantas de lechuga. Las de cadena corta (HDA y DDA) causan menor efecto negativo que las de cadena larga (OTAC y HDTMA), mientras que el ion acompañante (Cl y Br) puede incrementar la toxicidad. Los surfactantes DDA y HDA podrían utilizarse para diferentes productos químicos en la agricultura, ocasionar menor impacto en el ambiente y disminuir la toxicidad en las plantas.















