Introducción
El género Begonia L. (Begoniaceae) es pantropical y diverso, con 2168 especies herbáceas y arbustivas (Hughes et al., 2015-actual; Thomas et al., 2024). Es reconocido por su importancia ornamental y medicinal (Neale et al., 2006; Rajbhandary, 2015; Tian et al., 2018), con una gran cantidad de especies de distribución restringida e incluso, limitada a sustratos cálcicos (Thomas et al., 2024). La especificidad de los sitios donde se desarrollan estas especies, aunada al fuerte deterioro que sufren los ambientes tropicales y la extracción ilegal de ejemplares (Hughes et al., 2003; Siregar, 2017; Tian et al., 2018; Thomas et al., 2024), incluyen a un centenar de especies en algún criterio de la Lista Roja de la Unión Internacional para la Conservación de la Naturaleza (IUCN, 2024). Sin embargo, resalta la cantidad de especies que carecen de datos que evalúen el estado de las poblaciones (Thomas et al., 2024). Por otro lado, en México no hay especies de Begonia con algún estatus de protección (SEMARNAT, 2019). El análisis de parámetros poblacionales, tales como el tamaño poblacional y su dinámica, el patrón de distribución espacial y la estructura de edades, de tamaños y/o de sexos, sirve para comprender la salud o estado de conservación de una población, realizar planes de manejo e incluso, recuperar especies en peligro (Sher y Molles, 2022; IUCN SPC, 2024).
Begonia ostulensis Mart. Gord & M.F. Ramos, comúnmente llamada “Begonia de Ostula” o “flor de piedra”, es una herbácea rupícola, endémica del bosque tropical caducifolio de Michoacán, México. Fue encontrada en grietas de roca caliza, en el territorio indígena de Santa María Ostula, entre 604 y 828 m sobre el nivel del mar, con una fenología limitada a la época de lluvias (junio a octubre). A diferencia de la mayoría de especies del género, posee solo una hoja orbicular, en cuyo centro se produce la inflorescencia (Martínez-Gordillo y Ramos-Ordoñez, 2022), una característica atractiva para los interesados en este grupo de plantas (Neale et al., 2006).
El hábitat de B. ostulensis se caracteriza por un buen grado de conservación debido a que las tierras pertenecen a la comunidad indígena que se ha mantenido cerrada al menos hasta la última década, restringiendo la presencia de extraños dentro el territorio; además, la comunidad posee una cosmovisión que promueve el uso sustentable y el cuidado de los recursos naturales (Gledhill, 2004). No obstante, la ausencia de observaciones previas a su descripción (Martínez-Gordillo y Ramos-Ordoñez, 2022) sugieren que la población es pequeña, con un área de ocupación también pequeña; y la fenología, limitada a la época de lluvias, sugiere que la dinámica poblacional podría ser afectada ante cambios en el régimen de precipitaciones; también se desconocen datos asociados a la reproducción. Para determinar si B. ostulensis se encuentra en un buen estado de conservación, el objetivo de este trabajo fue analizar los siguientes parámetros poblacionales: (1) el tamaño y la densidad poblacional, (2) el patrón de distribución espacial, (3) la estructura de tamaños asociada a la estructura de sexos y la cosecha floral producida y (4) la tasa de crecimiento poblacional.
Materiales y Métodos
Características de la especie
Begonia ostulensis es una hierba perenne, se desarrolla anualmente a partir de un tubérculo globoso. Tiene una hoja solitaria, simple, verde, orbicular. La inflorescencia es terminal y solitaria, surge del centro de la hoja, con flores pistiladas y flores estaminadas, una por cada nudo, el fruto es una cápsula con tres alas, ligeramente colgante, las semillas se liberan mediante líneas de dehiscencia, son elipsoides de color marrón claro y con testa delgada. La hoja se observa adherida a las rocas durante julio una vez que han iniciado las lluvias, las flores se desarrollan entre julio y septiembre, los frutos pueden observarse en septiembre y octubre, en noviembre las partes aéreas de la planta se secan (Martínez-Gordillo y Ramos-Ordoñez, 2022). Durante el trabajo de campo, algunos pobladores refirieron que la hoja de B. ostulensis se utiliza como alimento, ya que tiene buen sabor, además se utiliza como infusión para aliviar las molestias del resfriado.
Área de estudio
El estudio se llevó a cabo en el territorio de la comunidad náhuatl de Santa María Ostula, municipio Aquila, Michoacán, entre las coordenadas 18°31’11.0’’N, 103°29’58.8’’W y 18°30’26.8’’N, 103°29’05.6’’W, que comprenden la ladera sur y la zona alta del cerro Mancira, donde fue descrita la especie (Martínez-Gordillo y Ramos-Ordoñez, 2022). La vegetación corresponde a bosque tropical caducifolio (BTC), caracterizado por una fuerte estacionalidad, con una época lluviosa de junio a octubre, y una seca de noviembre a mayo; la temperatura media anual es de 25 °C, con mínimos de 15.5 °C en los meses de febrero y marzo, y máximos de 32 °C de mayo a octubre; la precipitación media anual es de 974 mm, con 883 mm en los meses de lluvias (Nolasco-González, 2022). La zona presenta suelos ricos en hierro, con grandes afloramientos de roca caliza, en donde crece Beiselia mexicana Forman (Burseraceae), otra especie endémica de la región (Martínez-Gordillo y Ramos-Ordoñez, 2022).
Tamaño poblacional
Durante la tercera y cuarta semana de julio de 2022 se realizó una búsqueda intensiva de la especie en la ladera sureste del cerro Mancira, desde la orilla del río Ostula hasta la cima, cubriendo un gradiente altitudinal de 100 m a 1032 m sobre el nivel del mar y un área de 4.5 km2. Adicionalmente se pidió a los pobladores que brindaran información de algún avistamiento en otros sitios del territorio. Una vez ubicada la especie se utilizó el método de muestreo para especies rupícolas en zonas escarpadas (Goñi et al., 2006); es decir, un método dirigido que censa a todos los individuos presentes en la zona, con unidades de muestreo (UM) que pueden tener distinta área.
El hábitat de la especie se definió como el sustrato rocoso en el que se encontraba al menos un individuo, dado que no se encontraron organismos creciendo fuera de las rocas, cada UM cubrió la roca completa. Debido al terreno accidentado y en algunos casos con una pendiente cercana a los 90°, se utilizaron catorce unidades de muestreo, ocho de 5×5 m, una de 11×2 m, una de 10×2 m, una de 20×3 m, una de 5.8×2 m, una de 8×4 m y una de 3×6 m. Con la suma del área de todas las UM se calculó el área de ocupación de la especie; es decir, el área que la especie ocupa realmente dentro de la extensión de presencia, el área de ocupación excluye el hábitat no ocupado dentro de la distribución e indica el área más pequeña esencial para la supervivencia de las poblaciones (IUCN SPC, 2024). En la cuarta semana de julio 2022, en cada UM se censaron todos los individuos con hoja expuesta. No se consideró la búsqueda, entre las grietas, de tubérculos sin hojas ya que estos miden de 0.3 a 0.7 cm (Martínez-Gordillo y Ramos-Ordoñez, 2022). La búsqueda implica romper la roca y remover la tierra, alterando el hábitat y aumentando el riesgo de afectar negativamente las plantas que crecen entre las grietas. Para cada UM se calculó la densidad (número de individuos/m2) y se obtuvo la densidad promedio ± error estándar para toda la población.
Patrón de distribución espacial
Para obtener el patrón de distribución espacial se utilizaron los conteos realizados en cada UM y se calculó el Índice Estandarizado de Morisita (IEM), por no ser sensible al tamaño de la unidad de muestreo ni al cambio en la densidad de individuos (Sousa y da Cunha, 2018; Ramos-Ordoñez et al., 2022), el análisis se llevó a cabo con el programa PAST v. 4.10 (Hammer et al., 2001). Para el IEM existe una distribución al azar si se obtiene un valor entre -0.5 y 0.5, una distribución uniforme si el valor es menor a -0.5 y, una distribución agrupada cuando es mayor a 0.5 (Hammer et al., 2001; Sousa y da Cunha, 2018; Ramos-Ordoñez et al., 2022).
Estructura de tamaños y atributos reproductivos
La estructura de tamaño de una población puede analizarse por edades, tamaños o sexos y debe analizarse con el tamaño poblacional (Godínez-Álvarez et al., 2008; Krebs, 2009). En muchas plantas es complicado analizar la edad, por lo que se utiliza la estructura de tamaños que proporciona información sobre el reclutamiento y puede asociarse a etapas reproductivas (Krebs, 2009; Zepeda et al., 2017).
A cada organismo contabilizado en las UM en julio 2022, se le midió el diámetro de la hoja, la altura de la inflorescencia y se le contó el número de botones, flores pistiladas, flores estaminadas y frutos. Se calculó el diámetro promedio de la hoja ± desviación estándar y la altura promedio de la inflorescencia ± desviación estándar. Para estimar si el tamaño del organismo (representado en este caso por el diámetro de la hoja), tenía relación con su capacidad reproductiva y, suponiendo que plantas más grandes tienden a producir más estructuras reproductivas, se utilizó el análisis de correlación de Spearman (rs), previa prueba de normalidad Kolmogorov-Smirnov, con error alfa de 0.05, en el programa GraphPad Prism v. 5.01 (Motulsky, 2007).
Para describir la estructura poblacional se utilizó un histograma de tamaños, se obtuvo el rango de tamaños y se calculó el número de clases con el algoritmo de Sturges (K=1+(3.3×logN), donde N es el número total de datos. Para obtener el tamaño del intervalo de tamaño en cada clase, se dividió el rango entre el número de clases. Finalmente se obtuvo la frecuencia de individuos en cada clase de tamaño (Sousa y da Cunha, 2018). Posteriormente, para establecer en qué tamaño se observa la reproducción, en cada clase se contó el número de organismos con inflorescencia. Se obtuvo el porcentaje de individuos reproductivos por clase y el porcentaje de estructuras reproductivas (botones, flores en antesis y frutos) que cada clase aportó a la población. Adicionalmente se calculó la cantidad de estructuras reproductivas promedio (± desviación estándar) producidas por individuo en cada clase diamétrica.
Por otro lado, se obtuvo la proporción sexual de la población utilizando las flores en antesis de 747 individuos. Los brotes florales y los frutos no se consideraron en el cálculo, ya que, por un lado, existe la incertidumbre de que el desarrollo de la flor llegue a la antesis y en el caso de botones muy pequeños, es difícil distinguir el sexo cuando aún no se desarrollan las alas del ovario. Se observó que las flores estaminadas se desprenden de la inflorescencia una vez que se ha liberado el polen, incluso sin que se observe la senescencia del perianto, pero se desconoce si algún animal consume o se lleva las flores caídas, por ende, estas flores en el suelo no se contabilizaron. Por otro lado, los frutos se forman una vez que ha ocurrido la fecundación, por tanto, el fruto es una etapa análoga a la de la flor estaminada caída, y contabilizarlos llevaría a una sobreestimación de la proporción sexual femenina. Adicionalmente para establecer la sexualidad de las inflorescencias se analizaron aproximadamente 150 fotografías tomadas durante el muestreo.
Dinámica poblacional
Para determinar si el tamaño poblacional calculado en la cuarta semana de julio de 2022 aumentaba, disminuía o se mantenía constante, los censos se repitieron en la cuarta semana de julio de 2023, utilizando el mismo método en las mismas unidades de muestreo. No obstante, las lluvias que habían iniciado en la última semana de junio de 2023 se interrumpieron durante todo agosto, dando la oportunidad de analizar si esta alteración en el régimen de lluvias tenía efecto en la población de B. ostulensis y se realizó otro censo en la cuarta semana de septiembre considerando que, de septiembre a octubre, la hoja continúa asignando recursos para la maduración del fruto y las semillas, aunque ya no se produzcan flores. Las observaciones sobre las condiciones de sequía durante 2023 fueron corroboradas con el Monitor de sequía de México de la Comisión Nacional del Agua (CONAGUA, 2022), el cual mostró un clima anormalmente seco en los reportes de agosto y septiembre, mientras que en julio el sitio presentaba una sequía moderada y en octubre sin sequía; mientras que en 2022 no se reportó sequía durante julio a noviembre. Las condiciones ambientales y el estado de la población de B. ostulensis se siguieron durante 2022 y 2023 con ayuda de un proyecto de fototrampeo de mamíferos, en el cual se realizaron visitas mensuales y se colocaron dos cámaras trampa frente a parches de la planta. El proyecto consta de 500 registros (Datos abiertos UNAM, 2023; se puede consultar con el nombre de FOTOSTULA).
Para calcular la tasa de crecimiento poblacional anual (Lewontin y Cohen, 1969; Sæther y Engen, 2002; Compagnoni et al., 2021), se consideró que B. ostulensis es una especie con poblaciones discretas, al tener un solo episodio reproductivo en determinada época del año. Para el cálculo de la tasa de crecimiento poblacional anual (λ), se utilizó la formula λ = N f / N 0 , en donde N f es la cantidad de individuos de julio 2023 y N 0 es la cantidad en julio 2022.
Resultados
Tamaño poblacional y patrón de distribución espacial
El total de individuos en toda la zona fue de 1268, en un área de ocupación de 363.6 m², con una elevación de 275 a 840 m sobre el nivel del mar. La densidad promedio calculada por UM fue de 3.65 ± 0.53 individuos/m², con una densidad mínima de 1.23 individuos/m² y una máxima de 9.04 individuos/m². Se localizaron tres sitios con presencia de la especie, el primero conocido como Arroyo a 275 m sobre el nivel del mar, con 234 individuos y una densidad de 4.68 individuos/m² en un área de 50 m2, aquí se encontraron dos rocas separadas por 16.2 m. A 1.3 km al norte se encontró el segundo sitio llamado Potrerito, a 687 m de altitud y presentó una densidad de 2.17 individuos/m², este fue el sitio más pequeño, con 39 organismos y una superficie de 18 m2. El tercer sitio se conoce como Palmita, se localizó a 1.4 km al oeste de Potrerito y a 1.7 km al noreste de Arroyo; se encontraron 11 parches separados por una distancia promedio de 64.2±41 m, (mínimo=12.2 m, máximo=120.3 m), con una elevación de 691 a 840 m; la densidad fue de 3.37 individuos/m², con 995 organismos en un área de ocupación de 295.6 m². En Palmita la especie presentó un patrón de distribución agrupado con un IEM de 0.515, al considerar las UM de todos los sitios el patrón sigue siendo agrupado (IEM=0.509). Los individuos se encontraron creciendo en grietas y pequeñas cavidades de la roca, con humedad y materia orgánica, en donde las irregularidades de la misma roca y herbáceas cercanas proveían sombra; usualmente se encontraron musgos, licofitas y helechos junto a la especie (Fig. 1).
Estructura de tamaños y atributos reproductivos
El diámetro promedio de la hoja fue de 4.39±2.43 cm (mínimo=0.5 cm, máximo=20 cm) y la altura promedio de la inflorescencia fue de 8.57±4.26 cm (mínimo=1 cm, máximo=30 cm). Se observó que las hojas de mayor diámetro desarrollan inflorescencias más largas (rs =0.77, P=<0.0001, n=799) y producen más estructuras reproductivas (rs =0.60, P=<0.0001, n=1268). Del total de la población, 58.9% se encontró en etapa reproductiva. La estructura poblacional mostró una forma gaussiana (Fig. 2), sugiere que la clase diamétrica más pequeña (menos de 2.1 cm de diámetro de hoja) contiene a los individuos inmaduros o en proceso de iniciar con la vida reproductiva ya que 10.6% de la población (n=135 individuos), aportan apenas 0.4% de estructuras reproductivas, con un promedio de 0.07±0.35 de estructuras producidas por individuo. La segunda clase diamétrica (2.2 a 3.8 cm), reúne el doble de individuos que la primera (21.7%); sin embargo, estos producen más estructuras reproductivas (7.4%) y aumentan el promedio de estructuras (0.6±1.1), aunque la variación continúa siendo grande. En contraste, la tercer y cuarta clase representan 52.4% de los individuos (n=665), presumiblemente contienen el grueso de la población madura, con un tamaño entre 3.9 y 7.1 cm de diámetro, 490 individuos aportan 57.6% de estructuras reproductivas, con una producción promedio de 1.6±1.5 y 2.8±2.2 estructuras por individuo, respectivamente. Las siguientes clases representan 15.2% de la población (n=193), aunque la mayoría de los individuos son reproductivos (12.7%) y la producción promedio de estructuras reproductivas alcanza un máximo de 6.3±3.8, su frecuencia muestra una clara tendencia a disminuir sugiriendo una alta tasa mortalidad al alcanzar estos tamaños.
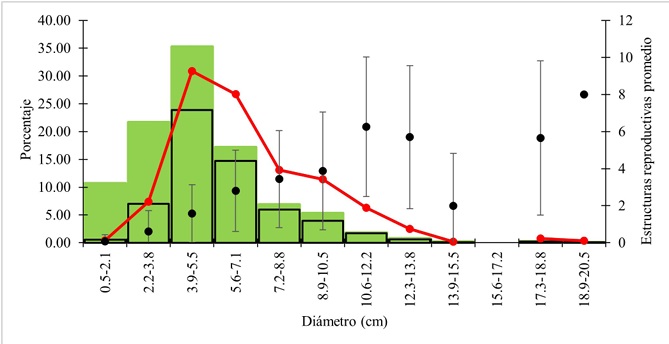
Figura 2: Estructura poblacional de Begonia ostulensis Mart. Gord. & M.F. Ramos. Las barras verdes representan el porcentaje de individuos en cada categoría diamétrica; las barras negras corresponden al porcentaje de individuos reproductivos; la línea representa el porcentaje de estructuras reproductivas y; los puntos representan el número promedio (± DE) de estructuras reproductivas producidas por individuo.
En cuanto a la producción de botones, flores y frutos en la población se encontró que 33.9% fueron botones, 34.3% flores masculinas en antesis, 10.9% flores femeninas en antesis y 20.9%, frutos. La proporción sexual de la población fue 1:3.1, es decir, por cada flor pistilada, en antesis, se encontraron 3.1 flores estaminadas (n=1 033 flores). Al analizar la población por sitios, se encontró que la proporción sexual fue similar: en Arroyo 1:3.14; en Potrerito 1:3.12; en Palmita 1:3.15. Esto indica que la proporción se mantiene independiente de la cantidad de individuos.
El máximo de estructuras reproductivas encontradas en un individuo fue de 14, y se presentó en dos organismos con 10.6 cm y 11 cm de diámetro (séptima clase diamétrica). El registro fotográfico muestra que las inflorescencias protandras (Fig. 3A) son las más comunes, con maduración de flores estaminadas antes que las pistiladas; no obstante, también se encontraron inflorescencias protóginas, en las que las flores pistiladas maduran antes que las estaminadas (Fig. 3B), y casos en donde las estructuras reproductivas eran frutos recién formados en la zona basal, botones florales femeninos en la zona media y flores masculinas en antesis en la zona apical. Además, se observaron inflorescencias en las que las flores de ambos sexos tenían antesis simultánea (Fig. 3B).
Dinámica poblacional
En el inicio de la floración de julio 2022, fue común observar las hojas turgentes de color verde oscuro con un botón floral en el centro de la hoja (Fig. 4A); entre la cuarta semana de julio y septiembre de 2022, los individuos presentaban características similares entre ellos, la hoja adherida a las rocas y el tallo de la inflorescencia turgente, con estructuras reproductivas en diferentes estadios de desarrollo (Fig. 4A,B), en este periodo no se observó que los parches disminuyeran la cantidad de organismos. En octubre se observaron infrutescencias de tallo turgente y erecto con frutos alados de apariencia seca (Fig. 4C). En julio de 2023 las características de los individuos (Fig. 4D) fueron similares al año anterior; sin embargo, en septiembre (Fig. 4 E,F), en la mayoría de los individuos, la inflorescencia se secó y no presentaba flores o frutos. En pocos organismos se observó el desarrollo inicial del tallo de la inflorescencia con un pequeño botón floral en el ápice (Fig. 4F) y como ocurre al inició de las lluvias, también se observó gran cantidad de hojas senescentes de color verde pálido, o secas. En julio de 2023 se contabilizaron 1693 individuos, por lo que, con respecto a la población de julio 2022 (n=1268), se observó un crecimiento poblacional de 33.52% con una tasa de crecimiento anual creciente (λ=1.34). Sin embargo, en el censo de septiembre 2023 solo se encontraron 315 individuos; por tanto, en relación con el tamaño poblacional de julio 2022, se observó una reducción de 75.16% (λa=0.25). Finalmente, entre julio y septiembre de 2023 se observó una reducción de 81.4% de individuos, sugiriendo que la ausencia de lluvias afectó negativamente el desarrollo de los organismos.

Figura. 4: Etapas fenológicas de Begonia ostulensis Mart. Gord. & M.F. Ramos en los años 2022 (A-C) y 2023 (D-F). Inicio de la floración en la primera semana de julio 2022 (A), las hojas presentan un botón floral blanco (flechas) indicando que la inflorescencia comienza a elongarse; apariencia de julio a septiembre de 2022 (B) con inflorescencias en distintas etapas de desarrollo; apariencia en octubre de 2022 (C) con infrutescencias (in) turgentes y erguidas; floración en julio 2023 (D); apariencia en septiembre 2023 (D-E) con infrutescencias y/o inflorescencias secas.
Discusión
Tamaño poblacional y patrón de distribución espacial
El tamaño poblacional encontrado para Begonia ostulensis es mayor que el reportado para otras especies del género que habitan en ambientes similares, como B. satrapis C.B. Clarke con menos de 150 individuos, B. scutata Wall con menos de 50 (Nautiyal et al., 2009), B. austroyunnanensis W.G. Wang, H.C. Xi & J.Y. Shen con menos de 100 individuos reproductivos (Wang et al., 2019), B. barosma X.X. Feng, Y.N. Huang & Z.X. Liu con tres poblaciones de menos de mil individuos (Feng et al., 2023) o, B. jocelinoi Brade con 65 individuos reproductivos y algunos cientos de plántulas (Paglia et al., 2022).
El tamaño del área de ocupación de B. ostulensis es muy reducido, con condiciones de hábitat limitadas a sustratos rocosos, y régimen de lluvias marcadamente estacional, lo que coincide con las cinco especies ya mencionadas, con B. socotrana Hook. f., B. samhaensis M. Hughes & A.G. Mill (Hughes et al., 2003) y con 65 especies más de Indonesia (Thomas et al., 2024). Hughes et al. (2003) y Thomas et al. (2024) indican que es urgente establecer medidas de conservación, ya que este tipo de distribución, aunada a las actividades agropecuarias, la urbanización, el saqueo y, particularmente la fragmentación del hábitat, son factores que mantienen el tamaño poblacional bajo o, incluso, en un nivel crítico.
Actualmente, el hábitat de B. ostulensis no se encuentra sujeto a la urbanización o actividades agropecuarias, la densidad obtenida sugiere que el uso por parte de la comunidad indígena es moderado o bajo. Sin embargo, entre los principales factores que pueden afectar negativamente su hábitat se encuentran la minería a cielo abierto en la comunidad vecina de Aquila y las concesiones otorgadas por el gobierno dentro del territorio de Santa María Ostula, una actividad que reduce la fertilidad del suelo, contamina el agua y reduce la biodiversidad (Valois-Cuesta y Martínez-Ruiz, 2016; Bastidas Orrego et al., 2021; Veríssimo y Moura, 2021). En segundo término, Santa María Ostula se ubica dentro de una zona de alta sismicidad, por efecto de las placas de Cocos y de Norteamérica. En septiembre 2023 un sismo con magnitud de 7.7 causó el desprendimiento de grandes rocas en los cerros del territorio, incluyendo Mancira (obs. pers. M. González- Aguilar). Estos deslizamientos pueden actuar directamente en las rocas donde crece B. ostulensis, como sucede en B. minuta Sosef, una especie endémica de Camerún en peligro crítico por su área de ocupación reducida y menos de 500 individuos, sometidos a la amenaza de la caída de rocas sobre la población (Cheek, 2015).
El patrón de distribución espacial agregado puede asociarse con las condiciones microambientales de las rocas, entre ellas, la reducción de la radiación solar, pocas variaciones de temperatura y humedad, baja pérdida de agua por evaporación y disponibilidad de nutrientes (Larmuth y Harvey, 1978; Nobel et al., 1992; Gorbushina, 2007). No obstante, un patrón agregado en sitios muy reducidos hace más vulnerable a la población ante las perturbaciones del hábitat como deslizamientos o cambios en la cobertura vegetal (Cui et al., 2012; Thomas et al., 2024). Tanto el patrón de distribución espacial como la cantidad de organismos en tres sitios puede ser resultado de un potencial de dispersión de semillas limitado (Thomas et al., 2012; Chan et al., 2018). La cantidad de parches encontrados en Palmita pueden explicarse por una dispersión de tipo anemobalística, en la cual las alas del fruto son empujadas por el viento y las semillas son lanzadas desde poros o líneas de dehiscencia; no obstante, la distancia de dispersión es pequeña. Este tipo de dispersión ocurre en la mayoría de las especies de Begonia del Neotrópico, incluyendo a las de la sección Knesebeckia (Klotzsch) A. DC. (De Lange y Bouman, 1999).
Durante el trabajo de campo se observó que el fruto de B. ostulensis tiene líneas de dehiscencia en la base de las alas, por donde salen las semillas, apoyando este tipo de dispersión. En comparación con muchas especies del género las semillas de B. ostulensis son pequeñas, miden alrededor de 20 µm (Martínez-Gordillo y Ramos-Ordoñez, 2022) y tienen una testa ornamentada, lo que podría ayudar a que queden atrapadas fácilmente entre las grietas o entre el sustrato, aumentando el patrón agregado. Sin embargo, la presencia en dos sitios a más de 1 km de distancia, y en bajas cantidades, sugiere que puede haber otro vector de dispersión. En algunas especies se ha visto que la ornamentación en la testa facilita que estas se peguen al pelaje de mamíferos (De Lange y Bouman, 1999); sin embargo, su dispersión estaría limitada a mamíferos que se muevan entre las rocas y recorran distancias relativamente largas, por ejemplo, el coatí (Nasua narica Linnaeus, 1766), una especie abundante en Santa María Ostula. En este sentido, sería útil realizar la estructura genética de los tres sitios para determinar si los organismos pertenecen a una misma población.
Estructura de tamaños y atributos reproductivos
La estructura de tamaños puede asociarse con los atributos reproductivos observados (Godínez-Álvarez et al., 2008). Los individuos jóvenes no se reproducen o producen una muy baja proporción de flores dado que no han alcanzado el desarrollo óptimo para una producción alta. Por otro lado, los individuos adultos pueden presentar proporciones variables de flores, pero contribuyen notablemente a la reproducción. Finalmente, los organismos seniles se pueden identificar porque disminuyen su potencial reproductivo y son más sensibles a enfermedades (Komarov et al., 2003).
En B. ostulensis se observó que los individuos con mayor proporción de estructuras reproductivas constituyen el grueso de la población, mientras que los organismos con baja y alta proporción de estructuras representan menor cantidad, lo que resulta en una estructura poblacional gaussiana o en forma de joroba. Se ha indicado que las estructuras con esta forma tienen un alto riesgo de desaparecer, dado que el establecimiento de nuevos individuos se encuentra limitado por algún factor y la persistencia de la población en el tiempo está condicionado a la salud de los adultos; no obstante, en el largo plazo pasarán a estadios seniles con una tasa reproductiva en declive (Godínez-Álvarez et al., 2008; Hido et al., 2020; Lvončík et al., 2020). Ejemplo de este patrón se observa en B. satrapis y B. scutata que carecen de individuos jóvenes y los adultos se encuentran en números críticos (Nautiyal et al., 2009); otras especies con poblaciones en declive son B. asympeltata L.B. Sm. & Wassh, B. dodsonii L.B. Sm. & Wassh, B. harlingii L. B.Sm. & Wassh, B. serotina A. DC y B. ynesiae L.B. Sm. & Wassh que, aunque carecen de datos, disminuyen debido a la destrucción de hábitat (IUCN, 2024).
La ausencia de ramificación de B. ostulensis sugiere que su dinámica poblacional está limitada a la reproducción sexual, ya que no se han observado estolones u otras estructuras que permitan la reproducción vegetativa (Komarov et al., 2003), como ocurre en otras especies del género (Siregar, 2017; Tian et al., 2018). No obstante, el tubérculo le permite subsistir durante la época seca como en B. socotrana (Hughes et al., 2003); además, la proporción sexual encontrada sugiere que la disponibilidad de polen es alta (Ågren y Schemske, 1995) y la presencia de inflorescencias tanto protandras como protóginas favorecería la fecundación cruzada, incluso las inflorescencias con botones pistilados, flores estaminadas en antesis y frutos, podrían sugerir duodicogamia, una estrategia en la que las fases masculina y femenina se alternan en periodos de duración irregular (Endress, 2020). Aún se deben explorar varios aspectos reproductivos que influyen en el éxito de la población, tales como la polinización y formación de semillas, germinación y establecimiento de nuevos individuos.
Dinámica poblacional
La tasa de crecimiento poblacional anual registrada entre julio 2022 y julio 2023 mostró que la cantidad de individuos tiende a aumentar; no obstante, la estructura poblacional de forma gaussiana sugiere que hay factores que inciden negativamente en el desarrollo de organismos juveniles a través del tiempo, uno de ellos podría ser periodos de sequía anormal como la escasez de lluvias de agosto y septiembre en 2023. Es necesario dar un seguimiento anual, ya que es sabido que bajo condiciones de precipitación anormales la tasa de crecimiento poblacional es variable (Wojtyla et al., 2020). La dinámica poblacional de B. ostulensis está relacionada con la estacionalidad del bosque tropical caducifolio, ya que la foliación y floración ocurren en la temporada de lluvias como en muchas especies (Borchert et al., 2004). A reserva de realizar estudios enfocados a analizar la fenología de la reproducción, la evidencia de inflorescencias secas y hojas senescentes en septiembre de 2023, sugiere que las condiciones ambientales afectaron el desarrollo de las flores y los frutos (Borchert et al., 2002; Patra et al., 2024), lo que podría causar retrasos en la reproducción y baja cantidad de individuos en algunas clases diamétricas en el futuro (Hido et al., 2020; Lvončík et al., 2020).
Si bien los conteos se basaron en organismos que produjeron estructuras aéreas, en estado vegetativo o reproductivo, no se debe olvidar que B. ostulensis presenta un tubérculo subterráneo que le ayuda a sobrevivir en cada época seca, por lo tanto la tasa de crecimiento poblacional refleja la capacidad del tubérculo para romper la latencia al llegar la época húmeda y prepararse para la reproducción; sin embargo, el estrés hídrico posterior al rompimiento de la latencia tendría un efecto negativo en la planta, ya que muchos nutrientes se absorben con el agua a través de las raíces, disminuyendo el crecimiento de la planta y la producción de flores y frutos y por ende, disminuyendo el éxito reproductivo (Wojtyla et al., 2020). En Begonia semperflorens Hook, una especie de ornato común, se observó que, a mayor estrés hídrico, la cantidad de flores, hojas y ramas producidas disminuye, las hojas se hacen más cortas y delgadas y la planta se reduce en tamaño; incluso al simular la sequía severa y extremadamente severa las plantas sobreviven, pero pierden su valor ornamental; efectos similares se han observado en Helleborus orientalis Lam., Chrysanthemum morifolium Ramat y Hemerocallis fulva L. (Zhao et al., 2024).
Por otro lado, los organismos con inflorescencias pequeñas y con un botón floral apical en septiembre 2023, además del porcentaje de individuos de tamaño reproductivo, pero sin inflorescencia, sugieren que hay un porcentaje de la población que sufre algún retardo temporal en la reproducción; no obstante, el éxito reproductivo de estos individuos estaría limitado a que las lluvias continuaran sin alteración. Es posible que las fluctuaciones en la temporada de lluvias de 2023 observadas en el sitio sean un evento azaroso; sin embargo, se esperan sequías más largas y severas en la zona (Escalante-Sandoval y Nuñez-Garcia, 2017), por lo que la tasa de crecimiento poblacional de B. ostulensis podría sufrir modificaciones (Sæther y Engen, 2002). Si bien los organismos existentes podrían resistir el cambio en el régimen de lluvias, gracias al tallo subterráneo como ocurre en B. semperflorens, se sabe que las sequías tienen efectos negativos en las estructuras de perennación, por ejemplo, en la papa (Solanum tuberosum L.) y camote (Ipomoea batatas (L.) Lam.), el déficit hídrico durante la formación y elongación del tubérculo provoca crecimiento y rendimiento deficiente de este, además de agrietamiento; en la cebolla (Allium cepa L.) y el ajo (A. sativum L.), el déficit durante la formación del bulbo ocasiona el agrietamiento y formación de bulbos dobles, con bajo contenido de materia seca y baja supervivencia (Solankey et al., 2021).
Los parámetros poblacionales mostrados, y los riesgos a los que la población es susceptible ante los cambios ambientales, indican que B. ostulensis debería ser incluida en las listas de especies protegidas, tanto nacional como internacionalmente. De acuerdo con los criterios del Método de Evaluación del Riesgo de Extinción de Plantas de México (SEMARNAT, 2010), también conocido como MER, la especie clasifica como “En Peligro de Extinción” en vía directa por el área de distribución que ocupa, menor a 1 km2; así mismo califica como “Amenazada” con un puntaje de 1.87 por su distribución limitada, un hábitat definido como crestas de roca caliza en bosque tropical caducifolio y su rango altitudinal, además del tamaño poblacional, la ausencia de clonalidad, la reproducción sexual limitada por la estacionalidad y la importancia económica potencial debido al uso que se le da en la comunidad (MER disponible en González Aguilar, 2024). La protección internacional también es necesaria ya que de acuerdo con estos criterios (IUCN, 2024), la especie se encuentra en categoría de “Vulnerable” (VU) a través del criterio VU D2.
Declaración de disponibilidad de datos
El conjunto de datos que apoya los resultados de este estudio fue publicado en SciELO Data y puede ser accedido en: https://doi.org/10.48331/SCIELODATA.UZ1WOA.


















