Introducción
En la zona del altiplano central de México se aprovechan de manera preferente cuatro cultivares de Agave salmiana Otto ex Salm-Dyck subsp. salmiana: Ayoteco, Chalqueño, Manso y Púa Larga. En el estado de Tlaxcala el aprovechamiento de estos cultivares se limita a la producción de pulque, utilización de pencas para barbacoa y obtención de gusanos comestibles (Álvarez-Duarte et al., 2018), mientras que en algunas regiones los cultivares han sido seleccionados por los productores acorde a sus características para obtener aguamiel de buena calidad. Las características de los cultivares Ayoteco, Chalqueño, Manso y Púa Larga han sido reportadas por Madrigal et al. (2014) y Márquez-Pallares et al. (2024) y se detallan en el Cuadro 1.
Cuadro 1: Características de los cultivares de Agave salmiana Otto ex Salm-Dyck predominantes en Tlaxcala, México. (-) No reportado. Tomado de Márquez-Pallares et al. (2024) y Madrigal et al. (2014).
| Característica/cultivar | Ayoteco | Chalqueño | Manso | Púa Larga |
| Peso (Kg) | 1200 | 1200 | 800-900 | 1000 |
| Altura (m) | 4.3 | 2.87 | 2.93 | 2.83 |
| Longitud de la hoja (m) | 2.36 | 1.53 | 1.46 | 1.64 |
| Longitud de la espina apical (cm) | 6.0 | 5.17 | 6.37 | 6.17 |
| Producción de aguamiel | 10 a 12 l por la mañana y 7 l por la tarde | - | 6-7 l de aguamiel por la mañana y 3 l por la tarde | 8 l de aguamiel por la mañana y 4 l por la tarde |
| Producción de aguamiel (meses) | 5 | 5 | 4 | 4 |
| Grados Brix del aguamiel | 10-12 | 10-11 | 14-15 | 12-13 |
| Tiempo en llegar a su etapa productiva (años) | 12-14 | 12-14 | 9-10 | 8 a 9 |
El estudio integral del agave debe de considerar tanto el tipo de cultivar como la fenología. La fenología hace referencia al estudio de los eventos recurrentes en el ciclo de vida de las plantas (Tang et al., 2016) y en el agave pulquero los productores tienen identificado al menos cuatro etapas fenológicas: 1) edad media vegetativa, que corresponde al momento en que la planta alcanza la mitad de su tamaño de adulto, 2) capón, que es el momento en que el meyolote (cogollo o meristemo antes de su florecimiento) inicia su crecimiento y el maguey es capado con lo que iniciará el añejamiento y se esperará alrededor de ocho meses para ser raspado, 3) productivo, que es el momento en que el agave es raspado y se obtiene aguamiel y 4) senescencia, que es el momento en que la piña (tallo o bola) termina de ser raspada y solo quedan las pencas u hojas. La Figura 1 muestra imágenes de los tipos de cultivares y etapas fenológicas de Agave salmania subsp. salmiana.

Figura 1: Cultivares y etapas fenológicas de Agave salmiana Otto ex Salm-Dyck del estado de Tlaxcala, México. A. Ayoteco; B. Manso; C. Chalqueño; D. Púa Larga; E. Edad media; F. Capón; G. Productiva; H. Senescencia.
Actualmente, la siembra de A. salmiana presenta grandes desafíos, ya que su uso se ha destinado principalmente a la venta de pulque y para obtenerlo es necesario esperar entre 10 y 14 años. Sin embargo, es posible obtener el máximo beneficio si se conoce la etapa fenológica y el tipo de cultivar de las plantas. Algunos estudios que dirigieron sus esfuerzos en conocer los cultivares y/o aprovechar integralmente a A. salmiana son los de Michel-Cuello et al. (2012), quienes utilizaron el jugo de las plantas de A. salmiana obtenidas del estado de San Luis Potosí, México, con una edad aproximada de siete a nueve años y un año de castración (corte de pedúnculo floral) para realizar una hidrólisis enzimática de fructanos; sin embargo, no se indicó el tipo de cultivar de los agaves seleccionados. Por otro lado, Godínez-Hernández et al. (2016) cuantificaron fructanos de A. salmiana en el tallo o bola del agave, seleccionando diferentes tamaños y rasgos de madurez fisiológica; sin embargo, no se indicó el cultivar de los agaves. Láinez et al. (2018) realizaron la hidrólisis de azúcares simples de las hojas de A. salmiana obtenido en Veracruz, México; sin embargo, en este estudio no se indicó el tipo de cultivar ni etapa fenológica de los agaves. También se ha explorado el uso de residuos de A. salmiana para obtención de moléculas y elaboración de medios de cultivo, tal como lo reportaron Santos-Zea et al. (2019), quienes utilizaron el bagazo de A. salmiana obtenido como un subproducto de la recolección de la savia para la extracción de moléculas y la determinación de su capacidad antioxidante; en este estudio no se especificó el tipo de cultivar del agave. Por su parte, Balderas-Hernández et al. (2021) reportaron que el jarabe de A. salmiana aumentó la producción de interleucina 2 y demostraron el uso potencial de los agaves para generar productos biotecnológicos alternativos y valiosos, además de la producción de bebidas alcohólicas; en este estudio tampoco se indicó el tipo de cultivar de los agaves. Por otro lado, Velázquez-De Lucio et al. (2022) elaboraron medios de cultivo con el bagazo de la piña de A. salmiana provenientes de Tlaxcala, México, y cultivaron al hongo Pleurotus djamor (Rumph. ex Fr.) Boedijn; en este estudio no se indicó el tipo de cultivar de donde se obtuvo el bagazo. Márquez-Pallares et al. (2024) determinaron la morfología y la composición químico proximal de las pencas de los cultivares Chalqueño, Manso, Púa Larga y Ayoteco obtenidos en el estado de Tlaxcala, México y Robles-Arias et al. (2024) evaluaron la producción de fructooligosacáridos en las hojas de A. salmiana obtenido en el estado de Hidalgo, México, y con un estado de madurez fisiológico (cuando el pedúnculo floral emerge del meristemo); en este estudio no se especificó el tipo de cultivar.
Como se puede notar en los reportes anteriormente mencionados, solo se determina la actividad biológica o la producción de moléculas por A. salmiana en la etapa de madurez fisiológica y en la mayoría de los casos no se especifican el tipo de cultivar y etapa fenológica de la planta. Hasta donde sabemos, solo en el reporte de Aldrete-Herrera et al. (2019) se determinó el contenido de azúcares y perfil de fructanos en agaves a diferentes edades (2-4 años, 6-8 años y 10-12 años) y para Agave ssp., A. atrovirens Karw. ex Salm, A. salmiana subsp. crassipina (Trel.) Gentry, A. tequilana Weber cv. Cenizo y A. salmiana cv. Chino.
Es indispensable realizar estudios comparativos en las diferentes etapas fenológicas para aprovechar de forma eficiente, rentable y sustentable los cultivares de A. salmiana. El objetivo de esta investigación fue evaluar el perfil de inulina (INU), fructooligosacáridos (FOS), azúcares reductores directos (ARD) y totales (ART), ácidos grasos (AG), ésteres (ES) y otras moléculas detectadas por cromatografía de gases de los cuatro cultivares de la subespecie salmiana predominantes en Tlaxcala, México.
Materiales y Métodos
Material vegetal
Con la finalidad de determinar el perfil químico de los cultivares Ayoteco, Chalqueño, Manso y Púa Larga, se obtuvieron pencas completas de A. salmiana subsp. salmiana donadas por el rancho San Isidro, localizado en Nanacamilpa en el estado de Tlaxcala, México (19°29'32.4''N, 98°32'46.5''W). Se obtuvieron tres pencas completas de los cultivares en cuatro etapas fenológicas: edad media vegetativa, capón, productivo y senescencia. La edad media correspondió a cuatro años para los cultivares Púa Larga y Manso (cultivares precoces) y a seis años para los cultivares Ayoteco y Chalqueño.
Aunque en la plantación existió un control de las edades de los ejemplares de agave, las edades fueron aproximadas, ya que el criterio más importante fue la manifestación fenológica (etapa edad media, capón, productiva y senescencia). La edad media fue establecida cuando la planta alcanzó la altura media de una planta madura, la etapa capona cuando el pedúnculo floral emergió del meristemo. La etapa productiva fue establecida como el momento medio de producción de aguamiel, es decir a los tres meses después de iniciado el raspado. Finalmente, la senescencia fue establecida como el momento en que el agave terminó de producir aguamiel y se le consideró desecho. De cada penca se obtuvieron tres muestras por cultivar y etapa fenológica. A lo ancho de cada penca se trazó una línea que la dividía en dos partes iguales; de esta línea divisoria y a lo ancho de toda la penca, se cortó un trozo de penca con una dimensión de 1 cm que fue utilizada para la obtención del polvo de agave.
Obtención del polvo de agave
La parte media de las pencas fue procesada como se detalla a continuación para obtener un polvo, el cuál fue utilizado determinar el perfil químico (INU, FOS, ARD, ART y otras moléculas detectadas por cromatografía de gases). Las partes medias de las pencas fueron secadas a 60 °C en un horno (Thermo Fisher Scientific, 51028156, Waltham, EUA) hasta alcanzar un 6% de humedad determinada en un analizador de humedad (Mettler Toledo, MAC210/WH, Columbus, EUA). Las muestras fueron trituradas en un molino de martillos (Schutte Hammermill serie 18, Buffalo, EUA) y posteriormente, utilizando tamices malla 40 (0.420 mm), se tamizaron para eliminar los residuos de fibra. El polvo obtenido se guardó en recipientes herméticos y se almacenó en oscuridad a temperatura ambiente para su posterior análisis.
Extracción de carbohidratos
Para extraer los carbohidratos, se pesó un gramo de polvo de agave que se disolvió en 6 ml de agua destilada, y luego se agitó a 150 rpm por 60 min a 50 °C en una incubadora con agitación (Zhicheng, ZHWY-1102C, Jiangsu, China) (Montañez-Soto et al., 2011). Después, se centrifugó a 10,000 rpm durante 10 min (Hermle Labnet, Z326K, Middlesex, EUA) y el sobrenadante fue utilizado para la determinación glucosa (G), ARD, fructosa (F) y ART. Posteriormente, se realizó una hidrólisis enzimática para la determinación de FOS y INU. El procedimiento para estas determinaciones se menciona a continuación.
Azúcares reductores directos (ARD)
La cuantificación de azúcares reductores directos (ARD) se realizó de acuerdo con el protocolo propuesto por Miller (1959). En este ensayo solo se cuantificaron los ARD; es decir, aquellos que se extrajeron de manera directa en el extracto, sin que se realizará una hidrólisis química o enzimática. La determinación se basó en la reducción del ácido 3,5-dinitrosalícilico por la presencia de azúcares reductores. La mezcla de reacción contenía 1 ml del extracto de carbohidratos y 1 ml del reactivo DNS. La mezcla se llevó a ebullición por 5 min y después se enfrió con hielo. Simultáneamente se realizó una curva patrón de glucosa de 0 a 2 g/l. Finalmente, la absorbancia se determinó en un espectrofotómetro UV/VIS a 540 nm (Perkin Helmer, Genesys 10S, Hopkinton, EUA) y se calcularon las concentraciones de acuerdo con la curva patrón de glucosa.
Análisis de azúcares reductores totales (ART)
Se realizó una hidrólisis con ácido sulfúrico concentrado y la reacción con fenol al extracto de carbohidratos (Dubois et al., 1956). Para ello en un tubo de ensayo se agregó 1 ml de extracto de carbohidratos, 0.6 ml de fenol al 5% (p/v) y 3.6 ml de ácido sulfúrico concentrado. El tubo de ensayo fue enfriado por 30 min en una tina de hielo para evitar calentamiento por el agregado del ácido y se determinó la absorbancia en un espectrofotómetro UV/VIS a 540 nm (Perkin Helmer, Genesys 10S, Hopkinton, EUA). Se realizó una curva patrón de glucosa a concentraciones de 10 a 200 mg/ml tratada bajo las mismas condiciones del ensayo.
Cuantificación de glucosa (G)
La glucosa se cuantificó con la enzima glucosa oxidasa (EC 1.1.3.4) obtenida de la empresa Enziquim, México, y de acuerdo con el método descrito por Trinder (1969). Para el análisis se utilizaron 2 ml del reactivo compuesto por la glucosa oxidasa y la 4-aminofenazona, se adicionaron 20 µl del extracto de carbohidratos y se incubó a 37 °C por 10 min en un termobaño (ICB, BSD100755, Guadalajara, México). La absorbancia se determinó en un espectrofotómetro UV/VIS a 505 nm (Perkin Helmer, Genesys 10S, Hopkinton, EUA). Se realizó una curva patrón de glucosa de 0 a 200 mg/ml bajo las mismas condiciones de ensayo.
Cuantificación indirecta de fructosa (F)
La fructosa (F) se calculó como la diferencia entre los ARD y la G. Lo anterior se realizó bajo el supuesto que los ARD están constituidos únicamente por glucosa y fructosa.
Cuantificación de fructooligosacáridos (FOS)
Para cuantificar los FOS se realizó una hidrólisis enzimática al extracto de carbohidratos. La reacción catalítica contenía 10 ml del extracto de carbohidratos, 200 U de enzimas (inulinasa EC 3.2.1.7 y beta fructofuranosidasa EC 3.2.1.26) obtenidas de la empresa Enziquim, México, y que fueron disueltas en buffer de acetatos 0.2 M, pH 4.5. La reacción se mantuvo en agitación por 4 h a 50 °C en una incubadora con agitación (Zhicheng, ZHWY-1102C, Jiangsu, China). En los extractos ya hidrolizados se determinó nuevamente la concentración de azúcares reductores directos (ARD1), glucosa (G1) y fructosa (F1) de acuerdo con los métodos ya descritos anteriormente. La cuantificación de FOS se realizó según el algoritmo reportado por Montañez-Soto et al. (2011) donde FOS=ARD1-ARD. El grado de polimerización promedio (GPPFOS) se obtuvo como: (F1 - G1)/G1. El peso molecular promedio de los FOS (PMPFOS) se obtuvo con el siguiente algoritmo (Livingston III, 1990): PMPFOS=(GPPFOS) * 162.
Cuantificación de inulinas (INU)
La cuantificación de INU se realizó por el método propuesto por Guevara Apraez y Vallejo Castillo (2015). Para ello, se realizó una hidrólisis ácida, la cual consistió en tomar 5 ml del extracto de carbohidratos y adicionar 5 ml de HCl 2 N. La hidrólisis se llevó a cabo a 70 °C durante 30 min. Posteriormente la mezcla se enfrió en una tina con hielo para continuar con la neutralización con NaOH 2N aforando a 50 ml con agua destilada. A la muestra hidrolizada se le determinaron los azúcares reductores totales (ART2), glucosa (G2) y fructosa (F2) con los procedimientos ya descritos. La concentración de inulina se calculó con la siguiente expresión matemática: INU= ART2-ARD-FOS. El grado de polimerización promedio de las inulinas (GPPINU) se calculó de acuerdo con Livingston III (1990), utilizando el siguiente algoritmo: GPPINU = (F2+G2)/G2. De manera análoga a los FOS, se obtuvo el peso molecular promedio de las inulinas con el siguiente algoritmo: PMPINU=(GPPINU) * 162.
Análisis por cromatografía de gases acoplado a espectrofotometría de masas (CG/MSD)
La determinación de biomoléculas también se llevó a cabo por CG/MSD. Para ello se disolvió 1 g de polvo de agave en 5 ml de etanol grado absoluto, se agitó en un Vortex (Scientific Industries, Genie-2, New York, EUA) y se centrifugó a 10000 rpm durante 10 min (Hermle Labnet, Z326K, Middlesex, EUA). Se recuperó el sobrenadante para inyección en un equipo de cromatografía de gases acoplado a espectrometría de masas (Agilent Technologies modelo 7890A y 5975C respectivamente, Santa Clara, EUA). Se utilizó una columna capilar HP 5 ms de 30 m × 0.25 mm × 250 µm con un volumen de inyección de 2 µl con un método de 60 °C por un 1 min, rampa de temperatura de 15 °C/min hasta 300 °C por 15 min. Con un flujo de helio de 1.1 ml/min, en modo “scan” para la adquisición de datos con el software Chemstation v. 1.0 (Agilent Technologies, 2005). El detector de masas se operó en modo “scan” de masa relativa de 30 a 600 m/z con un “threshold” de 150, temperatura de la fuente de iones de 230 °C, temperatura del cuadrupolo de 150 °C, ionización electrónica a 70 eV y 300 µA. La identificación de biomoléculas se realizó por porcentaje de similitud mayor al 70% comparando los espectros obtenidos con la base de datos NIST v. 2.0 (Mass Spectropy Data Center, 2021). La abundancia se tomó en referencia al porcentaje área de cada compuesto que es una medida directa de la presencia de cada compuesto en la muestra.
Diseño experimental y análisis estadístico
Se diseñó un experimento completo de dos factores: cultivar y etapa fenológica. El primer factor tuvo los niveles Ayoteco, Púa Larga, Manso y Chalqueño. El segundo factor tuvo los niveles media vida, capón, productiva y senescencia. Todos los experimentos se realizaron con al menos tres réplicas. Se realizó un análisis de varianza con dos factores con una comparación de medias por la prueba de Tukey (α= 0.05) y se obtuvo el análisis correspondiente de componentes principales (ACP). Para el análisis se utilizó el software SPSS Statistics v. 25 (IBM Corp., 2017).
Resultados
Azúcares reductores directos
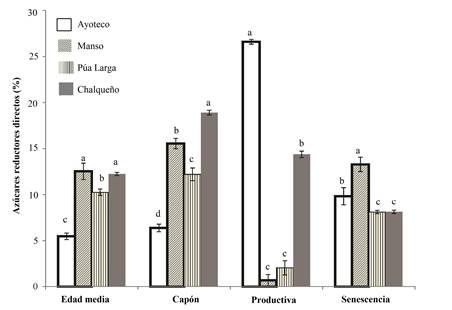
Se encontraron diferencias significativas en el contenido de ARD (Fig. 2). Las diferencias más evidentes se observaron en la etapa fenológica productivo (momento en el que se raspa la piña para obtener aguamiel) para el cultivar Ayoteco. Es de notar que los cultivares Manso y Púa Larga presentaron mayor cantidad de ARD en la senescencia respecto a la etapa productiva. Para el caso de Púa Larga se observó un incremento de cuatro veces la cantidad de ARD y en el Manso de 19 veces, en contraste con los cultivares Ayoteco y Chalqueño, los cuales disminuyeron 2.7 y 1.7 veces, respectivamente.
Azúcares reductores totales
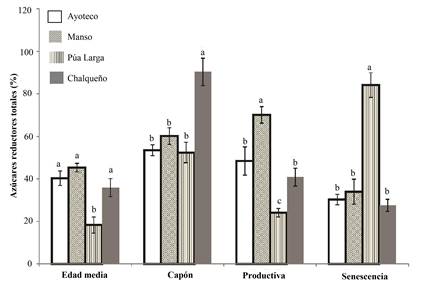
Los resultados de los ART se observan en la Figura 3. En la edad media no se encontró una diferencia estadística (p>0.05) entre los cultivares Manso, Ayoteco y Chalqueño, los cuales presentaron valores de alrededor del 40% de ART. Sin embargo, sí hubo una diferencia estadística con el cultivar de Púa Larga (18.32%). En la etapa capón, el cultivar Chalqueño presentó el contenido más alto de ART y también mostró el valor más alto de ARD. Se observó una correlación de los ART con los ARD para este cultivar y fue el único que presentó este patrón. Por otra parte, el cultivar Manso en la etapa productiva mostró los niveles más altos de ART (70%), lo que contrasta con sus bajos niveles de ARD. En esta misma etapa fenológica, la variante Púa Larga sólo presentó un 24% de ART. Respecto a la etapa senescencia, destacó el cultivar Púa Larga con 84% de ART y no se encontró diferencia significativa entre los cultivares Ayoteco, Manso y Chalqueño.
Fructooligosacáridos e inulina
Los FOS se encontraron en un amplio rango: 5.25 ± 0.9 hasta 20.66 ± 3.5% (Cuadro 2). El análisis estadístico mostró seis grupos (a, c, d, ab, bc y cd), los cuales no se correlacionaron con las etapas fenológicas. En la etapa capón no se encontró diferencia significativa por cultivar y en la senescencia el cultivar Púa Larga presentó un incremento de aproximadamente 2.5 veces en comparación con el resto de los cultivares. Se observó el mismo comportamiento en la etapa productiva donde el cultivar Ayoteco presentó un incremento de FOS de 2.4, 2.5 y 3.5 veces en comparación con Manso, Púa Larga y Chalqueño, respectivamente. Respecto a la INU, los resultados se distribuyeron en seis grupos estadísticos (a, b, c, d, cd y cb). El grupo de mayor contenido de INU fue conformado por Púa Larga-senescencia, Ayoteco-productivo y Chalqueño-capón. Los GPP de los FOS no mostraron diferencias contrastantes, a diferencia de los GPP de la INU que mostraron cuatro grupos estadísticos.
Cuadro 2: Fructooligosacáridos e inulina en las cuatro etapas fenológicas de cultivares de Agave salmiana Otto ex Salm-Dyck. *Promedio±desviación estándar. Letras distintas indican diferencias significativas, comparación entre columnas (p<0.05). FOS: fructooligosacáridos, GPP: grado de polimerización promedio e INU: inulina.
| Etapa fenológica | Cultivar | FOS (%) | GPP (Residuos) | INU (%) | GPP (Residuos) |
|---|---|---|---|---|---|
| Edad media | Manso | 13.25±0.7c* | 4.4±1.2a | 20.43±2.6c | 23.40±3.7c |
| Ayoteco | 13.93±3.5bc | 4.7±1.0a | 18.45±1.9cd | 25.60±2.6b | |
| Púa larga | 5.25±0.9d | 4.5±0.5a | 9.65±0.7d | 24.30±4.1cb | |
| Chalqueño | 10.65±1.8cd | 4.6±0.8a | 15.45±1.3cd | 21.01±1.9c | |
| Capón | Manso | 15.14±1.5ab | 3.0±0.2b | 25.69±5.6cb | 19.10±1.9c |
| Ayoteco | 17.55±3.8ab | 3.7±0.3b | 28.63±1.8b | 20.60±2.0c | |
| Púa larga | 17.98±3.4ab | 3.4±0.2b | 23.00±2.6c | 19.80±1.0c | |
| Chalqueño | 17.86±3.1ab | 3.5±0.1b | 41.42±5.4a | 19.20±1.2c | |
| Productivo | Manso | 8.45±0.7d | 4.3±0.5a | 11.98±2.2d | 24.10±2.4cb |
| Ayoteco | 20.06±1.9a | 4.4±0.7a | 40.34±3.7a | 21.90±2.8c | |
| Púa larga | 7.87±0.7d | 4.3±0.6a | 13.86±1.1d | 22.40±3.1c | |
| Chalqueño | 5.86±0.3d | 4.7±1.1a | 20.54±1.9c | 24.30±5.2cb | |
| Senescencia | Manso | 8.56±0.4d | 4.6±1.2a | 9.65±1.0d | 31.20±2.3a |
| Ayoteco | 8.45±1.1d | 4.8±1.3a | 13.81±2.1d | 32.50±3.3a | |
| Púa larga | 20.66±3.5a | 4.6±1.1a | 45.61±4.5ª | 35.40±2.1a | |
| Chalqueño | 8.22±2.2d | 4.1±0.7ab | 10.87±0.3d | 32.10±3.2a |
Análisis por factor: cultivar
Se analizaron los resultados por cultivar: para ello se obtuvieron los promedios de ARD, ART, FOS e INU de cada etapa fenológica (Cuadro 3). El cultivar Chalqueño mostró un incremento del 61.2% para los ARD en comparación con el cultivar Púa Larga. Con relación a los ART, el cultivar Ayoteco presentó los valores más altos en comparación con Manso. Respecto a los FOS se observó que Ayoteco tuvo los mayores valores comparando con el resto de los cultivares. En cuanto a la INU, no se detectaron diferencias significativas en los cultivares Ayoteco, Chalqueño y Púa Larga. La INU en Ayoteco se incrementó 1.4 veces en comparación con Manso.
Cuadro 3: Perfil de carbohidratos en cultivares de Agave salmiana Otto ex Salm-Dyck analizados por el factor cultivar. Para cada cultivar se presentan los promedios de las cuatro etapas fenológicas (edad media, capón, productivo, senescencia). *Promedio±desviación estándar. Letras distintas indican diferencias significativas, comparación entre columnas (p<0.05). ARD: azúcares reductores directos, ART: azúcares reductores totales, FOS: fructooligosacáridos, INU: inulina.
| Cultivar | ARD (%) | ART | FOS | INU |
| Ayoteco | 10.50±2.3b* | 52.49±6.1a | 15.05±2.1a | 24.19±1.3b |
| Manso | 12.00±1.1ab | 43.08±3.7c | 11.39±2.8bc | 16.94±4.3b |
| Chalqueño | 13.30±0.0a | 48.73±5.9ab | 10.67±1.7c | 22.06±1.2b |
| Púa Larga | 8.14±0.8c | 44.75±6.2bc | 12.99±1.1b | 21.22±2.1b |
Análisis por factor: etapa fenológica
Se analizaron los resultados por etapa fenológica: para ello se obtuvieron los promedios de ARD, ART, FOS e INU de cada cultivar (Cuadro 4). Se observaron dos etapas fenológicas con resultados contrastantes: en un extremo se encontró la etapa capón con los valores más altos para todos los carbohidratos (ARD, ART, FOS e INU) y en el otro extremo la etapa edad media con los valores más bajos para ART e INU.
Cuadro 4: Perfil de carbohidratos en cultivares de Agave salmiana Otto ex Salm-Dyck analizados por etapa fenológica. Para cada etapa fenológica se presenta el promedio de los cuatro cultivares (Ayoteco, Manso, Púa Larga y Chalqueño). *Promedio±desviación estándar. Letras distintas indican diferencias significativas, comparación entre columnas (p<0.05). ARD: azúcares reductores directos, ART: azúcares reductores totales, FOS: fructooligosacáridos, INU: inulina.
| Etapa fenológica | ARD (%) | ART | FOS | INU |
| Edad media | 10.11±1.0b* | 34.96±4.5c | 10.81±1.6b | 16.02±1.1bc |
| Capón | 13.23±2.9a | 64.10±8.3a | 17.16±3.6a | 27.84±3.3a |
| productivo | 10.91±1.1b | 45.89±5.8b | 10.62±0.9b | 21.68±2.3b |
| Senescencia | 9.84±0.9b | 44.10±6.2b | 11.50±1.3b | 18.90±2.0ab |
Análisis por componentes principales
La matriz de correlaciones obtenida por el análisis de componentes principales indicó que existe alta correlación entre los ART con la INU (0.871) y con los FOS (0.820) (ver Apéndice). Estas correlaciones se observan de manera gráfica en el plano de variables (Fig. 4). El componente 1 explicó 46.96% de la varianza de todas las variables y el componente 2 21.34%. Este resultado indicó que bajo las condiciones de estudio es posible correlacionar una medida relativamente sencilla a nivel laboratorio (ART) con mediciones más específicas (INU y FOS). La correlación de los ART con el GPPINU y GPPFOS es muy baja, lo que significa que los ART no explican los GPP, lo cual es una limitante del presente análisis. Finalmente, la matriz de componente mostró baja correlación de la componente 2 con los GPP tanto de INU como de FOS (<0.7), por lo que no es posible establecer alguna conclusión.
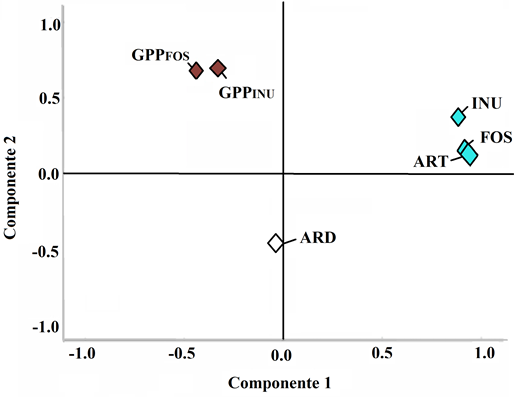
Figura 4: Plano de variables del análisis de componentes principales. Los dos componentes explican el 70% de la varianza en la matriz de datos. ART: azúcares reductores totales, ARD: azúcares reductores directos, FOS: fructooligosacáridos, INU: inulina, GPPINU: grado de polimerización promedio de INU, GPPFOS: grado de polimerización promedio de FOS.
Análisis por CG/MSD en cultivares a diferentes etapas fenológicas
En la Figura 5 se muestran los compuestos identificados por CG-MSD. Mayoritariamente se encontraron ácidos grasos y ésteres, aunque también se identificaron azúcares, alcoholes y ácidos. El ácido oleico estuvo presente en 15 de las 16 muestras, siendo más abundante en los cultivares Manso-senescencia y Ayoteco-senescencia. El ácido linoleico se detectó en 15 de las 16 muestras analizadas, siendo más abundante en el cultivar Manso-senescencia. El ácido vaccénico se encontró en todos los cultivares y etapas fenológicas, excepto en Chalqueño-productiva. De manera adicional algunas muestras presentaron ácido butanoico, acético, D-manoheptosa y L-treitol.
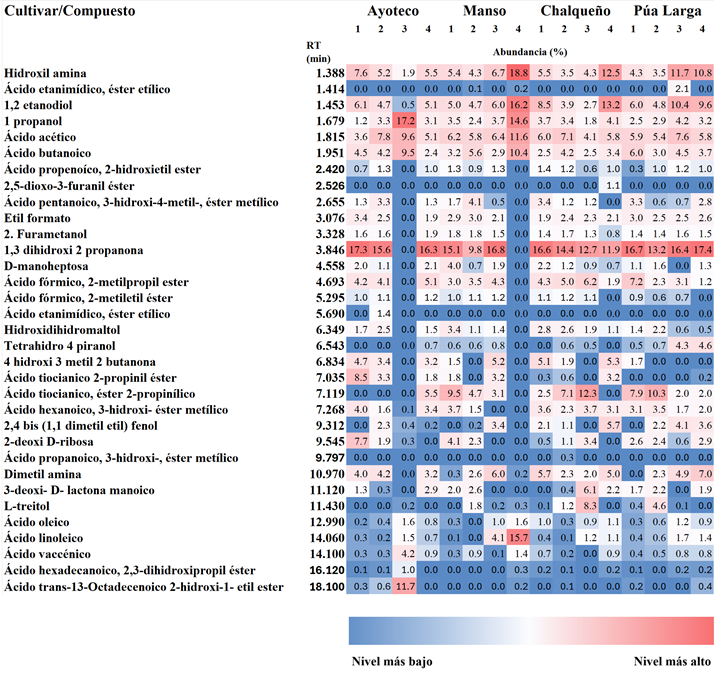
Figura 5: Compuestos identificados por CG/MSD en Agave salmiana Otto ex Salm-Dyck en cultivares de Tlaxcala, México. 1: edad media, 2: capón, 3: productivo, 4: senescencia. RT: Tiempo de retención.
Respecto a los ésteres, no se observó una consistencia en el tipo y contenido de estos compuestos, lo cual sugiere una gran diversidad en el tipo de ésteres para cada cultivar y etapa fenológica.
Discusión
Las diferencias encontradas en la concentración de los ARD para los cultivares y etapas fenológicas pueden ser causa de diversos factores en la fenología del agave, como la tasa de fotosíntesis, los azúcares liberados en forma de aguamiel y de la tasa de hidrólisis de fructanos. Es importante mencionar que los cultivares Manso y Púa Larga se distinguen por producir aguamiel con altos niveles de azúcares (14 °Bx) y llegan a su etapa productiva a edad más temprana (9 años), por lo que se les ha denominado “precoces”. Por otro lado, los cultivares Ayoteco y Chalqueño llegan a su etapa productiva entre los 12 y 14 años, produciendo aguamiel de 10 °Bx y debido a su gran tamaño se les denominan “gigantes”. Para la etapa productiva se observó que los cultivares gigantes tienen más azúcares directos en las pencas, lo que sugiere una baja migración de ARD a la piña, ya que su aguamiel suele ser menos dulce (10 °Bx), contrastando con los cultivares “precoces”, cuya aguamiel suele ser de 14 °Bx y la concentración de ARD en las pencas fueron un orden de magnitud menor respecto a los “gigantes”. Por otro lado, estos cultivares también se caracterizan por tener menor tamaño, lo que significa que una mayor cantidad de energía se destina a la reproducción y mantenimiento vegetativo.
Robles-Arías et al. (2024) reportaron la concentración de carbohidratos totales en A. salmiana en su madurez fisiológica (etapa capón) dividiendo las pencas en tres partes: punta, centro y base, y obtuvieron valores de 6.50, 11.98 y 16.70%, respectivamente. Sin embargo, en este estudio no se reportó el tipo de cultivar utilizado. Los resultados encontrados para Chalqueño-capón (Fig. 2) superan los valores encontrados por Robles-Arías et al. (2024) para la base de las pencas en un 11.68% y están dentro del rango para el resto de los cultivares. Esto indica que existen variaciones dependiendo del tipo de cultivar y también refleja la necesidad de hacer estudios para determinar las moléculas presentes en diversas secciones de las pencas para diversos cultivares y etapas fenológicas.
De acuerdo con Mora-López et al. (2011), el inicio del crecimiento del pedúnculo floral indica el cambio fisiológico del maguey de un estado vegetativo a reproductivo, a lo que los productores le denominan “maguey capón”; en esta etapa los fructanos se despolimerizan para proporcionar energía a los órganos reproductores. Esto indica que los mayores niveles de ARD están presentes en la etapa fenológica capón, lo cual es cierto para los cultivares Manso, Púa Larga y Chalqueño y no así para el cultivar Ayoteco, donde se observó su nivel más alto en la etapa productiva. Esto contrasta con el reporte de Aldrete-Herrera et al. (2019), quienes evaluaron la presencia de ARD en pencas de A. salmiana cv. Chino y reportaron que los ARD alcanzaron su máxima concentración en la primera etapa de crecimiento. A la edad de 2-4 años obtuvieron valores de 26.40 g/100 g de agave seco y disminuyeron conforme crecía la planta. A la edad de 10-12 años obtuvieron valores de 13.08 g/100 g de agave seco. Esto sugiere la disposición de azúcares simples para el crecimiento vegetativo de la planta.
En los cultivares Púa Larga y Manso, se observó la mayor concentración de ARD en la senescencia en comparación con la etapa productiva. Por lo tanto, se puede inferir para el cultivar Púa Larga que, al dejar de “raspar el maguey, los azúcares se concentran en las pencas y para el cultivar Manso que los azúcares se agotaron durante la extracción de aguamiel. En general, se observaron diferencias entre los cultivares en cada etapa fenológica, lo que sugiere que la composición química de la planta es un proceso dinámico.
Los diferentes cultivares pueden ser aprovechados de manera estratégica dependiendo su fin. Por ejemplo, si el objetivo es extraer ARD de las pencas con pocas operaciones unitarias, los cultivares recomendados serían Chalqueño y Ayoteco. Los ARD pueden ser aprovechados para generar jarabes, bioetanol y diversos productos fermentados (Láinez et al., 2019; Vicente-Magueyal et al., 2020). Si el objetivo es aprovechar el aguamiel, los cultivares Manso y Púa Larga son los candidatos adecuados, ya que producen aguamiel con mayor cantidad de azúcar. El aguamiel se podría utilizar para generar bebidas funcionales, pulque, destilado de pulque, concentrado de aguamiel o diversos productos como galletas, pan, dulces, etc.
Con respecto a los ART, no se observó un patrón uniforme para los cuatro cultivares respecto al momento en que alcanzan los mayores niveles de ART. Sin embargo, se ha reportado en las vacuolas de protoplastos de mesontle (tallo) de A. tequilana cv. Weber Blue que la mayor actividad de las hidrolasas de los fructooligosacáridos (que generan azúcares simples y contribuyen con los ART) ocurre entre los dos y cuatro años de crecimiento de la planta (Mellado-Mojica y López, 2012). Esto contrasta con los resultados encontrados para los cuatro cultivares estudiados (Fig. 3) y corrobora la propuesta de este trabajo: el mejor criterio para la determinación y caracterización de los agaves no se debe fundamentar en la edad, sino más bien en la etapa fenológica. La mayor concentración de ART para el cultivar Púa Larga se observó en la senescencia. Es destacable este último hecho, ya que en la senescencia la planta inicia su proceso de muerte y se esperarían niveles más bajos de azúcares, lo cual podría explicarse considerando que la mayoría de los azúcares están polimerizados (8% de ARD). Los resultados de ART para casi todos los cultivares y etapas fenológicas (excepto Púa Larga-edad media y Púa Larga-productiva) están dentro del rango reportado por Montañez-Soto et al. (2011) en pencas de ocho años de edad de A. tequilana cv. Weber Blue (26.30 a 80.20 %). En A. salmiana se han reportado valores de 85% de ART (Láinez et al., 2018). El contenido de INU y FOS de los cuatro cultivares predominantes en Tlaxcala hasta ahora no habían sido reportados.
Las diferencias encontradas en este trabajo son importantes para el proceso de extracción de azúcares y para estandarizar procesos como el aprovechamiento de la planta. Por ejemplo, el cultivar Ayoteco es atractivo, ya que después de producir aguamiel aún es posible obtener altos niveles de azúcares para otros procesos. Los métodos propuestos en el presente trabajo para extraer los azúcares son una alternativa viable. Sin embargo, también se ha experimentado con otros métodos para la obtención de azúcares por medio de la conversión de lignina y celulosa (Láinez et al., 2018), aunque esta conversión involucra métodos químicos agresivos que ambientalmente no son sustentables.
En cuanto a los FOS, las mayores concentraciones encontradas sugieren una despolimerización de INU a FOS o una alta tasa de biosíntesis de FOS. La concentración promedio de INU en la etapa capón fue de 20.6%, lo que sugiere que hay una transformación de INU a FOS (debido a que capón presentó altos niveles de FOS). Esto indica que el agave se prepara energéticamente para el desarrollo del escapo floral y por consiguiente a la reproducción. Montañez-Soto et al. (2011) reportaron en A. tequilana cv. Weber Blue el contenido de FOS para los tallos, bases de hoja y ápices de las hojas de 25, 14 y 6%, respectivamente. Esto sugiere que la despolimerización de la INU en FOS lleva un proceso de migración de los ápices de la hoja hacia la piña, en donde se acumulan para nutrir a las estructuras reproductivas del agave. Esta tendencia también fue observada por González-Llanes et al. (2018). El contenido de FOS en diversas especies de agave oscila alrededor de 12% (Guevara Apraez y Vallejo Castillo, 2015). Sin embargo, estos estudios se han realizado en una sola etapa fenológica. Los resultados encontrados en este trabajo para los FOS e INU están dentro del rango reportado por Montañez-Soto et al. (2011). Aunado a esto, Aldrete-Herrera et al. (2019) encontraron GPP de 19 para los fructanos de A. salmiana en la etapa fenológica capón y esta fue dependiente del lugar de origen del agave. Esto confirma la versatilidad de los agaves ya que sus respuestas químicas dependen de variables del clima y suelo (Mellado-Mojica y López, 2012).
En el análisis por cultivar y por etapa fenológica podemos notar que el valor máximo para INU fue de 24.19 y 27.84%, respectivamente (Cuadros 2, 3). Sin embargo, en A. tequilana y utilizando los mismos métodos analíticos se han reportado niveles de INU superiores (43%) (Montañez-Soto et al., 2011). Dichas diferencias se pueden deber a la especie de agave y a la etapa fenológica, aunado a la “plasticidad” de los agaves que se traduce en diversos fenotipos (Trejo et al., 2020). Estos resultados concuerdan con los de Regalado-Rentería et al. (2021) y Godínez-Hernández et al. (2016), quienes obtuvieron el mayor contenido de carbohidratos en los magueyes capones (quiotillo), en el momento en el que se adelgaza el cogollo con valores máximos de INU de 50%. Hasta ahora, las diferencias morfológicas eran los únicos parámetros para distinguir entre cultivares, ya que los análisis por marcadores moleculares (ITS) no son suficientes para establecer una diferencia molecular, lo cual se puede deber probablemente al poco tiempo de domesticación (Trejo et al., 2020).
Los AG identificados en este trabajo resultan interesantes desde el punto de vista tecnológico y de aplicación. Lo más importante de estos hallazgos radica en que los AG se identificaron en diferentes etapas fenológicas, por lo cual los cultivares pueden ser aprovechados en etapas tempranas. En este trabajo se han encontrado algunos AG como el oleico y linoleico identificados previamente reportados en A. salmiana, A. angustifolia Haw. y A. tequilana (Peña-Alvarez et al., 2004; Jiménez-Ferrer et al., 2022). En A. sisalana Perrine se han identificado AG alfa y omega (Gutiérrez et al., 2008). Es importante mencionar que, aunque se ha obtenido un perfil de AG y ES similar a lo ya reportado, hasta el momento no hay un estudio que evalúe la presencia de estos compuestos en diferentes etapas fenológicas. Tanto los AG como los ES pueden tener muy diversas aplicaciones, resaltando las industrias cosmética, de alimentos y farmacéutica, entre otras (Cerone y Smith, 2021). En otros trabajos han encontrado amplia gama de terpenos (Peña-Alvarez et al., 2004), lo cual contrasta con nuestros resultados ya que este grupo de compuestos no fueron detectados. Una diferencia sustancial es que dichos trabajos están orientados al aprovechamiento de los tallos (Martínez-Aguilar y Peña-Álvarez, 2009) para la industria tequilera o mezcalera, por lo que sus análisis fueron realizados con extractos de las piñas, durante el procedimiento de destilación para detectar los aromas característicos (Peña-Alvarez et al., 2004) o bien durante el procesamiento térmico.
El presente trabajo permite conocer los mejores cultivares y etapas fenológicas de la planta para la obtención de carbohidratos, AG, ES y otras moléculas y se brindan herramientas para distinguir los cultivares desde un punto de vista químico. Es importante mencionar que hasta este momento no existen reportes previos para los cultivares utilizados en este trabajo. El análisis por factor cultivar permite valorar el potencial de los cultivos de A. salmiana para algún propósito tecnológico, sobre todo para aquellos cultivos en los que prevalece un cultivar en particular. Aunado a esto, se confirma que es importante considerar la etapa fenológica y no la edad cronológica como criterio para seleccionar las plantaciones.
Conclusiones
Los cuatro cultivares en sus cuatro etapas fenológicas presentaron potencial para extraer compuestos de interés comercial. Para el aprovechamiento integral de Agave salmiana subsp. salmiana, es necesario conceptualizarlo como un elemento “cultivar-etapa fenológica”, ya que las características químicas de los cultivares dependen de la fenología y no directamente de la edad como se ha reportado. Es necesario realizar investigación para determinar la distribución de los GPP ya que en función de esto también es el destino tecnológico.