Introducción
El arroz (Oryza sativa L) requiere la aplicación constante de fertilizantes de origen químico que ha generado elevados costos de producción a cosechas afectando la calidad ambiental del suelo (Trujillo, Manchola y Santofimio, 2020) y de los recursos hídricos (Aveiga-Ortiz, Noles, Macías y Herrera, 2020). En este contexto los químicos producen efectos negativos en el sistema productivo de arroz como: resurgencia de patógenos (Vinchira-Villarraga y Moreno, 2019), eliminación de polinizadores (Cajamarca-Carrazco, Paredes, Cabrera, Velasco y Vaca, 2020), reducción de agentes biológicos (Herrera et al., 2023), degradación del suelo (Ali et al., 2020), contaminación de acuíferos por lixiviación de herbicidas (Gómez-Beltrán, Cano y Villar, 2021) y contaminación atmosférica por las emisiones de metano y óxido nitroso (Timilsina et al., 2020; Nikolaisen et al., 2023).
La búsqueda de prácticas agronómicas sostenibles con el medio ambiente permite mejorar la productividad de los cultivos y reducir los efectos negativos del uso excesivo de agroquímicos. Dentro de estas alternativas, están el uso de rizobacterias promotoras del crecimiento vegetal (PGPR). Las PGPR tienen efectos benéficos para las especies vegetales y genera diversos mecanismos como: liberación de ácidos cuyas propiedades quelante favorecen la formación de complejos insolubles con metales, con la consecuente liberación del fosfato y micronutrientes del suelo (Posada-Castaño, Mejía, Polanco y Cardona, 2021).
Las PGPR mejoran la capacidad fijación nitrógeno (Tang, Haruna, Majid y Jalloh, 2020), producción de fitohormonas (Narula, Deubel, Gans, Behl y Merbach, 2006), sideróforos, la reducción de los niveles de etileno, el incremento de la permeabilidad de las raíces (Grover et al., 2021). Además, las rizobacterias son capaces de generar metabolitos asociados al biocontrol de patógenos como: antibióticos, producción de quitinasas e inducción de resistencia en las plantas, contribuyendo a reducir, la dependencia de fertilizantes químicos y el empleo de pesticidas al control de plagas y enfermedades (Velazco-Jiménez, Castellanos, Acevedo y Aarland, 2020).
La aplicación de bioformulados a base de Pseudomonas spp. presentan un efecto bioestimulante en arroz, con un aumento de peso fresco de raíz, el número de brotes y mayor proceso de germinación (Chandra y Charma, 2021). Por otra parte, se identificaron que las bacterias Pseudomonas spp. y Bacillus spp. tienen la capacidad de solubilizar fosfatos inorgánicos lo que demuestra sus potencialidades en la estimulación del crecimiento vegetal (Rasul et al., 2019).
La generación de ácido Indol-3-acético (AIA) se encuentra extendida en diversas bacterias presentes en la rizosfera, estimándose que está presente en alrededor del 80% de estos microorganismos (Chaudhary et al., 2021). La función de la producción de AIA por parte de los microorganismos radiculares influye en la formación de la estructura de las raíces de las plantas, mejorando la solubilización de fósforo (P) y otros nutrientes en el suelo (Fierro-Coronado et al., 2014; Duca, Lorv, Patten, Rose y Glick, 2014).
Las rizobacterias actúan sobre la absorción en las plantas y la disponibilidad de nitrógeno, fósforo y potasio en el suelo (Hegyi, Nguyen y Posta, 2021). Los principales mecanismos para la solubilización del potasio es la producción de ácidos orgánicos como: ácido oxálico, ácido tartárico, ácido glucónico, ácido 2-cetoglucónico, ácido cítrico, ácido málico, ácido succínico, ácido láctico, ácido propiónico, ácido glicólico, ácido malónico, ácido fumárico y producción de protones (Etesami, Emami y Alikhani, 2017). De manera similar las PGPR tienen la capacidad de solubilizar fosfatos a partir de compuestos inorgánicos u orgánicos, empleando distintas vías como la actividad de enzimas: fosfatasas no específicas, fitasas, fosfonatasas y C-P liasas que solubilizan fósforo a partir de compuestos orgánicos en el suelo (Molina-Romero et al., 2015).
La aplicación de bioformulados bacterianos en cultivos de interés agrícola es una alternativa viable para los agricultores a nivel económico y ambiental. El objetivo se basó en determinar bacterias productoras de ácido indol acético (AIA) y solubilizadoras de fósforo (P) y potasio (K) como promotoras de crecimiento en Oryza sativa L.
Materiales y Métodos
La investigación se realizó en el Laboratorio de Microbiología y Biología Molecular ubicados en el Campus Experimental “La María”, perteneciente a la Universidad Técnica Estatal de Quevedo (UTEQ) localizada en el km 7.5 de la Vía Quevedo - El Empalme, cantón Mocache, provincia de Los Ríos, con coordenadas geográficas 1° 04’ 51.7” S 79° 30’ 10.0” O, a una altitud de 66 m de altitud.
Aislamiento de Bacterias Endófitas de Cultivares Nativos
Del Banco de Germoplasma del Laboratorio de Microbiología Molecular de la UTEQ, fueron seleccionadas las rizobacterias provenientes de cultivares endémicos de musáceas con su clasificación a metabolitos secundarios y sideróforos (Cuadro 1). Las rizobacterias se incubaron en 100 mL de King B (KB) líquido selectivo [(g L-1): peptona de carne 20.0; glicerol, 15.0 mL; fosfato dipotásico; 1.5; sulfato de magnesio heptahidratado, 1.5; agua destilada (pH 7,2)], suplementado con chloramphenicol (13 μg mL-1), ampicilina (40 μg mL-1) por 48 h (King, Ward y Raney, 1954).
Table 1: Color of squash fruit peel (Cucurbita pepo L.) var. ‘Grey Zucchini’s.
| Cepas | Metabolitos antagónicos | Sideróforos | ||
| PR | HCN | Prn | ||
| Pseudomona putida PB 3- 6 | + | + | - | + |
| Acinetobacter sp. BMR 2-2 | + | - | + | + |
| Klebsiella variicola BO3-4 | + | + | + | + |
| Enterobacter asburiae BA 4-19 | + | - | - | + |
| Enterobacter asburiae PM 3 -14 | + | + | + | + |
| Pseudomona putida BMR 2 -4 | - | - | + | + |
| Pseudomona protegens CHAO | + | + | + | + |
| Pseudomona veronii R4 | + | - | + | + |
| Acinetobacter calcoaceticus BMR 2-12 | - | - | + | + |
| Serratia marcescens PM 3-8 | + | + | + | + |
PR = proteasa; HCN = cianuro de hidrógeno; Prn = pirrolnitrina; Sideróforos (Peñafiel-Jaramillo et al., 2016; Chávez-Arteaga, Guato, Peñafiel, Mestanza y Canchignia, 2018; Montes et al., 2016).
PR = protease; HCN = hydrogen cyanide Prn = pyrrolnitrin; Siderophores (Peñafiel-Jaramillo et al., 2016; Chávez-Arteaga, Guato, Peñafiel, Mestanza, and Canchignia, 2018; Montes et al., 2016).
Capacidad Solubilizadora de P y K
De forma individual, se recuperó 5 μl del inóculo reactivado y se cultivó en placas Petri con medio Pikovskaya modificado (K) (g L-1): (C₆H₁₂O₆ 10 g, KNO₃ 5 g, KCl 0.2 g, (NH4)2SO4 5 g, MgSO₄ 7H₂O 0.1 g; C21H16Br2O5S 0.125 g y Agar 15 g) (Canchignia-Martínez et al., 2024a). Para determinar la solubilización de (P) se usó Pikovskaya (g L-1): (C₆H₁₂O₆ 10 g; Ca3(PO4)2 5 g; MgCl₂·6 H₂O 5 g; KCl 0.2 g; (NH4)2SO4 0.1 g; Agar 20 g) (Pikovskaya, 1948). Las muestras se incubaron a 28 °C y se monitorearon durante 72 horas las siguientes variables: halo de solubilización (HS, mm), diámetro de la colonia (DC, mm) y, mediante el cociente HS/DC, se calculó la eficiencia relativa de solubilización (ERS, %).
Producción de (AIA)
La producción de AIA se estimó por colorimetría basado en el reactivo de Salkowski (Patten y Glick, 1996). Las cepas se cultivaron en medio KB suplementado con L-triptófano (0.025 mM) a 150 rpm. Se colectó 1 mL del inóculo bacteriano y se centrifugó a 10000 G durante 5 min, de manera seguida se recuperó 250 μL del sobrenadante y se mezcló con el reactivo de Salkowski en relación (1:4) y se mantuvieron durante 30 min a oscuridad. Se registró una curva estándar de la solución de Salkowski y se leyeron con el espectrofotómetro modelo 1205 VIS a 530 nm. estándar. Las muestras positivas pasaron de tonos de rosa a rosa intenso, mientras que las muestras negativas presentarán coloraciones amarillo claro. Los tratamientos fueron evaluados a las 24, 48 y 72 h. Los datos se expresaron en microgramos por mililitro.
Desarrollo Radicular por la Inoculación de Rizobacterias en Semillas
Se usó el material genético de arroz INIAP FL - ÉLITE. Las semillas se esterilizaron de forma superficial con alcohol (70%) y NaOCl (1% V/V) durante un minuto. Las semillas fueron lavadas con agua destilada estéril y se sumergieron en una solución líquida de rizobacterias (1×108 UFC mL-1) de forma individual durante 60 minutos. Se seleccionaron rizobacterias por su mayor producción de AIA, solubilización de K y P. Los granos fueron lavados con abundante agua desionizada (pH 6.8) para retirar partículas de medio de cultivo. Se transfirieron cuatro semillas por caja Petri estériles que contenían 20 g L-1 de agar-agua con su respectivo control (semillas sin inoculantes bacterianos). Las cajas de Petri se incubaron a temperatura ambiente (25 °C) bajo un fotoperiodo de 12 h luz - 12 h oscuridad durante 15 días. A partir del día 5 al 15, se evaluó la longitud de la raíz principal con un calibrador de vernier marca ASIMETO, considerando la medida desde el cuello de la planta hasta el término de la raíz. Se evaluaron 36 plantas por tratamiento (Cuadro 2).
Aplicación de Bioformulados Bacterianos en Presencia de Fertilizantes de Nitrógeno y Fósforo para Mejorar el Estado Morfológico del Arroz.
Las semillas de arroz se desinfectaron con peróxido de hidrogeno al 10% por 3 minutos y se ubicaron en cámara húmeda para su proceso de germinación durante 48 h. Se usó un sustrato compuesto de turba, suelo y compost en relación (2:1:1), esterilizado en autoclave a 15 psi a 121 °C por 60 minutos. Se colocaron 300 g de sustrato en fundas plásticas de color negra con dimensiones de 5 cm × 8 cm y se trasplantaron 4 semillas germinadas por funda. Se utilizó P. protegens CHA0 seleccionada por su promoción de crecimiento vegetal y capacidad en la solubilización de nutrientes. La cepa se incubó en medio de cultivo KB líquido a 180 rpm durante 48 h con 27 °C. Del cultivo, se tomaron 20 uL (1×108 UFC mL-1) y se transfirieron a 100 mL de los medios de cultivos alternativos BIO-IMPULSE, BIO-QPGPRs y PGPRs-4N (Cuadro 3).
Table 3: Composition of the different formulations..
| Formulado | Ingrediente | Unidad | |
| PGPRs-4N | Melaza | g L-1 | 20 |
| Harina de maíz | 20 | ||
| Sal en grano | 5.0 | ||
| Roca fosfórica | 1.5 | ||
| Glicerina | mL | 7.0 | |
| p | 6.5 | ||
| BIO-IMPULSE | Melaza | g L-1 | 20 |
| Harina de maíz | 20 | ||
| Sal en grano | 5.0 | ||
| Roca fosfórica | 1.5 | ||
| Glicerina | mL | 7.0 | |
| Aceite mineral | 5.0 | ||
| pH | 6.5 | ||
| BIO-QPGPRs | Melaza | g L-1 | 10 |
| Harina de maíz | 20 | ||
| Sal en grano | 5.0 | ||
| Roca fosfórica | 1,5 | ||
| Glicerina | mL | 7.0 | |
| Fijador | 5.0 | ||
| Lixiviado de raquis de banano | 15 | ||
| pH | 6.5 | ||
| Agua | Agua desionizada | 6.8 pH | - |
Los cultivos se incubaron a 180 rpm durante 72 h con 26 °C. Las muestras se homogenizaron en relación v/v al 25 % (7.1×106), de esta solución se aplicó 15 mL durante el día 4 y 15 días después del transplante (DDT). Esta última aplicación fue de forma simultánea con las soluciones líquidas de Urea (N 46%), Superfosfato triple (P 46%) y su combinación (Cuadro 4).
Table 4: Fertilizer rates in rice plants.
| No. | Nutrientes | Descripción |
| 1 | Nitrógeno (N) | 2 g de Urea en 10 mL de agua desionizada* |
| 2 | Fosforo (P) | 1.4 g de DAP en 10 mL de agua desionizada* |
| 3 | (N, P) | 2 y 1.4 g de Urea y DAP en 10 mL de agua desionizada* |
* La solución corresponde a una 300 g de sustrato.
* The solution corresponds to 300 g of substrate.
Tratamientos y Variables a Evaluadas
El siguiente ensayo estuvo compuesto por 12 tratamientos (Cuadro 5), donde a los 40 DDT se evaluaron las siguientes variables: altura de planta (cm), longitud radicular (cm), biomasa seca del área foliar y radicular (g) y escala colorimétrica, donde en esta última se utilizó la escala de colores denominada carta de color de hoja (LCC) usada en fertilización en arroz planteado Maiti, Das, Karak y Banerjee (2004).
Diseño Experimental y Análisis de Datos
En el experimento de crecimiento, eficiencia y solubilización de P y K insoluble; producción de AIA y desarrollo radicular en O. sativa por rizobacterias se aplicó un diseño completamente al azar (DCA). Con tres réplicas. A nivel invernadero, se empleó un DCA con factorial, para bioformulado y fertilizante. Cada tratamiento contenía tres repeticiones.
Para garantizar la confiabilidad en la estadística paramétrica como ANDEVA, los datos fueron sometidos a normalidad mediante Shapiro-Wilk y se aplicó la prueba de Bartlett para verificar el supuesto de homogeneidad de la varianza. Los datos fueron sometidos al análisis de varianza (ANDEVA) y separados por procedimiento de comparación múltiple de Tukey, al nivel de significancia de (P ≤ 0.05). Para el análisis de varianza y pruebas de rangos múltiples, se utilizó el software estadístico Infostat 2020 (Di Rienzo et al., 2020), mientras para las pruebas de normalidad y homogeneidad de la varianza, la versión 19.1.0 del software Minitab (Minitab, 2021).
Resultados Y Discusión
Solubilización de K insoluble
Las cepas de rizobacteria no mostraron diferencia estadística significativas en el diámetro del halo (P = 0.699), colonia (P = 0.213) y eficiencia de solubilización (P = 0.151) durante las 72 h (Cuadro 6). Se evidenciaron que E. asburiae, P. protegens CHA0 y P. veronii R4 tuvieron una mayor solubilización (3.10; 2.60 y 2.50 mm) respectivamente. Existió una variabilidad en el desarrollo de la colonia, donde Acinetobacter sp. BMR 2-2, A. calcoaceticus, K. variicola BO 3-4 presentaron una mayor adaptabilidad y crecimiento en su morfología (1.20; 0.80 y 0.80 mm).
Cuadro 6: Rizobacterias solubilizadoras de K, Diámetro del halo y colonia; eficiencia relativa de solubilización (%).
Table 6: K-solubilizing rhizobacteria. Halo and colony diameter; relative solubilization efficiency (%).
| Cepas | Diámetro del halo | Diámetro de colonia | Eficiencia relativa de solubilización |
| - - - - - - - - - mm - - - - - - - - - | % | ||
| E. asburiae BA 4-19 | 3.10±1.50 | 0.65±0.06 | 472 |
| P. protegens CHA0 | 2.60±0.19 | 0.70±0.03 | 367 |
| P. veronii R4 | 2.50±0.71 | 0.75±0.51 | 337 |
| P. putida PB 3-6 | 2.10±0.28 | 0.65±0.08 | 321 |
| S. Marcescens PM 3-8 | 2.30±0.09 | 0.75±0.03 | 307 |
| E. asburiae PM 3-14 | 2.50±0.85 | 0.85±0.13 | 292 |
| P. putida BMR 2-4 | 2.20±0.38 | 0.75±0.10 | 291 |
| A. calcoaceticus BMR 2-12 | 2.20±0.23 | 0.80±0.13 | 271 |
| K. variicola BO 3-4 | 2.00±0.44 | 0.80±0.08 | 254 |
| Acinetobacter sp.BMR 2-2 | 2.55±0.09 | 1.20±0.16 | 213 |
| P (cepas) | 0.699 | 0.213 | 0.151 |
Los valores de promedio y desviación estándar (±) corresponden a n = 6.
Mean and standard deviation (±) values correspond to n = 6.
Sin embargo, E. asburiae BA 4-19, P. protegens CHA0 y P. veronii R4 evidenciaron una mayor eficiencia relativa de solubilización (472; 367 y 367%). Esto concuerda con Saxena, Kumar, Tomar, Singh y Purushottam (2020) que han reportados rizobacterias con una ERS de K superior al 300%. Las rizobacterias utilizan diferentes mecanismos para solubilizar el potasio insoluble y fijado, que incluyen la reducción del pH del suelo mediante la producción de ácidos orgánicos e inorgánicos de bajo peso molecular y la acidólisis (Ashfaq, Hassan, Ghazali y Ahmad, 2020). Por esta situación, la cepa en estudio tiene una característica específica en la solubilización, además podría ser una alternativa en suelos con baja solubilidad de K, aumentando su eficiencia y la promoción de crecimiento en plantas.
Solubilización de P Insoluble
Las cepas de rizobacteria mostraron diferencia estadística significativas en el diámetro del halo (<0.0001), colonia (0.0005) y eficiencia relativa de solubilización (<0.0001) durante las 72 h. Se demostró que P. protegens CHA0 es una especie con mayor capacidad para solubilizar el fósforo con un halo de 1.92 mm. Acinetobacter sp. BMR 2-2 y P. protegens CHA0 presentaron un mayor crecimiento de colonia (1.90 y 1.80 mm). Se evidenciaron un incremento de ERS en P. putida PB 3-6, S. marcescens PM 3-8 y A. calcoaceticus BMR 2-12 (116; 119 y 129 %) respectivamente (Cuadro 7). El reporte de Landa-Acuña, Toro, Santos y Zúñiga (2023) presentó una ERS de P (276%) a 28 °C durante 7 días, esto demuestra que las cepas incrementan su eficiencia de solubilización durante el tiempo. Sin embargo, E. asburiae BA 4-19, P. protegens CHA0 y P. veronii R4 evidenciaron una mayor eficiencia relativa de solubilización (111; 107 y 105%). El principal mecanismo para la solubilización del P inorgánico la producción de ácidos orgánicos, lo que reduce la acidificación del suelo, por la producción de fosfatasas ácidas y alcalinas, lo que provoca la mineralización de P. orgánico (Canchignia-Martínez et al., 2024b). El uso de solubilizadores de P, solos o en combinación con otras bacterias beneficiosas y micorrizas como inoculantes aumenta las perspectivas de aplicación directa de fosfato de roca (RP) en la absorción de P y la producción de cultivos. que promueven el crecimiento de las plantas como un consorcio microbiano ecológico, podría aumentar la absorción de P de los cultivos (Kour et al., 2021).
Cuadro 7: Rizobacterias solubilizadoras de P. Diámetro del halo y colonia; eficiencia relativa de solubilización (%).
Table 7: P-solubilizing rhizobacteria. Halo and colony diameter; relative solubilization efficiency (%).
| Cepas | Diámetro del halo | Diámetro de colonia | Eficiencia relativa de solubilización |
| - - - - - - - - - mm - - - - - - - - - | % | ||
| E, asburiae BA 4-19 | 1.50±0.07 bc | 1.40±0.04 bc | 111 |
| P, protegens CHA0 | 1.90±0.08 a | 1.80±0.07 ab | 107 |
| P, veronii R4 | 1.60±0.14 abc | 1.60±0.16 abc | 105 |
| P. putida PB 3-6 | 1.60±0.04 abc | 1.40±0.02 bc | 116 |
| S. Marcescens PM 3-8 | 1.30±0.12 c | 1.20±0.08 c | 119 |
| E. asburiae PM 3-14 | 1.70±0.12 abc | 1.60±0.08 abc | 105 |
| P. putida BMR 2-4 | 1.70 ±0.05 abc | 1.60±0.06 abc | 106 |
| A. calcoaceticus BMR 2-12 | 1.50±0.10 bc | 1.20±0.22 c | 129 |
| K. variicola BO 3-4 | 1.70±0.06 ab | 1.50±0.06 abc | 112 |
| Acinetobacter sp BMR 2-2 | 0.00±0.00 d | 1.90±0.30 a | 0.00 |
| P (cepas) | <0.0001 | 0.0005 | <0.0001 |
Los valores de promedio y desviación estándar (±) corresponden a n = 6.
Mean and standard deviation (±) values correspond to n = 6.
Producción de AIA
La producción de AIA en las rizobacterias presentaron diferencias estadísticas significativas (P < 0.0001) durante las 72 horas de evaluación. A las 24 y 48 h, P. putida PB 3-6 y A. calcoaceticus BMR 2-12 evidenciaron mayor producción de AIA con (18.5 y 13.2 μg mL-1; 28.9 y 28.3 μg mL-1) respectivamente. Sin embargo, a las 72 h A. calcoaceticus BMR 2-12 presentó (17.90 μg mL-1). Estos datos coinciden con Adhikari, Jain, Sharma y Pandey (2021) donde reportaron cepas de rizobacterias con producción de AIA (9.70 y 13.1 ug mL-1), además evidenciaron que los aislados de raíces producían mayor auxina que las bacterias de suelo. La síntesis bacteriana de AIA difiere entre especies y cepas está asociado a las condiciones de cultivo, la tasa de crecimiento y la disponibilidad de sustrato (Li et al., 2018). Hay que indicar que la producción de AIA disminuye hasta las 72 h, esta estrategia es clave para la aplicación de las rizobacterias en el momento idóneo para obtener mayor eficiencia en plantas (Cuadro 8).
Cuadro 8: Rizobacterias productoras de Ácido Indolacético (AIA) durante 24, 48 y 72 horas de evaluación.
Table 8: Indoleacetic acid (IAA)-producing rhizobacteria during 24, 48 and 72 hours of evaluation.
| Cepas | Producción de AIA (ug mL-1) | ||
| 24 h | 48 h | 72 h | |
| E. asburiae BA 4-19 | 2.90±0.21 d | 14.10±0.31 c | 2.54±0.08 f |
| P. protegens CHA0 | 1.70±0.32 d | 24.20±2.3 b | 10.80±0.71 cd |
| P. veronii R4 | 14.60±1.5 b | 9.00±1.5 d | 4.30±0.03 f |
| P. putida PB 3-6 | 18.50±0.76 a | 28.90±0.35 a | 7.70±0.33 e |
| S. Marcescens PM 3-8 | 4.80±2.6 cd | 26.30±2.6 b | 14.90±0.13 b |
| E. asburiae PM 3-14 | 2.70±0.63 d | 25.50±0.68 b | 12.60±0.45 c |
| P. putida BMR 2-4 | 2.10±0.19 d | 14.10±0.68 c | 15.10±1.7 b |
| A. calcoaceticus BMR 2-12 | 13.20±2.3 b | 28.30±0.30 a | 17.90±0.63 a |
| K. variicola BO 3-4 | 3.70±0.58 d | 7.60±0.63 d | 3.40±0.13 f |
| Acinetobacter sp.BMR 2-2 | 7.70±0.33 c | 16.40±0.18 c | 9.90±0.74 d |
| P (cepas) | <0.0001 | <0.0001 | <0.0001 |
Los valores con letras similares no presentan diferencias estadísticas significativas al nivel de (P ≤ 0.05) por el procedimiento de comparación múltiple de Tukey (24, 48 y 72 h). Los valores de desviación estándar ± corresponden a n = 6.
Values with similar letters do not present significant statistical differences at the level of (P ≤ 0.05) by Tukey's multiple comparison procedure (24, 48 and 72 h). Standard deviation ± values correspond to n = 6.
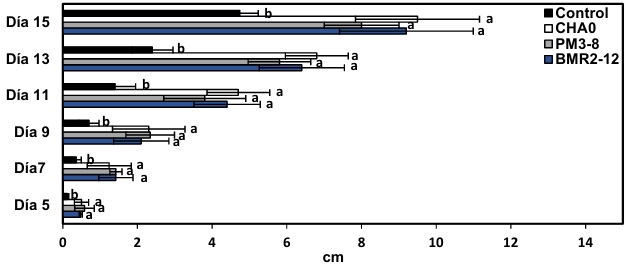
Desarrollo Radicular por la Inoculación de Rizobacterias en Semillas de Arroz
La aplicación de las rizobacterias promovió un desarrollo del sistema radicular en semillas de Oryza sativa L durante 15 DDT en comparación al control (Figura 1). Se demostró que el último día de evaluación, P. protegens CHA0 y A. calcoaceticus BM 2-12 incrementaron la longitud de la radícula (9.5 y 9.2 cm). Esto demuestra una mayor eficiencia en el proceso de germinación e incremento en longitud radicular. Esto coincide con los resultados de Rajer et al. (2022), quienes observaron que la inoculación de Pseudomonas spp. en semillas de arroz incrementó la velocidad de germinación y el vigor en plántulas, puesto que las bacterias promotoras del crecimiento de las plantas presentan un proceso acelerado de germinación mediante la producción de AIA (Ácido indol-3-acético). Castro, Inguanzo, del Monte y Badía (2019) y Jayaro, Ramírez, Hernández y Hernández (2020); aseveran que el AIA está involucrado en el crecimiento y desarrollo de las plantas, principalmente en una serie de procesos fisiológicos que incluyen el alargamiento y división celular, diferenciación de tejido, fototropismo, gravitropismo y en respuestas defensivas (Oliva-Hernández et al., 2021).
Aplicación de Bioformulados Bacterianos en Presencia de Fertilizantes de (N, P) para mejorar el Estado Morfológico del Arroz.
La altura de planta, longitud de raíz, biomasa seca foliar y radicular presentaron diferencia significativa en bioformulado (P < 0.0001). Se evidenció que la aplicación de BIO-IMPULSE + UREA incrementó la altura en la planta (71.70 cm) a los 40 DDT en comparación a las demás combinaciones. BIO-PGPRs + UREA demostró un mayor crecimiento longitudinal de la raíz (27 cm), por efecto de la producción de AIA y promoción de crecimiento por el bioformulado de rizobacteria y los nutrientes disponibles, sim embargo, cuando se aplicó solamente fertilizante mostraron valores que no superaron los 20 cm. La biomasa foliar aumentó con la aplicación de PGPRs-4N + DAP (2.60 g), situación similar se evidenció con la aplicación BIO-IMPULSE UREA+DAP que presentó un aumento en el peso radicular (3.0 g) (Cuadro 9).
Cuadro 9: Altura de planta, longitud de raíz, biomasa seca foliar y radicular en tratamientos en O. Sativa L. Los valores de p indican el efecto de los factores sobre la variable dependiente mediante un ANDEVA de dos vías (bioformulado × fertilizante).
Table 9: Plant height, root length, leaf and root dry biomass in treatments in O. Sativa L. P values indicate the effect of factors on the dependent variable using a two-way ANDEVA (bioformulated × fertilizer).
| Bioformulado | Fertilizante | Altura de planta | Longitud de raíz | Biomasa seca | |
| Foliar | Radicular | ||||
| - - - - - - - - - cm - - - - - - - - - | - - - - - - - - - g - - - - - - - - - | ||||
| BIO-IMPULSE | UREA | 71.70±2.9 a | 21.70±0.6 bc | 1.90±0.1 ade | 1.80±0.4 ab |
| BIO-IMPULSE | DAP | 64.30±2.1 b | 20.30±0.6 bcd | 2.10±0.2 acd | 2.10±0.2 ab |
| BIO-IMPULSE | UREA+DAP | 64.70±3.5 b | 23.30±1.5 ab | 2.50±0.5 ab | 3.00±1.0 a |
| PGPRs-4N | UREA | 59.70±0.5 bc | 23.70±0.6 ab | 2.40±0.2 abc | 1.90±0.6 ab |
| PGPRs-4N | DAP | 58.30±2.5 bc | 22.30±0.6 bc | 2.60±0.5 a | 2.30±0.2 ab |
| PGPRs-4N | UREA+DAP | 60.00±1.5 bc | 23.70±0.6 ab | 2.20±0.2 abc | 2.40±0.5 ab |
| BIO-QPGPRs | UREA | 51.50±1.0 de | 27.00±1.0 a | 2.10±0.5 abc | 2.20±0.8 ab |
| BIO-QPGPRs | DAP | 62.50±1.0 bc | 23.00±1.0 b | 2.50±0.4 ab | 1.70±0.6 ab |
| BIO-QPGPRs | UREA+DAP | 57.50±1.5 cd | 22.30±3.2 bc | 2.10±0.0 abc | 1.30±0.6 b |
| CONTROL | UREA | 41.00±1.5 f | 18.70±0.6 cd | 1.50±0.1 f | 1.30±0.1 b |
| CONTROL | DAP | 45.00±2.9 f | 16.70±1.5 d | 1.50±0.2 ef | 1.20±0.3 b |
| CONTROL | UREA+DAP | 47.30±3.0 ef | 20.30±1.2 bcd | 1.40±0.2 f | 1.60±0.1 ab |
| P (Bioformulado) | <0.0001 | <0.0001 | <0.0001 | 0.0032 | |
| P (Fertilizante) | 0.1733 | 0.0008 | 0.2943 | 0.2836 | |
| P (Interacción) | <0.0001 | 0.0049 | 0.2045 | 0.0751 | |
Los valores con letras similares no presentan diferencias estadísticas significativas al nivel de (P ≤ 0.05) por el procedimiento de comparación múltiple de Tukey. Los valores de desviación estándar ± corresponden a n = 9.
Values with similar letters do not present significant statistical differences at the level of (P ≤ 0.05) by Tukey's multiple comparison procedure. Standard deviation ± values correspond to n = 9.
Esto demuestra que los bioformulados de rizobacterias influyen en la eficiencia del fertilizante por su capacidad solubilizadora de nutrientes, mejorando sus características morfológicas en las plantas de arroz, lo cual coincide con los resultados de Hernández-Montiel et al. (2018) quienes mostraron que la aplicación de Pseudomonas putida aumentó la biomasa fresca de planta de arroz. De manera similar Palmero et al. (2020), observaron un crecimiento combinando de plantas mediante la inoculación de bacterias con la fertilización con P y K en un sustrato estéril. Se ha demostrado que las bacterias del género Pseudomonas sp. poseen la propiedad de producir diferentes sustancias que estimulan la germinación de las semillas, aceleran el crecimiento de las plantas especialmente en sus primeros estadios, inducen la iniciación radicular e incrementan la formación de raíces y la producción de exudados radiculares (Kandaswamy, Ramasamy, Palanivel y Balasundaram, 2019; Macías-Holguín et al., 2023).
Las principales sustancias estimuladoras producidas son de tipo hormonal como auxinas, giberelinas y citoquininas, pero también producen sustancias de otro tipo como aminoácidos y promotores específicos del crecimiento (Barboza-Garcia, Pérez y Chamorro, 2023). De igual manera las rizobacterias tienen la habilidad para facilitar la asimilación de nutrimentos mediante la solubilización de fósforo (Paredes-Mendoza, Espinosa y Zavaleta, 2021), fijación biológica de nitrógeno atmosférico (Blanco y Castro, 2021) y quelatización de iones (Mora-Quilismal et al., 2021).
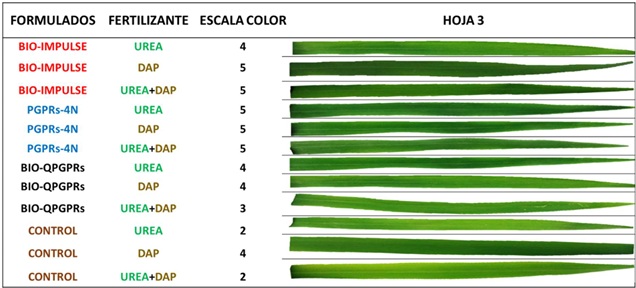
Los valores colorimétricos de la tabla LCC evidenciaron diferencias visuales dentro de cada tratamiento con sus respectivas interacciones (Figura 2). Las aplicaciones de PGPRs-4N con UREA, DAP, UREA + DAP y BIO-IMPULSE DAP y UREA+DAP mostraron mayor intensidad de color (5). Esto coincide con Melati, Sugiyanta y Evarist (2020) que demostraron que la aplicación de rizobacterias en la fertilización química (NPK + Urea) aumentó la escala de color en comparación al tratamiento sin aplicación. Esto evidencia una mayor eficiencia de fertilizante en el área foliar, además de la adaptabilidad de estos formulados en los suelos para cumplir sus actividades de solubilización en el suelo.
Conclusiones
La mayoría de rizobacterias tienen la capacidad de sintetizar fitohormonas de origen auxínico y solubilizar fósforo (P) y potasio (K) insoluble, sobresaliendo las cepas Enterobacter asburiae BA4-19, P. protegens CHA0, S. marcescens PM3-8 y A. calcoaceticus BM2-12 respectivamente. La bacteria Pseudomonas protegens CHA0 aceleró el proceso de germinación de arroz a partir del día 5, así mismo por efecto de las rizobacterias incrementó la longitud de radícula con un promedio 9.5 cm, por lo cual la inoculación con la misma resulta eficiente para mejorar la germinación del cultivo. La aplicación de BIO-IMPULSE de rizobacterias con fertilizante inorgánicos UREA y DAP se evidenciaron una mejoría en las características morfológicas e incrementaron la tonalidad foliar del cultivo de arroz.