Introducción
En el 2018, México cultivó 17 961 ha de pepino con una producción de 817 800 toneladas, sus principales estados productores fueron Sinaloa, Michoacán y Sonora aportando el 27, 21 y 8% respectivamente, contribuyendo con el 52% de la superficie cosechada a nivel nacional. Baja California se encuentra en el séptimo lugar con una producción de 43 397 toneladas, participando con el 4% (SIAP, 2020).
Alrededor del 7% de la superficie terrestre es afectada por un incremento anual de 1 al 2% en la concentración de sales (Munns y Tester, 2008; Plaut, Edelstein y Ben, 2013; Rizwan et al., 2015). El estrés salino afecta las plantas al aumentar el estrés osmótico y toxicidad iónica (Parvaiz y Satyawati, 2008; Horie, Karahara y Katsuhara, 2012). Así mismo, altas concentraciones de iones tóxicos como Na+ y Cl- afectan los procesos fisiológicos y enzimáticos, forman un desequilibrio iónico en la célula de la planta ocasionando alteraciones en el metabolismo y disminuyendo la absorción de iones esenciales como K+ y Ca2+ (Hajiboland, Aliasgharzadeh, Laiegh y Poschenrieder, 2010).
La fotosíntesis es uno de los procesos esenciales en plantas que mayormente se deteriora por la salinidad. Lo anterior se debe a que afecta la apertura y cierre de las estomas y por tanto provoca una disminución en la concentración de CO2 intercelular (Mehta, Kraslavsky, Bharti, Allakhverdiev y Jajoo, 2010, Ashraf y Harris 2013, Gupta y Huang 2014). Al mismo tiempo reduce los pigmentos verdes y el área foliar reduciendo el crecimiento (Brugnoli y Lauteri 1991, Gong, Zhu, Chen, Wang y Zhang 2005). Así mismo, una respuesta inmediata de la planta cuando está expuesta a elevadas concentraciones de salinidad es el cierre estomático (Tang, Mu, Shao, Wang, y Brestic, 2015; Reyes-Pérez et al., 2024). El cierre estomático implica una reducción de la fijación de CO2, y bajo condiciones de fluorescencia puede producir sobreexcitación de los centros de reacción del fotosistema II (PSII) (Ahmed, Rouina, Sensoy, Boukhris y Abdallah, 2009; Ashraf y Harris, 2013).
El Si es el segundo elemento mineral más abundante en el suelo después del oxígeno forma el 31% de la corteza terrestre (Gong, Randall y Flowers, 2006). En la solución del suelo se encuentra en forma de ácido monosilícico (H4SiO4) en concentraciones que van 0.1 a 0.6 mM (Epstein, 2009). El H4SiO4 es absorbido por las plantas y se transporta en la planta a través de xilema (Epstein, 1999; Tamai y Ma 2003). Posteriormente se deposita en la pared celular como sílice amorfa (SiO2.nH2O) interactuando con pectinas y calcio mejorando su rigidez y resistencia (Ma, 2004; Ma y Yamaji, 2008). El Si mitiga el estrés en plantas causado por un incremento de Na+ en el extracto de saturación del suelo o en la solución nutritiva (Ashraf et al., 2010; Rahimi, Mohammakhani, Roohi y Armand 2012; Ouzounidou, Giannakoula, Ilias y Zamanidis, 2016).
Los suelos salinos se caracterizan por presentar altas concentraciones de sales solubles como cloruro de sodio (NaCl), sulfato de sodio (Na2SO4), cloruro de magnesio (MgCl2), sulfato de magnesio (MgSO4), cuando la conductividad eléctrica (CE) es igual o mayor a 4 dS m-1 lo cual es equivalente a 40 mM NaCl (Munns, 2005), lo cual que genera una presión osmótica de 0.2 MPa (Munns y Tester, 2008). Se ha reportado tolerancia a la salinidad mediante la fertilización con Si en algunos cultivos como el arroz (Oryza sativa), trigo (Triticum durum), tomate (Solanum lycopersicum) y cebada (Hordeum vulgare). Hattori et al. (2005) encontraron una mayor tasa fotosintética, transpiración, conductancia estomática, mayor tamaño de estomas al adicionar Si en plantas de sorgo (Sorghum bicolor L.) cultivadas bajo condiciones de estrés salino. Resultados similares se encontraron en cultivares de maíz (Zea mays) (Parveen y Ashraf, 2010) y en plantas de okra (Albemoschus esculentus) (Abbas et al., 2015).
El efecto negativo de la salinidad en cultivos hidropónicos dependerá del tipo de sales utilizadas. Adams (1991) encontró que el aumento de la salinidad utilizando una alta concentración de macronutrientes en solución (en comparación con el cloruro de sodio [NaCl]), aumentó la acidez del jugo de tomate. En contraste, el crecimiento vegetativo de la planta se vio afectado negativamente, así como el tamaño, peso seco y contenido de azúcar en frutos. Algunos informes describen el efecto de la salinidad del NaCl y el efecto de mejora del Si (Zhu, Wei, Li, Qian y Yu, 2004; Wang et al., 2015). Sin embargo, los estudios que utilizan macronutrientes para incrementar el estrés por salinidad y Si como remediación en plantas de pepino son escasos. El objetivo de este estudio fue determinar el efecto del Si sobre el rendimiento, crecimiento y fisiología del pepino cultivado bajo condiciones de alta salinidad utilizando macronutrientes.
Materiales y Métodos
Lugar del experimento
El estudio se realizó en un invernadero ubicado en el área experimental del Instituto de Ciencias Agrícolas de la Universidad Autónoma de Baja California, México (32° 24’ N y 115° 11’ O) durante la temporada de invierno-primavera de 2018. Se utilizaron dos cultivares de pepino de polinización abierta Beit Alpha los cuales se sembraron el 25 de enero de 2017 utilizando bandejas de poliestireno. La fecha de trasplante fue el 16 de febrero, colocando dos plantas por maceta de 9.0 L. Se utilizó arena como sustrato y se aplicó solución nutritiva a través de un sistema de riego presurizado (López-Cuén et al., 2020). La solución nutritiva se aplicó a una concentración de nutrientes de 224 N, 47 P, 281 K, 212 Ca, 65 Mg, 0.2 Fe, 0.55 Mn, 0.33 Zn, 0.05 Cu, 0.28 B y 0.05 Mo mg L-1 (Gómez-Hernández y Sánchez, 2003).
Diseño experimental y tratamientos
Se realizó el experimento utilizando un diseño con parcelas divididas distribuidas completamente al azar. El primer factor (parcela principal) fue la aplicación diaria de tres dosis de Si (0, 4, 8 g L-1 de SiO2; Diatomix, Bio Agrinor®, Zapopan, Jalisco México); mientras que el segundo factor (subparcela) fue dos cultivares de pepino (“GVS” y “Alpha Garden”; Golden Valley Seeds, Irvine CA, U.S.A.) con tres repeticiones. Las dosis de Si se aplicaron diariamente a las macetas en forma manual a las 12:00 del mediodía. La parcela principal constó de 12 plantas y la subparcela de seis. La aplicación de Si se inició tres semanas después de que se trasplantaran las plántulas de pepino.
Manejo del cultivo
Las plantas de pepino fueron tutoradas de forma vertical para mantener erguida la parte área de las plantas a lo largo del ciclo del cultivo (Mendoza-Pérez et al., 2018). Los brotes secundarios se podaron para guiar el tallo principal (Hao, Wen, Papadopoulos y Khosla, 2010). El manejo del riego se llevó a cabo considerando la cantidad de drenaje ajustada al 30%. Los valores de pH de la solución nutritiva estuvieron entre 5,5 y 6,0. En relación con el manejo de plagas y enfermedades se controlaron mediante la aplicación de insecticidas habitualmente usados a dosis del 50% de las recomendadas por los fabricantes.
Durante el estudio, y en el transcurso de las 10:00 y 14:00 horas del día, se realizó mojado del piso con el objetivo de incrementar la humedad relativa dentro del invernadero. La temperatura y humedad relativa dentro del invernadero fueron monitoreadas usando un termo-higrómetro digital CEM DT-172 (Twin Light Instruments, Monterrey, México). El rango de humedad relativa fue de 26 al 48%, mientras la temperatura de 30 a 38 °C. El termo-higrómetro se instaló a 30 cm sobre la parte superior de las plantas en la hilera central del invernadero.
Variables de respuesta
A los 21 días después de trasplante (ddt), se evaluó la respuesta fisiológica de la planta a la adición de Si, utilizando una salinidad de 2.5 dS m-1 en la solución nutritiva. Posteriormente, a los 35 ddt la concentración de la solución nutritiva aumentó gradualmente la concentración de macronutrientes hasta alcanzar los 4.5 dS m-1, y 15 días después (60 ddt), se midió de nuevo la respuesta fisiológica de la planta. Las variables de respuesta fisiológica fueron la eficiencia fotoquímica máxima del PSII (Fv/Fm), fluorescencia mínima (Fo) y la conductancia estomática (gs). Adicionalmente, durante el tiempo que duró el estudio, se midió el crecimiento y rendimiento de fruta.
Fv/Fm, Fo
Se determinó la eficiencia fotosintética con un fluorómetro portátil Chlorophyll Fluorometer OS-30p (OPTI-SCIENCE, USA) usando una intensidad de luz actínica de 2100 µmol fotón m-2 s-1 de intensidad por un periodo de 2 s. Las mediciones se realizaron durante el transcurso del día sobre tres plantas por tratamiento, utilizando la cuarta o quinta hoja del ápice hacia abajo. Previo a la determinación, las hojas fueron aclimatadas por 30 min de oscuridad con pinzas de exclusión de luz para asegurar que todos los centros de reacción estuvieran abiertos (González, Perales y Salcedo, 2008).
Conductancia estomática (gs)
Se determinó con un porómetro de hoja modelo SC-1 Decagon Devices, Inc. (SC-1 Leaf Porometer®, Pullman WA, USA). Las mediciones se realizaron en tres plantas por tratamiento utilizando la cuarta o quinta hoja del ápice hacia abajo.
Crecimiento y rendimiento
La altura de la planta y el número de hojas se midió con una cinta flexible en tres plantas por tratamiento a partir de los 43 días después del trasplante (ddt). El número de hojas en la planta fue contabilizada una vez por semana en tres plantas por parcela. La cosecha de frutos se inició a los 48 ddt. Se realizaron un total de cinco cosechas y se midió el número de frutos por área (m2), el peso individual de las frutas y el rendimiento en peso fresco (g).
Análisis estadístico
A los datos obtenidos se les realizó una prueba de normalidad utilizando la prueba de Shapiro-Wilk. A los grupos de medias que resultaron con valores de P < 0.05, se les realizó transformación correspondiente antes de realizar su análisis de varianza. Sin embargo, para una mayor claridad de discusión, los valores se presentan sin transformación en las Figuras y Cuadros. A cada variable se les realizó un análisis de varianza con Minitab 17 (Minitab, 2017). La diferencia de medias fue realizada mediante la prueba de Tukey (P < 0.05).
Resultados y Discusión
Eficiencia fotosintética (Fv/Fm)
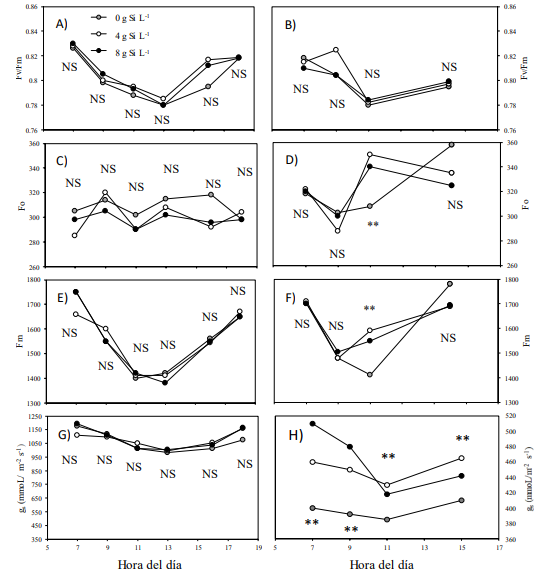
Al medir las variables fisiológicas, no se observó respuesta interactiva a la aplicación de Si y los cultivares de pepino (S × C), (P > 0.05). La Figura 1A muestra la eficiencia fotosintética (Fv/Fm) ocurrida durante el día en pepino por efecto de las tres dosis de silicio a una salinidad de 2.5 dS m-1. No se encontró diferencia significativa entre los tratamientos de silicio (P > 0.05). En general, conforme transcurrió el día, la Fv/Fm decreció de 0.83 a 0.78. Después de las 13:00 horas, se incrementó hasta alcanzar valores de 0.82. Este patrón de comportamiento de la Fv/Fm durante el día, ha sido documentada previamente y es el resultado de un incremento la tasa de flujo fotosintético que reciben las hojas al medio día incluso bajo distintas latitudes (Ayari, Dorais y Gosselin, 2000; Hastings, Oechel y Muhlia, 2005; Chen, Wang, Yin y Deng, 2018).
Cuando la salinidad se elevó a 4.5 dS m-1 (Figura 1B), los valores de la Fv/Fm fueron altos por la mañana (0.82) y bajos al medio día (0.78). Sin embargo, por la tarde no se logró la recuperación completa de la misma alcanzando valores de 0.80. Lo anterior pudo haber ocurrido por el daño sufrido durante el mediodía en el aparato fotosintético por el efecto de la salinidad (Hasan, Ohnuki, Kawasaki, Taniguchi y Miyake, 2005). El daño en el aparato fotosintético es el resultado de una degradación de la clorofila o una drástica y reducida velocidad de transferencia de electrones dentro de los tejidos fotosintéticos (Cao, Ma, Zhao, Wang y Xu, 2015).
Fluorescencia mínima (Fo)
La fluorescencia mínima de la clorofila (Fo) es el resultado de la aplicación de una cuota mínima de luz (˂ 0.1 μmol de fotones m-2 s-1) a un tejido foliar adaptado a la oscuridad. En este momento, los valores son obtenidos bajo un estado de oxidación de los centros de reacción del aparato fotosintético (Stirbet y Govindjee, 2011). Bajo condiciones de baja salinidad (Figura 1E), no se encontró efecto por las dosis de Si aplicada (P ˂ 0.05) y los valores de la Fo permanecieron relativamente estables durante todo el día (≈300). Sin embargo, cuando se incrementó la salinidad (Figura 1F) y a las 11:00 h del día se cuantificó el valor de la Fo, la aplicación de Si presentó los valores más altos que el testigo sin aplicar. Al finalizar el día, los valores de los tres tratamientos aumentaron y resultaron relativamente iguales.
Las diferencias entre los valores de la Fo han sido previamente documentadas. Al respecto, Hosseini et al. (2023) realizó una investigación incrementando los niveles de salinidad con NaCl en plantas de menta (Mentha spicata) e indicaron que los valores de Fo aumentan conforme se incrementa el nivel de salinidad. En el presente estudio, al parecer eso fue lo que ocurrió cuando se utilizó Si al medio día. Por el contrario, Pfündel, Latpuche, Mesiter y Cerovic (2018) encontraron una reducción de los valores de la Fo en plantas de Arabidopsis thaliana L. Estos autores indicaron que la reducción de valores fue el resultado del tipo de luz (azul) empleado en la cuota mínima utilizada para obtener la Fo. Señalan, que los valores obtenidos en la Fo son el resultado de la participación del fotosistema II (PS II), pero también de la participación del fotosistema I (PS I).
Conductancia estomática (gs)
Bajo condiciones de baja salinidad (2.5 dS m-1), (Figura 1E), no se identificó respuesta significativa (P ˃ 0.05) en la conductancia estomática (gs) a los tratamientos evaluados con Si. Por otro lado, bajo condiciones de alta salinidad (4.5 dS m-1) (Figura 1F) la conductancia estomática se redujo notablemente. Sin embargo, la aplicación de Si incrementó significativamente los valores de gs en comparación al tratamiento testigo (P ˂ 0.01). Durante la mañana y al medio día, el tratamiento sin Si mostró valores de gs por debajo de los 400 mmoL m-2 s-1, mientras que los tratamientos con Si, tuvieron valores por encima de los 420 mmoL m-2 s-1. Por la tarde, el tratamiento sin Si, mostró valores de 410 mmoL m-2 s-1, mientras que los tratamientos con Si, alcanzaron los 442 mmoL m-2 s-1, y valores superiores.
En el presente estudio, el estrés salino impuesto a las plantas de pepino fue llevado a cabo por el incremento de macroelementos en la solución nutritiva y no por la adición de Na+ como en otros estudios (Zhu et al., 2004; Ruiz-Espinoza, Villalpando, Murillo, Beltrán y Hernández, 2014; Ouzounidou et al., 2016). Lo anterior hace inferencia a la mínima o nula respuesta en la eficiencia fotosintética de las plantas (Fv/Fm, Fo) encontrada por la adición de Si. Sin embargo, para el caso de los resultados obtenidos en la variable de la conductancia estomática, los resultados encontrados concuerdan con estudios realizados en otros cultivos como tomate (Al-aghabary, Zhu y Shi, 2005), caña de azúcar (Saccharum officinarum L.) (Ashraf et al., 2010) algodón (Gossypium hirsutum L.) y frijol (Phaseolus vulgaris L.) (Brugnoli y Lauteri, 1991) señalando la importancia de la aplicación de Si sobre el beneficio de esta variable fisiológica.
Crecimiento de las plantas
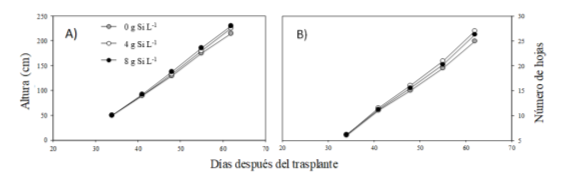
La Figura 2 muestra el crecimiento de las plantas expresado como altura (A) y número de hojas (B) por el efecto de las dosis de Si. No se encontró efecto interactivo ni respuesta significativa en ninguna de estas dos variables evaluadas (S × C), (P ˃ 0.05). Al final del experimento (62 ddt), las plantas tratadas con Si, alcanzaron una altura de 225 cm y un numero de 25 hojas. Tampoco se identificó una diferencia entre los cultivares evaluados (P > 0.05), (Dato no mostrado).
Rendimiento de fruta
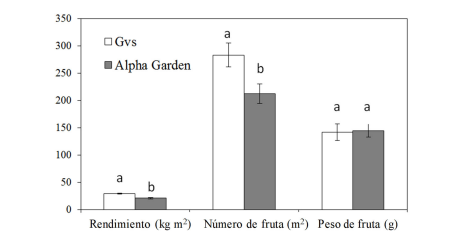
El Cuadro 1, muestra el rendimiento y numero de frutas obtenido en cinco cosechas de pepino. No se encontró una respuesta significativa a la aplicación de Si, ni a la interacción entre cultivares (S × C), (P ˃ 0.05). Durante las cinco cosechas, el cultivar GVS superó significativamente en rendimiento y número de frutas al cultivar Alpha Garden (P < 0.05). El peso de las frutas no resultó diferente entre los cultivares (P > 0.05), (148 g fruta-1). Al final de este estudio, el rendimiento total estuvo de 29.42 y 20.83 kg m2, y el número de frutas fue de 283 y 212 frutas m2, para los cultivares GVS y Alpha Garden respectivamente (Figura 3).
Cuadro 1: Rendimiento y número de frutas en dos cultivares de pepino cultivado bajo tres dosis de silicio.
Table 1: Yield and number of fruits on two cucumber cultivars growing under three Si rates.
| Tratamientos | Rendimiento (kg m2) | ||||
| Dosis Si (S)† | 1er cosecha | 2da cosecha | 3ra cosecha | 4ta cosecha | 5ta cosecha |
| 0 | 1.36 (± 0.35) | 3.69 (± 0.25) | 5.41 (± 0.41) | 7.79 (± 0.25) | 10.47 (± 0.35) |
| 4 | 1.39 (± 0.28) | 3.71 (± 0.29) | 5.66 (± 0.24) | 7.49 (± 0.19) | 10.69 (± 0.25) |
| 8 | 1.41 (± 0.31) | 3.75 (± 0.38) | 5.56 (± 0.28) | 7.56 (± 0.24) | 10.80 (± 0.26) |
| Significancia | 0.538 | 0.406 | 0.611 | 0.136 | 0.552 |
| Cultivares (C) | |||||
| GVS | 1.38 (± 0.15) | 3.79 (± 0.35) | 5.79 (± 0.55) | 7.65 (± 0.23) | 10.79 (± 0.15) |
| Alpha Garden | 0.87 (± 0.11) | 1.65 (± 0.17) | 3.61 (± 0.25) | 5.85 (± 0.19) | 8.83 (± 0.27) |
| Significancia | 0.044 | 0.031 | 0.023 | 0.041 | 0.047 |
| Interacción S × C | |||||
| Significancia | 0.581 | 0.321 | 0.416 | 0.754 | 0.185 |
| Número de frutos (Frutos m2) | |||||
| Dosis Si (S) | 1er cosecha | 2da cosecha | 3ra cosecha | 4ta cosecha | 5ta cosecha |
| 0 | 18 (± 4.29) | 28 (± 4.21) | 31 (± 6.35) | 37 (± 5.95) | 46 (± 5.14) |
| 4 | 26 (± 8.18) | 15 (± 5.19) | 49 (± 3.52) | 39 (± 4.89) | 39 (± 6.84) |
| 8 | 18 (± 4.15) | 16 (± 5.25) | 44 (± 6.16) | 45 (± 5.16) | 44 (± 8.02) |
| Significancia | 0.463 | 0.069 | 0.116 | 0.051 | 0.082 |
| Cultivares (C) | |||||
| GVS | 37 (± 9.15) | 35 (± 6.98) | 68 (± 8.15) | 70 (± 9.14) | 73 (± 9.49) |
| Alpha Garden | 25 (± 10.51) | 24 (± 5.19) | 56 (± 6.18) | 51 (± 10.24) | 56 (± 11.25) |
| Significancia | 0.104 | 0.069 | 0.116 | 0.051 | 0.082 |
| Interacción S × C | |||||
| Significancia | 0.263 | 0.149 | 0.229 | 0.117 | 0.191 |
† Dosis de silicio expresadas en g L-1.
† Silicon rates are expressed as g L-1.
De forma general, los resultados encontrados en este estudio indicaron que el factor de trabajo fotosintético de las plantas de pepino sometidas a salinidad por la adición de macronutrientes no fue un factor relevante en el funcionamiento de éstas. Por otro lado, la salinidad redujo el intercambio de gases al afectar la conductancia estomática, lo que en consecuencia provocó un malfuncionamiento de las estomas durante las condiciones de estrés (Hetherington y Woodward, 2003).
Debido a que el crecimiento de la planta, el rendimiento y número de frutas, así como las variables de eficiencia fotosintética no se modificaron por la adición de Si, es necesario realizar más estudios para clarificar el efecto benéfico de este mineral en pepino cultivado bajo condiciones de estrés salino provocado por un incremento de macronutrientes en la solución nutritiva. Al respecto una investigación debería ser realizada para comparar la salinidad inducida por incrementar los macronutrientes versus salinidad incrementada por la adición de Na (NaCl).
Conclusiones
Bajo las condiciones en que se realizó este estudio, la aplicación de Si no afectó las variables de eficiencia fotosintética, el crecimiento y el rendimiento en el cultivo de pepino. Cuando se incrementó la salinidad por la adición de macronutrientes a la solución nutritiva, la conductancia estomática se redujo considerablemente, sin embargo, se benefició por la adición de Silicio.
Contribución de los Autores
Conceptualización: F.N.R. y P.I.L.C. Metodología: J.R.R.I. Validación: R.E.V.G. y B.Y.S.G. Análisis formal: F.N.R. y P.I.L.C. Investigación: F.N.R. y P.I.L.C. Escritura, preparación del borrador original: P.I.L.C. Escritura: revisión y edición: F.N.R. y J.R.R.I. Visualización: M.A.P.A.