Introducción
A pesar de décadas de extensa investigación, la enterocolitis necrosante (ECN) persiste como una causa importante de mortalidad y morbilidad entre los recién nacidos pretérmino (RNPT).1-3 La gravedad de esta condición está relacionada inversamente con el peso al nacer y la edad gestacional.1 Estos prematuros enfrentan no sólo desafíos inmediatos como la dependencia prolongada de la nutrición parenteral (NPT) o la necesidad de cirugía, sino también la amenaza de alteraciones en su crecimiento y posible deterioro en su neurodesarrollo.1,4-6
Durante el tercer trimestre de gestación, el crecimiento ponderal fetal aumenta aproximadamente de 500 a 3,500 g.7 En los RNPT sin comorbilidades, es posible replicar estas tasas de crecimiento cuando la nutrición no se limita.7 Lamentablemente, cuando el neonato es un recién nacido pretérmino de muy bajo peso (RNMBP), a menudo este crecimiento se ve afectado con desviaciones por debajo de las curvas de crecimiento esperadas.2-7 Numerosos estudios lo atribuyen, entre otras cosas, a la alta frecuencia de comorbilidades, tales como: la ECN y la hemorragia intraventricular de forma temprana, y más tardíamente por el desarrollo de displasia broncopulmonar y la retinopatía de la prematuridad.2,8
Con el fin de optimizar el crecimiento postnatal y el neurodesarrollo, durante la última década se han realizado numerosos cambios y avances en el concepto y la práctica de la alimentación enteral y parenteral de los RNMBP.2 De esta forma, cuando nace uno de estos pacientes se considera una emergencia nutricional y, por tanto, sujeto a un inicio temprano y balanceado de NPT. Con estas acciones, diversos estudios han mostrado que aumenta su supervivencia y se reduce la falla de crecimiento postnatal.9,10
Para vigilar el crecimiento de estos neonatos se debe evaluar de manera frecuente el peso, talla y perímetro cefálico, y contrastar los datos con Tablas de crecimiento específicas.7,9,11
En nuestra unidad de cuidados intensivos neonatales (UCIN) hemos implementado acciones como la nutrición temprana en todo RNMBP,12 haciendo énfasis en su recuperación nutricional. El objetivo de este estudio fue determinar el impacto de la ECN en el crecimiento ponderal intrahospitalario de los RNMBP.
Material y métodos
Estudio de pronóstico, con un diseño de caso-cohorte, retrospectivo. Para ser más precisos, se generaron dos cohortes anidadas, una de casos o pacientes que presentaron ECN y otra, control (cohorte), con RN que no desarrollaron esta complicación durante estancia en la UCIN.
Se incluyeron RNMBP, nacidos en nuestro hospital entre los años 2018 y 2023. La edad de gestación fue establecida por fecha de última menstruación materna. Los criterios de exclusión fueron: pacientes con malformaciones múltiples o síndromes genéticos, o quienes requirieron atención por un estado crítico en los primeros ocho días de vida, o con riesgo muy alto de fallecimiento y RN ≤ 24 semanas de edad gestacional (SEG). Por último, dado que fue la variable principal en estudio, se excluyeron también los neonatos con menos de 21 días de estancia intrahospitalaria (ya sea por traslado o alta a domicilio).
De los pacientes incluidos, se revisó el expediente clínico para obtener la información sobre sexo, edad gestacional al nacer, evolución del peso (a los tres, siete, 10, 14, 18, 21 días y, posteriormente, cada siete días de vida hasta su egreso), manejo nutricional (edad de inicio, tipo nutrición, parenteral y/o enteral, así como el alimento enteral recibido), otorgamiento de probióticos; momento de presentación (o ausencia) de ECN, así como su estadio de ECN (según criterios de Bell modificados),13 y evolución (quirúrgica y/o defunción).
El crecimiento ponderal se determinó basado en los pesos registrados en los expedientes de enfermería. Es conveniente señalar que el protocolo de vigilancia de todo RN en esta UCIN contempla la somatometría en los tiempos señalados. La medición del peso se realiza con el neonato desnudo mediante el uso de una báscula electrónica marca SCALE-TRONIX ® modelo 4002 con precisión de 0.05 g, calibrada cada tres meses. Las mediciones son realizadas diariamente en el turno matutino, por enfermeras capacitadas, con técnica estandarizada.
Análisis estadístico
En primer lugar, se construyó una curva de probabilidad de supervivencia (ausencia de ECN) de Kaplan y Meier, para determinar el comportamiento de los egresos de los pacientes incluidos.
Para comparar el crecimiento entre los dos grupos se obtuvo la diferencia ponderal entre los momentos de medición (ej. cambio tres a siete días), así como el crecimiento acumulado durante la estancia hospitalaria. Para cada momento se obtuvo el promedio de crecimiento (en gramos) con su intervalo de confianza al 95% (IC95%).
Las variables cuantitativas se resumieron en promedio y desviación estándar, o bien, como mediana con rangos intercuartílicos según su distribución. La comparación entre grupos fue mediante prueba t de Student para grupos independientes (distribución normal) o prueba U de Mann Whitney (sin distribución normal). Las variables cualitativas se resumieron en frecuencias simples y porcentajes, y la contrastación entre grupos fue con la prueba χ2 de máxima verosimilitud.
Finalmente, para determinar y ajustar el posible efecto de la exposición a un episodio de ECN sobre el crecimiento ponderal -contemplando como posibles confusores el peso al nacer, las SEG al nacimiento, los días de estancia y los días de ayuno por ECN-, se realizó una regresión lineal múltiple, considerando como variable dependiente el incremento acumulado (gramos) al egreso. Para la comparación se obtuvieron los coeficientes estandarizados de las betas.
Todas las pruebas estadísticas se realizaron con hipótesis de dos colas y con un nivel de alfa de 0.05. Para todos los análisis se utilizó el paquete estadístico SPSS®, versión 24.
Resultados
Durante el periodo de estudio, 199 RNMBP cumplieron con los criterios de inclusión; 63 (31.6%) de ellos presentaron ECN. No se registraron diferencias estadísticamente significativas respecto a la distribución por sexo entre los grupos (Tabla 1), a pesar de predominar el sexo femenino en el grupo con ECN. Como también se observa, la edad gestacional fue categorizada en tres, y hubo un poco mayor número de neonatos de 24 a 28 SEG con el antecedente de ECN. En relación con el peso al nacimiento, los neonatos con ECN tuvieron en promedio 90 g menos (p < 0.003).
Tabla 1: Comparación entre los neonatos con y sin enterocolitis necrosante (ECN).
| Variable | ECN N = 63 n (%) |
Sin ECN N = 136 n (%) |
Todos N = 199 n (%) |
|---|---|---|---|
| Sexo | |||
| Masculino | 28 (44.4) | 72 (52.9) | 100 (50.3) |
| Femenino | 35 (55.6) | 64 (47.1) | 99 (49.7) |
| SEG al nacimiento | |||
| 24-28 | 14 (22.2) | 20 (14.7) | 34 (17.1) |
| 29-31 | 30 (47.6) | 59 (43.4) | 89 (44.7) |
| 32-36 | 19 (30.2) | 57 (41.9) | 76 (38.2) |
| Peso al nacimiento (g), promedio ± DE | 1,165 ± 199 | 1,255 ± 198* | 1,226 ± 202 |
| Uso de probióticos‡ | |||
| No | 52 (82.5) | 55 (40.4)‡ | 107 (53.8) |
| Sí | 11 (17.5) | 81 (59.6) | 92 (46.2) |
| NPT | |||
| Si | 62 (98.4) | 134 (98.5) | 196 (98.5) |
| No | 1 (1.6) | 2 (1.5) | 3 (1.5) |
| Días de vida al inicio de la NPT, mediana [Q1-Q3] | 1 [1-1] | 1 [1-1] | 1 [1-1] |
| Días de vida al inicio del estímulo enteral, mediana [Q1-Q3] | 5 [2-7] | 4 [3-6] | 4 [3-6] |
| Alimento recibido | |||
| Lecha materna | 11 (17.5) | 25 (18.5) | 36 (18.2) |
| Fórmula infantil | 39 (61.9) | 80 (59.3) | 119 (60.1) |
| Ambas | 13 (20.6) | 30 (22.2) | 43 (21.7) |
| Día de vida al diagnóstico de ECN, mediana [mín/Q1/Q3/máx] | 12 [3/8/20/62] | ||
| Estadio ECN | |||
| IA | 28 (44.4) | ||
| IB | 12 (19.0) | ||
| IIA | 12 (19.0) | ||
| IIB | 7 (11.1) | ||
| IIIB | 4 (6.3) | ||
| Días de estancia,mediana [Q1-Q3] | 62 [44-80] | 44 [35-59]§ | 49 [39-69] |
| Defunciones | 2 (2.3) | 2 (1.4) | 4 (2.0) |
DE = desviación estándar. NPT = nutrición parenteral total. Q1 = cuartil 1. Q3 = cuartil 3. SEG = semanas de edad gestacional.
* Prueba t Student 2 colas p = 0.003.
‡ χ2 p < 0.001,
§ U de Mann Whitney p < 0.001.
En cuanto al manejo, se encontró que la administración de probióticos (Bifidobacterium lactis y Lactobacillus reuteri) fue más frecuente en los controles que en los casos con ECN (p < 0.001). Sobre la nutrición, prácticamente a todos los neonatos se les inició con NPT desde el primer día de vida (Tabla 1). Los días de uso de NPT en el grupo control en promedio fue de 14, en comparación a 20 en el grupo de ECN. El inicio de estímulo enteral fue semejante en los dos grupos, durante su primera semana de vida. A su vez, la alimentación con fórmula, sola o en combinación con leche materna, predominó en 81.8% de los neonatos en ambos grupos; la lactancia exclusiva fue en 18.2% del total de los neonatos.
En el grupo con ECN, el estadio IA fue el más frecuente, seguido del IB y IIA. Solo cuatro neonatos presentaron una forma grave (IIIB). La mediana de presentación se encontró a los doce días de vida, y prácticamente en 95% aconteció antes de los 28 días de vida; solo en un caso fue tardía, a los 62 días (Figura 1).
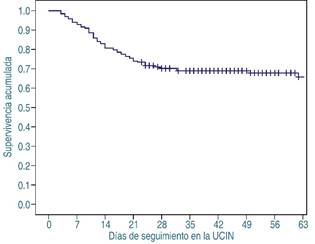
Figura 1: Curva de supervivencia a la presencia de enterocolitis necrosante en 199 neonatos ingresados en la Unidad de Cuidados Intensivos Neonatales (UCIN).
La estancia hospitalaria fue más prolongada entre los neonatos con ECN, con una diferencia de 18 días (p < 0.001). La mortalidad fue de 2%, y la proporción no fue diferente entre los grupos.
Crecimiento ponderal
La Figura 2 y la Tabla 2 muestran el análisis por momentos del crecimiento ponderal. En primer lugar, se observó mayor descenso del peso durante los tres primeros días de vida en el grupo control, contra una casi nula pérdida en el grupo que desarrolló ECN. A partir de este momento, el incremento ponderal por periodo fue, en promedio, entre 50 a 80 g hasta el día 18. Para el día 21, en ambos grupos se observó disminución del incremento ponderal, sin encontrarse diferencias significativas. Del periodo de 21 a 28 días, el grupo control presentó una recuperación de su crecimiento mayor al observado en el grupo con ECN (p < 0.01). A partir de ese tiempo, dado que varios neonatos fueron egresados, sólo se registró el cambio a los 35 y 50 días, siendo semejante entre los dos grupos.
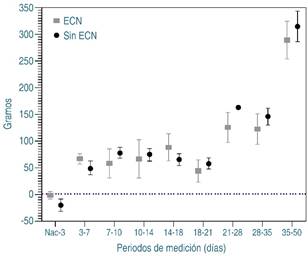
Figura 2: Incremento de peso en gramos entre dos mediciones (diferencia de peso) y sus intervalos de confianza al 95%, según presencia o no de enterocolitis necrosante (ECN).
Tabla 2: Crecimiento ponderal en gramos, por periodos de tiempo.
| Periodo (días) | Pacientes con ECN | Pacientes sin ECN | p | ||
|---|---|---|---|---|---|
| n | Promedio (IC95%) | n | Promedio (IC95%) | ||
| Nacimiento-3 | 3 | −1.67 (−4.9 - 1.6) | 196 | −19.9 (−30.8 - −9.1) | 0.002* |
| 3 a 7 | 14 | 66.4 (33.2 - 99.5) | 185 | 50 (37 - 63) | 0.500 |
| 7 a 10 | 23 | 58 (32.2 - 83.9) | 176 | 77.8 (67.2 - 88.3) | 0.210 |
| 10 a 14 | 38 | 66.2 (31.7 - 100.6) | 161 | 74.4 (62.8 - 88.8) | 0.580 |
| 14 a 18 | 45 | 88 (63.1 - 112.9) | 154 | 65 (53.2 - 76.8) | 0.070 |
| 18 a 21 | 52 | 44.1 (23.7 - 64.5) | 147 | 58.1 (47.7 - 68.5) | 0.200 |
| 21 a 28 | 56 | 124.8 (97.4 - 153.2) | 125 | 162.5 (146.8 - 178.2) | 0.010‡ |
| 28 a 35 | 56 | 122.1 (94.6 - 149.5) | 108 | 145.2 (137.5 - 152.8) | 0.110 |
| 35 a 50 | 45 | 287 (252.5 - 321.5) | 57 | 313.5 (286.0 - 340.9) | 0.250 |
ECN = enterocolitis necrosante. IC95% = intervalo de confianza de 95%.
Prueba t Student: * Varianzas no iguales,
‡ Varianzas iguales.
En el análisis acumulado, los incrementos fueron semejantes en ambos grupos (Tabla 3 y Figura 3), como se muestra en los dos grupos, el crecimiento ponderal promedio fue aproximadamente de 300 g a los 21 días, y de 500 g a los 50 días.
Tabla 3: Crecimiento ponderal acumulado, en gramos.
| Periodo (días) | Pacientes con ECN | Pacientes sin ECN | p | ||
|---|---|---|---|---|---|
| n | promedio (IC95%) | n | promedio (IC95%) | ||
| Nacimiento-3 | 3 | −1.67 (−4.9 - 1.6) | 196 | −19.9 (−30.8 - −9.1) | 0.002* |
| 3 a 7 | 14 | 42.1 (−14.7 - 98.9) | 185 | 30.6 (16.0 - 45.1) | 0.680 |
| 7 a 10 | 23 | 93.3 (42.9 - 143.7) | 176 | 108.7 (90.8 - 126.5) | 0.560 |
| 10 a 14 | 38 | 182.3 (131.3 - 233.0) | 161 | 179.2 (157.4 - 200.0) | 0.900 |
| 14 a 18 | 45 | 279.3 (224.0 – 334.1) | 154 | 241.1 (217.6 - 264.6) | 0.150 |
| 18 a 21 | 52 | 318.2 (260.3 - 376.0) | 147 | 299.3 (273.8 - 324.8) | 0.490 |
| 21 a 28 | 56 | 418.3 (373.2 - 463.0) | 125 | 452.0 (422.0 - 481.9) | 0.220 |
| 28 a 35 | 56 | 534.4 (482.0 - 586.7) | 108 | 573.8 (540.4 - 607.1) | 0.190 |
| 35 a 50 | 45 | 763.8 (704.0 - 823.2) | 57 | 812.0 (764.0 - 859.3) | 0.210 |
ECN = enterocolitis necrosante. IC95% = intervalo de confianza de 95%.
Prueba t de Student: * Varianzas no iguales.
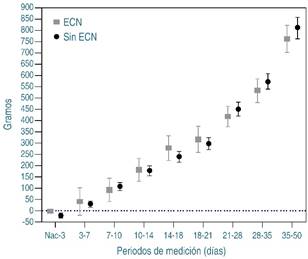
Figura 3: Incremento acumulado de peso en gramos entre mediciones y sus intervalos de confianza al 95%, según presencia o no de enterocolitis necrosante (ECN).
Finalmente, el análisis de regresión lineal múltiple evidenció que la presencia de ECN y la edad a la que se presentó no influyen sobre el crecimiento final en los RNMBP (Tabla 4). Mientras que, el peso al nacer (a mayor peso al nacimiento, incrementa la ganancia ponderal) y la edad gestacional al nacer (la mayor madurez, favorece el crecimiento) se asociaron con el mayor aumento de peso.
Tabla 4: Análisis de regresión lineal, para determinar la asociación de la presencia de enterocolitis necrosante (ECN) con el peso al egreso, ajustado por factores potencialmente confusores.
| Variables | Beta | IC95% | Beta estandarizada | t | p |
|---|---|---|---|---|---|
| Grupo de ECN* | −34.6 | −129.9 - 60.7 | −0.065 | −0.716 | 0.450 |
| Peso al nacimiento (g) | 0.7 | 0.49 - 0.91 | 0.518 | 6.72 | < 0.001 |
| Días de estancia | 5.6 | 4.1 - 7.1 | 0.563 | 7.39 | < 0.001 |
| SEG al nacimiento | 25.5 | 6.6 - 44.4 | 0.218 | 2.66 | 0.008 |
| Días a la presentación de ECN | −1.09 | −6.3 - 4.2 | −0.036 | −0.41 | 0.680 |
IC95% = intervalo de confianza de 95%. SEG = semanas de edad gestacional.
* Se consideró en escala ordinal: 0 = sin ECN, 1 = estadios I y II, 2 = estadio III.
Discusión
En estudios previos se ha mostrado que, en comparación a quienes no la desarrollan, los neonatos con ECN cursan con mayor número de complicaciones médico-quirúrgicas durante su estancia en una UCIN, así como una estancia más prolongada; estas condiciones parecen influir directamente sobre su crecimiento y neurodesarrollo a largo plazo.3 Sin embargo, pocos estudios han examinado el crecimiento durante la etapa neonatal y en condiciones de una atención crítica. Los datos de este estudio apoyan que el crecimiento ponderal no parece afectarse con la presentación de ECN en los RNMBP. El escaso impacto de la ECN sobre el crecimiento podría explicarse por los cambios en las recomendaciones para otorgar nutrición enteral y parenteral del RNPT en los últimos años, en los cuales se establecen los requerimientos nutricionales específicos para cada neonato, así como la manera de otorgar los macro y micronutrientes (vía enteral o parenteral), con el objetivo de mantener un balance energético que favorezca el crecimiento, considerando el incremento de las demandas por las comorbilidades.9,10,14-16
Una de las metas terapéuticas fundamentales en la UCIN es proporcionar nutrición que garantice el crecimiento más parecido al esperado en un ambiente intrauterino. Por ello, en la nuestra se implementó el inicio de la NPT en las primeras 24 horas de nacimiento en todo neonato crítico que no pueda recibir nutrición por vía oral o enteral.17 Como se mostró en los resultados, esta meta se alcanzó en 98% de los RNMBP.
En este estudio, el inicio de seguimiento de los pacientes fue a partir del tercer día de vida, ya que se espera una pérdida de peso en este periodo, ante la adaptación del tránsito de la vida intrauterina a la extrauterina. En neonatos sanos este momento suele relacionarse con la optimización de la nutrición postnatal temprana.7,8 Al respecto, se debe destacar que hubo menor pérdida de peso en los neonatos con ECN, lo cual posiblemente está relacionado con el mayor uso de medidas para prevención de pérdidas insensibles, como la capa de polietileno o la humedad de incubadoras, así como la prescripción de líquidos intravenosos más altos, en comparación al grupo sin ECN.
Como se mostró en los resultados, la velocidad de crecimiento fue semejante en el grupo con y sin ECN, hasta el día 21. Pero se debe considerar que, en ambos grupos, la velocidad fue menor a la esperada en neonatos de peso adecuado; lo anterior puede reflejar el mayor requerimiento calórico relacionado con el estado crítico de los RNMBP. Por otro lado, a pesar de numerosos estudios realizados, no se ha podido establecer cuáles Tablas de crecimiento, Intergrowth o Fenton, son ideales para llevar el seguimiento de estos neonatos, lo que sí se ha establecido es que es necesario el seguimiento somatométrico, a fin de identificar y atender tempranamente fallas en el crecimiento.2,8,9
En este trabajo, los datos de los pacientes fueron registrados meticulosamente para establecer cómo fue su crecimiento ponderal durante las tres primeras semanas de vida, ya que es en este periodo cuando es más frecuente la presentación de ECN en neonatos prematuros,18,19 y porque a esta edad la presencia de niveles elevados de citocinas inflamatorias, hipoxia y la sepsis asociada a la ECN pueden afectar de forma importante el cerebro inmaduro y favorecer un deterioro del neurodesarrollo en supervivientes de ECN.5,6 En revisiones sistemáticas se ha señalado que el riesgo de retraso en el neurodesarrollo a largo plazo es significativamente mayor en RNMBP con ECN ≥ II de Bell en comparación con aquellos sin ECN.5,20,21
Una observación para destacar es la mayor frecuencia de administración de probióticos en los RNMBP que no desarrollaron ECN. En un estudio previo llevado a cabo en este mismo hospital,22 se reportó que el uso de probióticos puede resultar benéfico para la prevención de ECN; sin embargo, hacen falta ensayos clínicos con esas cepas específicas, y la estandarización de protocolos para su administración.
Las fortalezas de este estudio son que el tamaño de muestra fue grande, así como un periodo de seguimiento suficiente para evaluar el crecimiento. También podemos considerar que la evaluación del peso de los prematuros fue cegada, ya que el personal de enfermería no distingue, para realizar esta medición, sí tienen o no comorbilidades (como la ECN); en caso de considerar que hubiera error en la medición, sería como un sesgo no diferencial. Así mismo, las pérdidas antes de los 21 días fueron mínimas (solo tres defunciones). Por el contrario, las principales limitaciones del estudio son su carácter observacional y retrospectivo; las dos cohortes se construyeron de acuerdo con el desenlace y, por tanto, los tiempos y pesos al momento de los eventos fueron diferentes. En los factores tiempo dependientes únicamente incluimos la edad a la presentación de la ECN y sólo ajustamos en factores basales (peso y edad gestacional).















