Introducción
Los aneurismas son dilataciones arteriales permanentes que comprometen a las tres capas de la pared vascular. Morfológicamente pueden ser fusiformes o saculares, dependiendo de si abarcan o no a la totalidad de la circunferencia arterial1. La aorta abdominal es susceptible a desarrollar aneurismas (aneurismas de aorta abdominal, AAA), principalmente del tipo fusiforme2. El AAA se define como un diámetro aórtico infrarrenal al menos 1.5 veces mayor que el diámetro normal esperado3. El manejo del AAA depende de su tamaño, los menores a 4 cm de diámetro se manejan conservadoramente, mientras que los mayores a 5.4 cm son reparados mediante una endoprótesis vascular, una reparación endovascular de aneurismas (EVAR), debido a su alto riesgo de ruptura4,5. La EVAR consiste en la implantación mediante fluoroscopia de injertos vasculares anclados con stents a las porciones no afectadas de la aorta6-8. Sin embargo, la EVAR puede complicarse con el desarrollo de una respuesta inflamatoria aguda sistémica (Tabla 1), caracterizada por fiebre elevada, elevación de reactantes de fase aguda y leucocitosis, conocida como síndrome postimplantación (SPI)9,10. EL SPI tiene una incidencia variable, del 11.2 al 60% de todas las EVAR, estimándose un promedio del 30 al 40% en ambos sexos11. Su etiología no es clara, aunque se han propuesto dos mecanismos fisiopatológicos principales: la manipulación del trombo en el AAA y la reacción inflamatoria desencadenada por el material protésico12. En el primer caso, la pérdida de la continuidad vascular activa al sistema simpático y la liberación de catecolaminas en la circulación, produciendo así los síntomas de fiebre y taquicardia. Asimismo, se secreta corticotropina, que induce la liberación de cortisol por la glándula suprarrenal, hormona de crecimiento y vasopresina13. Aunado a esto, el daño al tejido durante la cirugía libera citocinas proinflamatorias, como el factor de necrosis tumoral alfa (TNF-α), interleucina (IL) 6, IL-6 1β, IL-8, IL-12 e IL-18, que en conjunto desencadenan la leucocitosis, así como la elevación de los reactantes de fase aguda en el plasma del paciente14,15. De hecho, los niveles plasmáticos de IL-6 fungen como un indicador del daño tisular por isquemia-reperfusión o manipulación quirúrgica del trombo aneurismático16, por lo que sus concentraciones se correlacionan con la gravedad del SPI17,18. La segunda vía fisiopatológica indica la generación de reactividad inmunitaria a los materiales que conforman la endoprótesis vascular, siendo las elaboradas a base de dacrón las vinculados mayormente a este proceso reactivo en la generación del SPI (tasa de incidencia del 52.7 vs. 10.8%)19,20. Ensayos previamente realizados han indicado una incidencia del SPI menor (13.8 vs. 38.7%), con el uso de prótesis novedosas con sellado del aneurisma endovascular vs. endoprótesis estándar21. Adicionalmente, ensayos recientes concuerdan con esta tendencia, añadiendo un efecto benéfico mayor cuando se utilizan compuestos como el politetrafluoroetileno (PTFE) en lugar del dacrón (SPI 1.2 vs. 19.4%, respectivamente)22. El SPI debe ser evitado debido a su gran impacto en la salud del paciente, su incremento en los costos de atención, de la estancia hospitalaria y por el incremento del riesgo de eventos cardiacos mayores que conlleva18,23,24. No existen lineamientos universales en el tratamiento del SPI20, usualmente esta condición se trata mediante el uso agresivo de antinflamatorios orales25,26. Un ensayo clínico previo ha reportado éxito con la administración profiláctica de esteroides (tasa de SPI del 27 vs. 92%; p = 0.001) en comparación con el grupo control, aunque no se observaron beneficios adicionales tras 30 días de seguimiento27. Dado el uso cada vez más común de EVAR como tratamiento de los AAA, la identificación de factores de riesgo que permitan detectar a los pacientes más susceptibles a SPI es imperativo. Por ello se realizó un estudio con el fin de identificar la frecuencia del SPI y su asociación con factores de riesgo en pacientes sometidos a EVAR aórticos abdominales en la Unidad Médica de Alta Especialidad Hospital de Especialidades N.° 71.
Método
Estudio observacional, analítico y ambispectivo, realizado de acuerdo con los estatus de la guía STROBE para estudios observacionales. Se incluyeron pacientes sometidos a EVAR aórticos abdominales durante el periodo de julio de 2021 a enero de 2023 en el Servicio de Angiología, Cirugía Vascular y Endovascular del Instituto Mexicano del Seguro Social, Unidad Médica de Alta Especialidad, Hospital de Especialidades N.° 71, hospital de tercer nivel de atención en Torreón, Coahuila, México. Se incluyeron solo pacientes mayores de edad, de ambos sexos, que contaran con historial clínico completo, protocolo quirúrgico detallado y con modelo de procedimientos. Se excluyeron pacientes con antecedentes de autoinmunidad, consumo de esteroides crónicos (> 1 semana previo a la EVAR) y pacientes sometidos a EVAR en más de una ocasión. El tamaño muestral fue calculado en 50 sujetos con base en la fórmula de cálculo de proporción próxima, los cuales fueron seleccionados de forma no probabilística por casos consecutivos. Las variables primarias de interés fueron: sexo, edad, peso, índice de masa corporal, comórbidos, diámetro del AAA, tipo del AAA, así como tipo, duración y material de endoprótesis de la EVAR. Las variables de desenlace fueron: fiebre, leucocitosis, proteína C reactiva (PCR) y supervivencia. Todas las variables se obtuvieron de los expedientes clínicos de cada sujeto, se brindó seguimiento a corto (72 horas) y mediano plazo (un mes). Se utilizó estadística descriptiva en todas las variables, la distribución de los datos fue evaluada mediante la prueba de Komolgorov-Smirnov. Para el contraste de hipótesis se empleó la prueba de chi cuadrada, se calcularon los intervalos de confianza al 95% (IC95%). El nivel de significancia estadística mínimo que considerar en todas las pruebas fue de p < 0.05. Todos los cálculos estadísticos fueron ejecutados mediante el software IBM SPSS versión 25 para Windows. Este estudio fue aprobado por el Comité de Ética en Investigación de la Universidad Autónoma de Coahuila y el Instituto Mexicano del Seguro Social en la Unidad Médica de Alta Especialidad, Hospital de Especialidades N°71, con número de registro R-2021-501-079.
Resultados
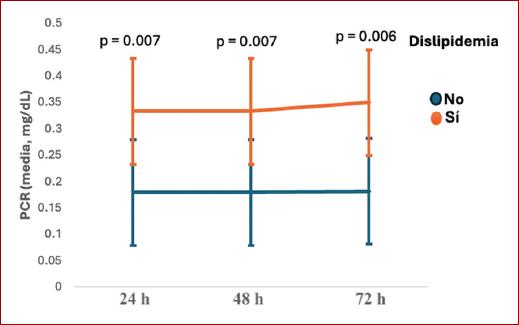
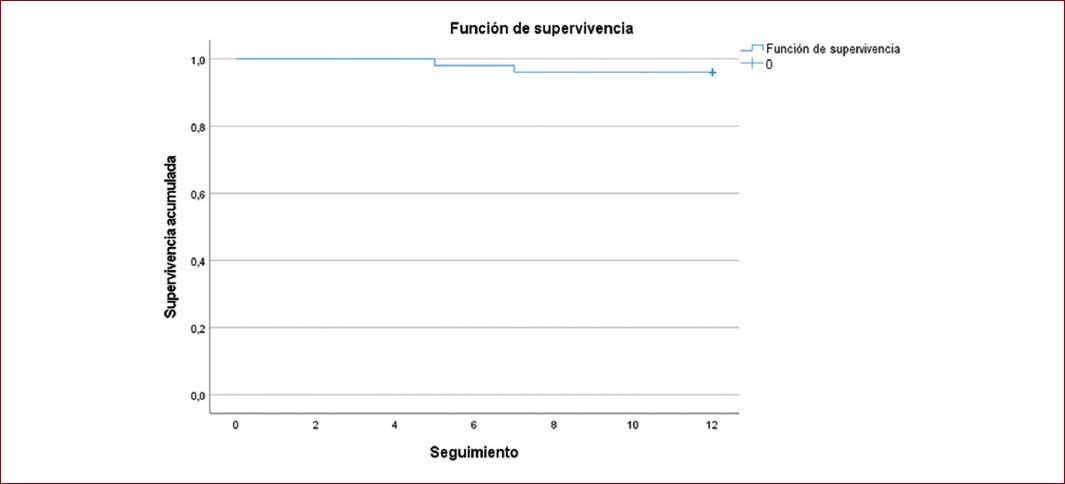
De los 50 pacientes incluidos, el 89.60% era del sexo masculino (n = 43/50), el resto eran mujeres, la edad promedio de los sujetos fue de 74 ± 8 años (rango: 61 a 90 años). Las características generales de los pacientes (somatometría, comorbilidades, caracterización del aneurisma) se resumen en la tabla 2. La comorbilidad más frecuente fue hipertensión arterial (75%, n = 36/50), seguida de diabetes (52.1%, n = 25/50). Con excepción de un caso (2.1%), el resto de los aneurismas fueron de tipo fusiforme; el diámetro medio de los aneurismas fue de 66.2 ± 17.5 mm (rango: 50-141 mm). Respecto a los EVAR, salvo un caso urgente (2.1%), los demás fueron electivos y tuvieron una duración promedio de 126 ± 16 min (rango: 100-170 min). El material de endoprótesis empleado fue dacrón en el 54.2% de los casos y PTFE en el restante 45.8%. Durante el seguimiento (Tabla 3), el 14.6% (n = 7/50) presentó fiebre en las primeras 24 horas, y en el caso de leucocitosis una misma proporción de pacientes la presentó, 14.6% (n = 7/50), aunque de forma continua, las primeras 48 horas y posteriormente descendió a solo el 12.5% (n = 6/50) en las próximas 72 horas. No hubo diferencia de medias de PCR a las 24, 48 ni 72 horas por tipo de material de endoprótesis. La media de PCR fue notablemente superior en los casos con SPI desde las 24 horas, a las 48 y 72 horas (Fig. 1), aunque fue muy similar por tipo de material de endoprótesis (Fig. 2). La media de PCR también fue mayor en aquellos pacientes con dislipidemia vs. los que no con contaban con tal historial, apreciándose la diferencia a las 24, 48 y 72 horas (Fig. 3). Un total de 7 casos (14.6%) presentaron el SPI, ocurriendo en similar proporción en ambos tipos de materiales de endoprótesis (15.4 vs. 13.6%; p = 0.864) y presentándose en todos los casos en las primeras 24 horas de seguimiento. En el seguimiento a largo plazo, el 95.8% (n = 46/50) permanecía con vida, en casi idéntica proporción al comparar por material de endoprótesis (96.2 vs. 95.5%; p = 0.904). Las dos muertes registradas ocurrieron en pacientes que no habían desarrollado SPI. La sobrevida global a 12 meses fue del 96% (n = 48/50), tal como se muestra en la figura 4, sin diferencia estadísticamente significativa entre quienes presentaron SPI y quienes no lo presentaron (prueba de Log Rank: 0.566). Se observó asociación de la dislipidemia con el desarrollo de SPI que incrementó 9.5 veces el riesgo (odds ratio [OR]: 9.500; IC95%: 1.416-63.724; p = 0.033).
Tabla 2 Características generales de los pacientes sometidos a EVAR, IMSS UMAE 71, 2021-2023
| Característica | Material de endoprótesis | Global, n = 48 | Valor de p | |
|---|---|---|---|---|
| Dacrón, n = 26 | PTFE, n = 22 | |||
| Edad (años) | 73 ± 8 | 74 ± 7 | 74 ± 8 | 0.704 |
| Sexo | 4 | 0.221 | ||
| Masculino | 22 (84.6%) | 21 (95.5%) | 3 (89.6%) | |
| Femenino | 4 (15.4%) | 1 (4.5%) | 5 (10.4%) | |
| Peso (kg) | 72.2 ± 7.5 | 77.0 ± 11.3 | 74.4 ± 9.6 | 0.087 |
| IMC (kg/m2) | 28 ± 3 | 30 ± 4 | 29 ± 4 | 0.140 |
| Comorbilidades | ||||
| Hipertensión arterial | 17 (65.4%) | 19 (86.4%) | 36 (75%) | 0.094 |
| Diabetes | 12 (46.2%) | 13 (59.1%) | 25 (52.1%) | 0.371 |
| Cáncer | 3 (11.5%) | 0 (0%) | 3 (6.3%) | 0.100 |
| Dislipidemias | 2 (7.7%) | 4 (18.2%) | 6 (12.5%) | 0.274 |
| Enfermedad coronaria | 2 (7.7%) | 7 (31.8%) | 9 (18.8%) | 0.033 |
| Insuficiencia cardiaca | 1 (3.8%) | 0 (0%) | 1 (2.1%) | 0.353 |
| Enfermedad renal crónica | 0 (0%) | 1 (4.5%) | 1 (2.1%) | 0.2.72 |
| Asma/EPOC | 1 (3.8%) | 0 (0%) | 1 (2.1%) | 0.353 |
| Enfermedad vascular cerebral | 0 (0%) | 1 (4.5%) | 1 (2.1%) | 0.272 |
| Tipo de aneurisma | ||||
| Sacular | 1 (3.8%) | 0 (0%) | 1 (2.1%) | 0.353 |
| Fusiforme | 25 (96.2%) | 22 (100%) 66.4 ± 15.5 | 47 (97.9%) 66.2 ± 17.5 | 0.943 |
| Diámetro del aneurisma (mm) | 66.0 ± 19.3 | |||
| Tipo de EVAR | ||||
| Electivo | 25 (96.2%) | 22 (100%) | 47 (97.9%) | 0.353 |
| Urgente | 1 (3.8%) | 0 (0%) | 1 (2.1%) | |
| Duración del EVAR (min) | 120 ± 16 | 133 ± 12 | 126 ± 16 | 0.006 |
EPOC: enfermedad pulmonar obstructiva crónica; EVAR: reparación endovascular de aneurismas; IMC: índice de masa corporal; IMSS: Instituto Mexicano del Seguro Social; PTFE: politetrafluoroetileno; UMAE: unidad médica de alta especialidad.
Tabla 3 Complicaciones observadas en las próximas 72 horas de seguimiento en pacientes sometidos a EVAR, IMSS UMAE 71, 2021-2023
| Característica | Material de endoprótesis | Global, (n = 48) | Valor de p | |
|---|---|---|---|---|
| Dacrón, (n = 26) | PTFE, (n = 22) | |||
| 24 horas | ||||
| Fiebre | 4 (15.4%) | 3 (13.6%) | 7 (14.6%) | 0.864 |
| Leucocitosis | 4 (15.4%) | 3 (13.6%) | 7 (14.6%) | 0.864 |
| PCR (mg/dl) | 0.200 ± 0.24 | 0.205 ± 0.25 | 0.202 ± 0.24 | 0.950 |
| Síndrome postimplantación | 4 (15.4%) | 3 (13.6%) | 7 (14.6%) | 0.864 |
| 48 horas | ||||
| Fiebre | 0 (0%) | 0 (0%) | 0 (0%) | N/A |
| Leucocitosis | 4 (15.4%) | 3 (13.6%) | 7 (14.6%) | 0.864 |
| PCR (mg/dl) | 0.200 ± 0.24 | 0.205 ± 0.25 | 0.202 ± 0.24 | 0.950 |
| Síndrome postimplantación | 0 (0%) | 0 (0%) | 0 (0%) | N/A |
| 72 horas | ||||
| Fiebre | 0 (0%) | 0 (0%) | 0 (0%) | N/A |
| Leucocitosis | 3 (11.5%) | 3 (13.6%) | 6 (12.5%) | 0.827 |
| PCR (mg/dl) | 0.204 ± 0.24 | 0.209 ± 0.26 | 0.206 ± 0.25 | 0.944 |
| Síndrome postimplantación | 0 (0%) | 0 (0%) | 0 (0%) | N/A |
| Sobrevida | 25 (96.2%) | 21 (95.5%) | 46 (95.8%) | 0.904 |
EVAR: reparación endovascular de aneurismas; N/A: no disponible; PCR: proteína C reactiva; IMSS: Instituto Mexicano del Seguro Social; PTFE: politetrafluoroetileno; UMAE: unidad médica de alta especialidad.
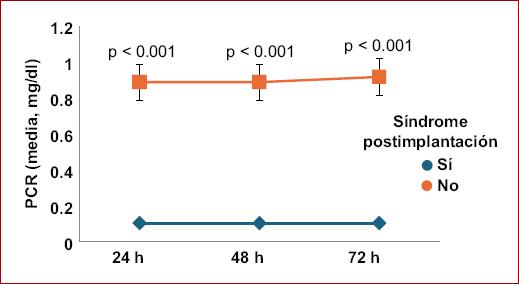
Figura 1 Diferencia de medias de PCR entre los pacientes sometidos a EVAR, IMSS UMAE 71, 2021-2023. EVAR: reparación endovascular de aneurismas; IMSS: Instituto Mexicano del Seguro Social; PCR: proteína C reactiva; UMAE: unidad médica de alta especialidad.
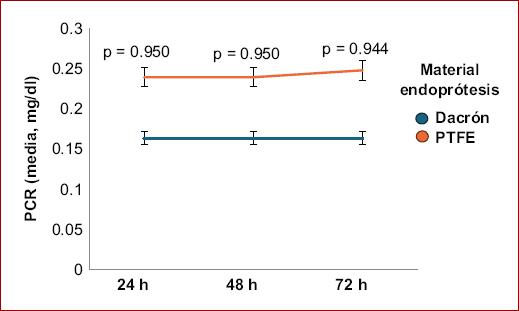
Figura 2 Diferencia de medias de PCR entre los pacientes sometidos a EVAR por material de endoprótesis, IMSS UMAE 71, 2021-2023. EVAR: reparación endovascular de aneurismas; PCR: proteína C reactiva; IMSS: Instituto Mexicano del Seguro Social; PTFE: politetrafluoroetileno; UMAE: unidad médica de alta especialidad.
Discusión
En la población analizada se identificó que el 14.6% (n = 7/50) de los sujetos desarrolló SPI y tuvieron una mortalidad a mediano plazo de solo el 4.2% (n = 2/50), esto fue similar a lo reportado en series de casos previos. Entre los estudios contra los cuales podemos efectuar comparaciones tenemos el de Hüsemann et al., quienes realizaron un estudio retrospectivo en Brasil comparando los desenlaces de pacientes con AAA sometidos a EVAR vs. reparación abierta del AAA con seguimientos de hasta 39 meses. En este estudio se identificó que la mortalidad general para la reparación abierta fue del 11.89 vs. el 7.69% en el caso de la EVAR (p = 0.263). Adicionalmente, los casos que presentaron complicaciones mayores fueron similares entre ambos grupos (24.83 vs. 25.27%; p = 0.35)28. Por otro lado, un estudio muy similar al nuestro fue el ejecutado por Sousa et al., quienes recolectaron prospectivamente 133 casos sometidos a EVAR, con un predominio casi absoluto de sujetos de sexo masculino (95.5%) y una edad media de 75.66 ± 7.13 años. En el estudio se identificó que un 11.4% de los pacientes desarrolló SPI. Durante el seguimiento ocurrieron dos defunciones, teniendo así una tasa de supervivencia del 86.5%. Asimismo, el presentar SPI no se asoció a un mayor riesgo de muerte, sin embargo, sí se reportó que el uso de injertos de poliéster aumentaba la frecuencia de SPI (p = 0.031)29. La disparidad de los resultados puede explicarse por los diferentes tipos de biomateriales, tal como lo señalan algunos investigadores, los cuales mencionan que el tipo de material puede provocar diversas respuestas inflamatorias, activar glóbulos blancos y plaquetas y promover la liberación de mediadores inflamatorios como las citocinas, y se postula que los injertos PTFE son más proclives a desarrollar tal tipo de reacciones21. Al respecto, Ito et, al tras efectuar un estudio retrospectivo que incluyó 128 pacientes sometidos a EVAR identificó que los injertos de poliéster se asociaron a mayor frecuencia de casos con fiebre (p < 0.001), PCR más elevada (2.9 vs. 1.1; p = 0.038) y leucocitosis (p < 0.001), y por tanto a mayor el riesgo de SPI30. Ante tal evidencia fue que se decidió comparar los eventos y variables analizados por el material de endoprótesis empleado, sin embargo no se identificó que tal factor impactara en la frecuencia de SPI ni de las medias de PCR durante el seguimiento inmediato (Fig. 2), lo que significa que deben existir más factores implicados en el incremento de la PCR que únicamente la reacción inflamatoria desencadenada por el material de la endoprótesis. Uno de los hallazgos más relevantes fue el hecho de que la dislipidemia se asoció de forma significativa con el desarrollo de SPI (Tabla 4); al respecto, en la última década se ha encontrado evidencia que sustenta la hipótesis que postula que la dislipidemia es capaz de inducir una respuesta inflamatoria en las paredes vasculares, siendo un marcador temprano de ateroesclerosis, la inflamación desencadenada es de bajo grado e involucra citocinas como IL-1, IL-6 y TNF-α, las cuales terminan por desencadenar la producción de PCR. Por ello, recientemente se ha planteado emplear determinaciones de PCR en pacientes con dislipidemia a fin de detectar oportunamente pacientes en elevado riesgo de ateroesclerosis y otros riesgos cardiovasculares31. En nuestros pacientes identificamos que efectivamente aquellos con dislipidemia tenían niveles de PCR mayores que aquellos sin tal historial médico, sin embargo, no se efectuaron determinaciones basales previo al EVAR, por tanto no es posible discernir si tal elevación de la PCR es resultado de los mecanismos de inflamación de bajo grado como se postula, o si se deben a la reacción inflamatoria desencadenada por el EVAR, ya que en los pacientes que efectivamente presentaron SPI las cifras de PCR fueron indiscutiblemente más elevadas, en más de cuatro veces, respecto a las medias de quienes no tuvieron SPI.
Tabla 4 Asociación de las variables con el desarrollo de síndrome postimplantación en pacientes sometidos a EVAR, IMSS UMAE 71, 2021-2023
| Característica | n (%) | OR | IC95% | Valor de p |
|---|---|---|---|---|
| Sexo masculino | 7 (100%) | 0.837 | 0.734-0.955 | 0.438 |
| Hipertensión arterial | 5 (71.4%) | 0.806 | 0.135-4.821 | 0.569 |
| Diabetes | 2 (28.6%) | 0.313 | 0.054-1.805 | 0.175 |
| Dislipidemia | 3 (42.9%) | 9.500 | 1.416-63.724 | 0.033 |
| Enfermedad coronaria | 2 (28.6%) | 1.943 | 0.312-12.118 | 0.396 |
| Cáncer | 0 (0%) | N/A | N/A | N/A |
| Insuficiencia cardiaca | 0 (0%) | N/A | N/A | N/A |
| Aneurisma sacular | 0 (0%) | N/A | N/A | N/A |
| Diámetro del aneurisma > 78 mm | 7 (100%) | N/A | N/A | < 0.0001 |
| Enfermedad renal crónica | 0 (0%) | N/A | N/A | N/A |
| Asma/EPOC | 0 (0%) | N/A | N/A | N/A |
| Enfermedad vascular cerebral | 0 (0%) | N/A | N/A | N/A |
| EVAR electivo | 7 (100%) | 0.851 | 0.755-0.959 | 0.854 |
| Duración EVAR > 129 min | 3 (42.9%) | 1.059 | 0.209-5.354 | 0.628 |
| Material endoprótesis: dacrón | 4 (57.1%) | 1.152 | 0.228-5.807 | 0.597 |
EPOC: enfermedad pulmonar obstructiva crónica; EVAR: reparación endovascular de aneurismas; IC95%: intervalo de confianza del 95%; IMSS: Instituto Mexicano del Seguro Social; N/A: no disponible; OR: odds ratio; UMAE: unidad médica de alta especialidad.











 nova página do texto(beta)
nova página do texto(beta)