Introducción
La ventilación con presión positiva (VPP) se utiliza en múltiples situaciones clínicas, siendo una de sus principales aplicaciones el soporte en patología cardiaca como puente a la recuperación mientras se ofrecen otros tratamientos o en la espera de un trasplante cardiaco. Se ha demostrado que, en entidades como insuficiencia cardiaca, choque cardiogénico y estado postquirúrgico de cirugía cardiaca, su aplicación aumenta la supervivencia al disminuir la demanda de oxígeno y optimizar el gasto cardiaco (GC) mejorando la perfusión tisular.1 Pese a lo anterior, no todos los pacientes con alguna condición cardiaca se benefician y por el contrario empeoran por las interacciones cardiopulmonares que se llevan a cabo en cada ciclo respiratorio; en este grupo se incluyen pacientes con cardiopatías congénitas (CC) que involucren una comunicación pulmonar-sistémica (defectos septales atriales, ventriculares, canal auriculoventricular y persistencia del conducto arterioso), hipertensión pulmonar y/o disfunción del ventrículo derecho (VD).
En la actualidad se estima que en Estados Unidos 2 millones de adultos viven con una CC y este número aumenta aproximadamente 5% cada año.2 En nuestro país no existen cifras oficiales, pero se estiman de 18 a 20 mil nuevos casos al año, siendo la más prevalente la comunicación interauricular (CIA).3 Al aumentar la tasa de personas viviendo con una CC, también aumenta la necesidad de cuidados y consideraciones médicas especiales incluyendo el manejo ventilatorio.
Según reportes de casos y teniendo en consideración las interacciones cardiopulmonares que se llevan a cabo durante la VPP, los pacientes portadores de una CC con comunicación pulmonar-sistémica presentan empeoramiento de la saturación de oxígeno, inestabilidad hemodinámica e hipoperfusión independientemente de la patología de base, esto debido principalmente al aumento de las resistencias vasculares pulmonares (RVP) y la aparición o empeoramiento del cortocircuito derecho-izquierdo.4-7
A continuación, se explica el caso de una paciente que ingresa a la unidad de cuidados intensivos obstétricos sin el conocimiento por parte del personal médico del antecedente de CC, y cómo el entender las interacciones cardiopulmonares en el manejo ventilatorio de este tipo de pacientes pueden cambiar el pronóstico.
Presentación del caso
Mujer de 30 años, quien cursaba con embarazo de 37.6 semanas de gestación, durante su embarazo niega síntomas de relevancia, solo disnea de grandes esfuerzos. Niega antecedentes de importancia como enfermedades crónicas y genéticas. Ingresa a hospital externo en donde diagnostican eclampsia con desaturación de hasta 47% en periodo postictal, por lo que aseguran vía aérea mediante intubación endotraqueal, pasan a cesárea de urgencia sin complicaciones, pero con requerimientos altos de FiO2 de hasta 80%, por lo que es regulada a nuestra institución.
Se recibe en nuestra unidad con presión arterial 102/64 mmHg, frecuencia cardiaca 82 latidos por minuto, saturando 92% con ventilación continua mandatoria controlada por volumen (VMC-CVs) programada con un volumen tidal (VT) de 360 ml, PEEP 6 cmH2O, FiO2 60%, frecuencia respiratoria (FR) de 16. A la exploración física los únicos hallazgos patológicos fueron disminución del murmullo vesicular en base izquierda, con matidez a la auscultación, así como soplo sistólico en foco mitral. Por dichos hallazgos se realiza rastreo pulmonar ultrasonográfico, encontrando sólo atelectasia de lóbulo inferior izquierdo. Se realiza radiografía de tórax en donde se confirma atelectasia en dicha anatomía y además se evidencia adecuada colocación de tubo endotraqueal. Por la presencia de atelectasia se decide incrementar la PEEP hasta 10 cmH2O y posterior a 16 cmH2O por nula respuesta; sin embargo, con empeoramiento del cuadro manifestado por mayor requerimiento de FiO2 (100%) por desaturación de 70%, inestabilidad hemodinámica con requerimiento de vasopresor por tensión arterial de 70/40 mmHg, y bradicardia de 35 lpm que mejora con la administración de dosis única de atropina. Se sospecha de tromboembolia pulmonar (TEP), por lo que se realiza rastreo ecocardiográfico en búsqueda de hallazgos sugestivos ante una paciente hemodinámicamente inestable. Se encuentra en primer rastreo ultrasonográfico cardíaco patrón hemodinámico hiperdinámico caracterizado por signo del beso papilar del ventrículo izquierdo (VI), pero probable defecto del septum (Figura 1), a nivel pulmonar derrame pleural bilateral no evidenciado en radiografía de tórax.
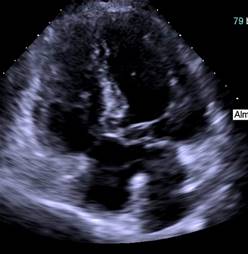
Figura 1: Ecocardiograma transtorácico en donde se evidencia la presencia de probable defecto septal.
Por el soplo en la exploración física y el probable defecto septal, se sospecha de shunt cardiaco, por lo que se baja PEEP a 10 cmH2O evidenciando mejoría de la saturación logrando disminuir FiO2 a 70%, y bajar dosis de vasopresor. Se corrobora shunt cardiaco tras realizar prueba de burbujas, al evidenciar un gran paso de éstas a cavidades izquierdas (Figura 2), por lo que se procede a realizar mediciones más avanzadas; fracción de eyección del ventrículo izquierdo (FEVI) 86%, relación ventrículo derecho (VD) - VI de 0.57, sin datos de insuficiencia del VD, hipertensión pulmonar leve por presión media de la arteria pulmonar de 24.7 mmHg por método de Chemla , presión de la aurícula derecha de 20 mmHg, GC de 6.3 L/min, índice cardiaco (IC) de 3.5 L/min/m2, resistencias vasculares pulmonares (RVP) elevadas de 2.7 unidades Wood mediante ultrasonido y formula descrita por Abbas.8 Por lo anterior, se presume que el deterioro hemodinámico y respiratorio de la paciente era debido a la VPP, y el consecuente aumento o aparición de shunt intracardiaco.
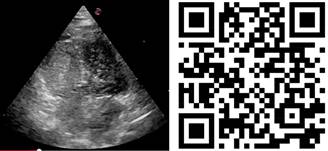
Figura 2: Prueba de burbujas con PEEP de 10 cmH2O. La prueba de burbujas o también conocida como prueba de solución salina agitada, se realiza mediante ecocardiografía con contraste de solución salina agitada para detectar cortocircuitos cardiacos. Implica la inyección de una mezcla de solución salina (8-10 mL ) y aire (0.5 mL ), a veces con una pequeña cantidad de sangre, a través de un acceso venoso ya sea central o periférico. En esta imagen vemos un paso importante de burbujas de cavidades derechas a izquierdas tanto a nivel ventricular como auricular, lo que confirma la presencia de shunt dinámico a este nivel de PEEP. V ideo al escanear el código QR.
Se decide bajar PEEP a 5 cmH2O con disminución del requerimiento de FiO2 a 50% y se inicia prueba de ventilación espontánea con presión soporte de 5 cmH2O, ya que se hipotetiza que el extubarla beneficiaría el intercambio de gases y el estado hemodinámico. Se realiza nuevo rastreo ecocardiográfico, con disminución importante del shunt demostrado por un menor paso de burbujas a través del defecto cardiaco (Figura 3), normalización de la presión media pulmonar y de las resistencias vasculares pulmonares. Además, mejora la SaO2 a 94%, y se suspende el apoyo vasopresor. Se decide extubar a la paciente, colocar cánulas nasales de alto flujo, se agrega al manejo fisioterapia para mejoría de atelectasias previniendo la vasoconstricción hipóxica y diurético para mejoría de las presiones del VI.
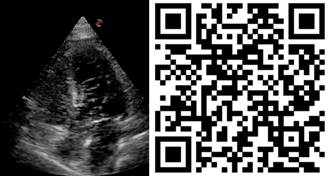
Figura 3: Prueba de burbujas con PEEP de 5 cmH2O. Se evidencia una mejoría significativa del paso de burbujas de las cavidades derechas a izquierdas, por lo que se confirma de manera objetiva una disminución del shunt dinámico. V ideo al escanear el código QR.
Paciente con adecuada evolución durante la hospitalización, se descartó TEP por angiotomografía, se le realiza ecocardiograma por parte de cardiología encontrando FEVI normal, y hallazgos compatibles con canal aurículo ventricular (CAV). Solicitan cardiorresonancia donde se evidencia FEVI de 68%, FEVD 63%, con dilatación leve de ambos ventrículos, CAV intermedio con hendidura e insuficiencia mitral severa, QP/QS: 1.5:1 por lo que se cataloga con shunt intracardiaco. La paciente es sometida a cirugía de corrección de defecto y actualmente continúa con rehabilitación cardiaca.
Discusión
Las interacciones cardiopulmonares durante la VPP pueden ser benéficas como soporte en múltiples patologías; sin embargo, a la fecha no existe información suficiente sobre los efectos y el manejo en pacientes que cursan con CC con conexión de la circulación pulmonar-sistémica.
La mayoría de la información actual se centra en la población pediátrica, y recomienda una estrategia basada en presiones de la vía aérea bajas, minimizando la presión pulmonar para que el flujo sea eficaz, como alternativas se mencionan la ventilación con presión negativa y la ventilación oscilatoria de alta frecuencia (VAFO). A pesar de la recomendación de mantener presiones positivas bajas, se deben prevenir a su vez las atelectasias para evitar la vasoconstricción hipóxica. Por lo anterior, se recomienda la extubación temprana, ya que esto mejora los resultados en esta población.9 Algunas otras estrategias estudiadas son el aumento de la FiO2; sin embargo, el efecto vasodilatador de esta estrategia es nulo en los adultos.10
Las interacciones cardiopulmonares están dadas por cambios en la presión media de la vía aérea durante la VPP que se transmiten al pulmón y corazón, pudiendo alterar el desempeño cardiovascular. De todos los componentes que influyen en la presión media de la vía aérea, el más estudiado es la PEEP.1,10-12
La fuerza responsable de la conducción del retorno venoso periférico a la circulación central es el gradiente de presión que existe entre el sistema venoso (vena cava superior e inferior) y la aurícula derecha (AD).
Las interacciones cardiopulmonares en respiración espontánea están dadas por la presión negativa pleural, que se hace más negativa con cada inspiración, lo que se traduce a la AD haciendo que su presión disminuya respecto a la sistémica creando un gradiente de presión que sumado a la contracción diafragmática aumenta el retorno venoso. Las resistencias vasculares sistémicas y pulmonares se mantienen dentro de rangos fisiológicos y no existen cambios en el gasto cardiaco.
Estas interacciones cambian de manera significativa al aplicar VPP, empezando por la presión pleural que es positiva durante todo el ciclo respiratorio, principalmente en inspiración, consecuentemente también la presión auricular, disminuyendo el gradiente de presión de la circulación sistémica, el retorno venoso y la precarga del VD. Se ha evidenciado que por cada aumento de 1 mmHg de presión en la AD, existe una disminución del retorno venoso de hasta 14%.13 La postcarga de las cavidades derechas aumenta por colapso del VD y los vasos pulmonares, lo que lleva a un aumento de las RVP. En el contexto en donde la VPP ayude a disminuir el colapso alveolar (volúmenes corrientes bajos, atelectasias) se disminuirá el efecto de vasoconstricción hipóxica que mantendrá o disminuirá las RVP, con una adecuada compensación.14 Sin embargo, en situaciones de sobredistensión alveolar, los capilares pulmonares se colapsan aumentando las RVP no sólo por efecto directo, sino también al aumentar el espacio muerto alveolar elevando el CO2, lo que puede ocasionar fallo del VD y estado de choque,15 siendo perjudicial en pacientes con disfunción del VD o hipertensión pulmonar. El aumento de las RVP en CC con conexión pulmonar-sistémica puede empeorar o crear un shunt cardiaco dinámico, incrementando la cantidad de sangre no oxigenada que pasa a la circulación sistémica, disminuyendo la saturación y la entrega de O2 a los tejidos con aparición de acidemia, inestabilidad hemodinámica y disminución de perfusión en tejidos distales, que puede culminar en falla orgánica múltiple. La precarga del VI es más baja por efecto de disminución de la precarga del VD, ya que la interdependencia ventricular dicta que el VI sólo puede eyectar la sangre que recibe del VD,16 además el cambio de posición del septum disminuye la distensibilidad del VI, lo que empeora este círculo vicioso. En pacientes con CC la aparición de un shunt cardiaco puede mantener e incluso aumentar la precarga del VI, lo que puede llegar a ocasionar disfunción diastólica y edema pulmonar.17 Mientras que la postcarga del VI disminuye ya que con la VPP al colapsar la aorta y elevar la presión de esta, hace que se active el efecto baroreceptor, con una potencial vasodilatación periférica compensadora.18,19 En disfunción sistólica del VI, esto es benéfico al disminuir la tensión de la pared ventricular, el consumo de O2, mejorando el GC y la entrega de O2 a los tejidos.20 En los pacientes con CC, esta vasodilatación puede empeorar el estado hemodinámico. Los efectos de la VPP en diferentes escenarios se resumen en la Tabla 1.
Tabla 1: Resumen de las interacciones cardiopulmonares en diferentes escenarios.
| Parámetro | Respiración espontánea | VPP | VPP+ Cardiopatía congénita con comunicación derecha izquierda | VPP + Hipertensión pulmonar o falla del VD | VPP + disfunción sistólica aislada del VI |
|---|---|---|---|---|---|
| Precarga del VD | Incrementa por presión inspiratoria negativa | Disminuye por aumento de la presión intratorácica en la inspiración | Disminuye por aumento de la presión intratorácica en la inspiración | Disminuye por aumento de la presión intratorácica en la inspiración | Disminuye por aumento de la presión intratorácica en la inspiración |
| Postcarga del VD | Pequeños incrementos por aumento de la presión transpulmonar y compresión de pequeños vasos intraalveolares por la expansión alveolar | Incremento por aumento de la presión transpulmonar en inspiración | Incrementa, lo que puede ocasionar aparición de un shunt dinámico | Incrementa, lo que puede ocasionar empeoramiento de la presión pulmonar y cor pulmonale agudo | Incremento por aumento de la presión transpulmonar en inspiración |
| Precarga del VI | Disminuye comparado con la espiración, pero es algo mínimamente perceptible | Disminuye el llenado y el volumen sistólico | Aumenta por incremento del flujo a cavidades izquierdas en inspiración, esto puede llevar a disfunción diastólica, inestabilidad y desaturación por paso de sangre desaturada a la circulación sistémica | Disminuye | Disminuye, lo que puede mejorar las presiones de llenado del ventrículo izquierdo y la regurgitación mitral |
| Postcarga del VI | Incremento leve por presión intratorácica inspiratoria negativa | Disminuye por aumento de la presión intratorácica y efecto barorreceptor aórtico | Disminuye por aumento de la presión intratorácica | Disminuye por aumento de la presión intratorácica | Disminuye, lo que ocasiona disminución del trabajo miocárdico, puede mejorar el volumen sistólico |
Existen algunos casos similares reportados en la literatura, en donde la VPP empeoró la clínica de los pacientes, y la mejor intervención fue dejar de aplicarla, se mencionan a continuación algunos de estos casos:
En la revista American Thoracic Society se comenta un paciente con ventrículo único postquirúrgico de cirugía paliativa de Fontan, que desarrolla insuficiencia respiratoria tras ser sometido a VPP, y de igual manera ante la sospecha de ser secundario a las interacciones cardiopulmonares se extuba con mejoría del cuadro.4
En la Revista Española de Cardiología, se publica el caso de un masculino de 26 años, ingresado por traumatismo cráneo encefálico, que desarrolla una neumonía asociada a la ventilación con grandes consolidaciones pulmonares y falla respiratoria, por lo que fueron incrementando la PEEP hasta 20 cmH2O sin mejoría del cuadro de falla respiratoria y presentando inestabilidad hemodinámica. Le realizan ecografía transtorácica encontrando un foramen oval permeable (FOP) con aneurisma del septum atrial, corroborando con prueba de burbujas un shunt cardiaco, por lo que bajan PEEP hasta 5 cmH2O, con mejoría inmediata de la saturación de 72 a 95%.21
Algo similar ocurrió en un paciente que se lleva a VPP por infección de SARS-CoV-2, que a pesar del manejo ventilatorio adecuado no mejoraba la saturación, por lo que realizan prueba de burbujas encontrando FOP con shunt dinámico derecha izquierda, mejorando con la disminución de la PEEP.5
En otro caso reportado, un hombre de 51 años es valorado por disnea y baja tolerancia al ejercicio, se conocía con SAOS y se manejaba VPP mediante CPAP. En la valoración ecocardiográfica encuentran un defecto auricular de tipo ostium secundum, con una presión media de la pulmonar de 18 mmHg, realizan prueba de solución salina agitada a diferentes niveles de PEEP, 0, 8 y 12 cmH2O, encontrando que el shunt aumenta conforme aumenta la PEEP, con desaturación concomitante, atribuyendo el empeoramiento de los síntomas del paciente a la VPP empleada de manera terapéutica.7
Analizando el caso de nuestra paciente, utilizar VPP generó presiones de la vía aérea elevadas, resultando en efectos deletéreos en lugar de mejoría en el contexto de una CC. Esto se confirma mediante ecocardiografía al disminuir el gradiente del shunt tras disminuir la PEEP, y la mejoría hemodinámica instantánea de intercambio gaseoso.
Interrogando nuevamente a la paciente, refirió parada cardiorrespiratoria en parto anterior y que es portadora de una cardiopatía diagnosticada en la infancia, con abandono del tratamiento desde entonces. De haber tenido conocimiento de esta información, probablemente la mejor estrategia desde el hospital externo hubiera sido no intubarla.
Conclusiones
Cada día suman más los pacientes adultos que viven con una CC, se debe tener especial atención en aquéllas que involucran una conexión de la circulación pulmonar-sistémica, ya que el manejo con VPP puede desarrollar un shunt cardiaco con insuficiencia respiratoria y en casos severos deterioro del estado hemodinámico.
Con la revisión de la literatura concluimos que se debe sospechar esta entidad en pacientes que tras ser sometidos a VPP empeoran su saturación, perfusión y estado hemodinámico, y que esto no es explicado completamente por las condiciones de la patología de base. En estos casos es recomendable realizar una prueba de burbujas con solución salina agitada para confirmar el diagnóstico. Esta técnica tiene una precisión diagnóstica muy buena, es fácil, reproducible, de nulo riesgo para el paciente y se puede realizar al pie de la cama.22
Por último, si se conoce o se diagnostica este tipo de CC, basándonos en los reportes actuales y entendiendo las interacciones cardiopulmonares, lo ideal es tratar al paciente con presiones positivas bajas de la vía aérea, manteniendo uso de PEEP mínima pero suficiente para no generar atelectasias con la consecuente vasoconstricción hipóxica, ya que ambas situaciones aumentarán las RVP con empeoramiento o aparición del shunt cardiaco. Y una estrategia que puede mejorar los desenlaces es la extubación temprana, ya que esto mejorará por los cambios en gradientes de presión tanto la saturación como el estado hemodinámico y la perfusión tisular. Una vez extubados estos pacientes es de vital importancia la fisioterapia pulmonar para prevención y manejo de atelectasias.











 nova página do texto(beta)
nova página do texto(beta)


