INTRODUCCIÓN
La bacteria Vibrio parahaemolyticus habita en ambientes marinos costeros y zonas estuarinas (Cariani et al., 2012); se encuentra libre en suspensión o asociada a partículas suspendidas, como: sedimento (Heitmann et al., 2005), plancton (Turner et al., 2013), peces (Aliaga et al., 2010), moluscos bivalvos (Rodríguez-Camacho et al., 2014) y crustáceos. En estos últimos, suele alojarse en el exoesqueleto de los camarones debido a que la quitina es utilizada por la bacteria como nutriente (Dulanto, 2013).
De acuerdo con los principales factores que influyen en la ocurrencia y distribución de V. parahaemolyticus en el agua de mar son la temperatura, salinidad, disponibilidad de nutrientes y las fluctuaciones en la concentración de plancton (Hernández-Ayón et al., 2003; Tantillo et al., 2004). Por lo que un desequilibrio en los factores físicos, químicos y biológicos puede ocasionar la proliferación de V. parahaemolyticus el cual es una bacteria patógena oportunista, anaerobia facultativa, Gram negativa, responsable de causar altas mortalidades (Cañigral-Cárcel, 2011). Una de las enfermedades causantes por V. parahaemolyticus es la enfermedad de la necrosis hepatopancreática aguda (AHPND), la cual se ha registrado en el continente asiático y en diversas especies de camarones, tal es el caso de Penaeus monodon; los primeros brotes de esta especie se registraron en el año 2009 en el sur de China, causando mortalidades masivas de hasta el 100 % en los cultivos (Kumar et al., 2021). Otra enfermedad altamente letal causada por Vibrio (HLVD, por sus siglas en inglés), conocida como “enfermedad de las postlarvas de vidrio” (GPD) o “enfermedad de las postlarvas translúcidas” (TPD), tuvo su primera aparición en 2019 y el agente causal ha sido identificado como cepas virulentas de V. parahaemolyticus (Vp HLVD) (Zou et al., 2020; Yang et al., 2023). La infección por Vp HLVD daña gravemente el túbulo del hepatopáncreas y el epitelio del intestino medio de los camarones infectados, provocando una mortalidad aguda y masiva en las postlarvas de camarón. Aunque tanto la HLVD como la AHPND son causadas por vibrios y comparten signos clínicos similares, la Vp HLVD es mucho más virulenta que la Vp AHPND (Yang et al., 2023).
En México, no hay evidencias de aparición de infección por HLVD, pero se tiene conocimiento que los primeros brotes de la AHPND se presentaron durante el 2013, afectando la producción de los cultivos de Penaeus vannamei en la región noreste principalmente en los Estados de Sonora, Sinaloa y Nayarit (Galaviz-Silva et al., 2021), estimando pérdidas de hasta el 65%, en aproximadamente 1,500 granjas de cultivo con una extensión de 92,962 ha (Nunan et al., 2014). Adicionalmente, es importante señalar que el tiempo de generación del Vibrio es entre 10 y 12 minutos beneficiado por la disponibilidad de nutrientes en su entorno y temperaturas cálidas (> 35°C), salinidades bajas (< 8 UPS) y pH alcalino (> 7.5) (Zamora-Pantoja et al., 2005). Por lo tanto, algunos autores mencionan que los factores anteriormente señalados serían los principales causantes del incremento de la ocurrencia y distribución de este patógeno en el agua de mar (Hernández-Ayón et al., 2003; Tantillo et al., 2004). De acuerdo con Lai et al. (2015), esta enfermedad se presenta cuando los camarones se encuentran bajo condiciones de estrés, o cuando su sistema inmune está deprimido, causando importantes pérdidas económicas a la industria camaronícola. Cabe destacar que las cepas de V. parahaemolyticus que causan AHPND en México muestran diferencias genéticas con las cepas asiáticas y han desarrollado resistencia a antibióticos de uso común como la oxitetraciclina y la sulfacloropiridazina-trimetoprima (Galaviz-Silva et al., 2021). Estos hallazgos resaltan la importancia de monitorear y manejar las poblaciones de Vibrio en la acuicultura de camarón.
A 14 años de la aparición del AHPND a nivel mundial, esta enfermedad continúa afectando a la industria del cultivo de camarón. A pesar de ello, no existen reportes de investigaciones in situ que confirmen las condiciones que favorecen el desarrollo de este microorganismo, tampoco usando un Modelo Lineal Generalizado (MLG). Aún así se han hecho predicciones e identificado correlaciones de la abundancia de especies de Vibrio utilizando el modelo paramétrico de regresión lineal (LRM) y el modelo binomial negativo (NBM), así como el modelo semiparamétrico aditivo generalizado (GAM) (Dequito et al., 2022). Los únicos trabajos que han analizado el efecto del AHNPD en los cultivos comerciales de camarón son los de Estrada-Pérez et al. (2019) y Estrada Pérez et al. (2020) con modelos de regresión múltiple con un modelo de stock y un modelo bioeconómico respectivamente. En el presente estudio, se evaluaron las diferentes variables físicas, químicas y biológicas que pudieran estar contribuyendo en el incremento de las densidades de este patógeno en el hepatopáncreas de los camarones Penaeus vannamei, cultivados en unidades de producción localizadas al noroeste de México. Además se determinó la asociación de variables físicas, químicas y biológicas de los cuerpos de agua costeros en la línea de costa al noroeste de México y del agua de los estanques de cultivo de las granjas camaroneras con el incremento de la densidad de V. parahaemolyticus en el hepatopáncreas del camarón Penaeus vannamei, utilizando como herramienta de análisis los Modelos Lineales Generalizados (Nelder & Wedderburn, 1972). Lo anterior con la finalidad de que se generen bases científicas acerca del comportamiento V. parahaemolyticus en los estanques de cultivo de camarón, misma que contribuirá a la toma de decisiones por parte del productor para el control y manejo del patógeno en sus instalaciones de cultivo.
MATERIAL Y MÉTODOS
Recolecta de muestras y medición de variables ambientales
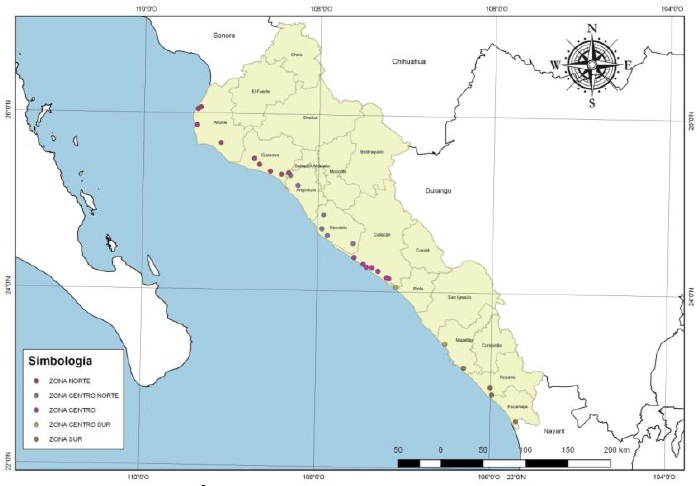
Se obtuvo una base de datos de cuerpos de agua costeros, así como en granjas de camarón ubicados al Noroeste de México, específicamente sobre la línea de costa del Estado de Sinaloa (Figura 1) durante el 2017 en el que se efectuaron diez muestreos en 26 granjas de cultivo en el primer ciclo (febrero-junio) y 18 en el segundo (julionoviembre). Las zonas de muestreo fueron zona norte: Ahome y Guasave, zona centro norte: Angostura y Navolato, zona centro: Eldorado y Cospita, zona centro sur: Elota y zona sur: Mazatlán. Durante los primeros 30 días de cultivo los muestreos se realizaron semanalmente, por considerarse como la etapa crítica (Hong et al., 2016), posteriormente, los muestreos se realizaron cada dos semanas.
Las muestras de organismos, agua y sedimento de cada una de las unidades de producción acuícola fueron obtenidas de un estanque seleccionado aleatoriamente en la compuerta de entrada y salida. Para las muestras de organismos se seleccionaron 15 camarones con trastornos de comportamiento alimentario y alteraciones fisiológicas (Soto-Rodríguez et al., 2010). Para el análisis en fresco y bacteriológico, los camarones se mantuvieron vivos y se depositaron en hieleras con agua del estanque para ser trasladados al laboratorio del Comité Estatal de Sanidad Acuícola de Sinaloa (CESASIN) donde fueron procesados. Las muestras de agua se tomaron entre los 20 cm por debajo de la superficie y 20 cm por encima del fondo. Para el análisis bacteriológico, las muestras se trasladaron al laboratorio antes mencionado, utilizando para el cultivo bacteriano placas de CHROMagar Vibrio para posteriormente cuantificar y expresar los resultados en unidades de volumen (UFC/ml) o masa (UFC/g) (Soto-Rodríguez et al., 2015). Las muestras de sedimento para análisis de materia orgánica y pHs del estanque en cultivo se recogieron con una sonda para sedimento. La materia orgánica (MO) se evaluó de acuerdo con la NOM-021-SEMARNAT-2000 a través del método de Walkley & Black (1934) mediante la oxidación del carbono orgánico (CO). En cada muestreo se registraron datos de salinidad (S), temperatura (T, °C), oxígeno (OD, mg L-1) y pH empleando un refractómetro de mano marca VITAL SINE SR6, un oxímetro marca YSI-55-12 y un potenciómetro marca YSI pH 10A respectivamente, y la transparencia (Tp, cm) con un disco de Secchi.
Las concentraciones de nitritos (NO2 -), nitratos (NO3 -), amonio (NH4 +) y fosfatos (PO4 3-) se realizaron a partir de los procedimientos descritos en el manual de análisis de agua sobre los kits LYSA, basados en el principio de Strickland & Parsons (1972). La alcalinidad (Alc) se midió por el método colorimétrico descrito por Hanna, utilizando un colorímetro manual HI755.
Modelo lineal generalizado y análisis estadístico
Para realizar un análisis exploratorio de los datos, se obtuvieron las medidas de tendencia central de las variables fisicoquímicas, nutrientes, materia orgánica, pH del sedimento y bacteriología (Figura 2). Con el objetivo de determinar la asociación entre las diferentes variables con respecto a la densidad de V. parahaemolyticus (UFC/g) en el hepatopáncreas del camarón, se ajustaron Modelos Lineales Generalizados (GLM) (Nelder & Wedderburn, 1972) utilizando la paquetería base del lenguaje de programación R Core Team 2021.
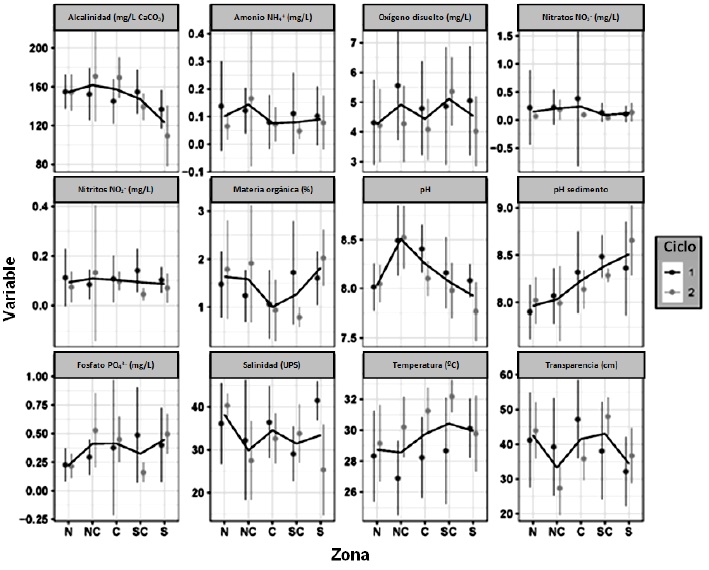
Figura 2 Promedio ± desviación estándar por zona y ciclo de cultivo de las variables fisicoquímicas y biológicas en las granjas de camarón en la región noroeste de México. N = Norte, NC = Norte Central, C = Central, SC = Sur Central y S = Sur. La línea negra marca la media entre ciclos de cultivo.
Para construir los MLG se establecieron como variables explicativas la T, OD, S, pH, Tp, NO2 -, NO3 -, NH4 + , PO4 3-, Alc, MO, pHs, mes de cultivo y densidad de V. parahaemolyticus (UFC/ml) en cuerpos de agua costeros y de los estanques de cultivo conforme a la Tabla 1. Debido a que todas las variables explicativas fueron cuantitativas, se le añadió al modelo un efecto cuadrático (polinomio de segundo grado), con la finalidad de mejorar el ajuste de las variables, intentando explicar de mejor manera la tendencia de los datos observados, lo cual fue evaluada previamente mediante un análisis exploratorio (Sokal & Rohlf, 1986). Debido a que los valores de UFC/g en hepatopáncreas, solo pueden ser valores iguales o mayores que cero, se asumió una distribución Gamma en el error del modelo, utilizando como variable de respuesta el valor de x + 1 para eliminar los ceros. Para asumir una distribución Gamma, se utilizó una función de enlace inversa (ƞ = 1/µ). La selección del modelo para las variables explicativas más relevantes, se utilizó el proceso de stepwise usando el criterio de Akaike como factor de selección (AIC), eligiendo como el mejor modelo, aquel que presentó el menor valor de AIC (Anderson & Burnham, 2002).
Tabla 1 Variables explicativas que se utilizaron para el Modelo Lineal Generalizado
| Variables | Febrero-Junio | Julio-Diciembre | Febrero-Diciembre |
|---|---|---|---|
| Promedio ± DE | |||
| Físico-químicas del agua | |||
| Temperatura (ºC) | 28.3 ± 2.8 | 30.2 ± 2.2 | 29.0 ± 2.8 |
| Oxígeno (mg/L) | 4.8 ± 1.7 | 4.2 ± 1.2 | 4.6 ± 1.6 |
| Salinidad (UPS) | 35.6 ± 10.0 | 31.8 ± 9.2 | 34.2 ± 9.9 |
| pH | 8.2 ± 0.3 | 8.1 ± 0.4 | 8.2 ± 0.4 |
| Transparencia (cm) | 40.9 ± 13.4 | 36.2 ± 9.9 | 34.2 ± 12.5 |
| Nutrientes del agua (mg/L) | |||
| Nitratos (NO3 -) | 0.242 ± 0.74 | 0.118 ± 0.125 | 0.197 ± 0.592 |
| Amonio (NH4 +) | 0.112 ± 0.139 | 0.098 ± 0.149 | 0.107 ± 0.143 |
| Nitritos (NO2 -) | 0.107 ± 0.091 | 0.094 ± 0.154 | 0.102 ± 0.118 |
| Fosfatos (PO4 -3) | 0.324 ± 0.371 | 0.406 ± 0.256 | 0.354 ± 0.335 |
| Alcalinidad | 149 ± 22 | 154 ± 38 | 151 ± 29 |
| Sedimento | |||
| MO (%) | 1.4 ± 0.7 | 1.6 ± 1.0 | 1.5 ± 0.8 |
| pH | 8.17 ± 0.41 | 8.19 ± 0.38 | 8.19 ± 0.40 |
| Hepatopáncreas (UFC/g) | |||
| Densidad de V. parahaemolyticus | 46102.9 ± 265988.73 | 13543.8 ± 54802.76 | 33786.1 ± 212785.82 |
| Bacteriología (UFC/ml) (UFC/g) | |||
| Agua-cuerpos | 104.58 ± 781.87 | 102.46 ± 246.12 | 103.80 ± 639.82 |
| Sedimento-cuerpos | 8256.34 ± 52608.30 | 12383 ± 35684.82 | 9765.47 ± 47131.54 |
| Agua-estanques | 47.44 ± 136.50 | 87.86 ± 391.54 | 62.22 ± 260.86 |
| Sedimento-estanques | 1931.99 ± 5508.59 | 2856.38 ± 7218.00 | 2270.04 ± 6197.39 |
Nota: MO, materia orgánica.
RESULTADOS
Bacteriología
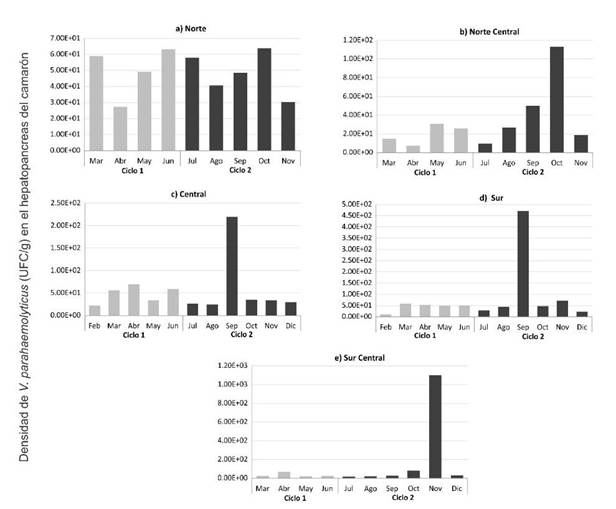
Con relación a la presencia de V. parahaemolyticus en el hepatopáncreas de los camarones, se observó que, en la zona norte del Estado, se encontró la mayor densidad de V. parahaemolyticus en ambos ciclos de producción (Figura 3a), conforme los muestreos se dirigieron al sur del Estado, se observa una clara tendencia a disminuir la concentración de V. parahaemolyticus. También se pudo observar que, en la zona norte central, hubo mayor concentración de bacterias durante el mes de octubre y solo durante el segundo ciclo de producción (Figura 3b), en la zona central y sur del estado destaca el mes de septiembre (Figura 3c y d); y para el caso de la zona sur central el mes de noviembre (Figura 3e).
Asociación de las variables físicas, químicas y biológicas con la densidad de V. parahaemolyticus en el hepatopáncreas del camarón
El efecto significativo (P<0.05) del OD, S, pH del agua de cultivo, NO3 -, NH4 +, Alc, MO, pHs, mes de cultivo y densidad de V. parahaemolyticus (UFC/ml) en cuerpos de agua costeros y de los estanques de cultivo explicó el fenómeno de la densidad de V. parahaemolyticus en el hepatopáncreas del camarón con una devianza nula de 5895.2, una devianza residual de 3840.2 y una devianza explicada de 34.85% (Tabla 2).
Tabla 2 Análisis estadístico de las variables físicas, químicas y biológicas que favorecen la densidad de V. parahaemolyticus en el hepatopáncreas del camarón Penaeus vannamei
| Variable | Coeficiente Estimado | Error Estándar | Valor t | P |
|---|---|---|---|---|
| (Intercepto) | -5.2964 | 7.7347 | -0.6847 | 0.4940 |
| UFC en agua | ||||
| UFC en agua (Cuerpos de Agua) | 0.0016 | 0.0011 | 1.4304 | 0.1537 |
| UFC en Agua (Granja) | -1.01E-05 | 1.94E-06 | -5.1911 | 4.05E-07 |
| UFC en Sedimento (Granja) | -1.33E-08 | 3.41E-09 | -3.9066 | 0.0001 |
| Ciclo: 2 | -1.7144 | 0.6305 | -2.7191 | 0.0069 |
| Mes: abril | -3.6409 | 3.8923 | -0.9354 | 0.3503 |
| Mes: mayo | -3.3051 | 3.8084 | -0.8678 | 0.3862 |
| Mes: junio | -4.1755 | 3.8211 | -1.0927 | 0.2754 |
| Mes: julio | -2.4848 | 3.8558 | -0.6444 | 0.5198 |
| Mes: agosto | -2.8677 | 3.8537 | -0.7441 | 0.4574 |
| Mes: septiembre | -4.1767 | 3.8496 | -1.0849 | 0.2788 |
| Mes: octubre | -2.7915 | 3.8384 | -0.7272 | 0.4676 |
| Mes: noviembre | -5.8335 | 3.9263 | -1.4857 | 0.1384 |
| Mes: diciembre | -7.2182 | 4.2012 | -1.7181 | 0.0868 |
| Oxígeno Disuelto (Granja) | -0.4408 | 0.1553 | -2.8375 | 0.0048 |
| Salinidad (Granja) | -0.0039 | 0.0019 | -2.0667 | 0.0396 |
| pH en Agua (Granja) | -0.1034 | 0.0394 | -2.6204 | 0.0092 |
| Materia Orgánica (Granja) | 0.3915 | 0.2429 | 1.6116 | 0.1081 |
| pH en Sedimento (Granja) | 0.0667 | 0.0358 | 1.8622 | 0.0636 |
| NH4 en Agua (Granja) | 4.4103 | 2.0688 | 2.1317 | 0.0339 |
| NO3 en Agua (Granja) | -2.3772 | 1.3827 | -1.7192 | 0.0866 |
| Alcalinidad en Agua (Granja) | -0.0005 | 0.0001 | -2.8160 | 0.0052 |
Variables en negritas P < 0.05
El modelo indicó que la densidad de V. parahaemolyticus en el hepatopáncreas se incrementa en la medida en que la concentración de bacterias encontradas en el agua de los cuerpos costeros aumenta (Figura 4). Una tendencia similar de la concentración de bacterias en los sedimentos y en el agua, mostraron que concentraciones intermedias aumentaron la densidad de V. parahaemolyticus en el hepatopáncreas, sin embargo, concentraciones mayores a valores intermedios, mostraron una disminución (Figura 4).
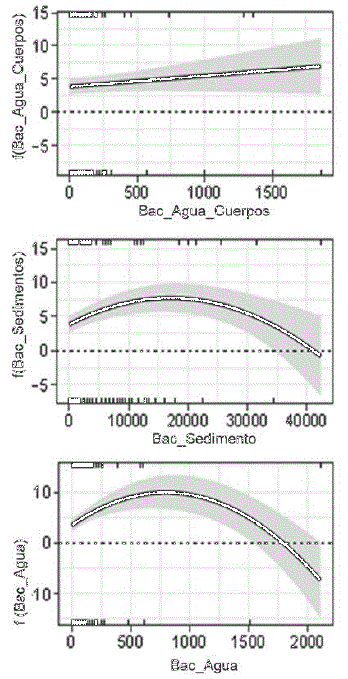
Figura 4 Efecto de la densidad (UFC/ml) de V. parahaemolyticus (Y) en agua de los cuerpos de agua costeros (a: X), en el sedimento de los estanques de (b: X) y en el agua de los estanques de cultivo (c: X)
En cuanto al ciclo de cultivo, el ciclo 1 favoreció mayormente la densidad de V. parahaemolyticus que el ciclo 2 (Figura 5a). De manera general, valores mayores del oxígeno disuelto, pH, Salinidad y los nitratos en el agua, la densidad de V. parahaemolyticus disminuyó (Figura 5b, c, d y h, respectivamente), contrario a lo que ocurrió con la materia orgánica, el pH del sedimento, la alcalinidad y el amonio, que mientras aumentaron sus valores, mayor densidad de V. parahaemolyticus se observó (Figuras 5e, f, g, e, i, respectivamente).
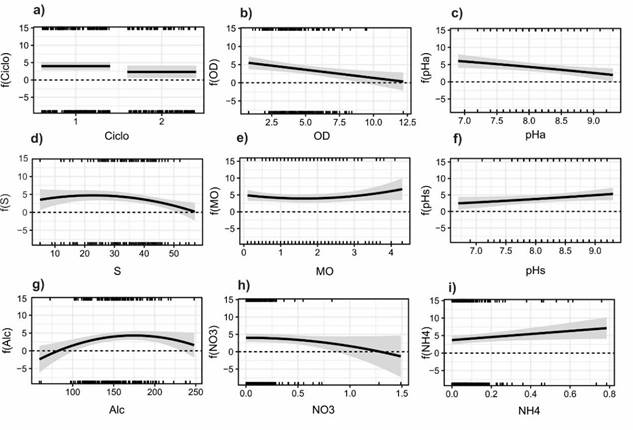
Figura 5 Influencia del ciclo de cultivo (a), oxígeno disuelto (mg/L) (b), pH en el agua (c), la salinidad (UPS) (d), materia orgánica (%) (e), pH de la materia orgánica de los estanques (f), alcalinidad (g), NO3 (h) y NH4 (i) sobre la densidad V. parahaemolyticus (UFC/g) en el hepatopáncreas de camarón f (Ciclo, OD, pHa, S, MO, pHs, Alc, NO3, NH4)
DISCUSIÓN
Las variables ambientales juegan un papel fundamental en el desarrollo del camarón, debido a su condición fisiológica y a que todos los procesos bioquímicos tienen efectos directos en la tasa de consumo de alimento y de oxígeno disuelto, excreción de amonio y crecimiento (Ferreira et al., 2011). En el presente estudio se observó para ambos ciclos de cultivo, promedios de temperatura, oxígeno disuelto, salinidad, pH y transparencia dentro del intervalo óptimo para P. vannamei en cultivo, valores de acuerdo a los reportados por otros autores como la temperatura de 25 °C a 32 °C (Carbajal-Hernández et al., 2011; Mateka et al., 2015); oxígeno disuelto de 4 a 7 mg/L (Alpuche et al., 2005); salinidad de 15 a 41 UPS (Pérez-Velázquez et al., 2007; Rivas-Montaño et al., 2018); pH de 6 a 9 (Carbajal-Hernández et al., 2013) y transparencia de 17 a 45 cm (García-Sánchez et al., 2018).
Los resultados del presente estudio mostraron que V. parahaemolyticus en agua de abastecimiento alcanzó máximos de 1.35E+04 UFC/ml y; en la zona Sur hasta un máximo de 4.94E+03 UFC/ml en agua de los estanques, por lo que presuntivamente el agua de abastecimiento funciona como un inoculo al ingresar al estanque de cultivo, como lo mencionan Orellana de Granados & Ayala-Mestanza (2017), estas bacterias muchas veces encuentran las condiciones para crecer por las combinaciones de múltiples factores como: las altas concentraciones de materia orgánica en los fondos, los suelos ácidos y la variación de los parámetros fisicoquímicos, entre otros. Esta proliferación de bacterias puede llegar a estar presentes en el hepatopáncreas y en la hemolinfa del camarón y ocasionar mortalidad (Orellana de Granados & Ayala-Mestanza (2017). Esto es de esperarse ya que el agua de cultivo de camarón utilizada en Sinaloa, naturalmente presenta densidades de Vibrio sp. superiores a 105 UFC/ml (Soto-Rodríguez et al., 2010). Esta información es trascendental si se tiene en cuenta la enfermedad de la necrosis hepatopancreática aguda (AHPND), ya que también Soto-Rodríguez et al. (2015) mencionan que entre los múltiples factores que afectan la virulencia de V. parahaemolyticus se encuentra la densidad, pues encontraron que la cepa M09-04 ocasionó 93 % de mortalidad a una densidad de 105 UFC/ml. Con respecto a la concentración de bacterias del género Vibrio en el hepatopáncreas del camarón Orellana de Granados & Ayala-Mestanza (2017) registraron densidades de Vibrio sp. de 1.10E+03 UFC/ml, presentando mortalidades de hasta 10 % en los primeros 30 días de cultivo. En este estudio se obtuvieron concentraciones superiores de V. parahaemolyticus de 3.00E+06 UFC/g con mortalidades máximas del 81 %, evidenciando la repercusión de las concentraciones de Vibrio sp. en las mortalidades. Estos resultados concuerdan con Soto-Rodríguez et al. (2015) señalando que la virulencia de las cepas de V. parahaemolyticus depende de la dosis, siendo la densidad infectiva umbral de 104 UFC/ml; no observando mortalidad por debajo de esa densidad. De igual manera Soto-Rodríguez et al. (2010) estima niveles de referencia de una posible vibriosis a partir de camarones enfermos a un umbral de 1.40E+05 UFC/g de Vibrio sp. en hepatopáncreas.
La supervivencia de Vibrio spp. en ambientes marinos depende de fuentes de carbono y energía, oxígeno disuelto, pH del agua, salinidad, temperatura e inanición (Takemura et al., 2014). En cuanto a las asociaciones de las variables fisicoquímicas, Hung-Sung et al. (2001) y Nelapati et al. (2012) mencionan que V. parahaemolyticus es un microorganismo que tiene la aptitud de vivir y desarrollarse en condiciones aerobias y anaerobias. Sin embargo, en el presente estudio se observó que en concentraciones superiores de 4.6 mg/L y cercanas a 12.5 mg/L de OD la densidad de V. parahaemolyticus disminuye considerablemente. Mientras que en concentraciones menores de 4.6 mg/L pero mayores que 2.5 mg/L de OD favorecen notablemente el incremento de la densidad de V. parahaemolyticus en el hepatopáncreas del camarón. Estos resultados son similares con los reportados por Van Wyk et al. (1999) quienes sugieren que a partir de registros de 3 mg/L de OD o menores en el agua de cultivo, se deben realizar acciones correctivas para disminuir la densidad de V. parahaemolyticus.
Con respecto a la asociación con la salinidad, V. parahaemolyticus puede tolerar un amplio rango de salinidades, pero sus condiciones óptimas de crecimiento varían. En aguas tropicales, V. parahaemolyticus fue encontrado en salinidades entre 20-35 ppt, con mayores densidades a 20 ppt (Rivera et al., 1989). Estudios experimentales mostraron una mejor adaptación a 10 y 20 UPS comparado con 39 y 60 UPS (Sami et al., 2022); esto concuerda con los resultados de este estudio donde se observó que a salinidades superiores a 34.2 UPS y cercanas a 50 UPS la densidad del V. parahaemolyticus disminuyó y a salinidades de 10-34.2 UPS la densidad de la bacteria fue mayor. Soto-Rodriguez et al. (2019) mencionan que la toxina puede expresarse a diferentes salinidades y que el manejo de la salinidad en el cultivo de camarón puede ser un factor importante para controlar la infectividad de V. parahaemolyticus.
Referente al pH en el agua, es importante resaltar que estudios sobre el impacto de pH en la aparición de Vibrio parahaemolyticus en el hepatopáncreas de camarones de cultivo son escasos, por lo que es fundamental seguir con este tipo de exploraciones para aclarar la influencia de este parámetro en la dinámica de la densidad de Vibrio parahaemolyticus. Los resultados de la presente investigación indican que las densidades de V. parahaemolyticus (UFC/g) aumentaron cuando el pH fue menor que 8.2 y la más elevada densidad del V. parahaemolyticus se presentó en valores de 7.0. Mientras que cuando el pH es mayor de 8.2 la densidad de Vibrio disminuyó hasta un pH de 9.0 en el que se encontró la menor densidad. Estos resultados contrastan con las investigaciones de Mancilla (2005) quien indica que V. parahaemolyticus tiene la capacidad de crecer en un intervalo de pH de 4.8 a 11; con un óptimo de crecimiento de 7.5 a 8.8 (FAO/WHO, 2011; Jurquiza, 2014).
En cuanto a la concentración de materia orgánica, diversos autores establecen que puede tener un efecto directo sobre la salud de los organismos en cultivo, dado que es capaz de modular las poblaciones bacterianas y la producción de metabolitos anaeróbicos tóxicos que dañan al camarón (Avnimelech & Ritvo, 2003; Nimrat et al., 2008). Merchán-Márquez (2017) establece que el porcentaje de materia orgánica óptimo en los suelos de los estanques de cultivo de camarón blanco es de 3 a 5%, ya que una acumulación excesiva de materia orgánica en los suelos, favorece la densidad de bacterias. Por otro lado, Díaz-Díaz & Arencibia-Carballo (1999), señalan que los valores de materia orgánica recomendados en el suelo del fondo de los estanques, es de 1.5% a 3 %. En la presente investigación la concentración promedio de MO fue de 2 %, concentración dentro del rango óptimo reportada por otros autores. Sin embargo, se observó que en concentraciones mayores que 2 % y menores que 0.5 %, la densidad de V. parahaemolyticus presente en el hepatopáncreas del camarón aumenta considerablemente, lo que podría deberse a la presencia del nitrógeno orgánico procedente del alimento balanceado presente en el sedimento, el cual promueve la formación de nueva biomasa bacteriana a partir de la metabolización de la misma (Paez-Osuna & Alonso-Rodríguez, 2017), o bien que, cuando la concentración de materia orgánica en el suelo del fondo de los estanques es muy alta o se encuentra en exceso (>4%), habrá condiciones idóneas para el desarrollo microbiano, por lo que existirán elevadas concentraciones de bacterias principalmente del género Vibrio (Díaz-Díaz & Arencibia-Carballo 1999; Nimrat et al., 2008).
La alcalinidad son ácidos bases como bicarbonato (HCO3 -), carbonato (CO3 2-) e hidróxido (OH-) responsables de neutralizar el agua. Ferreira et al. (2011) mencionan que el nivel de alcalinidad en los estanques de cultivo no debe pasar de los 140 mg/L de CaCO3 lo cual coincide con los resultados encontrados, ya que muestran que cuando el nivel de alcalinidad se encuentra entre los 150 y 200 mg/L, la densidad de V. parahaemolyticus en el hepatopáncreas del camarón es mayor, mientras que en niveles menores a 140 mg/L y mayores que 250 mg/L, la densidad de V. parahaemolyticus disminuye.
Con relación a los compuestos nitrogenados (NH4 +), (NO2 -) y (NO3 -) Tseng & Chen (2004), establecen que concentraciones altas de estos compuestos afectan el sistema inmune del camarón, dejándolo susceptible a la proliferación de bacterias o provocando trastornos fisiológicos como la oxidación de la hemocianina en meta hemocianina. Camargo et al. (2005) mencionan que el intervalo óptimo de (NO3 -) es de 0.4 a 1.3 mg/L, para (NO2 -), Boyd (1995) sugiere que una concentración adecuada para el desarrollo del camarón es <0.23 mg/L. Sin embargo, los resultados muestran que en concentraciones mayores que 0.5 mg/L de NO3 - la densidad de V. parahaemolyticus en el hepatopáncreas del camarón disminuye considerablemente, contrario a lo que ocurre con el NH4 + que la concentración de V. parahaemolyticus aumenta a mayor concentración de NH4 +. Este comportamiento es similar al reportado por Joseph et al. (1982) que establecen que la V. parahaemolyticus, no sobrevive en aguas con baja concentración de nutrientes; en tanto que Tantillo et al. (2004) informan que las sales de amonio constituyen la principal fuente de nitrógeno de V. parahaemolyticus, lo cual es coincidente con el presente estudio.
La predicción de la abundancia de presuntas especies de Vibrio puede ayudar a prevenir la aparición de enfermedades bacterianas, ya que esto proporciona información sobre cuándo y qué factores ambientales deben manejarse. Equito et al. (2022) utilizaron el modelo paramétrico de regresión lineal (LRM) y el modelo binomial negativo (NBM), así como el modelo semiparamétrico aditivo generalizado (GAM) para identificar correlaciones y predecir cambios en la abundancia de Vibrio con parámetros fisicoquímicos y biológicos del agua en estanques de biofloc con Penaeus vannamei. Estos autores encontraron que la abundancia de presuntas especies de Vibrio estaba altamente correlacionada con la alcalinidad, el pH y la densidad del fitoplancton. En el presente estudio, utilizando el modelo lineal generalizado (MLG) se mostró que a mayor salinidad, oxígeno disuelto, pH y nitratos en el agua la densidad de Vibrio disminuye (con valores fuera de los óptimos de V. parahaemolyticus), contrario a lo que se observó con los sedimentos, que a mayor pH, alcalinidad y amonio, aumentó la densidad de Vibrio; concluyendo que, al tener un incremento de concentración de bacterias en agua y sedimento, el modelo indicó un incremento en la concentración de bacterias en el hepatopáncreas del camarón. No obstante, Estrada-Pérez et al. (2019) y Estrada-Pérez et al. (2020) al utilizar un modelo estocástico de producción de camarón infectado por AHPND encontraron en el análisis de sensibilidad, que la mortalidad causada por la enfermedad, tiene una relación significativa con la salinidad y la transparencia del agua de los estanques. Estas diferencias en los resultados del presente trabajo, se deben a que no se consideró la enfermedad como tal, sino la densidad de bacterias de V. parahaemolyticus.
En esta investigación, la temperatura, transparencia y concentración de NO2 - y PO4 3- no exhibieron ningún efecto sobre la densidad de V. parahaemolyticus (UFC/g) en el hepatopáncreas del camarón. De acuerdo con el modelo que se utilizó, indirectamente se detectó que existe un 65.15% de factores que afectaron la densidad de V. parahaemolyticus en el hepatopáncreas del camarón, sin embargo, en la presente investigación, no fue posible medir o considerar fenómenos naturales en el ambiente de cultivo o variables de manejo, por lo que se recomienda incluirlos en investigaciones futuras para incrementar la capacidad predictiva. Se concluye que el modelo Lineal Generalizado explicó de manera adecuada la asociación de diversos factores con la concentración V. parahaemolyticus en el hepatopáncreas del camarón y cuyos resultados, de manera general son coincidentes con lo publicado en la literatura. Además, los resultados sugieren un monitoreo y manejo constante y efectivo para mantener los cultivos de camarón en los valores recomendados, que imposibiliten el aumento de las cargas bacterianas a niveles que afecten la salud del camarón.











 texto em
texto em