INTRODUCCIÓN
La carne de conejo desempeña un papel importante en la salud, economía rural y el desarrollo sostenible, por sus características nutricionales, como alto contenido de proteínas (20.3g/100g) y ácidos grasos insaturados (60.5%), bajo contenido en grasas (1.8-8.8g/100g), de colesterol (47mg/100g) y sodio (37-47mg/100g) (Siddiqui et al., 2023). Sin embargo, la cadena productiva enfrenta diversos problemas, principalmente relacionados con la sanidad animal y la calidad del producto. Los brotes de enfermedades, la mortalidad y los costos de alimentación afectan la rentabilidad (Mukaila, 2023). Una de las condiciones para el éxito de la cunicultura, es asegurar el bienestar epizootiológico de las UPC, la parasitosis afecta a la ganadería, ya que retrasan el crecimiento de los animales, pueden ocasionar su muerte y afectar la calidad de la carne (Gutyj et al., 2023).
El conocimiento de los factores de riesgo, del tipo de enfermedades, causas de muerte y tasas de prevalencia, permite implementar estrategias de manejo más eficientes (Espinosa et al., 2020). La coccidiosis del conejo es una enfermedad parasitaria causada por especies del género Eimeria (Xu et al., 2022). Los conejos afectados presentan diarrea, disminución del apetito, deshidratación, pérdida de peso, retraso en el crecimiento, lesiones hepáticas e intestinales y muerte (Exequiel et al., 2021).
Se reportan dos tipos de coccidiosis, la hepática causada por Eimeria stiedae, enfermedad devastadora, con alta morbilidad y mortalidad, que ejerce efectos patológicos sobre la integridad de los hepatocitos y la función hepática de los conejos (Athanasiou et al., 2023). A su vez Eimeria spp., causan coccidiosis intestinal que afectan a la mucosa, E. intestinalis y E. magna destruye la flora intestinal, lo que provoca cambios en los metabolitos y en los mecanismos moleculares de las interacciones conejo-parásito (Xu et al., 2022). Eimeria intestinalis induce inflamación intestinal, pérdida de células caliciformes, alteración de la microbiota (aumenta la población de Escherichia y Enterococcus) y los metabolitos yeyunales, así como la interacciones hospederomicrobioma (Xu et al., 2022).
El diagnostico morfológico, sigue siendo la herramienta para el diagnóstico de patologías asociadas a esta especie (Espinosa et al., 2020; Cordero del Campillo & Rojo, 2000). Mientras que la prevención y el control se logran implementando medidas higiénicas, con el uso de fármacos o productos anticoccidianos (Abd El-Ghany, 2020). El mecanismo de acción consiste en destruir las etapas intracelulares del parásito una vez que ha invadido las células hospederas, los productos sintéticos incluyen robenidina, decoquinato y diclazurilo (Kadykalo et al., 2018).
La administración de ionóforos ha sido un método eficaz para controlar las infecciones por Eimeria spp., sin embargo, por la presión política y social actual, se ha reducido y/o prohibido su uso en la ganadería (Ferreira et al., 2020). Compuestos fitoquímicos, han mostrado efectos preventivos, terapéuticos o inmunomoduladores contra la coccidiosis. Estos tratamientos se caracterizan por la ausencia de desarrollo de resistencia coccidial (Nahed et al., 2022).
En México, existen 11 mil 560 UPC con un millón 108 mil 350 conejos. Los estados con más UPC registradas son: el Estado de México con tres mil 885 y 293 mil 332 animales, e Hidalgo con mil 64 y 274 mil 811 conejos (SENASICA, 2020). Actualmente, se desconoce la situación sanitaria respecto a las especies del género Eimeria que prevalecen en las unidades de producción y la carga parasitaria presente en ellas; por lo que el objetivo, del presente estudio fue identificar morfológicamente y cuantificar especies del género Eimeria presentes en conejos naturalmente infectados en unidades de producción del Valle del Mezquital, Estado de Hidalgo.
MATERIAL Y MÉTODOS
El trabajo se realizó en 10 localidades de los municipios de Tezontepec de Aldama (20°11′26″ N, 99°16′27″ O, 2006 msnm), Mixquiahuala de Juárez (20°13′49″ N, 99°12′50″ O, 2002 msnm), Progreso de Obregón (20°14′50″ N, 99°11′24″ O, 1999 msnm), Francisco I. Madero (20° 14′ 43″ N, 99° 5′ 28″ O, 1980 msnm) y Ajacuba (20° 5′ 33″ N, 99° 7′ 10″ O, 2143 msnm) (Figura 1), pertenecientes al Valle del Mezquital Hidalgo, que por sus características presenta un clima semiárido, con suelos de riego y temporal, temperatura media anual de 18 °C y precipitación de 593 mm (Rosas et al., 2015).
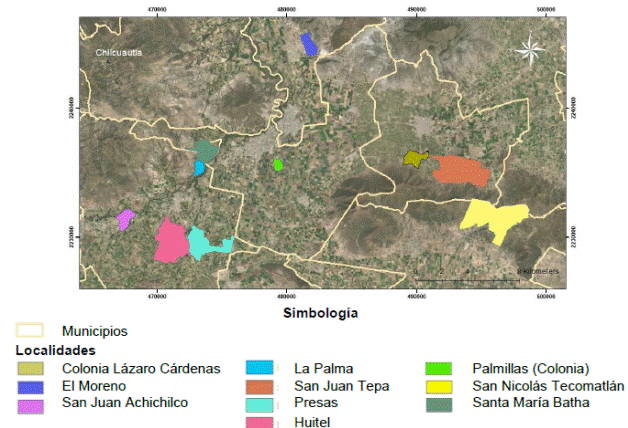
Figura 1 Ubicación geográfica de las localidades en las cuales se localizaron las UPC muestreadas para el estudio
Unidades de Producción
En las UPC se registró la raza, número de reproductores y tipo de alimentación, además de las características de las instalaciones y equipos que utilizan.
Colecta de las muestras
Se colectaron muestras de heces de 32 conejos (por unidad) en 10 UPC de 5 municipios del Valle del Mezquital con productores cooperantes, de razas Nueva Zelanda Blanco (NZB), California (CAL), Chinchilla (CH), Azteca Negro (AZN) y Satinado (ST), de entre 30 y 60 días de edad (período de engorda), alojados en jaulas de alambre galvanizado en grupos de 8 animales en promedio.
Para garantizar la integridad de las muestras, estas se transportaron a temperatura de refrigeración (4ºC) al laboratorio del Área Académica de Medicina Veterinaria y Zootecnia (AAMVZ), en el Instituto de Ciencias Agropecuarias (ICAp) de la Universidad Autónoma del Estado de Hidalgo (UAEH), para su identificación morfológica y determinación de carga parasitaria.
Identificación morfológica
Para la identificación de las especies del género Eimeria presentes en los conejos, se utilizó la técnica de flotación, usando una solución saturada de NaCl y observando al microscopio a 10X y 40X para su identificación cualitativa con criterios de medición y comparación morfológica (Cordero del Campillo & Rojo, 2000).
Determinación de carga parasitaria
Para determinar la cantidad de OPG, se utilizó la técnica de McMaster. El número de OPG fue calculado sumando el resultado del recuento de ambas cámaras y multiplicando por 50 (Sandoval et al., 2011). Se realizaron cuatro repeticiones por Unidad de producción cunícola.
Análisis estadístico
Los datos de carga parasitaria se normalizaron mediante √ꭓ+0.5 para realizar un análisis de media principal en el programa Minitab® Statistical Software MiniTab, (2021).
RESULTADOS
De acuerdo con el análisis de los resultados, la raza de conejo predominante en las unidades de producción fue Nueva Zelanda presente en el 80% de las granjas, seguido de la raza California con el 50%, y que corresponde a productores que utilizan cruzamiento con estas dos razas. En cuanto a la alimentación, en 7 de las 10 granjas proporcionan alimento comercial en forma de pellets, mientras que una alimenta únicamente con alfalfa verde, otra con alimento comercial y alfalfa y una más con una combinación de concentrado comercial, alfalfa y nopal (Tabla 1).
Tabla 1 Características de las Unidades de producción cunícola en la región Valle del Mezquital
| Raza | No. de reproductores | Alimentación | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| Granja | Nueva Zelanda Blanco | California | Chinchilla | Azteca Negro | Satinado | Hembras | Machos | Concentrado | Alfalfa | Concentrado + alfalfa | Concentrado + alfalfa + nopal |
| 1 | 1 | 1 | 13 | 2 | 1 | ||||||
| 2 | 1 | 1 | 40 | 5 | 1 | 1 | |||||
| 3 | 1 | 1 | 55 | 17 | 1 | ||||||
| 4 | 1 | 1 | 1 | 100 | 11 | 1 | |||||
| 5 | 1 | 30 | 5 | 1 | |||||||
| 6 | 1 | 30 | 4 | 1 | |||||||
| 7 | 1 | 35 | 5 | 1 | |||||||
| 8 | 1 | 1 | 36 | 8 | 1 | ||||||
| 9 | 1 | 1 | 17 | 3 | 1 | ||||||
| 10 | 1 | 36 | 10 | 1 | |||||||
| Total | 8 | 5 | 1 | 1 | 2 | 392 | 60 | 7 | 1 | 1 | 1 |
Respecto al diseño de instalaciones y equipo disponible, en la tabla 2 se observa que la mayoría de los techos de las granjas (9/10) están elaborados con láminas de hierro, solo una utiliza lámina de asbesto. El 50% de las paredes de las granjas es de block y el 50% utiliza malla ciclónica. El 60% tienen piso de cemento y el 40% no cuenta con piso firme (tierra).
Las jaulas son americanas de alambre galvanizado en el 80% de las UPC, acomodadas en flat deck (calibre 14), el 20% utiliza módulos de alambre galvanizado (calibre 12). El 50% utiliza comederos tipo tolva que permite un uso más eficiente del alimento, el 40% alimenta en comederos tipo J y solo un productor alimenta con alfalfa sobre las jaulas (10%). El 70% proporciona agua en recipientes de plástico o de acero inoxidable y sólo el 30% utiliza bebederos automáticos de chupón (Tabla 2).
Tabla 2 Tipo de instalaciones y equipo que se utilizan en UPC del Valle del Mezquital, Hidalgo
| Techo | Piso | Pared | Jaula | Comedero | Bebedero | Nidos | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Granja | Lámina | Asbesto | Tierra | Concreto | Block | Malla | Individual | Modulo | Tipo J | Tipo tolva | Forrajera | Plástico | Acero | Automático | Lámina | Plástico | Madera |
| 1 | X | X | X | X | X | X | X | ||||||||||
| 2 | X | X | X | X | X | X | X | ||||||||||
| 3 | X | X | X | X | X | X | X | ||||||||||
| 4 | X | X | X | X | X | X | X | ||||||||||
| 5 | X | X | X | X | X | X | X | ||||||||||
| 6 | X | X | X | X | X | X | X | ||||||||||
| 7 | X | X | X | X | X | X | X | ||||||||||
| 8 | X | X | X | X | X | X | X | ||||||||||
| 9 | X | X | X | X | X | X | X | ||||||||||
| 10 | X | X | X | X | X | X | X | ||||||||||
| Total | 9 | 1 | 4 | 6 | 5 | 5 | 8 | 2 | 4 | 5 | 1 | 4 | 3 | 3 | 3 | 6 | 1 |
Identificación de especies del género Eimeria
En las UPC del área de estudio, se identificaron los dos tipos de coccidiosis, la hepática ocasionada por E. stiedae y la coccidiosis intestinal causada por diferentes especies de Eimeria spp (Tabla 3). E. stiedae fue identificada en 8 UPC, en un rango de 19 al 100%, seguido de E. irresidua con presencia en 5 UPC con un mínimo de 17 y un máximo de 63.6 %, y de E. exigua, al encontrarse en 4 UPC entre el 23.5 y 100%. E. intestinalis y E. flavescens son las que producen coccidiosis intestinal más severa y se identificaron en 2 y una UPC, con una tasa de infección de 26 y 9%, respectivamente. Se identificaron además E. magna, E. media, E. piriformis, E. perforans, E. coecicola.
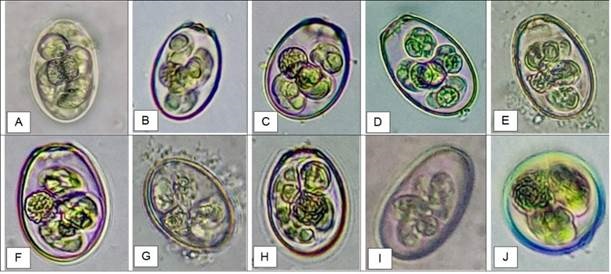
Figura 2 Morfología de los ooquistes de las especies del género Eimeria identificadas en las UPC del Valle del Mezquital, Hidalgo. A) E. stiedae, B) E. flavescens, C) E. intestinalis, D) E. magna, E) E. media, F) E. irresidua, G) E. piriformis, H) E. perforans, I) E. coecicola, J) E. exigua
Cuadro 3 Porcentaje de especies del género Eimeria en UPC del Valle del Mezquital, Hidalgo
| Especie | Unidades de Producción Cunícola | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | |
| E. stiedae | 23.4 | 19 | 44 | 45 | 48 | 100 | 30.9 | 36 | ||
| E. flavescens | 9.3 | |||||||||
| E. intestinalis | 28 | 24 | ||||||||
| E. magna | 24 | 11.7 | ||||||||
| E. media | 47.6 | 39 | 14.7 | |||||||
| E. irresidua | 63.6 | 17 | 28 | 28 | 31 | |||||
| E. piriformis | 9 | |||||||||
| E. perforans | 18 | 4.5 | ||||||||
| E. coecicola | 19.7 | 29 | 14.7 | |||||||
| E. exigua | 36.4 | 100 | 23.5 | 33 | ||||||
Porcentaje de infección de especies de Eimeria spp. en UPC
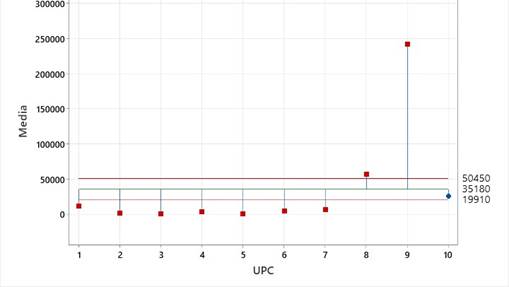
De las 10 UPC analizadas, el 100% resultaron positivas a Eimeria spp., en la figura 3, se observa que existen diferencias estadísticas significativas en la cantidad de OPG entre UPC, siendo las UPC 9 (241450 ± 33555) y 8 (56817 ± 3907) las que presentaron una cantidad superior a la media de OPG, mientras que las cargas inferiores a la media se encontraron en la UPC 1 (11417 ± 1051), 7 (6367 ± 1614), 6 (4500 ± 816), 4 (3217 ± 437), 2 (1583 ± 246), sin mostrar diferencias significativas entre la UPC 5 (583 ± 125) y 3 (433 ± 85), siendo solo la UPC 10, la que presentó una cantidad de OPG que se encontró dentro de los límites de decisión.
DISCUSIÓN
Las especies del género Eimeria que se identificaron en el presente estudio corresponden a diez de las 11 especies reportadas a nivel mundial que afectan al conejo. La presencia de varias especies obliga a determinar si pueden actuar sinérgicamente, y si con dos o más especies, aumenta la patogenicidad (García et al., 2017). Según Gabriele & Daniel, (2019), Clostridium spiroforme y Eimeria spp., se asocian con enfermedades gastrointestinales en conejos jóvenes y pueden provocar altas tasas de morbilidad y mortalidad. Serge et al., (2020), refieren que los conejos son susceptibles a la coccidiosis al principio y al final de la lactancia mientras que la sensibilidad de los gazapos es más evidente en los días posteriores al destete, donde las reproductoras juegan un papel importante en la transmisión de la coccidiosis.
Las UPC se clasificaron como pequeño y mediano cunicultor según la clasificación de Vélez et al., (2023), quienes las clasifican con base en su capacidad productiva, capacidad del cunicultor y eficiencia técnica: pequeño cunicultor familiar (37%), mediano cunicultor familiar (50%) y cunicultor empresarial (13%), y de acuerdo con Shkromada & Nedzheria, (2020), tanto en granjas comerciales como familiares, la infección más común es por E. perforans, E magna, E. media, E. irresidua, E. piriformes y E. іntestinalis.
En el Valle del Mezquital, las razas NZB y CAL son las más utilizadas, observándose también que presentan la mayor carga parasitaria, coincidiendo con lo reportado por Shola et al., (2019), quienes mencionan que la raza y el tipo de alojamiento son factores de riesgo significativos asociados con la infección de Eimeria spp. Por su parte, Pilarczyk et al., (2020), no reportan diferencias significativas en la infección por especies del género Eimeria con respecto al género, pero sí por la edad y densidad por jaula, siendo mayor en conejos menores de 6 meses y agrupados, en relación con los alojados individualmente.
Las características de las jaulas (modelo y calibre) y equipo (comederos y bebederos) utilizados en las UPC del Valle del Mezquital permiten la reproducción de especies del género Eimeria, y coincide con Legendre et al., (2019), quienes mencionan que los gazapos se infectan por vía oral, al consumir alimentos o agua contaminados con ooquistes, incrementado la posibilidad de ser infectados cuando son alimentados con forrajes. Henneb et al., (2022), mencionan que la población de Eimeria spp., es significativamente mayor en las granjas que no cumplen con buena higiene, agua y alimento de calidad. Gerbil et al., (2023), indican que el tipo y la calidad de los equipos utilizados en la producción de conejos, debe cubrir las necesidades de alimento y confort, evitando su contaminación con heces.
Por su parte, Shkromada et al., (2019), describen que el parásito se propaga a través de animales enfermos y se conserva bien en el ambiente externo. Los ooquistes de coccidios viven en las células durante mucho tiempo, por lo que el desalojo temporal de los animales no previene la infección. Shola et al., (2019), reportan que los conejos mantenidos en "batería" presentan una tasa de prevalencia más alta (95.2%) en comparación con los criados en el sistema "flat-deck" (71.9%). Según Shkromada & Nedzheria, (2020), el manejo en jaulas metálicas, cumpliendo con las normas sanitarias e higiénicas y la desocupación oportuna, reduce el nivel de la infección por Eimeria spp. Mientras que Hamid et al., (2019), mencionan que los parásitos son ubicuos en el medio ambiente y se transmiten por vía fecal-oral.
En las UPC del Valle del Mezquital, se identificaron 10 de las 11 especies del género Eimeria reportadas en conejos de acuerdo con Qin et al., (2023), son. Además, de encontrarse de 8 a 1 especie en la misma UPC, datos similares a lo reportado por Serge et al., (2019), quienes al registrar por siete meses la dinámica de excreción de ooquistes en reproductoras y sus crías, en el 100% de los animales encontraron altas concentraciones de ooquistes, con 7 especies de coccidios, coexistiendo en un mismo individuo. Maziz et al., (2018), al evaluar la prevalencia de coccidias en granjas de conejos en el norte de Argelia, identificaron ocho especies del género Eimeria, reportando que las infecciones mixtas con cuatro especies fueron comunes, siendo E. magna la especie dominante, en comparación con E. media y E. irresidua con frecuencias respectivas de 42.5%, 17.6% y 14.9% (p<0.001).
De las especies identificadas en el presente estudio, según Takami et al., (2023). E. intestinalis y E. flavescens, causan coccidiosis intestinal, y E. stiedae, causa coccidiosis hepática, presentando alta virulencia. A su vez, Athanasiou et al., (2023), reportan que Eimeria stiedae, es una enfermedad devastadora con altas tasas de morbilidad y mortalidad, sin embargo, Laha & Goswami, (2023), afirman que sólo la coccidiosis intestinal puede causar alta mortalidad en conejos. Anak & Sarayati, (2023), mencionan que la vía de transmisión ocurre cuando los conejos consumen alimentos y bebidas contaminados con ooquistes. Por su parte Eimeria magna se caracteriza por ser levemente patógena y moderadamente inmunogénica (Geru et al., 2017). Provocando letargo, pérdida de peso, diarrea e incluso la muerte en casos graves (Chen et al., 2023).
En las UPC del presente estudio, las muestras se recolectaron en conejos de engorda (30 a 60 días de edad) por ser una etapa donde se presentan grandes pérdidas económicas, asociadas a diarreas. Elhendy et al., (2018), reportan una prevalencia del 88% en conejos menores de 4 meses. Según estudios de El-Ashram et al., (2020), el 86.50% (198/229) de los conejos después del destete, fueron infectados por E. media, E. perforans, E. intestinalis, E. magna, E. coecicola, E. exigua y E. flavescens.
Sun et al., (2016), refieren que las especies del género Eimeria en conejos, solo son capaces de infectar a ciertos hospederos, y que, durante la infección, se produce la división y crecimiento celular, inflamación en el intestino para reemplazar los enterocitos dañados, siendo necesario el colesterol como constituyente esencial de la membrana celular. A su vez, Manjunatha et al., (2019), observaron en los conejos afectados, retraso en el crecimiento, anorexia, pérdida de peso, diarrea, dolor abdominal y muerte súbita, mientras que en la bioquímica sanguínea se reporta un aumento de las enzimas hepáticas y la bilirrubina.
Por su parte, Petrova et al., (2022), al realizar la necropsia de conejos infectados con Eimeria stiedae, revelaron hepatomegalia, nódulos amarillentos multifocales difusamente repartidos por la superficie del hígado y en el parénquima, conductos biliares dilatados e hiperplasia biliar, además, Manjunatha et al., (2019), identificaron numerosos ooquistes de E. stiedae, encontrándose múltiples áreas de necrosis coagulativa de células hepáticas rodeadas de células inflamatorias. Según Chatterjee et al., (2023), esta situación clínica prevalece en diferentes órganos como páncreas, hígado y ciego.
De acuerdo con Taraneh et al., (2011), los animales afectados presentan pérdida de peso, con reservas de grasa reducidas y atrofia muscular, pelo hirsuto y material fecal adherido al pelo en el perineo, se observan cambios patológicos macroscópicos en el intestino delgado, distendidos y llenos de una ingestión semisólida de color verde grisáceo, la mucosa intestinal severamente hiperémica y edematosa. De igual forma, Sidorenko et al., (2020), identificaron en secciones histológicas del intestino delgado, merozoitos, enterocitos dañados, así como acumulaciones de linfocitos y eosinófilos.
La variabilidad de OPG de las UPC del Valle del Mezquital fue alta, solo una UPC registró una población <500 OPG, que de acuerdo con Anak y Sarayati et al., (2023), se considera una infección leve y sin capacidad de generar daño. A su vez, Sidorenko et al., (2020), al evaluar la intensidad de infección de E. perforans y E. irresidua inoculando con 50-60 mil ooquistes por conejo de 40 días de edad, reportaron que la ganancia máxima de peso vivo y el rendimiento en canal, disminuyen en conejos híbridos F1 Chinchilla x California. Por su parte, Balicka et al., (2020), reportan que el número de OPG muestra también grandes fluctuaciones en el año, siendo más alta en el mes de mayo (21100 OPG).
Tokiwa et al., (2022), mencionan que las especies del género Eimeria pueden transmitirse horizontalmente a través de ooquistes, siendo problemático en entornos cerrados. Mientras que Chatterjee et al., (2023), reportan que la temperatura adecuada puede desencadenar la esporulación y complementar su ciclo de vida. Además, Shkromada et al., (2019), señalan que es imposible eliminar totalmente los coccidios, a pesar de acidificar todos los días el agua, porque al disminuir la concentración terapéutica los conejos se enferman. La acidificación con ácidos fórmico, ortofosfórico, sórbico y ácido cítrico a un pH de 3,5 y una exposición de 60 minutos elimina del 50 al 90 % de ooquistes. Un pH 3,5 a 4,5 no causa destrucción del epitelio de la mucosa. De igual forma Hamid et al., (2019), reportan que la aplicación de medidas de bioseguridad mediante la eliminación de los ooquistes en las heces antes de que esporulen reduce la cantidad de ooquistes con capacidad infecciosa.
La alta concentración de OPG en por lo menos 9 de las 10 granjas evaluadas podrían afectar de manera considerable las utilidades de las UPC, ya que según Chatterjee et al., (2023), aproximadamente el 70% de los costos estimado por coccidiosis subclínica, se debe a que se afecta la ganancia de peso y la conversión alimenticia, siendo necesario implementar medidas eficientes de prevención y control para evitar pérdidas económicas.
De acuerdo con Chen et al., (2023), un método para prevenir la coccidiosis en conejos es usar fármacos anticoccidiales en la dieta, sin embargo, existe preocupación sobre la resistencia y la presencia de residuos (de los fármacos) en la canal. A su vez, Xiao et al., (2022), recomiendan el uso de vacunas como estrategia de medicina preventiva. Por su parte, Rivero et al., (2019), proponen el uso de productos antimicrobianos obtenidos a partir de plantas y árboles como Salix babylonica (Sauce llorón) como alternativa para el control de coccidiosis en conejos naturalmente infectados, ya que con la administración de 25 y 50 mg/kg de peso vivo, logró disminuir la eliminación OPG, efecto asociado a su composición fitoquímica (cumarinas, triterpenos, flavonoides, lactonas sesquiterpénica, saponinas, terpineno, linalol, timol y carvacrol). Mientras que Nahed et al., (2022), reportan que, en pollos, los compuestos fenólicos disminuyen el recuento de ooquistes de Eimeria spp. al reaccionar con las membranas citoplasmáticas, causando lisis y destrucción del protozoario.
CONCLUSIONES
Eimeria spp., están presentes en el 100% de las Unidades de Producción Cunícola muestreadas en el Valle del Mezquital, en el 80% de los casos se presentaron como infecciones mixtas con la presencia de más de una especie. La cantidad de OPG (más de 500) pone en riesgo la salud de los animales y obliga a implementar programas de prevención y/o controles efectivos que consideren la reducción en el uso de fármacos.











 texto em
texto em