INTRODUCCIÓN
La mastitis bovina es la inflamación de la glándula mamaria, causada por la invasión de microorganismos patógenos que destruyen los tejidos secretores de leche. En la etiología bacteriana se reportan más de 100 especies asociadas a mastitis bovina (Sharun et al., 2021; Morales et al., 2023). Las bacterias más frecuentes en los casos de mastitis son: Staphylococcus aureus, Streptococcus agalactiae, Streptococcus uberis, Streptococcus dysgalactiae, Escherichia coli, Klebsiella pneumoniae, Pseudomonas aeruginosa y Staphylococcus coagulasa negativos (Pascu et al., 2022; Morales et al., 2023).
El tratamiento de la mastitis se realiza con la administración de antimicrobianos de origen químico, sin embargo, su uso continuo y desmedido ha inducido el desarrollo de resistencia antimicrobiana, generando una problemática mundial en la salud animal y humana, por la interacción de las bacterias de estas dos poblaciones y la transferencia de resistencia intergénica (Galarza et al., 2021; Wang et al., 2021; Li et al., 2023). La resistencia bacteriana genera un incremento del costo en el tratamiento y eliminación prematura de animales, lo anterior ha estimulado a la comunidad científica a la búsqueda de nuevas alternativas para el tratamiento de la mastitis bovina (Kovačević et al., 2022; Morales et al., 2023).
Dentro la diversidad florística, el orégano mexicano Lippia graveolens es una planta de interés por su composición fitoquímica, esta arbustiva silvestre se ha utilizado con fines culinarios y en medicina tradicional para tratar enfermedades respiratorias, digestivas, cuadros de inflamación, dolores de cabeza y reumatismo (Bautista et al., 2021). Existen reportes que evidencian la actividad antibacteriana de L. graveolens con diferentes metodologías de extracción de metabolitos secundarios y concentraciones a las cuales se ha determinado la actividad antibacteriana contra diversas géneros bacterianos incluyendo los asociados a mastitis bovina (Bautista et al., 2021;Cortés et al., 2021; Kovačević et al., 2022; Garcia et al., 2022). El objetivo de la presente investigación fue realizar una revisión bibliográfica de L. graveolens y su actividad contra bacterias asociadas a mastitis bovina.
METODOLOGÍA
Para llevar a cabo la presente revisión se realizó una búsqueda exhaustiva en las siguientes bases de datos: PubMed, ScienceDirect y Google académico, de estudios publicados hasta 2024. Se utilizaron los siguientes encabezados y palabras clave: L. graveolens, extractos vegetales, mastitis bovina y actividad antibacteriana. Se revisaron los documentos de texto completo y se eliminaron los documentos duplicados. Los criterios de exclusión fueron métodos inadecuados y falta de acceso al texto completo.
BOTÁNICA DE LA PLANTA
L. graveolens es una planta arbustiva perenne, alcanza dos metros de altura, presenta ramas de corteza exfoliante con hojas pecioladas opuestas, ovaladas lanceoladas, haz rugoso escabroso, estrigoso glandular, envés densamente piloso, ápice obtuso y margen diversamente crenado (Ocampo et al., 2009). La floración se presenta en época con mayores precipitaciones (Bueno, 2014), su inflorescencia es indeterminada de tipo espiga subglobosas, corolas blancas, zigomorfas, con flores pequeñas de 4 mm hermafroditas, en cantidades de 2 a 20 flores, presenta frutos pequeños de cápsulas indehiscentes, con semillas sin endospermo (Figura 1) (Ocampo et al., 2009).
La planta es silvestre, se encuentra en cerros de zonas templadas, áridas y semiáridas de México, se adapta entre 1400 a 2300 metros de altitud, en suelos pedregosos de textura franco-arenosa, prefiere clima tipo seco y semiseco, con temperatura de 20 a 24ºC y precipitación de entre 182 a 267 mm (Figura 1) (Martínez et al., 2014). Es una planta aromática, su uso es culinario y en la herbolaria para el tratamiento de padecimientos digestivos. En Chihuahua, Durango, Tamaulipas, Coahuila, Jalisco, Zacatecas, Querétaro, Hidalgo y Baja California, se colecta su follaje para su comercialización en los mercados locales (Bueno, 2014).
COMPOSICIÓN FITOQUÍMICA
La caracterización fitoquímica de L. graveolens a partir de extractos acuosos, hidroalcohólicos y aceites esenciales, muestra diferencias en su composición fitoquímica (González et al., 2017; Bernal et al., 2022). La extracción se ha realizado con técnicas convencionales como la maceración con alcoholes y agua a diferentes proporciones, y por tecnologías actuales como extracción asistida por ultrasonido con uso de solventes eutécticos y extracción con fluido supercrítico mediante dióxido de carbono como disolvente (Bernal et al., 2023). La presencia de metabolitos difiere por los métodos de extracción como se observa en la Tabla 1, destacando los compuestos fenólicos y monoterpenos (González et al., 2017).
Tabla 1 Compuestos fitoquímicos identificados en extractos vegetales de Lippia graveolens
| Extracto | Método de extracción | Solvente | Compuestos | Referencia |
|---|---|---|---|---|
| Acuoso | Ultrasonido y fluido supercrítico mediante CO2 | Cloruro de colinaetilenglicol, cloruro de colina-glicerol y Cloruro de colinaácido láctico. | Ácido cafeíco, protocatequico y rosmarínico. Quercetina, luteolina, naringenina, eriodictiol. carvacrol | Garcia et al. (2022) González et al. (2017) Soto et al. (2019) Bernal et al.(2023) |
| Hexano | Maceración | Hexano | Timol, m -cimen-8-ol, salicilato de metilo, carvacrol y linalol. | González et al., 2017 |
| Acetato de etilo | Maceración | Acetato de etilo | p –cimeno, timol, cirsimaritina, naringenina | |
| Etanólico | Maceración | Etanol CO2 supercrítico modificado con etanol después de destilación al vapor | Naringenina, taxifolina, eriodictiol, ácido cafeico, luteolina, ácido cummarico, Quercetina 3 O-glucósido, Ácido 2-hidroxibenzoico, apigenina, quercetina, floridzín, acacetina, sakuranetina, cirsimaritina, crisoeriol. | Arias et al. (2023) Bernal et al. (2023) González et al. (2017) |
| Hidroalcohólico | Maceración | Metanol y Cloroformo | Loganina, secologanina, secoxiloganina, dimetilsecologanosido, ácido logánico, ácido 8-epi-logánico, ácido carioptosídico y sus derivados 6-O-p-coumaroil y 6-O-cafeoil, naringenina,pinocembrina, lapachenol e icterogenina, luteolina-7-O-glucósido, apigenina 7-O-glucósido, floridzina, taxifolina, eriodictiol, escutellareína, luteolina, quercetina y galangina. | Cortes et al. (2021) Picos et al. (2021) Leyva et al. (2016) Rastrelli et al. (1998) Lin et al. (2007) |
| Aceite esencial | Hidro- destilación | Carvacrol, acetato de α-terpinilo, m-cimeno, timol, β-pineno y α-thujeno, linalool humuleno Sesquiterpeno: isocariofileno, γ-terpineno. | Hernández et al.(2009) Martínez et al. (2014) Nonato et al. (2022) Castillo et al. (2023) |
En L. graveolens los flavonoides de mayor presencia son: la quercetina, luteolina, naringenina, eriodictiol, luteolina, hesperidina y floridzina (Bernal et al., 2023). Los metabolitos; naringenina, quercetina floridzina y cirsimaritina son marcadores químicos del género de Lippia (Bernal et al., 2022). En extracto metanólico de hojas se obtiene mejor perfil de flavonoides, se han encontrado tres iridoides mayoritarios: ácido carioptosídico con dos derivados: 6’-O-p-coumaroil y 6’-O-cafeoil, y siete iridoides minoritarios: loganina, secologanina, secoxiloganina, dimetil, secologanosido, ácido logánico, ácido 8-epi-logánico y carioptosido (Rastrelli et al., 1998; Lin et al., 2007). Los monoterpenos son los componentes principales de los aceites esenciales del género Lippia (Cortés et al., 2021; Bernal et al., 2023). En extractos a base de agua, hexano, acetato de metilo y en procesos de hidrodestilación para la obtención de aceite esencial, se reportan la presencia de los monoterpenos: timol, carvacrol, limoneno, b -cariofileno, r -cimeno, canfor, linalol, a -pineno, los cuáles pueden variar de acuerdo al quimiotipo y método de extracción (Calvo et al., 2014; Garcia et al., 2022). Al respecto Vernin (2001) reportó que el aceite esencial de L. graveolens de México y Centroamérica presentan concentraciones del 35 al 71 % de carvacrol y del 5 al 7 % de timol. Calvo et al. (2014) reportaron la presencia de más de 70 compuestos en sus aceites esenciales, identificaron tres quimiotipos de la planta: dos fenólicos (carvacrol y timol) y un quimiotipo no fenólico de sesquiterpenos oxigenados (β-cariofileno, α-humuleno y óxido de cariofileno). El hábitat de la planta determina la composición de aceite, la mayor concentración de carvacrol se ha obtenido de plantas que crecen en clima semiárido, con suelos delgados y rocosos (Torres et al., 2022). Sin embargo, existen reportes de plantas jóvenes que crecen en condiciones menos áridas y con suelos profundos, lo que proporciona mayor presencia de timol y las que crecen en clima subhúmedo presentan mayor cantidad de sesquiterpenos oxigenados (Llamas et al., 2022).
METABOLITOS Y ACTIVIDAD ANTIBACTERIANA
Terpenos
El carvacrol y el timol son de mayor presencia en L. graveolens (Calamaco et al., 2023), su concentración se afecta por factores edáficos y climáticos del hábitat de la planta (Cortés et al., 2021). El carvacrol (2-metil-5-1-metiletilfenol) proporciona el aroma característico del orégano (Ultee et al., 2000). Se sintetiza a partir del cimeno por la vía del mevalonato, es un monoterpeno insoluble en agua y soluble en etanol, tetracloruro de carbono y éter dietílico (Lee et al., 2017). Su estereoquímica (Figura 2) de un solo anillo fenólico con tres sustituyentes de grupos funcionales (Memar et al., 2017) le otorgan propiedades antibacterianas, antioxidantes, anticancerígenas y antiinflamatorias (Tapia et al., 2017).
En bacterias el carvacrol induce lisis celular por cambios en los compuestos lipofílicos y las partes hidrofóbicas de la membrana citoplasmática, incrementa la permeabilidad de los cationes (H + y K +), genera salida de lipopolisacáridos y producción de especies reactivas de oxígeno, inhibe actividad de las ATPasas, la replicación del ADN microbiano y la síntesis de energía, causando muerte celular (Gallegos et al, 2022). Sin embargo, Ultee et al. (2000) reportaron que las bacterias pueden adaptarse al carvacrol y modificar la composición de ácidos grasos de la membrana y reducir su permeabilidad.
El timol es un isómero de Carvacrol (Figura 2), es una sustancia aromática de coloración cristalina blanca, de baja solubilidad en agua y alta en solventes orgánicos, con pH neutro, pero puede tener características alcalinas en soluciones acuosas debido a la desprotonación del fenol (Chizzola, 2013). Presenta actividad bactericida, fungicida, insecticida, nematicida, varroocida (Gallegos et al., 2022). Se ha reportado su efecto antibacteriano in vitro contra Escherichia coli, Salmonella spp. y S. aureus a una concentración de 0.75 mg/mL (Shapira-Mimran 2007; Gallegos et al., 2019). En concentraciones de 1 % y 2 % en aceite esencial de orégano, tiene mayor actividad antimicrobiana contra bacterias Gram positivas y menor sobre bacterias Gram negativas (Du et al., 2015; Erazo et al., 2017). En estudios in vitro sobre enterobacterias Gram negativas se encontró mayor actividad antibacteriana del timol de Lippia berlandieri a diferencia de otros antimicrobianos (Garcia et al., 2022; Garcia et al., 2022). El mecanismo de acción antibacteriano es similar al de carvacrol, se une a las membranas bacterianas de manera hidrofóbica por puentes de hidrógeno afectando la membrana externa e interna, incrementando la permeabilidad y la pérdida de iones de potasio y ATP intracelular, ocasionando la muerte celular (Di Pasqua et al., 2010).
Flavonoides
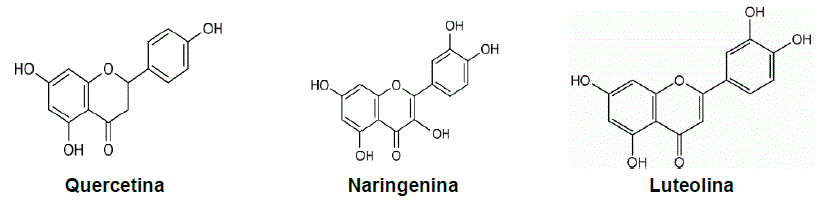
En L. graveolens los flavonoides (Figura 3) con mayor reporte de actividad biológica son naringenina, quercetina y luteolina (Lin et al., 2007). La naringenina es un compuesto bioactivo con actividad hepatoprotectora, antiaterogénica, antiinflamatoria, antimutagénica, anticancerígena y antimicrobiana (Ke et al., 2017). En reacción con yoduros de alquilo forma compuestos de O-alquilo de naringenina con potencial antibacteriano contra Escherichia coli, Staphylococcus aureus y Bacillus subtilis (Kozłowska et al., 2019). Un derivado de O-alquilo naringenina, es la sakuranetina (7-Ometilnaringenina) con importante actividad antimicrobiana frente a bacterias Gram negativas y Gram positivas. La naringenina inhibe el crecimiento de Staphylococcus aureus, afectando la membrana celular y la composición de ácidos grasos. En Escherichia coli actúa a nivel de los genes asociados a la biosíntesis de ácidos grasos de la membrana (Wang et al., 2018).
La quercetina es un flavonol, basado en la estructura de flavona nC6 (anillo A)-C3 (anillo C)-C6 (anillo B). Su actividad antibacteriana es de amplio espectro, rompe la pared celular de las bacterias, inhibe la síntesis de ácidos nucleicos y reduce de la actividad enzimática (Wang et al.,2018), específicamente en Escherichia coli altera la actividad del trifosfato de adenosina (Plaper et al., 2003). Según Hooda et al. (2020), la impregnación de quercetina con nanopartículas de plata inhibe el crecimiento de bacterias: Klebsiella pneumoniae (ATCC790603), Enterococcus faecalis (ATCC51299), Proteus vulgaris (ATCC426), Escherichia coli (ATCC25922), Staphylococcus aureus (ATCC4330), Pseudomonas aeruginosa (ATCC27853).
La luteolina (3’,4’,5,7-tetrahidroxiflavona) es un polifenol de familia de las flavonas, con estructura molecular (C6-C3-C6) de dos anillos bencénicos y un tercer anillo que contiene oxígeno, y un doble enlace entre los carbonos C2 y C3 (Figura 3). Su estructura favorece su actividad bioquímica y biológica (Wu et al., 2019). Este flavonoide tiene diversas actividades biológicas, tales como: antioxidante, antiinflamatoria, antimicrobiana, anticancerígena, y efecto hipoglucémico, hipolipidémico, hipotensor e inmunomodulador (Wu et al., 2019). En las bacterias la luetolina afecta la integridad de la pared y membrana celular, inhibiendo la síntesis de ácidos nucleicos, la expresión de proteínas e interfiere con el metabolismo energético (Guo et al., 2022). En un estudio Qian et al. (2021) encontraron que la luteolina deteriora la morfología celular de la membrana y afecta la formación de biopelícula en Staphylococcus aureus y Escherichia coli. En estudios contra Trueperella pyogenes se reporta una Concentración Mínima Inhibitoria (MIC) de luteolina de 78 μg/mL, y con la mitad de la MIC se aumenta la susceptibilidad para Staphylococcus resistentes a metiilcilina y a macrólidos, lo que permite una alternativa de tratamiento a patógenos resistentes (Guo et al., 2022).
ACTIVIDAD DE Lippia spp. CONTRA BACTERIAS RESISTENTES ASOCIADAS A MASTITIS BOVINA
Existen reportes de la actividad antibacteriana de extractos de Lippia spp. en bacterias resistentes como Streptococcus spp., Staphylococcus aureus, Pseudomonas aeruginosa, Klebsiella pneumoniae y Escherichia coli (Gupta et al., 2020; Pinheiro et al., 2022; Nonato et al., 2022). La Concentración Mínima Inhibitoria en la evaluación de extractos y metabolitos de Lippia spp. sobre bacterias presenta variación por la especie evaluada, metodología de extracción y evaluación (Rani et al., 2022; Nonato et al., 2022; Suarez et al., 2024).
En Streptococcus spp. se reporta una MIC de fluido supercrítico de L. graveolens de 67 mg/mL, mientras que para los metabolitos: timol se reportan MIC de 0.31 a 8.0 mg/mL y para carvacrol de 0.31 a 9 mg/mL (Tabla 2). En Staphylococcus spp. la MIC para extractos etanólicos de Lippia spp. se reporta de 128 a 512 µg/mL, para aceite esencial de 53.3 a 512 µg/mL, mientras que para timol fue de 0.15 a 0.75 µg/mL y carvacrol de 0.38 a 1.3 µg/mL (Dal Pozzo et al., 2011; Rani et al., 2022; Gallegos et al., 2019; Nonato et al., 2022).
Tabla 2 Actividad antibacteriana de Lippia spp y sus metabolitos contra patógenos resistentes asociados a mastitis bovina
| Bacteria | Extractos y compuestos | Concentración Mínima Inhibitoria (MIC) | Referencia |
|---|---|---|---|
| Streptococcus spp. | Timol Carvacrol | 0.31-0.63 µL/mL 0.16-0.63 µL/mL | Gupta et al. (2020) |
| Streptococcus agalactiae | Fluido supercrítico de L. graveolens | 67 mg/mL | García et al. (2019) |
| Timol Carvacrol | 8.0 mg/mL 9.0 mg/mL | Gupta et al. (2020) | |
| Staphylococcus aureus | Extracto etanólico de L. alba
Extracto etanólico de L. sidoides Extracto etanólico de L.gracilis Aceite esencial de L. alba Aceite esencial de L. sidoides Aceite esencial de L.gracilis |
853 µg/mL
128 µg/mL 512 µg/mL 256 µg/mL 53.3 µg/mL 512 µg/mL |
Nonato et al. (2022) |
| Aceite esencial de L. graveolens | 12 µL/mL | Suarez et al. (2024) | |
| Timol | 0.15-0.75 mg/mL | Gallegos et al. (2019) | |
| Carvacrol | 0.38-0.45 mg /mL | Rani et al. (2022) | |
| Staphylococcus spp. | Aceite esencial de L. graveolens
Timol Carvacrol |
1.6 mg /mL 0.4 a 0.5 mg/mL 0.8 a 1.3 mg/mL |
Dal Pozzo et al. (2011) |
| Pseudomonas aeruginosa | Extracto etanólico de L. alba
Extracto etanólico de L. sidoides Extracto etanólico de L.gracilis Aceite esencial de L. alba Aceite esencial de L. sidoides |
213.3 µg/mL 128 µg/mL 512 µg/mL 1024 µg/mL 298.6 µg/mL |
Nonato et al. (2022) |
| Aceite esencial de L.gracilis | 682 µg/mL | ||
| Aceite esencial L. berlandieri | 80 µg/mL | Reyes et al. (2020) | |
| Aceite esencial de L. origanoides | 2500 μg/mL | Pinheiro et al. (2022) | |
| Mezcla de aceites esenciales de L. salvifolia: L. sidoides (9:1) | 0.37 µg/mL | >Gupta et al. (2020) | |
| Escherichia coli | Extracto etanólico de L. origanoides | 5.0 μL | Castellanos et al. (2020) |
| Extracto etanólico de L. alba
Extracto etanólico de L. sidoides Extracto etanólico de L.gracilis Aceite esencial de L. alba Aceite esencial de L. sidoides Aceite esencial de L.gracilis |
768 µg/mL 74.6 µg/mL 256 µg/mL 106.6 µg/mL 106.6 µg/mL 426.6 µg/mL |
Nonato et al. (2022) | |
| Aceite esencial de L. origanoides | 312 μg/mL | Pinheiro et al. (2022) | |
| Aceite esencial L. berlandieri | 4 μg/mL | Bautista et al. (2021) | |
| Mezcla de aceites esenciales de L. salvifolia: L. sidoides (9:1) | 0.37 µg/mL | Gupta et al. (2020) | |
| Timol | 0.15-0.38 mg/mL | Gallegos et al. (2019) | |
| Carvacrol | 0.15-0.75 mg/mL | Rani et al. (2022) | |
| Klebsiella pneumoniae | Aceite esencial de L. origanoides
Timol Carvacrol |
312 μg/mL 0.75 mg/mL 0.75 mg/mL |
Pinheiro et al. (2022) Rani et al. (2022) |
En Pseudomonas aeruginosa se reporta una MIC para extractos etanólicos de 128 a 512 µg/mL, mientras que en aceites esenciales de 0.37 a 80 µg/mL. Para el caso de Escherichia coli se encontraron los siguientes reportes de MIC: extractos etanólicos (74.6 a 256 µg/mL), aceites esenciales (0.37 a 426 µg/mL), timol (0.15 a 0.38 µg/mL) y carvacrol (0.15 a 0.75 µg/mL). Los aceites esenciales y sus compuestos (carvacrol y timol), son los que presentan mayor actividad antibacteriana en bacterias resistentes aisladas de mastitis (Rani et al., 2022; Nonato et al., 2022; Suarez et al., 2024). Pinheiro et al. (2022) mencionan que el aceite esencial tiene acción inhibitoria y bactericida contra cepas de Escherichia coli y Klebsiella pneumoniae, no así contra Pseudomonas aeruginosa donde su efectividad disminuye por la formación de biopelícula y la acción de bombas de eflujo, características intrínsecas de esta especie. La combinación de extractos etanólicos de Lippia spp. con antimicrobianos reducen las MIC de amikacina, gentamicina, y cefalotina, sin embargo, tienen efecto antagonista con bencilpenicilina y con otros extractos naturales (Nonato et al., 2022). En la actualidad se investigan las sinergias entre extractos y antimicrobianos para mejorar la eficacia, reducir toxicidad y resistencia bacteriana (Garcia et al., 2019; Pinheiro et al., 2022; Nonato et al., 2023; Suarez et al., 2024).
CONCLUSIONES
Los principales metabolitos secundarios de L. graveolens son flavonoides y monoterpenos y su concentración es variable de acuerdo a las condiciones de suelo y clima del hábitat de la planta. Se ha demostrado su actividad antibacteriana contra diversos géneros bacterianos de importancia en salud, incluyendo las asociadas a mastitis bovina. La mayor actividad antibacteriana de L. graveolens se ha asociado a timol y carvacrol, sin embargo, también se ha reportado actividad por la presencia de naringenina, quercetina y luteolina. En la búsqueda de alternativas para combatir bacterias resistentes o multirresistentes asociadas a mastitis bovina, los metabolitos secundarios de Lippia graveolens representan una opción de estudio de nuevos tratamientos.











 texto em
texto em