Introducción
De acuerdo con la Organización Mundial de la Salud, los tipos de cáncer infantil más comunes son leucemia, cáncer cerebral, linfoma y tumores sólidos como el neuroblastoma y el tumor de Wilms1. Según la Agencia Internacional para la Investigación del Cáncer, en 2015 hubo entre 344,543 y 360,114 casos de cáncer infantil en todo el mundo (178.0 por millón), de los que 29,002 casos se ubicaron en América Latina y el Caribe2. En México, el cáncer es la segunda causa de muerte en menores de 15 años, debido a que los niños están sobreviviendo hasta los 2-6 años, edad en que la incidencia del cáncer es más alta. En 2007 se inició el Registro Nacional de Cáncer Infantil y se reportó que entre 2007 y 2015 hubo 24,039 casos nuevos tan solo del Seguro Popular, lo que representó un incremento en la incidencia de 133.5 por millón en 2007 a 150.1 por millón en 2015. En nuestro país, la tasa de mortalidad por cáncer es de 8.6/100,000 niños por año entre los 15 y 18 años, con una sobrevivencia global del 75% en instituciones con más de 15 camas y al menos tres oncólogos3. En el Instituto Mexicano del Seguro Social, la sobrevivencia global a 5 años fue del 56.1% (mediana de tiempo: 3.4 años) en el periodo de 2006 a 20124, y ha continuado con esa tendencia3.
Debido a los avances en la atención de pacientes con cáncer pediátrico ha mejorado la supervivencia a largo plazo, por lo que la cirugía, la quimioterapia (QT) y la radioterapia (RT) pueden provocar efectos tardíos en los sobrevivientes de cáncer infantil3,5, creando una población creciente de sobrevivientes que pasarán parte de sus vidas en riesgo de afecciones crónicas y mortalidad tardía, con pérdida potencial de años de vida o viviendo con discapacidad6. Entre los efectos discapacitantes se encuentra la pérdida auditiva relacionada con el uso de QT, común en estos niños, ya que se ha detectado que cuando son tratados con RT y QT experimentan una alta incidencia de hipoacusia neurosensorial a lo largo del tiempo como efecto secundario, encontrándose asociación entre la hipoacusia neurosensorial más grave y las dosis recibidas7. En particular, la RT ha mostrado que con más dosis mayor será el riesgo y más grave la discapacidad auditiva, como respuesta retardada a la radiación fraccionada. La hipoacusia es permanente cuando se provoca daño irreversible al oído interno, y se ha propuesto que la vuelta basal es más susceptible a la radiación, aunque la cóclea se considera como un órgano completo para el análisis de dosis-respuesta8.
El cisplatino es de uso común para algunos cánceres frecuentes en los niños, pero en ocasiones se combinan la RT y la QT9, y aunque existen trabajos que señalan que la dosis de cisplatino supera la importancia de la dosis de RT sobre la cóclea, parece que la irradiación previa reduce el umbral de dosis de cisplatino para la pérdida auditiva10, por lo que adquiere trascendencia determinar el impacto ototóxico aditivo de la QT que permita a los oncólogos encontrar dosis más seguras para la cóclea11.
El cisplatino es uno de los más potentes agentes citostáticos antitumorales disponibles, comúnmente utilizado como tratamiento estándar contra una amplia gama de cánceres infantiles, que en regímenes combinados permite un alto índice de cura12, con el inconveniente de que atraviesa la cóclea y provoca pérdida auditiva neurosensorial permanente, cuya repercusión se refleja en deficiencias en áreas neurocognitivas, que provocan alteraciones en el proceso de aprendizaje y contacto social, y problemas de conducta que afectan la calidad de vida, más evidente cuanto más pequeño sea el niño, por la deprivación del estímulo auditivo sobre el sistema nervioso central13,14. El platino reside en el oído durante meses o años después del tratamiento, por lo que el 70% de los niños tratados con platino desarrollan una pérdida auditiva irreversible y el 40% necesitarán audífonos en una etapa temprana15. Al igual que la RT, más dosis de cisplatino provocan mayor ototoxicidad, pero existen dudas sobre la dosis acumulada, lo que dificulta desarrollar enfoques ajustados al riesgo para su administración y para orientar mejor los nuevos agentes otoprotectores, como el tiosulfato de sodio13, lo que apoyaría la prevención de la pérdida auditiva inducida por cisplatino, carboplatino u oxaliplatino, con influencia positiva en la calidad de vida de los supervivientes de cáncer infantil16. Cuando los compuestos de platino se generalizaron tenían una mayor incidencia de pérdida auditiva, pero actualmente parece que la detección de daño se ha estabilizado en los sobrevivientes y se propone que puede ser porque los nuevos regímenes de tratamiento tienen menos radiación ototóxica y los compuestos de platino se dosifican con mayor cuidado17.
Considerando todo lo anterior, el objetivo del presente trabajo fue medir los cambios en la audición de niños con cáncer manejados con cisplatino en diferentes dosis, mediante la realización de audiometría tonal con frecuencias convencionales y altas frecuencias, así como emisiones otoacústicas por productos de distorsión (EOAPD).
Método
Para lograr el objetivo, se realizó un estudio de cohorte retrospectiva mediante revisión de expedientes de niños con diagnóstico de cáncer y que incluyeron cisplatino como parte de la QT. Los criterios de selección fueron edad entre 4 y 17 años, registro en el expediente de las dosis administradas de QT y un mínimo de dos valoraciones audiológicas relacionadas con la administración de cisplatino en cualquier combinación. Se excluyeron los pacientes que tenían antecedente de hipoacusia antes del diagnóstico de cáncer o del inicio del tratamiento, aquellos con antecedente de RT en cabeza o cuello, antecedente de infección aguda o crónica, o cirugía de oído previa. Las evaluaciones audiológicas fueron audiometría tonal liminar (0.125 Hz a 8 kHz), audiometría tonal de altas frecuencias (10 a 16 kHZ) y EOAPD.
La ototoxicidad se evaluó utilizando los criterios de la American Speech-Language-Hearing Association (ASHA), que incluyen:
- Disminución ≥ 20 dB HL nivel de audición (Hearing level), por sus siglas en inglés, en el umbral de tonos puros en una sola frecuencia de prueba.
- Disminución ≥ 10 dB HL en el umbral en dos frecuencias adyacentes.
- Pérdida de respuesta en tres frecuencias consecutivas en las que se obtuvieron respuestas previamente.
Los criterios de la ASHA detectan cambios ototóxicos tempranos antes de la clínica, con existencia de hipoacusia neurosensorial, pero no detectan pérdida auditiva clínicamente significativa en oncología, por lo que cuando se encontró hipoacusia neurosensorial significativa se clasificó la pérdida con el uso de la escala de grados propuesta por Chang para ototoxicidad, específicamente desarrollada para cambios clínicamente significativos inducidos por platino. Los criterios de ototoxicidad de Chang para la gravedad de la pérdida auditiva, son:
- 0 = umbrales ≤ 20 dB en 1, 2 y 4 kHZ.
- 1a = umbrales ≥ 40 dB en 6-12 kHZ.
- 1b = umbrales > 20 y < 40 dB en 4 kHZ.
- 2a = ≥ 40 dB en frecuencias ≥ 4 kHZ.
- 2b = umbrales > 20 y < 40 dB en frecuencias < 4 kHz.
- 3 = ≥ 40 dB en frecuencias ≥ 2 kHZ.
De acuerdo con los hallazgos en las pruebas audiológicas para umbral tonal, los pacientes se clasificaron utilizando los criterios de Brock para la pérdida auditiva:
- Ninguna: hipoacusia bilateral, menos de 40 dB en todas las frecuencias.
- Leve: hipoacusia bilateral, superior a 40 dB en 8000 Hz.
- Moderada: hipoacusia bilateral, superior a 40 dB desde 6000 Hz.
- Marcada: hipoacusia bilateral, superior a 40 dB desde 4000 Hz.
- Grave: pérdida auditiva bilateral, mayor de 40 dB desde 2000 Hz20,21.
Resultados
Se revisaron 140 expedientes de niños y adolescentes con cáncer en el Hospital Infantil de México Federico Gómez, tratados con cisplatino en combinación con otros medicamentos, de los cuales 42 cumplieron con los criterios de inclusión (30%). De estos, hubo 22 (52.4%) mujeres y 20 (47.6%) hombres, con una edad promedio de 10.9 ± 3.38 años. En la tabla 1 se muestran el resto de las características generales de los 42 casos y su división en pacientes con criterios para ototoxicidad (pCCO) (n = 37; 88.1%), ubicados en grado 1a, y pacientes sin criterios para ototoxicidad (pSCO) (n = 5; 11.9%), correspondientes al grado 0 de Chang, así como el esquema terapéutico y la dosis de cisplatino prescrita, independientemente del número de administraciones en las que fue otorgada. Se puede observar el predominio de mujeres, sin diferencia significativa en la edad promedio (p > 0.05). El osteosarcoma fue el tipo de cáncer más frecuente (78.6%). Todos recibieron cisplatino como parte del esquema de tratamiento y se puede apreciar que se utilizaron siete diferentes esquemas de QT, siendo cisplatino con adriamicina la combinación más común (71.4%). La administración del medicamento se proporcionó en tres dosis en la mayoría de los pacientes (69%). También se muestra la dosis administrada de cisplatino, en la población general y dividida en pCCO y pSCO.
Tabla 1 Características generales, esquema terapéutico y dosis otorgada de cisplatino de los 42 pacientes seleccionados y separados de acuerdo con la presencia o ausencia de ototoxicidad
| Característica | Variable | Población general (n = 42) | Pacientes con ototoxicidad (n = 37) | Pacientes sin ototoxicidad (n = 5) |
|---|---|---|---|---|
| Sexo | Masculino, (%) | 20 (47.6%) | 20 (54.1%) | 0 |
| Femenino, (%) | 22 (52.4%) | 17 (45.9%) | 5 (100%) | |
| Edad (años) | X ± DE | 10.9 ± 3.38 | 10.89 ± 3.35 | 11 ± 4 |
| Diagnóstico (tipo de cáncer) | Osteosarcoma | 33 (78.6%) | 29 (78.4%) | 4 (80%) |
| Meduloblastoma | 3 (7.1%) | 3 (8.1%) | 0 | |
| Rabdomiosarcoma | 2 (4.8%) | 2 (5.4%) | 0 | |
| Tumor germinal | 2 (4.8%) | 2 (5.4%) | 0 | |
| Sarcoma | 1 (2.4%) | 1 (2.7%) | 0 | |
| Adenoma suprarrenal | 1 (2.4%) | 0 | 1 (20%) | |
| Esquema de tratamiento | Cisplatino ± adriamicina | 30 (71.4%) | 27 (73%) | 3 (60%) |
| Cisplatino ± adriamicina ± doxorrubicina | 2 (4.8%) | 1 (2.7%) | 1 (20%) | |
| Cisplatino ± etopósido | 2 (4.8%) | 1 (2.7%) | 1 (20%) | |
| Cisplatino ± adriamicina ± ciclofosfamida | 2 (4.8%) | 2 (5.4%) | 0 | |
| Cisplatino ± adriamicina ± etopósido | 1 (2.4%) | 1 (2.7%) | 0 | |
| Cisplatino ± ciclofosfamida | 1 (2.4%) | 1 (2.7%) | 0 | |
| Cisplatino ± etopósido ± ciclofosfamida | 1 (2.4%) | 1 (2.7%) | 0 | |
| Cisplatino ± doxorubicina | 1 (2.4%) | 1 (2.7%) | 0 | |
| Cisplatino ± doxorubicina ± vincristina | 1 (2.4%) | 1 (2.7%) | 0 | |
| Cisplatino ± etopósido ± doxorubicina | 1 (2.4%) | 1 (2.7%) | 0 | |
| Número de fármacos combinados | 2 | 34 (81.0%) | 30 (81.1%) | 4 (80%) |
| 3 | 8 (19.0%) | 7 (18.9%) | 1 (20%) | |
| Número de dosis recibidas | 2 | 13 (31%) | 9 (24.3%) | 4 (80%) |
| 3 | 29 (69%) | 28 (75.7%) | 1 (20%) | |
| Primera dosis de cisplatino (mg/m2 sc) | 155.19 ± 37.55 | 150.48 ± 31.27 | 190 ± 62.7 | |
| Segunda dosis de cisplatino (mg/m2 sc) | 153.57 ± 34.16 | 152.8 ± 36.16 | 159 ± 12.4 | |
| Tercera dosis de cisplatino (mg/m2 sc) | 155.5 ± 37.5 | 155.7 ± 38.17 | 150 ± 0 | |
| Dosis acumulada de cisplatino (mg/m2 sc) | 416.1 ± 118.8 | 421.16 ± 118.9 | 379 ± 124.56 |
n: número de pacientes; X±D.E.: promedio y desviación estándar; mg/m2 sc: miligramos por metro cuadrado de superficie corporal.
En la tabla 2 se puede apreciar que la mayoría recibieron los fármacos en tres dosis (37 pacientes). A pesar de ser pocos los sujetos sin ototoxicidad (cinco pacientes), en ellos se observaron las mayores dosis promedio por administración en dos y tres dosis (rango: pSCO 150-300 vs. pCCO 146.11-155.71 mg/m2 de superficie corporal), y fue estadísticamente significativo entre grupos para la primera dosis administrada (p = 0.025), pero no para la segunda (p = 0.71) y la tercera dosis (p = 0.88), así como para la dosis acumulada (rango: pSCO 294.44-461.89 vs. pCCO 323.75-600) (p = 0.46). Sin embargo, sí hubo significancia en la dosis acumulada al separarlos entre los que recibieron dos y tres dosis, entre los grupos con y sin ototoxicidad (p = 0.0001). En la comparación intragrupo no hubo diferencias para las diferentes dosis administradas.
Tabla 2 Número de dosis recibidas y cantidad administrada de cisplatino en la población general y en pacientes con y sin criterios de ototoxicidad
| Número de dosis de cisplatino recibidas (mg/m2 sc) | Población general (n = 42) | Pacientes con ototoxicidad (n = 37) | Pacientes sin ototoxicidad (n = 5) | ||||
|---|---|---|---|---|---|---|---|
| Dosis | X ± DE | 2 dosis (n = 13) | 3 dosis (n = 29) | 2 dosis (n = 9) | 3 dosis (n = 28) | 2 dosis (n = 4) | 3 dosis (n = 1) |
| Primera dosis | X ± DE | 151.2 ± 19.2 | 157 ± 43.6 | 146.1 ± 19.5 | 151.9 ± 34.4 | 162.5 ± 14.4 | 300 |
| Segunda dosis | X ± DE | 152.3 ± 18.7 | 154.1 ± 39.5 | 148.3 ± 20 | 154.3 ± 40.2 | 161.3 ± 13.1 | 150 |
| Tercera dosis | X ± DE | 155.5 ± 37.5 | 155.7 ± 38.2 | 150 | |||
| Dosis acumulada | X ± DE | 303.5 ± 34.5 | 466.7 ± 107.8 | 294.4 ± 36.8 | 461.9 ± 106.7 | 323.8 ± 18.4 | 600 |
sc: superficie corporal; X ± DE: promedio y desviación estándar.
En la tabla 3 se muestran los umbrales auditivos de los 42 pacientes de la investigación, y separados en pCCO y pSCO. Puede observarse que las frecuencias graves y medias se mantuvieron en promedio dentro de los límites de la normalidad en todos los estudios (< 20 dB), aunque las frecuencias agudas sí mostraron alteraciones mayores en el tercer estudio, en el grupo con ototoxicidad; no obstante, se puede apreciar un incremento promedio en todas las mediciones y los rangos permiten evidenciar que sí había pacientes con deterioro auditivo en cada medición audiológica. El análisis inferencial en pCCO mostró que solo hubo diferencia significativa en el nivel auditivo intragrupo entre el primero y el segundo estudios en las frecuencias medias (p = 0.043) y en las agudas (p = 0.046).
Tabla 3 Umbral auditivo promedio por frecuencias (graves, medias y agudas) en la población general y separada por pacientes con y sin ototoxicidad
| Umbral auditivo por frecuencias | X ± DE/Rango | Población general (n = 42) | Con ototoxicidad (n = 37) | Sin ototoxicidad (n = 5) | p |
|---|---|---|---|---|---|
| Graves dosis 1 (dB) | X ± DE | 13.4 ± 3.3 | 13.7 ± 3.2 | 11.4 ± 3.3 | 0.142 |
| Rango | 8-21 | 8-21 | 8-15 | ||
| Graves dosis 2 (dB) | X ± DE | 14.8 ± 6.3 | 15.27 ± 6.5 | 11.6 ± 3.6 | 0.228 |
| Rango | 8-47 | 8-47 | 8-16 | ||
| Graves dosis 3 (dB) | X ± DE | 17.7 ± 8.3 | 17.6 ± 8.5 | 19.0 | 0.874 |
| Rango | 7-56 | 7-56 | |||
| Medias dosis 1 (dB) | X ± DE | 14.1 ± 6.6 | 14.49 ± 6.9 | 11.4 ± 2.07 | 0.335 |
| Rango | 7-47 | 7-47 | 8-13 | ||
| Medias dosis 2 (dB) | X ± DE | 13.8 ± 7.6 | 14.68 ± 7.6 | 7.4 ± 3.3 | 0.043 |
| Rango | 4-34 | 5-34 | 4-12 | ||
| Medias dosis 3 (dB) | X ± DE | 12.2 ± 6.9 | 12.3 ± 7.0 | 8.0 | 0.547 |
| Rango | 3-34 | 3-34 | |||
| Agudas dosis 1 (dB) | X ± DE | 19.17 ± 12.7 | 19.8 ± 13.5 | 14.4 ± 1.1 | 0.379 |
| Rango | 8-63 | 13-16 | |||
| Agudas dosis 2 (dB) | X ± DE | 31.1 ± 18.2 | 33.16 ± 18.4 | 16 ± 1.7 | 0.046 |
| Rango | 10-76 | 10-76 | 15-19 | ||
| Agudas dosis 3 (dB) | X ± DE | 44.6 ± 20.9 | 45.7 ± 20.3 | 11.0 | 0.104 |
| Rango | 11-91 | 11-91 |
X ± DE: promedio y desviación estándar.
Al separar los grupos considerando el número de dosis (Tabla 4), se encontró que en aquellos que recibieron dos dosis también hubo diferencia significativa en las frecuencias medias (p = 0.043) y altas (p = 0.018) entre los estudios. En los que recibieron tres dosis se encontró diferencia significativa desde las frecuencias bajas entre el primero y el tercer estudios (p = 0.003), y entre el segundo y el tercer estudios (p = 0.010); para las frecuencias medias solo hubo diferencia en los umbrales auditivos entre el segundo y el tercer estudios (p = 0.001); y en las frecuencias agudas, la diferencia se ubicó en todas las comparaciones entre estudios (primero-segundo, primero-tercero y segundo-tercero) (p = 0.0001).
Tabla 4 Promedio y desviación estándar, y rango, por frecuencias del umbral auditivo en tonos graves (0.125, 0.250 y 0.500 kHZ), medios (1-2 kHZ) y agudos (4-8 kHZ) en la población general y separada por pacientes con y sin ototoxicidad, considerando el número de dosis recibidas (dos o tres)
| Población general | Con ototoxicidad | Sin ototoxicidad | |||||
|---|---|---|---|---|---|---|---|
| Umbral auditivo por frecuencias | X ± DE/Rango | 2 dosis (n = 13) | 3 dosis (n = 29) | 2 dosis (n = 9) | 3 dosis (n = 28) | 2 dosis (n = 4) | 3 dosis (n = 1) |
| Graves dosis 1 (dB) | X ± DE | 11.69 ± 2.175 | 14.2 ± 3.41 | 12.2 ± 1.64 | 14.18 ± 3.47 | 10.5 ± 3.0 | 15 |
| Rango | 8-15 | 8-21 | 10-15 | 8-21 | 8-14 | ||
| Graves dosis 2 (dB) | X ± DE | 11.69 ± 2.17 | 16.2 ± 7.07 | 12.2 ± 1.64 | 16.25 ± 7.2 | 10.5 ± 3.0 | 16 |
| Rango | 8-15 | 8-47 | 10-15 | 8-47 | 8-14 | ||
| Graves dosis 3 (dB) | X ± DE | 17.8 ± 8.4 | 17.79 ± 8.56 | 19 | |||
| Rango | 7-56 | 7-56 | |||||
| Medias dosis 1 (dB) | X ± DE | 11.46 ± 2.47 | 15.3 ± 7.55 | 11.6 ± 2.69 | 15.39 ± 7.68 | 11.0 ± 2.160 | 13 |
| Rango | 7-16 | 8-47 | 7-16 | 8-47 | 8-13 | ||
| Medias dosis 2 (dB) | X ± DE | 8.3 ± 3.75 | 16.28 ± 7.6 | 9.0 ± 3.8 | 16.5 ± 7.67 | 6.75 ± 3.59 | 10 |
| Rango | 4-16 | 6-34 | 5-16 | 6-34 | 4-12 | ||
| Medias dosis 3 (dB) | X ± DE | 12.5 ± 6.8 | 12.68 ± 6.89 | 8 | |||
| Rango | 3-34 | 3-34 | |||||
| Agudas dosis 1 (dB) | X ± DE | 16.3 ± 4.49 | 20.45 ± 14.9 | 17.0 ± 5.3 | 20.7 ± 15.15 | 14.75 ± 0.95 | 13 |
| Rango | 13-28 | 8-63 | 13-28 | 8-63 | 14-16 | ||
| Agudas dosis 2 (dB) | X ± DE | 21.2 ± 9.46 | 35.5 ± 19.49 | 23.4 ± 10.7 | 36.29 ± 19.4 | 16.25 ± 1.89 | 15.00 |
| Rango | 14-45 | 10-76 | 14-45 | 10-76 | 15-19 | 15 | |
| Agudas dosis 3 (dB) | X ± DE | 45.38 ± 20.8 | 46.6 ± 20.13 | 11.00 | |||
| Rango | 11-91 | 11-91 | 11 | ||||
X ± DE: promedio y desviación estándar.
En los pacientes sin ototoxicidad no hubo diferencia intragrupo en los umbrales de las frecuencias graves (p = 0.99), medias (p = 0.141) ni agudas (p = 0.180) entre los estudios de aquellos que recibieron dos dosis (p > 0.05); no fue procedente el análisis en el único paciente con tres dosis.
En la tabla 5 se muestran los hallazgos auditivos en frecuencias supraumbrales (10-16 kHZ), donde se aprecia que desde el primer estudio el umbral promedio se ubicaba arriba de los 20 dB, con un incremento constante en las frecuencias evaluadas en todos los pCCO (dos y tres dosis). En contraste, los pSCO que recibieron dos dosis tuvieron umbrales promedio normales, aunque el análisis al interior de los datos muestra que ya había pacientes con afección > 20 dB en el segundo estudio (20.0 ± 3.4 dB y rango 18-25); así como el único paciente que recibió tres dosis, que desde el segundo estudio mostró un umbral anormal y se incrementó en el tercer estudio. Al comparar a los pCCO se observó mayor daño auditivo cuando se compararon con pSCO, desde el primer estudio, pero solo fue significativo en el segundo (p = 0.004) y el tercer estudios (p = 0.008). La comparación intragrupo evidenció que la diferencia fue significativa para pCCO entre el primero y el segundo estudios (p = 0.0001), y entre el primero y el tercer estudio (p = 0.0001), pero no entre el segundo y el tercer estudios (p = 0.319). A pesar del incremento constante en los umbrales de los pSCO, las diferencias no fueron significativas (p > 0.06). Se encontró una correlación entre la dosis acumulada y el umbral auditivo del segundo estudio en tonos graves (rs = 0.38; p = 0.013), tonos medios (rs = 0.53; p = 0.0001) y tonos agudos (rs = 0.32; p = 0.034).
Tabla 5 Promedio y desviación estándar, y rango, por frecuencias supraumbral (tonos agudos 10-16 kHZ) en la población general y separada por pacientes con y sin ototoxicidad, considerando el número de dosis recibidas (dos o tres)
| Población general | Con ototoxicidad | Sin ototoxicidad | |||||
|---|---|---|---|---|---|---|---|
| Umbral auditivo para altas frecuencias | X ± DE/Rango | 2 dosis (n = 13) | 3 dosis (n = 29) | 2 dosis (n = 9) | 3 dosis (n = 28) | 2 dosis (n = 4) | 3 dosis (n = 1) |
| Primer estudio (dB) (dosis 1) | X ± DE | 22.3 ± 10.7 | 23.8 ± 16.8 | 24.7 ± 12.3 | 24.0 ± 17.0 | 17.0 ± 1.6 | 18.0 |
| Rango | 15-53 | 2-71 | 17-53 | 2-71 | 15-19 | ||
| Segundo estudio (dB) (dosis 2) | X ± DE | 35.9 ± 18.2 | 45.0 ± 19.9 | 43.0 ± 17.6 | 45.8 ± 19.9 | 20.0 ± 3.4 | 23.0 |
| Rango | 18-70 | 14-87 | 25-70 | 14-87 | 18-25 | ||
| Tercer estudio (dB) (dosis 3) | X ± DE | - | 58.8 ± 19.8 | - | 60.0 ± 19.1 | - | 26.0 |
| Rango | - | 21-102 | - | 21-102 | - | - | |
X ± DE: promedio y desviación estándar.
Las alteraciones en las altas frecuencias fueron evidentes desde la primera administración del fármaco en los pCCO, con pérdidas promedio siempre mayores de 20 dB hasta la tercera dosis, aunque fueron significativas solo entre el primero y el segundo estudios (p = 0.0001) y entre el primero y el tercer estudios (p = 0.001) tanto en pacientes con dos como con tres dosis, pero no entre el segundo y el tercer estudios (p = 0.793). En los pSCO apareció alteración leve en la segunda y la tercera dosis, pero no significativa (p > 0.05) (Tabla 5). De igual forma, la comparación entre pCCO y pSCO fue significativa solo en el segundo (p = 0.001) y el tercer estudios (p = 0.006) (Tabla 5). Considerando el daño en las altas frecuencias, hubo diferencia en la tercera dosis (p = 0.001) y con la dosis acumulada (p = 0.0001), y una correlación excelente entre la pérdida auditiva después de la tercera dosis con haber recibido tres dosis (rs = 0.80; p = 0.0001) y con la dosis acumulada (rs = 0.54; p = 0.0001), así como una mayor pérdida con dosis superiores a 300 y 325 mg/m2 de superficie corporal en la segunda dosis (p = 0.036) y en la dosis acumulada (p = 0.009), y también entre el tercer estudio y la dosis acumulada (p = 0.006). Se documentó un riesgo (odds ratio [OR]) de 1.125 (intervalo de confianza del 95% [IC95%]: 0.893-1.417) para presentar daño en frecuencias supraumbrales en el tercer estudio con dosis de cisplatino de 300 mg/m2 de superficie corporal.
Las EOAPD mostraron cambios relacionados con la dosis administrada de cisplatino. En la tabla 6 se puede apreciar que, en el primer estudio, la mayoría de los pacientes tenían respuestas presentes en pCCO (33 pacientes; 89.2%) y pSCO (5 pacientes; 100%). Hubo cambios posterior a la segunda dosis en pCCO, en los que la mayoría no presentaron emisiones (22 pacientes; 60%), pero la variación no fue significativa (p = 0.11; χ2), y para la evaluación después de la tercera dosis todos presentaron ausencia de respuesta (28 pacientes; 100%) (p = 0.05). En los pSCO no hubo cambios, pues solo un paciente no tuvo respuesta (p = 0.34). El único paciente que recibió tres dosis siempre presentó respuesta en las diferentes mediciones. La presencia/ausencia de respuestas en las EOAPD mostraron una diferencia significativa solo después de la segunda dosis de cisplatino (p = 0.034), con una OR de 1.973 (IC95%: 1.097-3.549) para la ausencia de respuestas con dosis superiores a 300 y 325 mg/m2 de superficie corporal. En los pacientes con tres dosis la diferencia fue significativa, con ausencia de respuestas (p = 0.0001). Se encontró una asociación (rs = 0.67; p = 0.036) con la dosis acumulada de 300 mg/m2 de superficie corporal en los pCCO después de la segunda dosis y una OR de 4.0 para la ausencia de respuestas (IC95%: 0.733-21.838) con la misma dosis (p = 0.034).
Tabla 6 Proporción de pacientes con presencia/ausencia de emisiones otoacústicas por productos de distorsión en la población general y separada por pacientes con y sin ototoxicidad, considerando el número de dosis recibidas (dos o tres)
| Población general | Con ototoxicidad | Sin ototoxicidad | |||||
|---|---|---|---|---|---|---|---|
| EOAPD (presentes/ausentes) | Presentes/ausentes | 2 dosis (n = 13) | 3 dosis (n = 29) | 2 dosis (n = 9) | 3 dosis (n = 28) | 2 dosis (n = 4) | 3 dosis (n = 1) |
| Primer estudio (dosis 1) | Presentes | 12 | 26 | 8 | 25 | 4 | 1 |
| Ausentes | 1 | 3 | 1 | 3 | 0 | 0 | |
| Segundo estudio (dosis 2) | Presentes | 7 | 12 | 4 | 11 | 3 | 1 |
| Ausentes | 6 | 17 | 5 | 17 | 1 | 0 | |
| Tercer estudio (dosis 3) | Presentes | - | 1 | 0 | 0 | - | 1 |
| Ausentes | - | 28 | 0 | 28 | - | 0 | |
EOAPD: emisiones otoacústicas por productos de distorsión.
Discusión
Uno de los hallazgos más importantes del presente estudio fue identificar el deterioro auditivo en niños con cáncer tratados con cisplatino en tonos agudos y altas frecuencias (10,000-16,000 Hz) desde la primera dosis de cisplatino, combinado con uno o dos fármacos más (Tablas 3 a 5). Es importante señalar que la prevalencia de pérdida auditiva al término del tratamiento es considerada como el hallazgo primario más importante, pues refleja la toxicidad de la QT al final (Tablas 3 a 5). En esta investigación se encontró que los 37 pCCO (100%) presentaron deterioro en las altas frecuencias desde la primera dosis y tuvieron daño en las agudas a partir de la segunda dosis, de acuerdo con la clasificación de Brock (Tablas 4 y 5), coincidiendo con otras publicaciones15.
Se ha publicado que la pérdida auditiva ocurre en alrededor del 10% de los sobrevivientes de cáncer infantil en general22, pero en nuestro trabajo la prevalencia fue mucho mayor (88.1%), más acorde con lo reportado por Diepstraten et al.15, quienes señalan que hasta el 70% de los niños tratados con platino desarrollan una pérdida auditiva irreversible, y el 40% necesitan usar audífonos en etapa temprana. No obstante, nuestra cifra puede estar sobrecalculada, ya que todos usaron cisplatino y contaban con estudios audiológicos, aunque congruente con el reporte de que las estimaciones de prevalencia de pérdida de audición después de cisplatino varían ampliamente entre diferentes trabajos, debido a factores de riesgo adicionales como el uso de aminoglucósidos y diuréticos de asa, o de otros agentes antineoplásicos que causan hipoacusia22.
Algunos autores proponen que en la evaluación de estos niños es conveniente el uso de más de un estudio que evalúe la función auditiva, por la credibilidad de los resultados considerando la edad del menor al momento de realizar estudios conductuales. En este trabajo se usó la audiometría tonal y la de altas frecuencias, así como los EOAPD, porque no se consideran relevantes los hallazgos de impedanciometría ni los potenciales auditivos de tallo cerebral15,23.
De acuerdo con otros autores, encontramos que la dosis acumulada de cisplatino se asoció con la pérdida de la audición11, pues las dosis cíclicas más altas pueden aumentar la administración coclear del fármaco a través de la saturación de los mecanismos de transporte activo y pasivo en la cóclea, y una vez en ella, el cisplatino se acumula y se retiene, en particular después de dosis altas repetidas24. Fue interesante que una dosis acumulada superior a 300 y 325 mg/m2 de superficie corporal se relacionó con la presencia de lesión en altas frecuencias y en tonos agudos, y con ausencia de respuesta en las EOAPD (p < 0.05)15.
Keilty et al.7 encontraron, para el desarrollo de hipoacusia, una OR de 1.48 para la dosis de cisplatino, tomando en cuenta 100 mg/m2 de superficie corporal (p < 0.001), con incrementos en la incidencia acumulada de hipoacusia de alta frecuencia (> 4 kHz) a los 5 años de edad y en todas las frecuencias después de los 5 años7. Nuestro análisis permitió evidenciar una OR de 1.125 (IC95%: 0.893-1.417) de presentar daño en altas frecuencias en el tercer estudio con dosis de cisplatino de 300 mg/m2 de superficie corporal, y una OR de 1.973 (IC95%:1.097-3.549) para la ausencia de respuestas en las EOAPD con dosis por arriba de 300 y 325 mg/m2 de superficie corporal al término del tratamiento7,15. A pesar de que encontramos diferencias significativas en la pérdida de audición entre las dosis administradas, segunda y tercera dosis, así como en la dosis acumulada, parece que no importa el tiempo de duración de las infusiones16.
Bass et al.18 identificaron efectos subclínicos de pérdida auditiva después de la exposición a RT en pacientes con cáncer particularmente en el rango de las altas frecuencias y en las EOAPD, mientras la audición se mantuvo normal para las frecuencias convencionales. Nuestros hallazgos son congruentes con este comportamiento, con relación al uso de cisplatino, aunque sin seguimiento a largo plazo (Figs. 1 y 2, y Tabla 6). No obstante, es importante seguir la recomendación del seguimiento durante varios años para controlar los posibles efectos auditivos tardíos18, por la exposición a ototóxicos con QT o RT. También Moke et al.13 reportaron que el riesgo para hipoacusia aumentó en un 10-20% por cada 100 mg/m2 de superficie corporal de dosis acumulada de cisplatino (OR: 1.11; IC95%: 1.01-1.23). Nosotros encontramos un riesgo similar (OR: 1.125; IC95%: 0.893-1.417) con una dosificación de cisplatino de 300 y 325 mg/m2 de superficie corporal en la segunda dosis (p = 0.036), mientras que en el trabajo de Moke et al.13 la pérdida fue moderada/grave al final del tratamiento con dosis de cisplatino, encontrando que por cada aumento de 50 mg/m2/ciclo, identificaba un OR = 2.16 (IC95%:1.37-3.51). Además, encontramos que diferencias en la dosificación de cisplatino confirieron una OR de 4.0 (IC95%: 0.733-21.838) en pérdida de respuestas en las EOAPD. Si bien se debe considerar que el aumento de la dosis acumulada de cisplatino administrado (± 100 mg/m2 de superficie corporal) protegió contra la muerte, fue al contrario con la progresión de la enfermedad13.
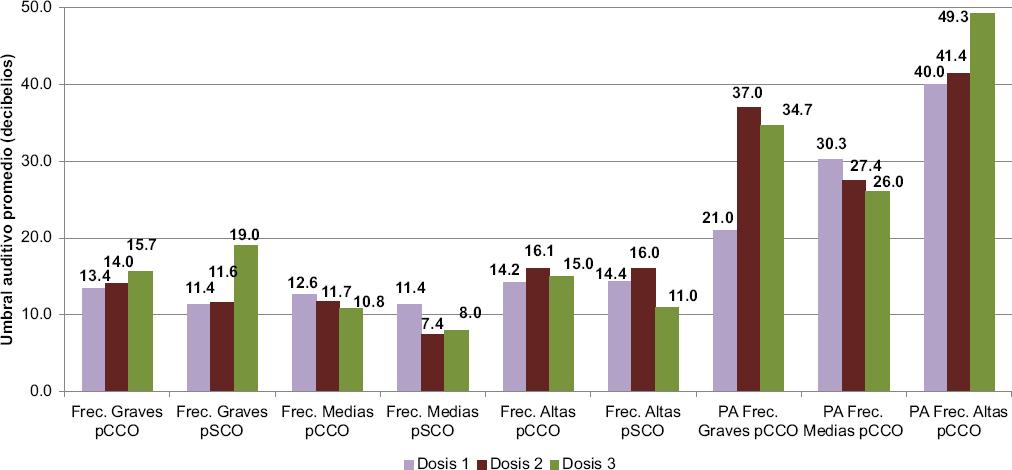
Figura 1 Comportamiento de los umbrales auditivos, con y sin criterios de ototoxicidad, según número de dosis. PA: pérdida auditiva; pCCO: pacientes con criterios para ototoxicidad; pSCO: pacientes sin criterios para ototoxicidad.
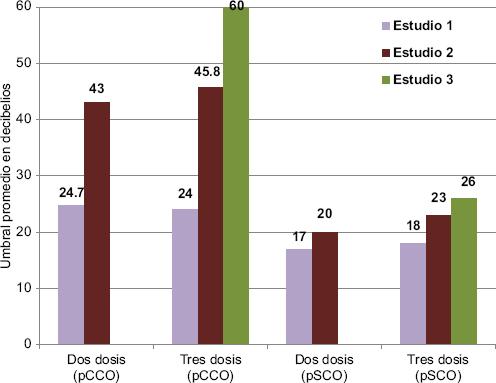
Figura 2 Comportamiento de las respuestas supraumbral, con y sin criterios de ototoxicidad, de acuerdo al número de estudio. pCCO: pacientes con criterios para ototoxicidad; pSCO: pacientes sin criterios para ototoxicidad.
Contrario a lo expuesto por Moke et al.13, se cree que sea probable que el cisplatino retenido solo contribuya a la toxicidad a largo plazo, pues se ha detectado cisplatino circulante en el plasma de sobrevivientes incluso décadas después de la terapia. Por ello, se justifica una mayor investigación sobre las posibles intervenciones para reducir la hipoacusia inducida por cisplatino mediante la alteración de la intensidad de la dosificación de cisplatino con o sin la introducción de agentes otoprotectores, mientras se mantienen la citotoxicidad y el potencial curativo de la dosificación acumulativa, como el uso de amifostina y tiosulfato de sodio en niños como una intervención otoprotectora13 o el uso de nanopartículas de dexametasona y antioxidantes, que previnieron eficazmente la apoptosis y la producción de especies reactivas de oxígeno causadas por estímulos ototóxicos25.
Los datos audiológicos encontrados muestran que la pérdida de audición es frecuente en los sobrevivientes de cáncer infantil. Es difícil establecer la relación entre la pérdida de audición y otros antineoplásicos (como la vincristina)13, debido a que el tratamiento con cisplatino fue un criterio de inclusión, lo que dificulta la identificación de la contribución de otros factores. Sin embargo, las pruebas de audición no son invasivas, son baratas y fáciles de realizar, y cada niño las realiza varias veces durante la infancia con fines de cribado. Por lo tanto, nuestros resultados son congruentes con la necesidad de que los estudios futuros tengan criterios de inclusión más amplios y ofrecer pruebas de audición a todas las personas que recibieron alguna QT, no solo a los que recibieron fármacos que ya se sabe que son ototóxicos22. Estudios con criterios más amplios permitirán detectar nuevos factores de riesgo en el paisaje en constante evolución de los tratamientos contra el cáncer26.
Las pruebas audiológicas precisas y la detección oportuna de la ototoxicidad contribuyen a la detección de hipoacusia en etapa temprana, que puede conducir indirectamente a una mejor calidad de vida. Además, se logró recopilar datos de alta calidad sobre la relación entre el estado de la enfermedad, el tipo de tratamiento y el funcionamiento audiológico en niños con cáncer durante el tratamiento, que en el futuro podrían usarse para identificar a los niños que están en riesgo y que podrían beneficiarse de los agentes otoprotectores15. También consideramos relevante este trabajo porque algunos autores mencionan que hay una sorprendente falta de trabajos que investiguen específicamente los efectos tardíos en los sobrevivientes de cáncer infantil, considerando que actualmente ha aumentado la cantidad de sobrevivientes27.
Conclusiones
El cisplatino es un fármaco antineoplásico ampliamente utilizado en el tratamiento del cáncer en la infancia, y la ototoxicidad es uno de sus efectos adversos más frecuentes. Nosotros encontramos un 88.1% de pacientes con deterioro auditivo y hasta un 100% cuando se incluyeron las altas frecuencias en los casos estudiados. Se documentó que la hipoacusia neurosensorial inicia en las altas frecuencias, pero con el incremento en la dosis acumulada de cisplatino (≥ 300 mg/m2 de superficie corporal) el daño continúa a frecuencias agudas y medias, comprometiendo el área del lenguaje después de la segunda y la tercera dosis. Evaluar la función auditiva de los niños con cáncer durante su tratamiento con cisplatino puede permitir la detección oportuna del deterioro de los umbrales auditivos. La audiometría tonal de altas frecuencias y los EOAPD mostraron ser útiles, ya que revelaron de manera temprana cambios en la función auditiva con respecto a la audiometría tonal en las frecuencias convencionales, por lo que los protocolos de monitorización auditiva en los pacientes tratados con cisplatino deben incluir, por lo menos, estos estudios audiológicos.
En conclusión, debido a que el número de sobrevivientes de cáncer infantil ha incrementado en las últimas décadas, es de suma importancia establecer protocolos de cribado y monitorización de ototoxicidad en pacientes tratados con cisplatino y otros agentes potencialmente ototóxicos para conocer la función auditiva desde las etapas iniciales del tratamiento, y poder intervenir oportunamente con la rehabilitación auditiva, ya que la hipoacusia en este grupo de población tiene repercusiones en el lenguaje, el aprendizaje, la integración social y el desarrollo de la personalidad.











 nova página do texto(beta)
nova página do texto(beta)


