Introducción
Bemisia tabaci (Gennadius) es un insecto chupador ampliamente distribuido en el mundo, que ocasiona pérdidas millonarias por los daños directos e indirectos hacia los cultivos agrícolas [1]. Desde que se registraron los primeros indicios de la resistencia de B. tabaci (Gennadius) (Hemiptera: Aleyrodidae) a los insecticidas [2], varias han sido las estrategias de manejo que se han propuesto para este problema en los cultivos agrícolas intensivos. Sin embargo, la implementación de un manejo integrado de plagas hacia una especie de artrópodo en particular involucra aspectos económicos, ecológicos y los respectivos a la magnitud del sistema de producción [3]. El diseño de una estrategia de manejo integrado de plagas (MIP) acorde a los sistemas de producción se justifica en el sentido que las plagas se adaptan con relativa facilidad a las nuevas condiciones microclimáticas, sin importar su magnitud de cambio [4].
Bemisia tabaci es conocido por su diversidad genética y se considera un complejo de biotipos o de especies crípticas; se identifican al menos 40 especies morfológicamente indistinguibles [1]. Actualmente se investigan dos especies crípticas de B. tabaci que invaden a los cultivos: MEAM1 y MED/Q; esta última es más resistente a los insecticidas [5]. Ante esto, se ha sugerido alternar los ingredientes activos que se emplean para su control. Con esa finalidad han surgido organismos independientes, tal como el Comité de Acción contra la Resistencia a los Insecticidas (IRAC, por sus siglas en inglés) en España, los cuales ofrecen una respuesta coordinada de las industrias de agroquímicos para proteger las plantas y para prevenir o retrasar el desarrollo de resistencia de las plagas a los insecticidas. Si bien se ha logrado comprender la selección correcta de los insecticidas, aún siguen presentándose nuevos casos de resistencia en todo el mundo [6]. Lo anterior invita a redireccionar en la búsqueda de nuevas estrategias de control, o a la innovación de las ya existentes para que puedan ser insertadas de manera correcta en los diversos sistemas de producción agrícola.
La implementación de estrategias de control eficientes y sustentables serán cruciales para implementar nuevos programas de MIP contra esta plaga, acorde a los sistemas de producción agrícola. El objetivo del presente escrito es revisar los avances en las estrategias de control de la mosquita blanca (Bemisia tabaci), así como también brindar información de los materiales y organismos biológicos más empleados en los sistemas de producción de cultivos agrícolas intensivos.
Estrategias de control antes de la plantación
Entre las estrategias de control de la mosquita blanca, las más importantes son las que se ejercen antes de la plantación. Los invernaderos con ventanas frontales y cenitales y ventilas cubiertas con mallas antiáfidos proporcionan una alta protección contra los adultos de mosquita blanca y reducen los problemas de virus transmitidos por esta plaga. Se comprobó recientemente que esta protección, en conjunto con el acolchado plástico aluminizado reflectivo como cubierta de suelo, logra mejores resultados de control [7]. Esto se debe a que la reflectividad del material del suelo provoca desorientación a los insectos voladores. El empleo de materiales plásticos producidos con tecnología reciente presenta como característica principal una alta capacidad absorbente o bloqueadora de radiación UV, con lo cual se registran reducciones significativas en la densidad poblacional de mosquita blanca en comparación a los plásticos convencionales [8].
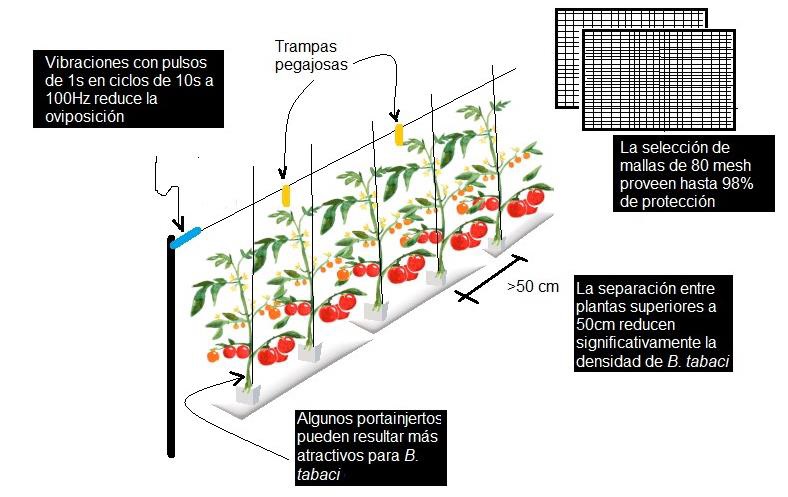
Los plásticos de color amarillo se han usado especialmente como trampa y para el monitoreo de la incidencia a pequeña y a gran escala de la mosca blanca; sin embargo, los alcances en su captura han presentado limitaciones. Se ha progresado en la implementación del conteo automático de ninfas de áfidos que podría reducir los esfuerzos e incrementar la precisión en el monitoreo y muestreo de la mosquita blanca [9]. Aunada a esta técnica, se ha practicado la vibración de las plantas establecidas en sustrato, a través de la cual se logra aumentar un 15 % la eficiencia de captura [10]. El principio de esta técnica se basa en impedir que los adultos de mosquita blanca se posen en las hojas para ovipositar y al mismo tiempo son interceptadas por las trampas amarillas (Figura 1). Estudios en etapa de pilotaje han demostrado que la aplicación artificial de radiación UV-C en un invernadero logra reducir la densidad de la población de mosquitas hasta en un 75 % [11]; asimismo, se evalúa el uso de lámparas led para la desorientación de los insectos fitófagos [12].
Estrategias de control durante la producción
Los insectos hemípteros de la familia aleyrodidae seleccionan a sus hospederos mediante estímulos visuales y olfativos, por lo que una estrategia ha sido alterar esta habilidad, para así reducir su incidencia. Una manera de modificar la habilidad olfativa y visual de los insectos fitófagos se logra con la aplicación de caolín. El caolín es un mineral compuesto de aluminosilicato, inerte, no tóxico que se ha empleado en el procesamiento de alimentos y como aditivo de cosméticos y productos de la salud. Se ha probado exitosamente para el control de la mosquita blanca, ya que reduce la tasa de oviposición y el número de adultos cuando es asperjado a las hojas de las plantas. Su aplicación se realiza por aspersión, hasta formar una película. Se ha observado que esta afecta el comportamiento de los insectos, por el contacto con superficies tratadas o su reflectividad, ya que emite un color blanquecino.
El caolín es fácilmente disuelto en agua. Para su aplicación, se debe cubrir uniformemente las plantas para asegurar la efectividad del producto. Han sido pocos los intentos de combinar el caolín con otras sustancias para aumentar su efectividad insecticida. Sin embargo, recientemente se reportó que la combinación de caolín con el limoneno muestra efectos aditivos en la repelencia de adultos de mosquita blanca comparado con los tratamientos por separado [13].
Por su parte, las tierras diatomeas también pueden funcionar como insecticidas no tóxicos, por lo que se han empleado para la protección de granos almacenados y el control de las plagas de los hogares y jardines. Si bien no existen registros del control directo de las tierras diatomeas sobre la mosquita blanca, se reportó recientemente que las plantas tratadas con este insecticida natural fueron menos preferidas para la oviposición por B. tabaci[14]. Hay diferentes teorías respecto de su efecto insecticida, la más aceptada es que las partículas se incrustan en la cutícula de los insectos, lo cual les causa muerte por desecación. También se considera que la abrasión puede ser una acción secundaria, ya que solo de este modo ocasionaría microheridas. Debido a su modo de acción, se considera que los insectos no presentan mecanismos de resistencia [15].
Los aceites minerales y los jabones agrícolas han mostrado altos porcentajes de control contra B. tabaci y B. argentifolli[16]. Los aceites de pulverización a base de petróleo se han usado por muchos años para controlar un amplio rango de insectos plaga. Actualmente, estas sustancias se consideran no tóxicas para los vertebrados, en comparación con los insecticidas sintéticos, y presentan actividad insecticida, principalmente por causar anoxia o por los efectos tóxicos hacia los insectos.
Los jabones agrícolas, por su parte, se les considera efectivos contra estados inmaduros de mosquita blanca. Recientemente se reportó que el control de B. tabaci con hongos entomopatógenos como Beauveria bassiana aumenta considerablemente cuando los insectos se tratan previamente con jabones agrícolas [17]. El efecto principal de los jabones agrícolas es el bloqueo de los espiráculos de los adultos y la remoción de cera, lo cual facilita que los insectos sean infectados por los hongos [18].
El control de las plagas con extractos botánicos es actualmente una alternativa real al uso de insecticidas químicos, han sido reportados como compuestos que no dañan al ambiente. Además, su toxicidad hacia los mamíferos, artrópodos depredadores, parasitoides, y polinizadores es casi nulo. El neem (Azadirachta indica) es un biopesticida botánico ampliamente conocido por sus propiedades bactericida, herbicida, fungicida, nematicida e insecticida, por lo que ofrece una alternativa ecológica a los insecticidas sintéticos. Hoy en día, más de 200 compuestos bioactivos han sido extraídos del neem y varias formulaciones comerciales han sido desarrolladas y registradas como biopesticidas de amplio espectro [19]. El mayor compuesto constituyente de las semillas y hojas de neem es la azadiractina, la cual presenta una acción insecticida equiparable a los agroquímicos convencionales.
Actualmente se evalúa el potencial de repelencia de los aceites esenciales extraídos de varias especies vegetales contra B. tabaci MED/Q con resultados promisorios. Si bien la acción insecticida y de repelencia es el efecto inmediato de los aceites esenciales, se ha reportado que su combinación con otros compuestos incrementa sus propiedades insecticidas. El efecto de control de los extractos vegetales se ha atribuido a los metabolitos que contienen algunas especies. Por ejemplo, Momordica charantia es una especie vegetal de la familia Cucurbitaceae que produce compuestos triterpenoides en las hojas, frutos y semillas, los cuales inducen un comportamiento antialimentario y tienen propiedades de inhibición de la oviposición en B. tabaci[20].
El campo del control biológico ha crecido y cambiado en muchas maneras desde inicios del siglo XXI. Los enemigos naturales como depredadores, parasitoides y entomopatógenos para el control de las plagas en la agricultura, tanto en la producción a cielo abierto como en ambiente protegido, se han diversificado significativamente. Entre los depredadores que actualmente se emplean en invernadero contra mosquita blanca durante la producción agrícola se encuentran los siguientes: Dicyphus hesperus Fieber (Miridae: Bryocorine: Dicyphini), Nesidiocoris tenuis (Hemiptera: Miridae), varias especies del género Macrolophus Fieber, Orius laevigatus (Hemiptera: Anthocoridae) [21], [22], [23] y Chrysoperla zastrowi (Neuroptera: Crisopidae), aunque C. carnea está disponible comercialmente en mayor proporción [24]. Delphastus catalinae Horn (Coleoptera: Coccinellidae) es el depredador que más se emplea para el control de la mosca blanca a nivel mundial [21]. N. tenuis es un depredador que se está introduciendo en invernaderos de Sur América contra otras plagas como la polilla del tomate Tuta absoluta (Lepidoptera: Gelechiidae) [25]; sin embargo, este depredador es dañino a los cultivos cuando hay escasez de su presa [26]. Entre los ácaros depredadores que se liberan actualmente encontramos a los del género Amblyseius (Acarina: Phytoseiidae) tales como A. tamatavensis, A. cucumeris, y A. swirskii[29]. Dicyphus hesperus es particularmente efectivo contra las ninfas de B. tabaci[27].
Los parasitoides más efectivos en invernadero son: Encarsia formosa (Hymenoptera: Aphelinidae) y Eretmocerus eremicus (Hymenoptera: Aphelinidae) [28]. Se ha demostrado que la población de Encarsia sophia puede aumentar rápidamente y puede llegar a tener un potencial de parasitación más alto que Eretmocerus hayati contra B. tabaci[29]. Para aumentar la eficiencia del control biológico contra mosquita blanca en invernadero, se ha analizado la liberación simultánea de depredadores y parasitoides. Eretmocerus mundus coexiste con los depredadores Macrolophus pygmaeus y Nesidiocoris tenuis (Figura 2). Se ha registrado que para la liberación de dichos insectos depredadores y parasitoides es necesario cuidar el tiempo de la última aplicación de insecticidas; aunque actualmente varios proveedores de estos insectos benéficos reportan compatibilidad de los insectos con algunos ingredientes activos, lo cual permite planear anticipadamente su inserción en un programa de MIP.
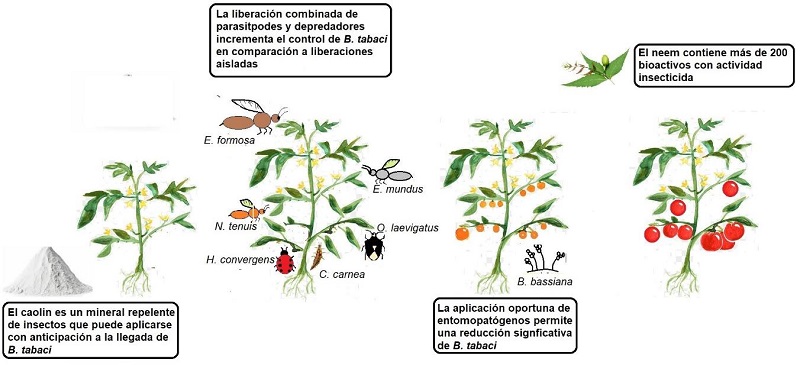
Figura 2 Algunas estrategias que actualmente se emplean para el manejo y control de B. tabaci durante la producción y que reducen significativamente la problemática (elaboración propia)
El empleo de hongos entomopatógenos registra avances significativos. Éstos presentan la capacidad de degradar la cutícula del insecto plaga a través de enzimas proteasas tales como lipasas y quitinasas, seguido por la penetración de los tubos germinativos fúngicos al interior del insecto; posterior a ello, sucede la liberación de micotoxinas [30]. Los hongos entomopatógenos disponibles en forma comercial para el control de la mosquita blanca son Beauveria bassiana, Metharhizium anisopliae y Lecanicillium lecanii. En específico, L. lecanii ha mostrado capacidad para reducir la densidad de población de B. tabaci hasta en un 60 % en cultivos de chile (Capsicum annum L.) [31]. El uso sinérgico de los enemigos naturales de B. tabaci (depredadores y parasitoides) con entomopatógenos, o insecticidas botánicos ha resultado exitoso, salvo en ciertas excepciones, ya que los entomopatógenos afectan a las poblaciones de parasitoides con relativa facilidad [32].
Nuevas tecnologías contra la problemática de la mosquita blanca
Actualmente se proponen nuevas estrategias de control que prometen una afectación directa a los insectos sin causar disturbios en los agroecosistemas. La interferencia del ARN es un tipo de silenciamiento postranscripcional en el cual se introduce en una célula del insecto objetivo un ARN doble cadena (ARNdc). Lo anterior se conduce con el objetivo de producir generaciones de fenotipos de la plaga con limitaciones genéticas o pérdida de funciones. Actualmente, numerosos estudios se conducen alrededor del mundo con el objetivo de afectar todos los estadios de las plagas. Recientemente se reportó la reducción en la expresión de genes que codifican para las hormonas esterasas juveniles en moscas alimentadas con 2.5-1.0 µg/µL de ARNdc [33]. También se registró una significativa mortalidad y disminución en la expresión de genes involucrados en el metabolismo energético y la biosíntesis de la quitina de adultos de mosquita blanca a través del silenciamiento de los genes BtTPS [34]. Con la tecnología de la interferencia ARNdc también se pretende afrontar los daños secundarios que causa B. tabaci. En 2021, se reportó que la supresión de la Bta11975, una alfa glucosidasa, por interferencia ARN redujo la transmisión del Virus de la Clorosis del Tomate por esta plaga [35] (Figura 3).
Figura 3 Tecnología de la interferencia ARNdc (doble cadena de ARN) que actualmente se utiliza para el control de B. tabaci y efectividad que se ha registrado con su aplicación (elaboración propia).
La nanotecnología (NT) a través del uso de los nanomateriales ha sido una herramienta muy útil en el desarrollo de la ciencia. En años recientes, la NT aplicada a la agricultura ha sido enfocada al desarrollo de productos antimicrobianos y antiparasitarios. Las nanopartículas (NPs) a base de metales incrementan la actividad antimicrobiana por su bioreactividad, la cual es causada por el aumento de su área superficial al convertirse en nanopartícula. Esto ha conducido al desarrollo de nanomateriales, entre los que se incluyen las NPs metálicas de Ag, Cu, Fe, ZnO, entre otros. Su aplicación en el control de B. tabaci ha registrado buenos resultados, por ejemplo, la combinación del caolín con nanopartículas de óxido de zinc causó mayor mortandad de la mosquita blanca en el cultivo de algodón [36]; el tamaño de las nanopartículas facilita su entrada a través de la cutícula de los insectos. Por otra parte, se ha demostrado que el caolín y la zeolita como nanopartículas presentan alta adhesión a las plagas y reducen su capacidad de locomoción sobre la superficie vegetal [36]. Recientemente se reportó que el aceite esencial de Xylopia aromatica (Annonacee) en formulación como nanoencapsulado disminuye hasta un 98 % la oviposición de B. tabaci en plantas de frijol en comparación con tratamientos convencionales [38].
Conclusión
Ante la resistencia de la mosquita blanca a los insecticidas y a las tecnologías que emergen como alternativa de control, se avizora cada vez más la necesidad de un nuevo planteamiento de control de plagas enfocado a los sistemas de producción agrícola intensivos. Estas estrategias de control se deberán considerar para emplearse de manera conjunta durante un ciclo completo de producción intensiva, por lo que requerirán de una evaluación técnico-económica para ser aplicadas a escala mayor con el fin de propiciar una aplicación más precisa de los recursos. También, en el futuro inmediato, el uso de las tecnologías emergentes tales como los nanopesticidas representarán un reto: deberán adaptarse a un entorno arduo que requiere respuestas inmediatas de control, tal como la producción intensiva de cultivos agrícolas. Por ello, para facilitar esta labor, deberán observarse en todo momento fuentes fidedignas de información. Asimismo, el descubrimiento de nuevos agentes de control (depredadores, parasitoides, y entomopatógenos), preparados botánicos y nanopartículas sugieren retos relacionados con la inocuidad que debe guardarse durante la producción. En este contexto, el conocimiento de las respuestas biológicas de los organismos resulta primordial antes de emplear cualquier nuevo agente en el MIP.











 nova página do texto(beta)
nova página do texto(beta)