Antecedentes
El angiomiolipoma renal (AML) se define como un tumor renal compuesto de grasa, músculo y vasos sanguíneos.1-3 Representa del 2 al 6% de todos los tumores renales.4 Se estima que existen más de 10 millones de personas en todo el mundo con AML renales y el 10% de ellos también tienen el complejo de esclerosis tuberosa (CET).3 Existe una alta prevalencia de AML renal en pacientes con CET del 55-90%, los cuales son generalmente multifocales y bilaterales.5-7
Es más común en mujeres (61.8%).6-8 La edad de presentación en los pacientes con CET es entre los 20 y 30 años.9,10 Generalmente el diagnóstico es incidental. Cuando el tamaño del tumor excede los 4 cm, la mayoría de los pacientes desarrollan síntomas relacionados con el sangrado tumoral y el efecto de masa.11
La hemorragia renal espontánea (HRE), o síndrome de Wünderlich, se describió por primera vez en 1856, contando únicamente con 450 casos reportados para el año 2000, y se caracteriza por un inicio agudo de formación de hematoma subcapsular y perirrenal no traumático.9,12 El primer caso de angiomiolipoma descrito en México fue en el año 1973.13
El riesgo de hemorragia por angiomiolipoma renal oscila entre el 25% y 50%. En su mayoría debido a neoplasias renales (56,9%), con un 74,1% debido a AML y el carcinoma de células renales (CCR).3,5,12
La TC (tomografía computada de abdomen) identifica la hemorragia perinéfrica con una sensibilidad del 100% y los AML como masas renales bien circunscritas con grasa intratumoral (−20 a −40 UH).12
La HRE suele poner en peligro la vida debido a un shock hemorrágico y requiere un reconocimiento rápido y un manejo adecuado.9,11,14,15
En el tratamiento de la HRE, la embolización y la nefrectomía son intervenciones recomendadas a pacientes con mayor riesgo de complicaciones hemorrágicas potencialmente mortales y dolor lumbar debido a grandes AML, que no respondieron al manejo conservador.4,16
Presentamos un caso raro de choque hipovolémico debido a la ruptura de un AML renal (síndrome de Wünderlich), que tras el fracaso al tratamiento con embolización transarterial selectiva, se manejó mediante nefrectomía total urgente.
Caso clínico
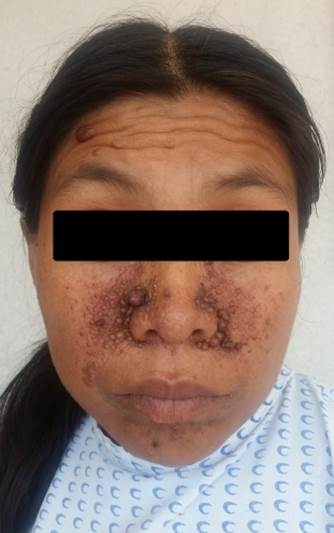
Acudió una mujer de 34 años a la sala de urgencias con síntomas de dolor abdominal moderado de hipocondrio derecho, con una duración de 3 h, acompañado de distención progresiva y dolorosa del área abdominal lateral derecha. Su historia clínica no revelaba datos de importancia, ni antecedente de trauma previo al ingreso. Tras el examen clínico, la paciente presentaba hamartomas cutáneos centrofaciales (Figura 1), se observó un incremento de volumen, dependiente de una masa indurada y dolorosa a lo largo del hemiabdomen derecho, así como palidez, sudoración, taquicardia y hematuria. La presión arterial fue de 75/50 mmHg, pulso 110 por minuto. El análisis de sangre original mostró Hct 23% y Hb 7,6 g/dl y hematuria macroscópica.
En estudio tomográfico contrastado (Figura 2) se reveló una tumoración sólida heterogénea que contenía grasa en riñón derecho, con un diámetro máximo de 14 cm y un hematoma renal sangrante que se desplaza hacia el espacio perirrenal, así como riñón contralateral con múltiples lesiones heterogéneas con densidad -20 UH, sin otras alteraciones. La paciente se trató en forma conservadora de manera inicial mediante transfusión de hemoderivados, estabilización hemodinámica, reposo absoluto y vigilancia clínica. Durante 18 horas de seguimiento en hospitalización evolucionó de manera favorable, sin embargo la paciente desarrolló taquicardia e hipotensión; la hemoglobina se redujo a 7.2 g/dl y el hematocrito al 22.9%, por lo que se sometió a una embolización transarterial de emergencia (Figura 3) a través de la arteria renal derecha utilizando un microcatéter y partículas de alcohol polivinílico, tras lo cual remitió el sangrado estabilizándose el estado hemodinámico. Sin embargo, presentó nuevamente datos de choque hipovolémico, hematuria recurrente y nuevo descenso de la concentración de hemoglobina de 11,2 g/dl a 6,9 g/dl. La paciente describió dolor intenso y sudoración. Considerando la condición inestable y hemorrágica creciente, se tomó la decisión de realizar manejo quirúrgico definitivo mediante nefrectomía total derecha.
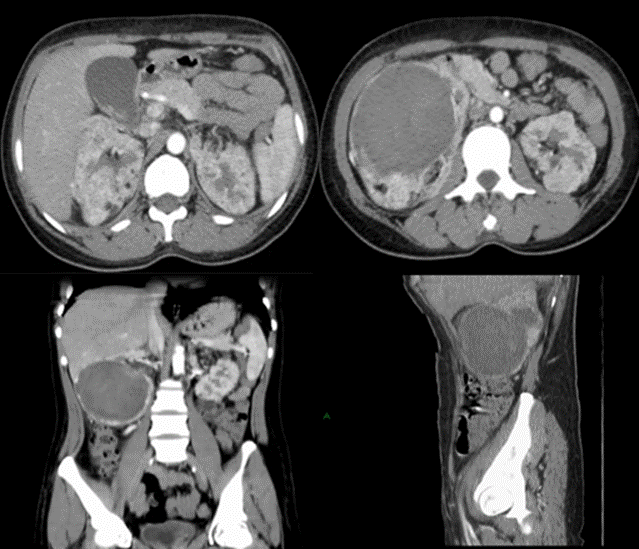
Figura 2 Tomografía contrastada de abdomen donde se aprecia hematoma dependiente de riñón derecho y angiomiolipomas en ambos riñones
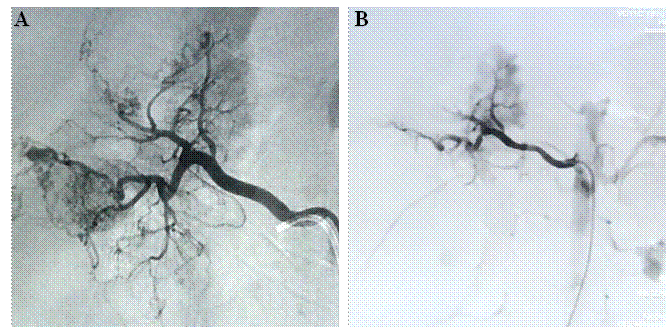
Figura 3 Angiografía renal mostrando (A) riñón derecho con angiomiolipoma y vasos tortuosos que lo irrigan abarcando polo inferior, medio y parte del superior; tras angioembolización selectiva de arteria renal segmentaria inferior derecha (B)
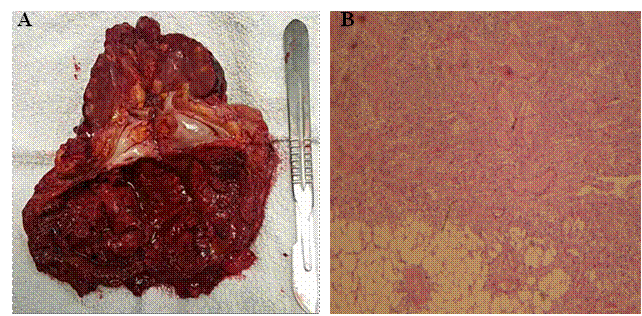
Durante la cirugía, se encontró un tumor hemorrágico grande compuesto por abundantes vasos sanguíneos, que se originó en el riñón derecho, eliminado en bloque con el riñón (Figura 4A). Un examen patológico macroscópico de la muestra reveló un tumor marrón oscuro que mide 11×9×13 cm, principalmente en la región del parénquima renal. Microscópicamente, estaba compuesto de vasos en proliferación, células grasas y células del músculo liso del huso con hemorragia extensa, sin evidencia de malignidad. Se transfundieron 4 unidades de sangre en el trans y postoperatorio. La paciente fue dada de alta al quinto día postoperatorio. La bioquímica de rutina y el análisis de sangre a los 3 meses de seguimiento postoperatorio fueron normales. Su recuperación transcurrió sin incidentes.
Discusión
En México existe una serie de AML renales, la cual se realizó en el Hospital de Especialidades Centro Médico La Raza. En ésta, en un periodo de 10 años se encontraron nueve AML renales en 302 tumores renales, lo cual representó 2.9% de los casos. Solo tres de sus pacientes tuvieron esclerosis tuberosa, sin presentar hemorragia por ruptura espontánea del tumor.17 Por otra parte, un hospital privado de la Ciudad de México evaluó su casuística en un periodo de 15 años encontrando solo 10 casos de AML renales en un total de 310 nefrectomías (3.2%) y 4.6% de todos los tumores renales, de los cuales cuatro pacientes presentaron hemorragia espontánea.18
Los angiomiolipomas pertenecen a una familia de tumores denominados neoplasias con diferenciación epitelioide perivascular (o PEComas). Las células epiteliales perivasculares (PEC, por sus siglas en inglés), que dan lugar a los 3 tipos celulares identificados en el AML renal son las células progenitoras del AML.16,19
Pueden ser unilaterales o bilaterales. Los bilaterales guardan una gran relación con la esclerosis tuberosa, presentándose hasta en el 50-80% de los pacientes con este complejo. En pacientes sin ET, la presentación de AML bilaterales es relativamente rara.6,10
La esclerosis tuberosa es un síndrome multisistémico caracterizado por síntomas neurológicos y tumores en múltiples órganos que incluyen riñón, cerebro, piel, ojos, corazón y pulmonares.6
El complejo de esclerosis tuberosa es una enfermedad autosómica dominante con una prevalencia estimada de 1 en 12,000.5,15,20 El síndrome de Wünderlich es una entidad con incidencia baja, en nuestro país, se han reportado casos esporádicos en hospitales de concentración.21
Los AML se han considerado hamartomas debido a su mezcla de músculo liso, tejido adiposo y vasos sanguíneos. La clonalidad en un hamartoma apoyaría un origen pluripotencial de células madre de diferentes componentes de la lesión.2,19 Se ha encontrado una frecuencia de AML en autopsias de 0.02% hasta 0.29% en población sin estigmas de CET.3
Predomina en mujeres, con crecimiento más rápido durante el embarazo, por probable influencia hormonal. El promedio de edad al diagnóstico es de 41 años.6,11 Los AML asociados con CET crecieron un promedio de 1.25 cm / año en comparación con los esporádicos de solo 0.02-0.19 cm / año.4,9,10
Histológicamente, estos vasos no tienen una lámina elástica interna y su capa de músculo liso se rompe, por lo que son propensos a la formación de aneurismas y a la ruptura.11,22
El tamaño de los tumores varía y se clasifican como pequeños (<4 cm), medianos (4-8 cm) y grandes (>8 cm). El AML <4 cm generalmente es asintomático y su diagnóstico es incidental. Los mayores de 8 cm, son responsables de una morbilidad significativa, requieren tratamiento antes de desarrollar sintomatología y potenciales complicaciones.15,19,23
Hasta dos tercios de los pacientes tienen mutaciones esporádicas a TSC1 y TSC2. TSC1 y TSC2 codifican proteínas que llevan los mismos nombres, también conocidos como hamartina y tuberina, respectivamente.5,15
La pérdida de TSC1 o TSC2 conduce a una activación no controlada de la vía de la rapamicina (mTOR), lo que conduce a una síntesis de proteínas no regulada y a un mayor crecimiento y proliferación celular, mayor angiogénesis y cambios en la orientación y migración celular.5
Las complicaciones más comunes son las lesiones cutáneas, que incluyen máculas hipomelanóticas, fibromas ungueales y angiofibromas faciales. El 90% también presenta manifestaciones neurológicas, caracterizadas por convulsiones, disfunción cognitiva y trastornos del comportamiento, siendo las convulsiones el síntoma más frecuente, que ocurre en 70 a 80% de los pacientes con CET.15,24
Histológicamente, un angiomiolipoma típico se compone de tres componentes (Figura 4B): vasos (angio); células fusiformes (mio) y tejido adiposo (lipo). Los vasos son típicamente excéntricos y de paredes gruesas. Inmunohistoquímicamente, HMB-45 y melanina A, marcadores melanocíticos, a menudo son positivos en el componente de células fusiformes de AML.5,9
La complicación más grave e indeseable del AML renal es el sangrado, que puede ser mortal. El sangrado en AML renal puede ser espontáneo o puede seguir a un trauma. Casi la mitad de los casos que son mayores de 4 cm desarrollan sangrado espontáneo.11 El primer reporte de ruptura espontánea del parénquima renal fue descrito por Bonet en 1700; sin embargo, en 1856 Wunderlich informó un síndrome caracterizado por hemorragia perirrenal espontánea de localización intraperirrenal o subcapsular.25,26
El principal predictor de hemorragia es el tamaño tumoral.27 En un estudio se demostró que los pacientes que presentaban hemorragia retroperitoneal mayor (54 de 441 pacientes) tenían tumores significativamente más grandes que los pacientes sin hemorragia.28
Los factores principales que aumentan el riesgo de hemorragia son el tamaño del tumor en el momento del diagnóstico, el aumento de tamaño en un tumor que está bajo seguimiento y un tumor sintomático y esclerosis tuberosa que acompaña al AML renal.11 Hasta el 80% de los pacientes adultos con CET desarrollan angiomiolipoma, que generalmente es bilateral y múltiple con un riesgo de hemorragia de por vida alrededor de 20%.24
La segunda morbilidad de los angiomiolipomas renales es la invasión insidiosa del angiomiolipoma en el tejido renal normal, que puede conducir a insuficiencia renal. Aproximadamente el 1% de la población de pacientes con CET recibe terapia de reemplazo renal dialítico, estimándose que más de 30,000 pacientes con CET están en diálisis en el mundo.29,30
Algunos pacientes pueden presentar la tríada de Lenk que consiste en dolor lumbar agudo o abdominal, un tumor palpable en el flanco e hipovolemia.14,15
Aunque los angiomiolipomas pequeños suelen ser asintomáticos, los angiomiolipomas ≥4 cm se vuelven sintomáticos en el 68-80% de los pacientes, y el 50-60% se presenta como hemorragia, teniendo hasta el 20% estado de choque al momento de la presentación inicial.27,29 La causa principal de los casos de hemorragia renal espontánea es un tumor, y representa el 57% al 63% de los casos.31
Las modalidades radiológicas utilizadas en la evaluación del AML renal incluyen ultrasonido, TC y resonancia magnética (RMN). El ultrasonido por sí solo no se puede utilizar en el diagnóstico de AML renal porque el carcinoma de células renales también puede ser hiperecoico al igual que el AML.11
La TC es 100% sensible a la presencia de hemorragia retroperitoneal, y tiene una mayor sensibilidad y especificidad que la ecografía para la identificación de una masa renal subyacente.30-32 Un umbral de atenuación de -10 UI o menos con una región de interés de al menos 19-24 mm2 es óptimo para el diagnóstico de angiomiolipoma.33
En el 4-5% de los AML, la grasa intralesional no se puede detectar en la TC debido a la pequeña cantidad de grasa dentro de la lesión o por puede verse oculta por una hemorragia. En estos casos, la RMN puede ser útil. La RMN, como la TC, es precisa y específica para la AML, con nula exposición de radiación ionizante del paciente.5,10
Además, se puede hacer RMN sin contraste, vital en pacientes con función renal comprometida. Las desventajas de la RMN son el costo, el tiempo y la disponibilidad reducida en comparación con la TC.5
La práctica contemporánea se ha desplazado hacia el tratamiento inicial mínimamente invasivo centrado en preservar el tejido renal para controlar y potencialmente prevenir futuras hemorragias, que comprenden embolización transarterial (TAE) (42,2%) y tratamiento conservador/médico (29,4%), con la cirugía inicial (incluida la exploración/lavado) realizada menos comúnmente (27,5%).34,35 La vigilancia activa es la opción más común para el manejo de la enfermedad AML esporádica que no involucra una intervención renal invasiva, aunque el objetivo de los inhibidores de la rapamicina (mTOR) puede usarse en algunos pacientes con AML.4
El mecanismo de acción de los inhibidores de mTOR es actuar como un freno y bloquear la señalización constitutivamente ascendente de fosfatidilinositol-3- quinasa (PI3K)/proteína quinasa B (Akt)/mTOR responsable de las manifestaciones de CET. Se han evaluado dos inhibidores de mTOR, sirolimus y everolimus. Everolimus actualmente es el único aprobado por la Administración de Alimentos y Medicamentos (FDA) para el tratamiento de pacientes con CET y AML así como pacientes con CET-astrocitoma subependimario de células gigantes (SEGA).8,29
En el ensayo de fase III más grande jamás realizado en pacientes con CET que tienen AML renal (EXIST-2), 10 mg diarios de everolimus oral resultaron en una reducción significativa de todos los volúmenes de AML renales ≥50% en relación con el valor basal; además redujo el tiempo hasta la progresión del AML.8
Para el AML renal hemorrágico, las principales alternativas de tratamiento son la embolización transarterial conservadora, la nefrectomía parcial o total y la cirugía inmediata o tardía después de la embolización.36 El 43.3% de los pacientes que se someten a un tratamiento conservador ameritan tratamiento adicional por tasa de recidiva de la hematuria.5,12
Históricamente, los criterios de intervención en casos de AML renal han sido lesiones sintomáticas, tamaño >4 cm, sospecha de malignidad y mujeres en edad fértil. También se incluyen un diámetro del aneurisma >2.5 cm, hipertensión renovascular con valores de renina lateralizante, aneurisma sintomático, expansión documentada y embarazo actual o anticipado. CET concomitante y acceso deficiente al seguimiento o atención de emergencia como consideraciones adicionales para el tratamiento.9,12
La embolización transarterial selectiva es una técnica de preservación del parénquima que brinda al intervencionista la oportunidad de embolizar solo aquellos vasos que irrigan el tumor con partículas de alcohol polivinílico (PVA) logrando resultados duraderos a largo plazo y con mayor preservación de tejido renal funcional. La primera embolización electiva de la arteria renal se realizó en 1973, y desde entonces se han publicado varios informes.36-38
Las principales complicaciones de la embolización selectiva con una incidencia del 10% son sangrado, disección, oclusión, sepsis, fístulas urinarias, embolización fuera del objetivo y síndrome posterior a la embolización caracterizado por fiebre, dolor lumbar y leucocitosis que se presenta hasta en un 80% y se maneja de forma conservadora. Además, puede haber necrosis del tumor, infarto renal y, en caso de infección, pueden desarrollarse abscesos. Si esto último ocurre, puede ser necesario el drenaje percutáneo o la nefrectomía.22,38
Reportes anecdóticos de informes sobre el uso de terapias ablativas laparoscópicas y percutáneas para la AML se limitan en gran medida a tumores pequeños y asintomáticos.5,9
Sin embargo, para los pacientes con hematuria refractaria, deterioro del estado hemodinámico o en quienes ha fallado el tratamiento mediante embolización selectiva, es necesario intervención quirúrgica para evitar desenlaces catastróficos. Tradicionalmente, la nefrectomía radical o parcial se ha preferido para el tratamiento en hasta el 73% de los pacientes, para controlar la hemorragia aguda y extirpar la neoplasia renal como posible causa subyacente.12,19
Las nefrectomías parciales corren el riesgo de una hemorragia significativa y, por lo tanto, solo deben realizarse si se indica inequívocamente, sin embargo Vega-Castro et al., la han descrito en casos de AML bilateral para prevenir la enfermedad crónica terminal.3,39 En pacientes con insuficiencia renal o funciones renales limitadas, es muy importante preservar el tejido renal sano. Si el tumor no ha invadido totalmente el riñón, podría considerarse la nefrectomía parcial en casos individualizados.11
La paciente en nuestro estudio presentaba inestabilidad hemodinámica, caída de los niveles de hematócrito y se encontró un tumor renal grande compuesto de abundantes vasos sanguíneos, de fácil sangrado durante la cirugía (Síndrome de Wünderlich); por lo tanto, fue necesaria una nefrectomía total para preservar la vida.
Conclusión
En resumen, el angiomiolipoma puede causar complicaciones graves a través de rupturas espontáneas y hemorragias potencialmente mortales. Estos pacientes requieren una intervención urgente, ya que el sangrado retroperitoneal puede provocar complicaciones graves y aumentar la morbilidad. En caso de angiomiolipoma con hemorragia intratumoral masiva o compromiso renal completo y síntomas del síndrome de Wünderlich, la nefrectomía total es una buena opción de tratamiento para preservar la vida del paciente, después de haber realizado manejo conservador y/o angioembolización selectiva.











 nova página do texto(beta)
nova página do texto(beta)