Introducción
En los últimos años, la modelación matemática ha tomado relevancia en el estudio de procesos biológicos para el tratamiento de agua, en donde se usan bacterias en suspensión o en crecimiento adherido (biopelícula). Para sistemas en suspensión, la modelación matemática juega un papel importante, ya que permite diagnosticar problemas y optimizar procesos (Shi, Long, Meng y Raajeevan, 2008). En cuanto a sistemas que usan bacterias con crecimiento adherido, la modelación matemática igualmente resulta fundamental, pues permite integrar componentes y procesos que ocurren en este microsistema, permitiendo entender su comportamiento (Wanner et al., 2006).
Uno de los procesos que ha sido modelado matemáticamente es la desnitrificación biológica, donde se han estudiado tanto sistemas en suspensión de aguas residuales como en aguas subterráneas (Calderer, Jubany, Perez, Marti y De Pablo, 2010; Henze, Gujer, Mino y van Loosdrecht, 2000; Shi et al., 2008); de igual forma, se han estudiado sistemas desnitrificantes de crecimiento adherido usando reactores de membranas (Matsumoto, Terada y Tsuneda, 2007), y en reactores fluidizados y biofiltros (Horn y Telgmann, 2000; Lin, 2008). El factor común en cada condición de tratamiento (en suspensión o adherido) es la dosificación de carbono orgánico, que además se usará como fuente de energía (Mateju, Cizinska, Krejci y Janoch, 1992). Los carbonos orgánicos comunes usados en el estudio de desnitrificación son glucosa, etanol y metanol (Horn y Telgmann, 2000; Lin, 2008; USEPA, 1993; Mateju et al., 1992); esta dosificación constante de carbono simplifica las condiciones iniciales y de borde al momento de hacer un planteamiento matemático.
Aunque la condición de dosificación constante de carbono simplifica la modelación matemática de los procesos de desnitrificación, los costos asociados con la operación de sistemas desnitrificantes han generado una incursión en estudios de fuentes alternas más económicas. Esto confirma lo expuesto por Garzón-Zúñiga (2005), quien señala la necesidad de investigar más sobre mecanismos no convencionales para el tratamiento del nitrato. En este sentido, los sustratos sólidos orgánicos naturales (SSON) se han convertido en fuentes alternativas de carbono para la desnitrificación debido a ciertas características que podrían ser aprovechados. Boley, Muller y Haider (2000) señalan que una de las ventajas de contar con un sustrato sólido biodegradable, de donde las bacterias obtengan su fuente de carbono y energía, es que se elimina la necesidad de dosificar carbono soluble, y además funcionan como un portador o soporte para las bacterias formadoras de biopelícula. Esto se ha demostrado en estudios de rendimientos (Tabla 1).
Tabla 1 Comparación de costos y rendimientos de sustratos convencionales y sustratos sólidos orgánicos naturales.
| Sustrato | Costo de sustrato ($/kg) | Costo por kg nitrato removido ($/kg N-NO3-) | Consumo de sustrato (kg/kg N-NO3-) | Tasa de desnitrificación (kg N-NO3-/m3día) | Referencias |
|---|---|---|---|---|---|
| Metanol | 1.13 | 2.26 - 4.52 | 2.08 - 3.98 | 3.48 | Boley, Muller y Haider (2000) |
| Etanol | 1.36 | 2.71 | 2.0 | 1.29-1.59 | |
| Algodón | 0.53 | 1.48 | 2.8 | 2.8 | Soares et al. (2000); Volokita et al. (1996a) |
| Gracilaria verrucosa | 1.13 | 1.05 - 1.62 | 0.93-1.43 | 0.27 | Ovez, Mergaert y Saglam (2006a) |
Adicional a estudios de SSON como los presentados en la Tabla 1, experimentalmente es mucho lo que se ha continuado investigando sobre el uso de SSON. Entre los trabajos con SSON realizados están los siguientes: algodón (Della-Rocca, Belgiorno, y Meric, 2007; Della-Rocca, Belgiorno, y Meric, 2005; Soares y Abeliovich, 1998); aserrín (Healy, Rodgers, y Mulqueen, 2006; Schipper & Vojvodic-Vukovic, 1998); virutas y cortezas de árboles (Aslan y Turkman, 2003; Gibert, Pomierny, Rowe, y Kalin, 2008; Saliling, Westerman, & Losordo, 2007); paja de trigo (Aslan & Turkman, 2003; Aslan y Turkman, 2004; Aslan y Turkman, 2005); algas marinas (Ovez, Ozgen, & Yuksel, 2006b); y gramíneas (Deago y Pizarro, 2013; Deago y Pizarro, 2015). Con estas investigaciones se demuestra que es posible remover nitrato, usando SSON como fuente de carbono tanto para aguas residuales como para agua potable.
Se ha comprobado experimentalmente que la liberación de carbono orgánico en ensayos de desnitrificación usando SSON ocurre en una serie de procesos secuenciales iniciando por la lixiviación; luego, la colonización del SSON por las bacterias que forman la biopelícula; después se da el proceso de hidrólisis enzimática por un consorcio especializado de bacterias que degradan el carbono biodisponible; por último se presenta la desnitrificación biológica (Deago y Pizarro, 2015). En estas condiciones, la hidrólisis es el factor limitante en la biodegradación de SSON (Angelidaki y Sanders, 2004). Sin embargo, la modelación matemática de desnitrificación usando SSON es una tarea pendiente necesaria para entender mejor cómo ocurren los procesos de liberación de carbono, la reducción de nitrato y la evolución de las bacterias de crecimiento adherido alrededor de estos materiales.
Por lo tanto, para este trabajo se usó la Saccharum spontaneum L. (paja canalera) como SSON de referencia, la cual fungió como portador o soporte para el crecimiento adherido de bacterias (biopelícula) y como la única fuente de carbono. Los datos de la Saccharum spontaneum L. se obtuvieron del trabajo de Deago y Pizarro (2013). El objetivo de la investigación fue evaluar la desnitrificación a través de un planteamiento matemático de sistemas de crecimiento adherido con un comportamiento en contragadiente del sustrato orgánico (donante de electrones) y del nitrato (aceptor de electrones). Para ello, la simulación del planteamiento matemático se realizó con el software libre AQUASIM.
Materiales y métodos
Desarrollo del modelo matemático
La representación conceptual de la desnitrificación usando sustratos sólidos orgánicos naturales (SSON) está basada en resultados obtenidos de estudios en reactores batch (Deago y Pizarro, 2013; Deago y Pizarro, 2015) (Figura 1). Para este modelo conceptual de desnitrificación se han identificado los siguientes componentes: a) SSON que actúa como portador o soporte de la biopelícula y, a su vez, la fuente de carbono orgánico; b) membrana permeable hipotética ubicada entre el SSON y la biopelícula, para representar el flujo de carbono (JDQO ); c) la biopelícula que crece alrededor del SSON; d) una capa difusa de agua entre biopelícula y la masa de agua; y e) la masa de agua (Figura 1).
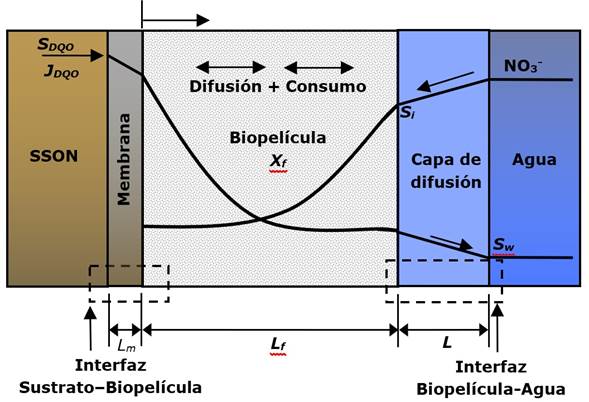
Figura 1 Esquema a nivel micro de transferencia y consumo de donante y aceptor de electrones en la interfaz SSON-biopelícula-agua; donde Xf es la densidad de la biopelícula activa; Lf , el espesor de biopelícula; Lm , espesor de membrana hipotética; L, es espesor de capa difusa; SDQO es concentración de carbono en SSON medido como DQO.
La desnitrificación del agua usando SSON básicamente es un proceso de biodegradación donde se usa al nitrato como el aceptor de electrones. Angelidaki y Sanders (2004) mencionan que la biodegradación está en función de la disponibilidad del aceptor de electrones y que la liberación de energía de las reacciones redox es usada para el crecimiento de las poblaciones microbianas. Este tipo de procesos de desnitrificación se presentan en sistemas naturales como humedales, donde la biodegradación de materiales detríticos ocurre bajo el agua (Reddy y DeLaune, 2008).
Para el desarrollo del modelo matemático se consideraron tres aspectos: compartimientos (descritos previamente), componentes (particulado y disuelto) y procesos (transformación y transporte) (Wanner et al., 2006). Los componentes se dividieron en solubles y particulados. Los compuestos solubles están representados por el aceptor de electrones (NO3-) y donante de electrones, que es el carbono orgánico liberado desde el SSON (representado como DQO). En tanto, el componente particulado corresponde a la biomasa (biopelícula). Finalmente, los procesos del sistema se definen así: consumo de donante y aceptor de electrones; crecimiento y decaimiento de bacterias; transporte (difusión); e hidrólisis de carbono estructural desde los SSON.
Para el desarrollo matemático de la desnitrificación se plantearon una serie de supuestos y consideraciones para los compartimientos, procesos, componentes y condiciones de operación, que a continuación se detallan.
Compartimientos
Se establece que el SSON es uniforme en su estructura, o sea que se considera homogéneo. La biopelícula cubrirá totalmente el SSON de forma uniforme y tendrá un espesor constante (modelo 1D) en estado estacionario. Rittmann et al. (2018) señalan que una buena aproximación para modelos de biopelícula es que se plantee unidimensional (1D). Esta biopelícula se considerará profundo, dado que es un sistema en ausencia de oxígeno y tendrá un comportamiento similar a la oxidación de carbón en el fondo de un filtro por goteo, cuyo espesor de biopelícula está en el rango de 100 µm (Rittmann y McCarty, 2001; Rittmann et al., 2018). Para representar el aporte de carbono orgánico desde el SSON, el cual será representado por la DQO, se asumió que la conexión con la biopelícula sería una membrana, en donde el movimiento del sustrato se basará en la primera Ley de Fick.
Procesos
A lo interno de la biopelícula se consideró la transformación tanto del donante de electrones (DQO) como aceptor de electrones (NO3-) y el movimiento por difusión en contragradiente de ambos compuestos. La transformación de los donantes y aceptores de electrones se definió como doble Monod, porque ambos sustratos pueden ser factores limitantes del sistema (USEPA, 1993). Esta cinética de Monod capta el efecto de concentraciones de sustrato en el comportamiento de las tasas de síntesis de las bacterias (Wanner et al., 2006).
El transporte a lo interno de la biopelícula fue considerado por difusión en contragradiente y en dirección normal al plano de la biopelícula, en donde la DQO tiene la dirección desde el SSON hacia la biopelícula y el nitrato se mueve desde la masa de agua hacia la biopelícula (Figura 1). Se asume que estas condiciones de transformación y transporte ocurren en condiciones similares a un reactor de biopelícula por membrana. Según Nerenberg (2016), este tipo de sistema en contragradiente es muy favorable, pues permite que los procesos ocurran en la parte central de la biopelícula.
Componentes
Se asumió que la biopelícula tendría una densidad constante. Esta asunción es consecuente con lo reportado de sistemas en contragradiente de rectores de membrada, donde se desarrolla una única estructura microbiana (Nerenberg, 2016). El carbono liberado (DQO) desde el SSON será representado por el flujo JDQO , similar a modelación en rectores de biopelícula por membranas (Matsumoto et al., 2007; Zhu et al., 2018). Se estableció que el carbono orgánico será aportado por la hidrólisis de carbono estructural presente en el SSON. Se asumió que la liberación de la DQO desde el SSON será homogénea; es decir, que en cualquier punto de la interfaz SSON-biopelícula tendrá la misma concentración. Además, se estableció que el nitrato será el único aceptor de electrones y fuente de nitrógeno, dado que el sistema opera en condiciones anóxicas.
Condiciones de operación
La temperatura de operación será constante de 30 °C y, por lo tanto, se desprecia el efecto inhibitorio de la variación de este parámetro. El sistema se operó a pH entre 6.5 y 8.5. Se ha definido este rango de pH para la desnitrificación con SSON como fuente de carbono, pues varios investigadores han comprobado que las bacterias se han adaptado bien en este rango de valores (Gibert et al., 2008; Ovez, 2006; Xu, Shao, Yin, Chu, y Yao, 2009). Los coeficientes de difusión dentro de la biopelícula para los sustratos se consideraron constantes e igual a 0.8 veces el coeficiente de difusión en el agua (Wanner et al., 2006). Se descarta la difusión de material particulado a través de la biopelícula.
Para el caso de modelación de desnitrificación en reactores batch se descarta el desprendimiento de biopelícula por fuerzas de corte, dado a que el periodo de simulación fue corto (< 24 horas). En tanto, para reactores continuos también se desprecia desprendimiento por fuerza de corte, porque se usaron velocidades del flujo bajas. En este caso se considera desprendimiento por envejecimiento de la biopelícula. Rittmann y McCarty (2001) describen el desprendimiento de bacterias por envejecimiento y su influencia en procesos de crecimiento adherido.
Con estas consideraciones se estructuraron las ecuaciones de balance demasa en el nivel de la biopelícula (microescala), así como en el sistema global (reactores).
Balance de masa en la biopelícula
A escala de la biopelícula, el planteamiento matemático se estableció inicialmente con base en la matriz de coeficientes estequiométricos y cinéticos del sistema, considerando consumo de sustratos (DQO y nitrato), crecimiento y decaimiento de bacterias (Tabla 2). El comportamiento de la liberación de DQO desde el SSON se considera de primer orden (hidrólisis) y se refleja en las condiciones de borde.
Tabla 2 Matriz de coeficientes estequiométricas cinéticos del sistema de desnitrificación.
|
Componente, → i J procesos, ↓ |
1 Xb |
2 XI |
3 SCOD |
4 SNO3 |
Tasas de Reacción (M L-3 T-1) |
|---|---|---|---|---|---|
| Incremento | 1 | -1/Y |
|
|
|
| Decaimiento | -1 | -1 | bXf | ||
| Inactivación | -1 | -1 | kHXf |
De la matriz se derivaron las ecuaciones diferenciales que describen los procesos de consumo de nitrato y del crecimiento de bacterias (Tabla 2).
Utilización de DQO en la biopelícula:
Utilización de nitrato en la biopelícula:
Proceso cinético de biomasa:
Para estos sistemas de ecuaciones diferenciales, las condiciones de borde son las siguientes:
Condiciones de borde para el sustrato (DQO):
Condiciones de borde para el nitrato:
Balance de masa del reactor general
Definidas las ecuaciones diferenciales que describen el proceso de desnitrificación, se procedió a realizar el balance de masa para el reactor, en donde se integraron las ecuaciones (1), (2) y (3). Se definieron flujos de nitrato (JNO3 ) y de DQO (JDQO ) para la fase líquida de todo el sistema. El flujo de nitrato va de la masa de agua hacia la biopelícula (Ecuación (10)) y el flujo de DQO está en dirección contraria, desde la biopelícula hacia la masa de agua (Ecuación (11)):
Se asume que la DQO que se libera a la masa de agua es aquel que atraviesa la biopelícula y no fue consumido por las bacterias. Esta condición se plantea porque en estudios de desnitrificación con SSON se registraron concentraciones de carbono orgánico en la masa de agua (reactor batch) o en el efluente (reactor continuo) (Della-Rocca, Belgiorno, y Meric, 2006; Gibert et al., 2008; Soares y Abeliovich, 1998; Volokita, Abeliovich, y Soares, 1996a). Por lo tanto, definidos los flujos de nitrato y DQO se procedió a plantear el balance de masa para el reactor (escala macro), como sigue (Ecuación (12)):
Donde VB es el volumen de agua en el reactor; Qin y Qout son los caudales de salida, respectivamente; Sin y Sout , las concentraciones de DQO a la entrada y a la salida del reactor; AF , el área de biopelícula; y rB es la reacción que ocurre en suspensión (en la masa de agua). Si se considera iguales los caudales de entrada y salida (Q = Qin = Qout ), tenemos:
Para un reactor batch, la Ecuación (13) quedó como sigue:
Para un reactor de flujo continuo se descartaron reacciones en la masa de agua, porque se asumió que las bacterias en suspensión son eliminadas rápidamente del reactor por el flujo; por lo tanto, la Ecuación (13) quedó de la siguiente forma:
Aplicación del programa AQUASIM para la simulación del modelo matemático propuesto
La modelación del sistema de ecuaciones diferenciales descritas para la desnitrificación se hizo con el programa AQUASIM (Reichert, 1998c). Este programa fue diseñado para simular sistemas acuáticos; emplea el esquema de diferencias finitas para resolver las ecuaciones diferenciales (Reichert, 1998a; Reichert, 1998b).
Para la simulación en el programa AQUASIM del sistema SSON-biopelícula-agua (Figura 1), se definió un primer reactor que corresponde al SSON, de donde se aportará la DQO y que es de tipo completamente mezclado con flujo (Reichert, 1998c); y un segundo reactor, donde se presentan los procesos de transformación y consumo de aceptor y donante de electrones (Reichert, 1998c). Para vincular estos reactores, se usó la opción de membrana permeable que tiene el programa AQUASIM (Reichert, 1998c), dado que es la forma de representar el flujo de DQO desde el SSON.
El reactor SSON que representa al volumen de SSON, que está dentro del reactor general, se consideró como completamente mezclado con el propósito de representar el flujo de DQO obtenido por la hidrólisis del carbono orgánico presente (Ecuación (5)). El comportamiento de la liberación de la DQO se consideró de primer orden (hidrólisis) debido a reportes de estudios usando SSON como fuente de carbono (Deago y Pizarro, 2013; Deago y Pizarro, 2015).
A pesar de que se estableció en el modelo conceptual la capa difusa entre la biopelícula y la masa de agua (Figura 1), para esta primera aproximación matemática dicha capa se omitió. Se definió simplificar esta capa difusa, dado que es uno de los modelos de biopelícula más simples de simular (Wanner et al., 2006). Además, para simular el sistema en contragradiente de donante y aceptor de electrones usando AQUASIM se usaron parámetros cinéticos y estequiométricos seleccionados de estudios de desnitrificación (Tabla 3). En lo que respecta a los rectores batch y completamente mezclado con flujo, sus características se describen a continuación (Tabla 4).
Tabla 3 Parámetros usados en la modelación matemática obtenidos de estudios similares.
| Parámetros | Valores | Referencia |
|---|---|---|
| Coeficiente de difusión del nitrato, Df NO3 (m2/día) | 0.00016 | Picioreanu, Kreft y van Loosdrecht (2004) |
| Coeficiente de difusión de la DQO, Df DQO (m2/día) | 0.00015 | Matsumoto, Terad y Tsuneda (2007) |
| Coeficiente de inactivación, b (d-1) | 0.03 | Horn y Telgmann (2000) |
| Coeficiente de agotamiento endógeno, kH (d-1) | 0.04 | Horn y Telgmann (2000) |
| Espesor inicial de la biopelícula, Lf (µm) | 100 | Rabah, Dahab y Zhang (2007) |
| Densidad de biomasa activa en la biopelícula, Xf (g/m3) | 65 000 | Horn y Telgmann (2000) |
| Constante de afinidad de Monod del sustrato KDQO (g DQO/m3) | 19.50 | Deago y Pizarro (2013) |
| Constante de liberación de carbono orgánico, (kh) (d-1) | 0.0837 | |
| Constante de afinidad de Monod (Ks) (g N-NO3-/m3) | 20.15 | |
| Máxima tasa de asimilación de nitrato (qmax ) (g N-NO3-/g SSV/d) | 5.61 | |
| Rendimiento neto de bacterias (YH) (g DQO/g DQO) | 0.55 | |
| Razón estequiométrica DQO/NO3- (Z) (g DQO/g N-NO3-) | 2.225 | Deago y Pizarro (2015) |
Tabla 4 Características físicas de los reactores modelados.
| Parámetros | Valores |
|---|---|
| Volumen de reactor SSON (m3) | 1.6E-5 |
| Volumen de reactor general (m3) | 0.00015 |
| Área de membrana (m2) | 0.0008 |
| Área de biopelícula (m2) | 0.0008 |
| Espesor de membrana hipotética entre SSON y biopelícula (m) | 0.0001 |
| Caudal en el reactor SSON (m3/d) | 0.0004 |
| Caudal en el reactor principal completamente mezclado (m3/d) | 0.007 |
Análisis de sensibilidad
El análisis de sensibilidad es una forma de evaluar o cuantificar la relación o dependencia de parámetros usados en modelos con respecto a condiciones de entrada de un sistema (De-Pauw y Vanrolleghem, 2003). Para el análisis de sensibilidad del sistema de biopelícula de desnitrificación usando SSON, se aplicó la función de sensibilidad relativa-absoluta del programa AQUASIM (Reichert, 1998c). Esta función es una de la más usadas, porque sus unidades de medidas son independientes de las unidades de los parámetros considerados (Reichert, 1998a).
Al aplicar esta función de sensibilidad, el 100 % de cambios fue aplicado a los parámetros a evaluar, con respecto a las concentraciones de donante y aceptor de electrones del sistema. El análisis de sensibilidad se aplicó a los parámetros cinéticos y estequiométricos (Ks , qmax, YH ), así como la constante de hidrólisis (kh ). El análisis de sensibilidad de estos parámetros se hizo con respecto a los valores de entrada del sistema, los cuales fueron nitrato (aceptor de electrones) y DQQ (donante de electrones). Este tipo de análisis de sensibilidad usando AQUASIM ha sido aplicado en estudios similares de biopelícula (Arcangeli y Arvin, 1999; Matsumoto et al., 2007).
Resultados y discusión
Resultados de la simulación de reactores batch
La simulación del reactor batch se comparó con los resultados de ensayos experimentales realizados por Deago y Pizarro (2013), los cuales contenían trozos del material detrítico de Saccharum spontaneum L., usado como fuente de carbono y soporte para el crecimiento de biopelícula. Por ser un reactor batch, una de las simplificaciones del sistema fue eliminar el caudal de entrada y salida, quedando el balance de masa como se presenta en la Ecuación (14). En tanto, para representar el aporte del carbono desde la Saccharum spontaneum L., se incluyó la ecuación que representa las condiciones de borde de sistemas batch (Ecuación (5)) (Zaman, 2010).
Los parámetros de la Tabla 3 y Tabla 4 se ingresaron en el programa AQUASIM y el sistema fue modelado asumiendo que todos los procesos se llevaron a cabo en lo interno de la biopelícula.
Comportamiento de nitrato en el sobrenadante
La simulación de la desnitrificación en el reactor batch fue para un pulso de nitrato con una concentración de 100 g/m3. Se muestra que el nitrato desciende en la masa de agua con respecto al tiempo. El agotamiento de nitrato en el reactor batch se presentó a los 340 minutos de iniciada la simulación (Figura 2). Los resultados de la modelación estuvieron muy cercanos a los valores experimentales.
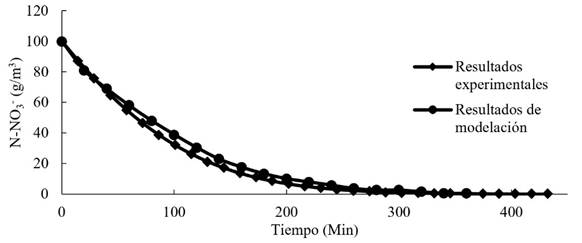
Figura 2 Resultados matemáticos y experimentales de agotamiento de nitrato en sobrenadante del reactor batch, teniendo a la Saccharum spontaneum L. como fuente de carbono.
Los resultados de la simulación de la remoción de nitrato se ajustaron de forma muy cercana a los resultados experimentales debido a que los valores obtenidos por Deago y Pizarro (2013) para los parámetros biocinéticos (qmax, Ks y Y) correspondían a ensayos con carbono orgánico liberado desde el material detrítico de Saccharum spontaneum L. De igual forma, los supuestos y asunciones permitieron ajustar el modelo matemático.
Simulación de liberación de DQO desde SSON
La simulación de DQO arrojó una rápida liberación en las primeras horas hacia el sobrenadante del reactor batch (Figura 3). Este comportamiento se asocia con que se estableció un espesor bajo de biopelícula y por ende hay una menor capacidad de desnitrificación. Luego se presenta una reducción de dicho nivel de DQO al ser usado en la desnitrificación. Una vez agotado el nitrato en el sobrenadante, cercano a las cinco horas de simulación, empieza una acumulación de DQO.
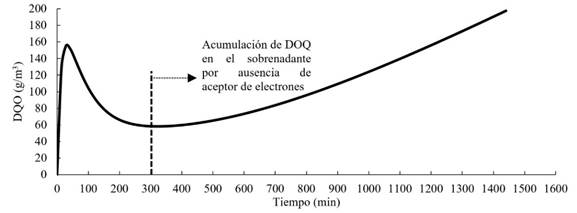
Figura 3 Resultados de la simulación de la liberación de DQO desde la Saccharum spontaneum L. Estos valores corresponden a la DQO teórica acumulada en sobrenadante del reactor batch.
Los resultados de la simulación del carbono orgánico (representado por la DQO) liberada desde Saccharum spontaneum L. corresponde a un planteamiento teórico, ya que a nivel experimental no fue posible determinar los valores de DQO en el rango de horas. Sin embargo, la simulación del comportamiento de la liberación de la DQO fue similar a resultados experimentales con Saccharum spontaneum L. reportados por Deago y Pizarro (2013), donde se observó una acumulación en el sobrenadante del reactor batch de carbono orgánico. Deago y Pizarro (2013) indican que el DQO acumulado en el sobrenadante corresponde al exceso de DQO liberado de la Saccharum spontaneum L. y que no fue consumido por las bacterias. Esta acumulación de carbono orgánico también se reportó en otros estudios (Zhang, Feng, Hong, Hao, & Yang, 2012), lo cual es un tema que requiere controlarse si se desea usar SSON en la desnitrificación del agua potable. Si esta liberación de carbono al agua no se controla, podría convertirse en una contaminación secundaria (Zhang et al., 2012).
Evolución del espesor de biopelícula
Para la simulación de la biopelícula en AQUASIM se definió una densidad y espesor inicial de 65 000 mg SSV/L y 100 µm, respectivamente (Tabla 3). El comportamiento del espesor de la biopelícula mostró un rápido crecimiento en los primeros 200 minutos de simulación y luego llega a una condición breve de estado estacionario hasta los 300 minutos (Figura 4). Posterior a los 300 minutos de simulación hay un leve descenso del espesor de la biopelícula (Figura 4).
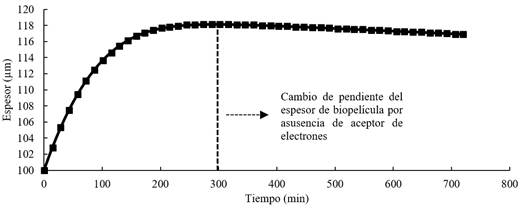
Figura 4 El comportamiento del espesor de biopelícula refleja la dependencia que tiene con respecto al nitrato, lo cual representa el factor limitante en un reactor batch.
La disminución del espesor de biopelícula indica que en los reactores batch la concentración de nitrato es un factor limitante. Si el nitrato se mantuviera constante, el comportamiento de la biopelícula podría llegar a un estado estacionario, siempre y cuando no se agote el carbono presente en la Saccharum spontaneum L. Esto se realizó y comprobó en la simulación del reactor completamente mezclado. Para el sistema batch no se consideró inactivación ni desprendimiento de bacterias, ya que el tiempo de simulación fue corto (< 24 horas) y sólo se evaluó para un pulso de nitrato. Esta investigación es similar a la reportada en el estudio de desnitrificación de aguas subterráneas (Calderer et al., 2010).
Simulación de reactores completamente mezclados con flujo
Para la simulación de reactor completamente mezclado con flujo se estableció que la máxima DQO biodisponible en la Saccharum spontaneum L. fue de 3 638.5 g DQO/m3 (Deago y Pizarro, 2013). El volumen de este reactor fue igual al usado en el ensayo batch (Tabla 4). Se estableció un caudal de 0.0007 m3/d para mantener un tiempo de retención hidráulica equivalente al tiempo en que el nitrato fue consumido en su totalidad en los reactores batch (300 minutos). En esta simulación se consideraron condiciones con y sin desprendimiento de biopelícula. Además, la liberación de la DQO desde la Saccharum spontaneum L. se representó con la Ecuación (6), para sistemas continuos en estado estacionario (Mata-Alavarez, 2003).
Simulación del nitrato en el sobrenadante de un reactor completamente mezclado con flujo
La concentración de nitrato en el influente del sistema continuo es el mismo que el usado en los ensayos batch (100 g N-NO3-/m3). Durante la simulación en el programa AQUASIM, el comportamiento del nitrato disminuyó de manera rápida en las primeras ocho horas hasta una concentración de 20 g/m3 (Figura 5b); luego el nitrato disminuyó levemente hasta un valor mínimo de 18 g/m3 y se mantuvo en una condición de estado estacionario para el caso con desprendimiento de bacterias hasta 10 días de simulación (Figura 5b). Luego del décimo día se inició un ascenso en la concentración de nitrato en el efluente del reactor completamente mezclado hasta llegar a un valor aproximado de 80 g/m3 hacia el periodo de 100 días de simulación (Figura 5a).
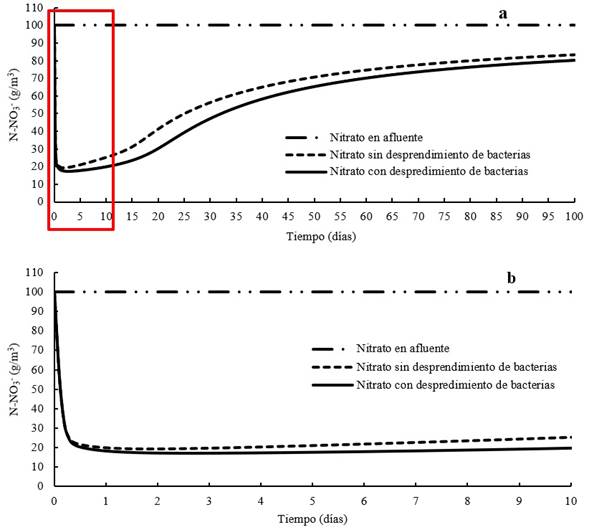
Figura 5 Simulación de nitrato en rectores completamente mezclados con y sin desprendimiento de biopelícula: a) el nitrato aumentó en el tiempo, producto de la escasez de carbono orgánico; b) en las primeras ocho horas de operación del reactor hubo una rápida reducción de nitrato.
Los resultados de la modelación, para el comportamiento del nitrato en el efluente, reflejan que la mayor remoción se presenta en la condición con desprendimiento de bacterias (Figura 5). Esto se asocia con una menor resistencia a la penetración en la biopelícula, lo cual depende de su densidad y espesor. Matsumoto et al. (2007) realizaron una modelación matemática de un reactor de membrana para procesos simultáneos nitrificación-desnitrificación, y encontraron que la biopelícula con espesores gruesos eran desfavorables para el sistema. Lakshmi y Setty (2008) encontraron que el coeficiente de transferencia externa de nitrato (KL ) aumentó al incrementarse el espesor de biopelícula. Según Martin y Nerenberg (2012), el efecto del espesor de la biopelícula es una limitante en sistemas de biopelícula en contragradiente, ya que retarda el flujo de sustratos a lo interno de la biopelícula, limitando la actividad metabólica. Esta característica debe estudiarse con mayor detalle para sistemas desnitrificantes que usan SSON como fuente de carbono y soporte para crecimiento de la biopelícula.
El comportamiento del nitrato en el efluente (Figura 5) se puede atribuir a varios aspectos: el primer factor en influenciar la reducción de la tasa de desnitrificación es el tiempo de retención definido en el reactor. Se ha demostrado que el tiempo de retención hidráulica es un factor que afecta la eficiencia de remoción de nitrato (Hashemi, Heidarpour, y Mostafazadeh-Fard, 2011; Soares, 2000; Wang y Wang, 2013). El otro aspecto que afectaría la remoción de nitrato es la cantidad de SSON disponible. Si se aumenta la masa de SSON, mayor será el tiempo de remoción de nitrato; o sea, que la vida útil de los SSON se extenderá. Ovez (2006) indica que a mayor masa de SSON mayor será su área superficial y por ende habrá mayor crecimiento de biopelícula, que aumentará el consumo de nitrato. La mayor área disponible de SSON se traduce en mayor hidrólisis de carbono, que se libera a una tasa constante.
Simulación del comportamiento de DQO en el efluente del reactor completamente mezclado
Para el reactor continuo, la simulación de la DQO arrojó concentraciones elevadas en el efluente en el primer día; luego se presentó un rápido descenso hasta llegar a cero hacia el día 30 (Figura 6). La DQO varió poco con la condición de desprendimiento de bacterias con respecto a aquella en donde no se consideró desprendimiento. Este comportamiento indica que en los primeros días hubo una mayor concentración de DQO en el efluente de la que podían asimilar las bacterias. Posteriormente, al generarse un aumento en el espesor de la biopelícula (Figura 6), la DQO disminuyó en el efluente del reactor completamente mezclado. Esto sugiere que toda la DQO es asimilada por las bacterias dentro de la biopelícula para la reducción de nitrato y síntesis celular.
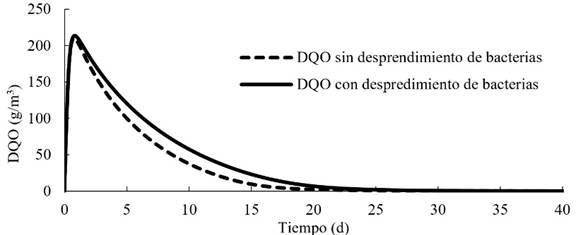
Figura 6 Resultados de la modelación matemática para la DQO en el efluente del reactor completamente mezclado. Los resultados son similares asumiendo condición con y sin desprendimiento de biopelícula
Este sistema en contragradiente donde la DQO proviene de los SSON y el nitrato de la masa de agua es similar a lo que se presenta en remoción de nitrato en sistemas de reactores de biopelícula con membranas, donde se plantea un sistema de ecuación de doble Monod. Martin y Nerenberg (2012) determinaron que en estos sistemas de membranas en contragradiente se cumple la condición de actividad relativa, la cual ocurre cuando se agota uno de los sustratos (aceptor o donante de electrones); dicha actividad relativa se hace cero.
A diferencia de los sistemas basados en membranas, el factor limitante en la desnitrificación usando SSON es el aporte constante en el tiempo del carbono orgánico. Dicha liberación del carbono orgánico depende del contenido de lignina (Chandler, Jewell, Gossett, Vansoest, & Robertson, 1980), y de la capacidad de las bacterias heterótrofas de colonizar e hidrolizar el carbono biodisponible del área superficial de los materiales (Vavilin, Rytov, y Lokshina, 1996).
Simulación de la evolución de biopelícula en reactores completamente mezclados con flujo
La simulación en AQUASIM del crecimiento de la biopelícula no logró una condición de estado estacionario en la condición sin desprendimiento; mientras que en la condición con desprendimiento hubo una disminución en la pendiente de la gráfica hacia el final de la simulación, con lo cual se aprecia una tendencia a estabilizarse (Figura 7). Al finalizar la simulación, el espesor de biopelícula con la condición sin desprendimiento fue de 2 150 µm; mientras que al considerar desprendimiento de bacterias, el espesor final fue de 1 500 µm.
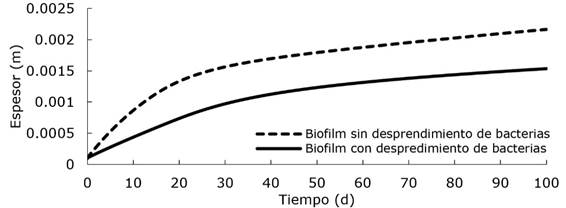
Figura 7 Resultados de la simulación de la biopelícula adherida a la Saccharum spontaneum L. en reactor completamente mezclado con flujo. La DQO en el reactor sin desprendimiento de biopelícula tuvo un mayor crecimiento por la condición dada.
El proceso de desprendimiento de bacterias ha sido modelado en sistemas desnitrificantes usando AQUASIM (Horn y Telgmann, 2000). Esta herramienta es muy útil para estimar el espesor de biopelícula, ya que éste es uno de los parámetros más difíciles de determinar en condiciones experimentales. Por ejemplo, con tal modelación es posible conocer cómo es el comportamiento del crecimiento de la biopelícula. En el caso del rector completamente mezclado, se observa que hay un rápido crecimiento de la biopelícula, especialmente en el caso del reactor sin desprendimiento (Figura 7). Dicho comportamiento se asocia con la disminución en el aporte de carbono orgánico soluble (Figura 6).
El fenómeno de desprendimiento debe considerarse en sistemas de tratamiento a base de biopelícula, a pesar de que los flujos de agua sean bajos. Rittmann y McCarty (2001) afirman que los esfuerzos de corte generado por la velocidad del agua sobre la superficie del biopelícula obedecen a efectos erosivos; mientras que condiciones anaeróbicas, en la profundidad del biopelícula, pueden ser causantes del desprendimiento de grandes porciones de biomasa. Este proceso de desprendimiento aporta biomasa de la matriz de biopelícula hacia la masa de agua (Wanner et al., 2006). El desprendimiento de bacterias desde sistemas desnitrificantes hacia el efluente de ensayos experimentales ha sido reportado (Soares, 2000; Soares y Abeliovich, 1998; Volokita, Belkin, Abeliovich, y Soares, 1996b).
El efecto del espesor de biopelícula no fue relevante para el caso del comportamiento de la DQO en el efluente (Figura 6), ya que hacia el día 30 de simulación, el comportamiento de la DQO era muy similar en ambas condiciones. Sin embargo, en el caso de nitrato sí se aprecia mayor influencia del espesor de la biopelícula (Figura 5), lo cual se asocia con la resistencia a la transferencia de la biopelícula. Por ejemplo, a los 30 días de operación en el sistema con desprendimiento, la concentración de nitrato en el efluente fue de 47 g/m3; mientras que en el escenario sin desprendimiento fue de 56 g/m3 (Figura 5a). Esto concuerda con lo indicado por Di-Capua, Papirio, Lens y Esposito (2015), quienes señalan que la transferencia de masa del nitrato se afecta de forma severa a causa de un mayor incremento del espesor de biopelícula.
Simulación en contragradiente de nitrato y DQO dentro de la biopelícula en un reactor completamente mezclado con flujo
En las secciones anteriores se mostró el comportamiento del donante y aceptor de electrones a nivel general o escala macro; es decir, el compartimiento del volumen de agua o efluente. Sin embargo, para comprender el sistema de forma integral, es necesario conocer lo que ocurre en la biopelícula (escala micro). En este sentido, la simulación con AQUASIM permitió obtener perfiles de concentración tanto del donante de electrones (DQO) como del aceptor de electrones (nitrato). Los resultados de DQO muestran una disminución a medida que el espesor de biopelícula aumentaba (Figura 8a). En tanto, los perfiles de nitrato reflejaron que, al transcurrir el tiempo de simulación, disminuía la capacidad de reducción de nitrato; es decir, que el nitrato se consumía rápidamente en los estratos más superficiales de la biopelícula, pero su concentración era mayor en la superficie de la biopelícula (Figura 8b).
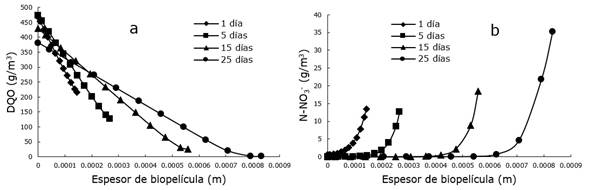
Figura 8 Perfil de concentraciones de DQO (a) y de nitrato (b) en la biopelícula para diferentes tiempos de simulación.
El consumo de DQO fue mayor dentro de la biopelícula a medida que se incrementa su espesor, lo cual se asocia con la adaptación favorable de las bacterias que lo conforman. En tanto, el comportamiento de nitrato mostró que a medida que aumentaba el espesor de biopelícula, su concentración se hacía cero cada vez más distante con respecto al origen (Figuras 8b). Al comparar los perfiles de DQO y nitrato dentro de la biopelícula (por ejemplo, al día cinco), se observa que la DQO decrece de forma lineal; mientras que el nitrato decrecía rápidamente en forma exponencial (Figura 9).
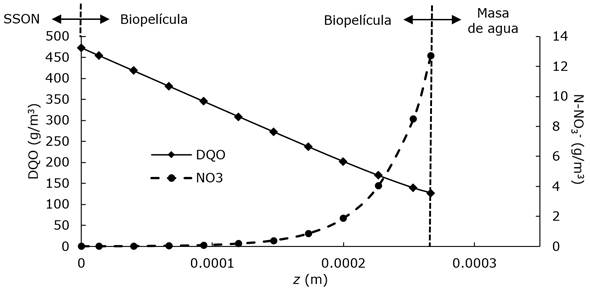
Figura 9 Comparación de los perfiles de concentración de DQO y nitrato dentro de la biopelícula en el quinto día de simulación.
Se presume que estos comportamientos de DQO y nitrato dentro de la biopelícula son causados por la limitación a la transferencia de masa debido al incremento del espesor de biopelícula. A escala micro se refleja lo encontrado en el sistema general, donde se evidencia mayor resistencia a transferencia de masa del nitrato aportado desde la masa de agua; esto corrobora lo señalado por Di-Capua et al. (2015). De forma similar, Nicolella, Pavasant y Livingston (2000) encontraron que la eficiencia de remoción de un sustrato en un sistema de membrana en contragradiente disminuye al aumentar el espesor de la biopelícula.
Análisis de sensibilidad
El grado de sensibilidad para las variables de control (nitrato y DQO) se ponderó según Arcangeli y Arvin (1999): gran efecto, significativo, moderado e insignificante. Estas ponderaciones se definen en la Tabla 5. De igual forma, los análisis de sensibilidad para cada parámetro evaluado se presentan gráficamente (Figura 10 y Figura 11).
Tabla 5 Valoración del análisis de sensibilidad de parámetros evaluados.
| Parámetros | DQO | Nitrato |
|---|---|---|
| Rendimiento neto de bacterias (YH ) g SSV/g DQO | +++ | +++ |
| Constante de hidrólisis de carbono orgánico, kh (d-1) | +++ | +++ |
| Máxima tasa específica de crecimiento (µ) (d-1) | + | ++ |
| Constante de afinidad de Monod (Ks) (g N-NO3-/m3) | - | ++ |
Gran efecto (+++); significativo (++); moderado (+); insignificante (-).
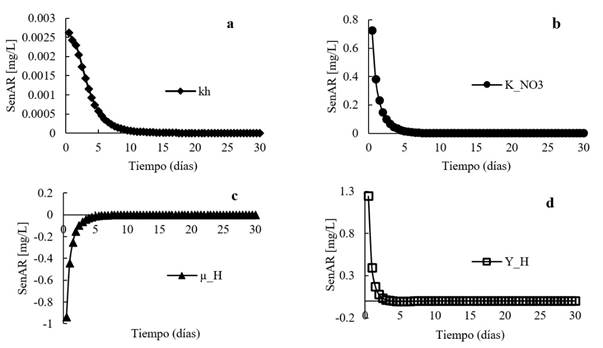
Figura 10 Resultados de análisis de sensibilidad para las concentraciones de nitrato en la matriz de la biopelícula con respecto a los parámetros: a) kh; b) K_NO3; c) µ_H; y d) Y_H.
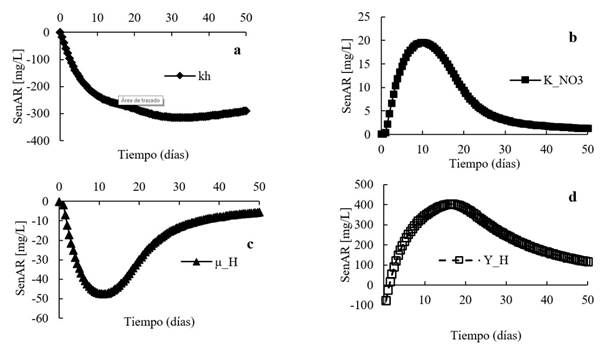
Figura 11 Resultados de análisis de sensibilidad para las concentraciones de DQO en la matriz de la biopelícula con respecto a los parámetros: a) kh; b) K_NO3; c) µ_H; y d) Y_H.
El análisis de sensibilidad obtenido con el modelo AQUASIM mostró que la significancia para el nitrato en orden descendente de los parámetros evaluados fue YH , kh , µH y KNO3 (Tabla 5). Los parámetros YH y kh son altamente significativos, mientras que el parámetro µH tiene una significancia moderada. Para el parámetro KNO3 , el grado de sensibilidad es insignificante. Gráficamente, se observa que la sensibilidad de la concentración de nitrato con respecto a los parámetros YH , kh y KNO3 es máximo cercano a cero y todos presentan un comportamiento exponencial decreciente hasta llegar a valores de cero en diferentes tiempos (Figura 10d, Figura 10a y Figura 10b). La sensibilidad de la concentración de nitrato con respecto a µH también tiene un comportamiento exponencial, pero su máximo valor es negativo (Figura 10c). Este signo negativo indica que el nitrato disminuye a medida que el parámetro µH aumenta.
La importancia o significancia de los parámetros analizados con respecto a las concentraciones de DQO tiene el mismo orden que la obtenida para para el nitrato, el cual fue YH , kh , µH y KNO3 . Sin embargo, para la DQO todos tienen un grado de sensibilidad de muy significativo a significativo (Tabla 5). Para el caso del parámetro YH , la función de sensibilidad parte de cero hasta un valor negativo y luego aumenta hasta un máximo, y posteriormente decrece (Figura 11d). Para el parámetro kh , los valores de la función de sensibilidad parten de cero y van aumentando negativamente (Figura 11a). Para el caso del parámetro µH , se observa que también parte de cero y se incrementa negativamente hasta un tiempo cercano a los 10 días, y luego fue disminuyendo (Figura 11c). En tanto, el resultado gráfico del análisis para el parámetro KNO3 mostró que parte de cero y se incrementa positivamente hacia un valor máximo, disminuyendo posteriormente (Figura 11b). Este comportamiento fue similar al obtenido con el parámetro YH.
Como se ha descrito, los parámetros YH , kh, y µH son fundamentales para representar de modo adecuado el modelo matemático de desnitrificación en el sistema de biopelícula en contragradiente, usando el SSON como el portador y fuente de carbono. Este análisis de sensibilidad corrobora la importancia que tiene la hidrólisis como un proceso que controla la liberación de carbono orgánico para la reducción de nitrato. El comportamiento del análisis de sensibilidad fue similar a la modelación en AQUASIM de reactores de membranas con biopelículas, donde los parámetros µH y YH fueron los más significativos, y el parámetro KNO3 fue el menos significativos (Matsumoto et al., 2007).
Los resultados de la simulación permiten visualizar ventajas y limitaciones como las que se han descrito. En el caso de la presencia de DQO en el efluente tratado, se observó que en los primeros cinco días (Figura 6) las concentraciones fueron elevadas. Esta información permitiría evaluar la posibilidad de aplicar tratamientos posteriores, como el uso de filtros de arena, los cuales han sido probados para controlar excesos de DQO y desprendimiento de biopelícula en efluentes de sistemas desnitrificantes (Aslan, 2005; Aslan y Cakici, 2007; Della Rocca et al., 2005).
Conclusiones
Con esta investigación fue posible generar una aproximación matemática de la desnitrificación, usando SSON como portador de biopelícula y única fuente de carbono orgánico. A pesar de que se establecieron supuestos y se hicieron simplificaciones, se logró predecir el comportamiento de la liberación y el agotamiento del carbono orgánico desde los SSON. De igual forma, se simuló la remoción de nitrato en función del comportamiento del carbono y de la biopelícula formada alrededor los SSON. Estos resultados nos permitieron demostrar que la modelación matemática es una herramienta útil en el estudio de la desnitrificación, usando SSON como soporte para el crecimiento de bacterias y fuente de carbono orgánico; así como entender el comportamiento en la interacción entre los SSON, la biopelícula y el nitrato. De igual forma, es una herramienta predictiva para estimar la vida útil de los SSON como fuentes de carbono orgánico. Todas estas simulaciones se hicieron gracias al apoyo del software libre AQUASIM.
En estas simulaciones se identificó que en reactores batch el factor limitante fue la concentración del nitrato y en rectores continuos fue el aporte de DQO desde SSON. En reactores batch, la dosificación de nitrato fue puntual y una vez agotado el consumo de DQO se detuvo. Posteriormente, esta DQO se acumuló en el sobrenadante. En tanto, en reactores continuos hubo dosificación continua de nitrato, lo cual estimuló la hidrolización del carbono biodisponible en los SSON, pero avanzado el tiempo de simulación, este carbono se agotó y en consecuencia disminuyó la reducción de nitrato, incrementando su concentración en el efluente.
Con el análisis de sensibilidad realizado se mostró que los parámetros más significativos fueron el rendimiento neto de bacterias (YH ) y la constante de hidrólisis (kh ). La significancia de estos parámetros cinéticos muestra la relevancia de profundizar en el estudio de la interacción entre el SSON y la biopelícula que actúa sobre estos materiales. Además, se requiere fortalecer aún más el entendimiento de SSON como fuente de carbono para desnitrificación, estudiando escenarios con variaciones de caudal, temperatura, carga de nitrato y masa de SSON usada.
Con el desarrollo de este modelo matemático se podrán hacer simulaciones de desnitrificación en sistemas de tratamiento de aguas residuales usando SSON como fuente de carbono. De igual forma, se podría realizar el monitoreo de sistemas de agua potable, evaluando, por ejemplo, tasas de liberación de carbono desde los SSON, ya que esto es un riesgo si no se controla.











 texto em
texto em 



