Introducción
En el tratamiento de agua y de aguas residuales es necesario determinar las impurezas para entonces establecer las tecnologías de depuración más adecuadas. Los contaminantes presentes en el agua son de naturaleza muy variada e incluyen, entre otros muchos, a los materiales orgánicos. Los análisis globales de sustancias orgánicas en agua, demanda bioquímica de oxígeno (DBO), demanda química de oxígeno (DQO) y carbono orgánico total (COT), dan una aproximación adecuada de la suma de los contaminantes orgánicos que comparten alguna propiedad en común. Estos tres parámetros, basados en procesos de oxidación, son cuantificaciones indirectas de los constituyentes orgánicos del agua, cuya determinación suele ser rutinaria en las plantas de tratamiento de aguas residuales, así como en muchos laboratorios certificados.
De acuerdo con Metcalf & Eddy Inc. (2004), la demanda química de oxígeno (DQO) total es el oxígeno equivalente a los materiales orgánicos en la muestra de agua que pueden ser oxidados químicamente mediante una solución de dicromato (oxidante más común) en medio ácido, junto con un catalizador e inhibidores de interferencias. En tanto, APHA, AWWA y WEF (1985) definen a la DQO de forma más general, indicando que es la medición del oxígeno equivalente al contenido de materia orgánica de una muestra que es susceptible a la oxidación química por un oxidante químico fuerte (no necesariamente dicromato).
En la obra de APHA, AWWA y WEF (1985) se establece que, durante la cuantificación de la DQO, la oxidación con dicromato logra oxidar entre el 95 y 100 % de las sustancias orgánicas, resistiendo a esta oxidación sólo los compuestos piridínicos y los compuestos orgánicos volátiles (COVs); los primeros, por ser químicamente estables ante las condiciones de reacción propuestas, y los últimos porque sólo pueden ser oxidados al estar en la fase líquida en contacto con el oxidante y, al estar en reflujo, son fácilmente transferidos a la fase gas.
De entre los métodos disponibles para determinar la DQO, el colorimétrico con reflujo cerrado a pequeña escala es bastante usado (como en la norma NMX-AA-030/2-SCFI-2011) (DOF, 2011) y su importancia va en aumento. Esto, porque con él se requiere solamente de un espectrofotómetro visible, y los volúmenes de muestra y de reactivos son mucho menores que en el caso del reflujo abierto, generando menor cantidad de residuos peligrosos (con toxicidad ambiental por las especies de cromo y/o de mercurio, que son de alta reactividad por ser medios fuertemente ácidos y por la presencia del oxidante fuerte dicromato): 50 a 150 ml con reflujo abierto en comparación con 5 a 7.5 ml con los métodos de reflujo cerrado convencionales.
De forma general, la Ecuación (1) muestra la reacción que se tiene durante el análisis de DQO (considerando especies orgánicas nitrogenadas donde la valencia del nitrógeno es -3 hay nitritos en cantidad importante (mayor que 2 mg de nitrógeno de nitritos por litro), y no hay concentración importante de especies inorgánicas reducidas como Fe2+, S2-, Mn2+, etc.) (APHA, AWWA, & WEF, 1985; APHA, AWWA, & WEF, 2017; ASTM, 2012). Para el caso de que se use biftalato de potasio como material orgánico a oxidar (curva de calibración), la reacción en el sistema de reflujo será la de la Ecuación (2) (ASTM, 2012). Por último, en la Ecuación (3) se tiene la reacción química si se planteara la oxidación del biftalato de potasio con oxígeno molecular (ASTM). Así, de acuerdo con las reacciones (2) y (3), un mol de dicromato tiene la misma capacidad de oxidación que 1.5 moles de oxígeno molecular y, con base en la reacción (3), la DQO teórica del biftalato es de 1.175 g de oxígeno por cada gramo de biftalato de potasio:
Por otra parte, las principales interferencias en la determinación de la DQO son las siguientes: presencia en concentraciones importantes de compuestos orgánicos volátiles alifáticos lineales, de halógenos, de nitritos y de especies reducidas inorgánicas (Fe2+, S2-, Mn2+, etc.). Para el método 5220 D original se establece que, en muestras con baja presencia de nitritos y de interferencias químicas (los cloruros son las únicas que suelen estar presentes en la mayoría de las muestras), las soluciones requeridas son dos solamente: la de digestión (dicromato de potasio) y la catalítica (sulfato de plata en ácido sulfúrico concentrado). Si la cantidad de cloruros es de importancia, entonces es necesaria la adición de sulfato de mercurio a la solución de dicromato). En el caso del método 5220 D original, el volumen recomendado de la muestra y de las otras soluciones se presenta en la tabla 508:I de APHA, AWWA y WEF (1985), donde se establece también que puede trabajarse con otros volúmenes de estas soluciones siempre y cuando la relación entre ellas se conserve en 1:0.6:1.4 (volúmenes de muestra:solución de digestión:solución catalizadora), con las concentraciones indicadas en la misma referencia y en sus ediciones posteriores.
Materiales y métodos
En este trabajo se desarrolló la validación parcial de un método de análisis de la DQO mediante reflujo cerrado 5220 D (APHA, AWWA, & WEF, 1985), que fue adaptado a microescala. Para ello, se analizó la linealidad del sistema y la precisión. Se realizaron soluciones con un patrón primario: el biftalato de potasio de alta pureza (Sigma-Aldrich). El patrón se secó a 105 °C por 60 minutos y luego disuelto en agua tridestilada (Ventas Químicas, S.A.), para tener soluciones con concentraciones de 0, 200, 400, 600 y 800 mg/l del compuesto (equivalentes a DQO de 0, 235, 470, 705 y 940 mg O2 /l, respectivamente).
Los tubos de vidrio borosilicato se lavaron previamente con una solución 1:10 (en volumen) de ácido sulfúrico concentrado en agua tridestilada, se enjuagaron con agua y se secaron al aire. Se prepararon las soluciones catalizadora y de digestión de manera tal que en la adaptación a microescala se mantuvo la misma concentración que la del método 5220-D original de dicromato, sulfato de plata y ácido sulfúrico en el tubo de vidrio, justo antes de comenzar la digestión (excepto la concentración inicial de sulfato de mercurio, que se redujo al considerar que el método a microescala se aplicará a aguas residuales municipales con bajas concentraciones de cloruros; con ello se buscó reducir la peligrosidad y el impacto ambiental de los residuos generados en el análisis).
Posteriormente, las soluciones (Tabla 1) y luego las muestras (soluciones de biftalato de potasio) se agregaron a los tubos de vidrio del digestor, como se indica en la Tabla 2. Los tubos se taparon firmemente, se agitaron de forma lenta y se colocaron en el bloque digestor (HANNA Instruments, HI839800) precalentado a 150 °C. Ahí se efectuó la digestión de las soluciones patrón a 150 °C durante dos horas (reflujo cerrado). Culminada la digestión, los viales se enfriaron lentamente al aire hasta temperatura ambiente y se agitaron con suavidad sin invertir el tubo de vidrio. Las absorbancias de las soluciones digeridas y enfriadas se leyeron en el espectrofotómetro (Shimadzu UV1601), en una celda de vidrio rectangular con longitud de paso óptico de 1 cm, usando agua tridestilada como blanco (o referencia) del espectrofotómetro, midiendo la absorbancia a 600 nm (debida a la generación de cromo III). Para esta adaptación a microescala se utilizó agua tridestilada como blanco en lugar de la solución a 0 mg O2/l no digerida que se establece en APHA, AWWA y WEF (2017) para determinar el desempeño del método con un blanco no específico para este parámetro. El blanco de agua se indica para la medición a 420 nm por APHA, AWWA y WEF (2017), de manera que su uso como referencia a 600 nm constituye una opción de interés práctico en los laboratorios de análisis de calidad del agua.
Tabla 1 Soluciones para el método 5220 D y su modificación a microescala. Basado en APHA, AWWA y WEF (2017).
| Método original | Método adaptado a microescala | |
|---|---|---|
| Solución catalítica (Ag2SO4) | 5.5 g de Ag2SO4 por cada kilogramo de H2SO4 concentrado | Solución comercial a 10 g/l de Ag2SO4 en H2SO4 concentrado |
| Solución de digestión (Cr2O72-) | 10.216 g de K2Cr2O7, 33.3 g de HgSO4, (secados a 105 °C por dos horas); 400 ml de agua tridestilada; 167 ml de H2SO4 concentrado (lentamente añadido); aforar a 1 000 ml con agua tridestilada; tal fue el orden | 10.22 g de K2Cr2O7, 0.75g de HgSO4 (secados a 105°C por 2 horas); 400 ml de agua tridestilada; 500 ml de H2SO4 concentrado (lentamente), enfriando a temperatura ambiente con hielo externamente; aforar a 1 000 ml con agua; tal fue el orden |
Tabla 2 Dosificación de cada reactivo en el tubo de reacción para el Método 5220-D. Basado en APHA, AWWA y WEF (2017).
| Método original | Método adaptado a microescala | |
|---|---|---|
| Muestra | 2.5 ml | 1.0 ml |
| Solución catalizadora (Ag2SO4) | 3.5 ml | 1.0 ml |
| Solución de digestión (Cr2O72-) | 1.5 ml | 0.5 ml |
| Volumen total en el tubo (ml) | 7.5 | 2.5 |
En algunas muestras se formó un precipitado blanco, que depositó en la boca de los tubos; en esos casos, se le retiró mecánicamente antes de leer las muestras en el espectrofotómetro. Los datos se analizaron usando el software Origin Pro v. 8 y en Microsoft Excel.
Para la linealidad se midió la curva de calibración por triplicado para cinco niveles de concentración; para la precisión del método se realizaron digestiones por sextuplicado de muestras de tres niveles de concentración, todo por duplicado. Con los valores de DQO determinados, se calculó el coeficiente de determinación (r 2) para evaluar el ajuste al modelo lineal y el coeficiente de variación (CV) para evaluar la precisión.
En el método 5220 D adaptado a microescala se cuidó que las adiciones de reactivos y muestras fueran con pipetas volumétricas clase A y no con pipetas de émbolo o graduadas, como sería necesario en el método original 5220 D o en la norma técnica mexicana NMX-AA-030/2-SCFI-2011. En la Tabla 3 se muestran las concentraciones de los reactivos en los tubos justo antes de iniciar la digestión de las muestras. Para cumplir con la igualdad de concentraciones iniciales en ambos métodos (el original y el adaptado a microescala), se adecuó la cantidad de H2SO4 en la solución de digestión en la propuesta a microescala.
Tabla 3 Concentraciones de especies químicas de interés para el Método 5220-D justo antes de iniciar la digestión (basado en APHA, AWWA, & WEF, 2017).
| Método original | Método adaptado a microescala | |
|---|---|---|
| Ag2SO4 | 4.697 g/l | 4.000 g/l |
| K2Cr2O7 | 2.043 g/l | 2.044 g/l |
| H2SO4 | 901.720 g/l | 901.600 g/l |
| HgSO4 | 6.660 g/l | 0.150 g/l |
Es importante establecer que la concentración de HgSO4 en la solución de digestión fue reducida drásticamente en la adaptación a microescala, pues en la mayoría de las muestras de agua residual municipal y de agua residual tratada no se esperan altas concentraciones de cloruros. Para este estudio se consideró una concentración de cloruros máxima en el agua de 4.5 mg Cl-/l (7.4 mg NaCl/l). Además, en el método original se establece que la cantidad de sulfato de mercurio puede modificarse de acuerdo con los cloruros esperados en la muestra a analizar. Se considera que la interferencia por los cloruros se elimina de modo apropiado con concentración de mercurio en el tubo de digestión 10 veces mayor que la de cloruros (APHA, AWWA, & WEF, 2017).
Resultados y discusión
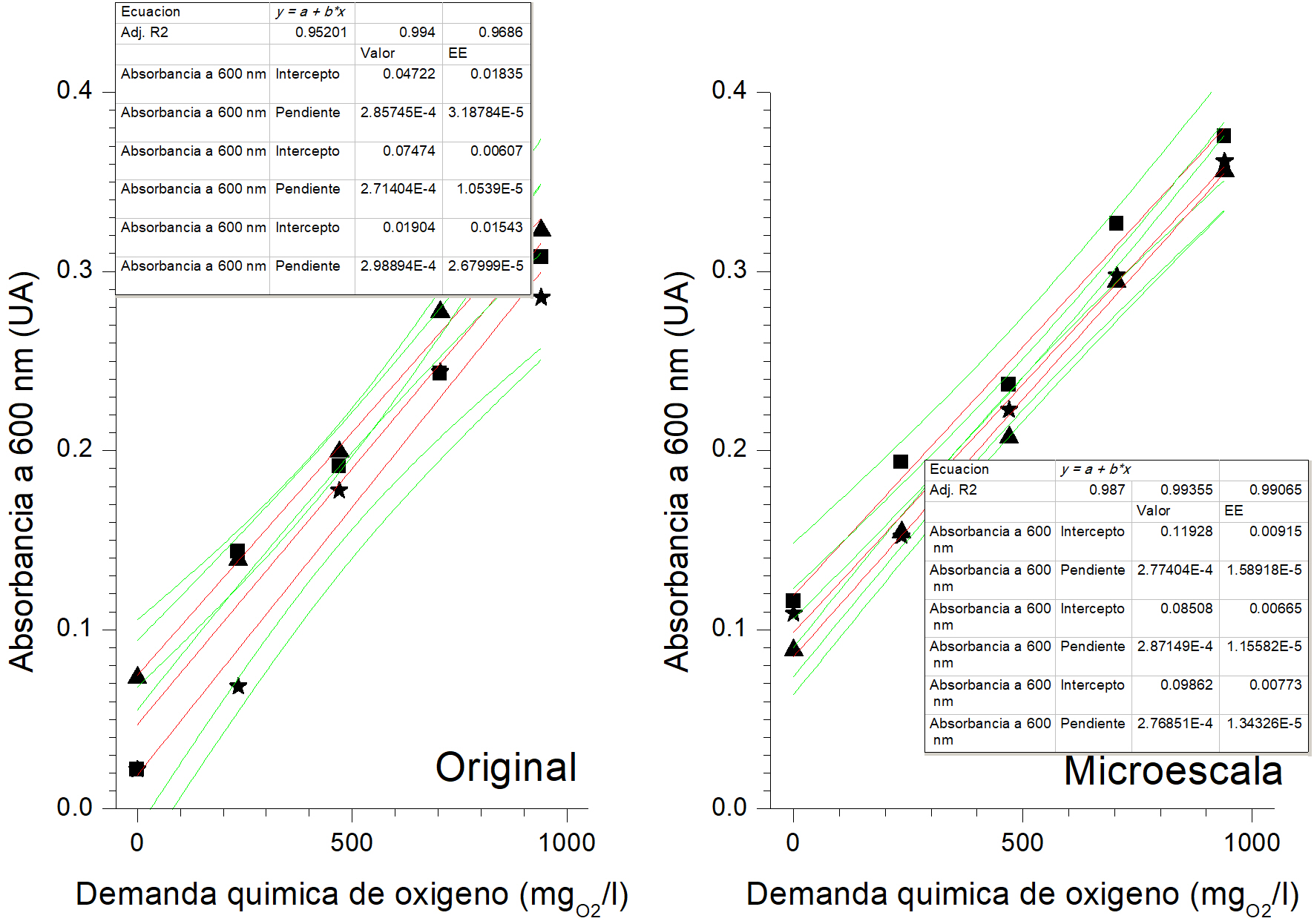
Tras realizar la digestión de las muestras patrón por triplicado se graficaron las curvas de calibración tanto para los resultados del análisis con el método original (convencional) como para los obtenidos del adaptado a microescala (Figura 1). En este segundo caso, todas las gráficas resultantes tuvieron un coeficiente de determinación (r 2) mayor que 0.98. Por ello, de acuerdo con Colegio Nacional de Químicos Farmacéuticos Biólogos México, A.C. (2002), el método a microescala es válido para linealidad del sistema. El método 5220-D original ya ha sido ampliamente validado y no se repitió su validación en este trabajo.
En la Tabla 4 se presentan los coeficientes de determinación (r 2) para el ajuste lineal de ambos métodos de DQO a reflujo cerrado. Es importante indicar que el ajuste al modelo (r 2) es más repetible para la adaptación a microescala que para el método original. Un aspecto importante es la modificación de las proporciones de los reactivos con respecto al método original, lo cual obedece a que en el procedimiento 5220 D se requieren adiciones de volúmenes para los cuales no existe una pipeta volumétrica exacta; ello implica emplear al menos dos pipetas, lo que incrementa el error en el procedimiento (en particular si se emplean pipetas de émbolo sin una propia calibración). Emplear 0.5 y 1 ml de los reactivos permite realizar cada dosificación con una sola pipeta volumétrica y en una sola adición, y se reduce el error asociado con la toma de la alícuota.
Tabla 4 Coeficientes experimentales de determinación de ajuste lineal (r 2) para el método 5220-D.
| Método original | Método adaptado a microescala | |
|---|---|---|
| Repetición 1 | 0.9520 | 0.9870 |
| Repetición 2 | 0.9940 | 0.9933 |
| Repetición 3 | 0.9686 | 0.9906 |
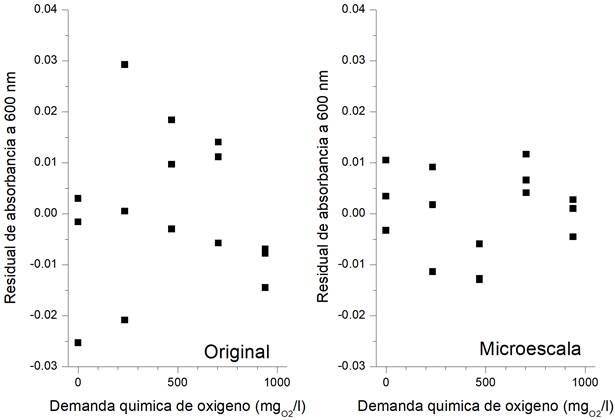
Para la precisión del método adaptado a microescala (Tabla 5), las muestras mostraron una buena repetibilidad, de forma que el valor del coeficiente de variación (CV) fue siempre inferior que 3 %. Este valor de CV indica que el método 5220-D adaptado a microescala es suficientemente preciso como para poder usarse en un análisis rutinario. De hecho, en el mismo método original 5220 D (APHA, AWWA, & WEF, 1985) se establece que en cinco laboratorios se analizaron 48 muestras y que el CV fue de 8.7 % para una DQO media de 193 mg O2/l en ausencia de cloruros, y de 9.6 % para una DQO promedio de 212 mg O2/l en presencia de 100 mg/l de cloruros, por lo que los resultados aquí obtenidos tienen un menor valor de CV (Figura 2).
Tabla 5 Precisión para el método 5220-D adaptado a microescala.
| Repetición | DQO promedio (mg O2/l) | Desviación estándar, S (mg O2/l) | Precisión (CV) |
|---|---|---|---|
| 1-a | 225.86111 | 5.30512 | 2.34884 |
| 2-a | 563.80417 | 10.20365 | 1.80978 |
| 3-a | 800.24028 | 22.61028 | 2.82544 |
| 1-b | 225.33889 | 4.33083 | 1.92191 |
| 2-b | 523.52778 | 13.43289 | 2.56584 |
| 3-b | 774.71667 | 19.37226 | 2.50056 |
Conclusiones
La adaptación a microescala del método 5220-D permitió cuantificar la demanda química de oxígeno en agua de manera análoga a su versión original.
El método 5220-D adaptado a microescala fue descrito exitosamente por un modelo simple lineal en el rango de DQO de 0 a 940 mg O2/l, con base en la determinación exitosa de la linealidad (r2 > 0.98).
El método 5220-D adaptado a microescala fue preciso, con un coeficiente de variación inferior a 3 % en todas las pruebas (análisis para tres niveles de concentración).
Los residuos peligrosos generados tras implementar el análisis de agua con la adaptación a microescala (2.5 ml por análisis) se han reducido en hasta 50 % en volumen con respecto al proceso de análisis de la norma mexicana NMX-AA-030/2-SCFI-2011 (5.2 ml de residuo por prueba) y hasta el 75 % en volumen con respecto a los análisis basados en el método 5220-D original (7.5 ml de residuo por determinación).











 texto em
texto em