Los brotes y raíces tienen funciones complementarias, ya que el vástago aéreo cosecha energía radiante del sol, mientras que las raíces absorben nutrientes minerales y agua1. Según Ramos-Hernández y Martínez-Sánchez2 la biomasa subterránea suele ser igual o superior a biomasa aérea. Poorter y Nagel3 afirman que, ante una baja disponibilidad de nutrientes, la raíz tiene prioridad en la asignación de carbohidratos sobre la parte aérea. Así mismo, las propiedades físicas, químicas y biológicas de los suelos tienen un rol importante en el crecimiento radicular4. Los sistemas radiculares permiten a las plantas crecer y nutrirse, por lo que son determinantes en el rendimiento de los cultivos agrícolas5. Sin embargo, se sostiene6, que en forrajeras el crecimiento y producción de raíces está mucho menos estudiada y comprendida que el de hojas.
Las raíces tienen una intensa actividad biológica; entre la más importante es la asociación simbiótica entre miembros de la familia Leguminosae y bacterias diazotróficas del suelo (rizobios), la cual es bien conocida por su capacidad de fijar nitrógeno atmosférico7. Por consiguiente, las leguminosas desempeñan un papel clave en la intensificación sostenible de los sistemas agrícolas, mejorando la biodiversidad, los servicios ecosistémicos y reduciendo la dependencia de la producción de alimentos de los fertilizantes nitrogenados8. Es por esto que, las leguminosas forrajeras han sido seleccionadas por su capacidad de nodulación, siendo el trébol blanco el que mayor capacidad desarrolla9. Sin embargo, la fijación de N es muy variable por los rizobios; existen varios factores que determinan el éxito de la relación simbiótica leguminosa-rizobios10), uno de los más importantes es hacer coincidir simbiontes adecuados con las plantas hospedantes11.
Por lo anterior, el objetivo de esta investigación fue valorar la biomasa radicular del raigrás perenne (Lolium perenne L.) como monocultivo, con diferentes fuentes nitrogenadas y en mezclas con trébol blanco (Trifolium repens) y trébol rojo (Trifolium pratense), así como la capacidad de nodulación de los tréboles blanco o rojo, en dos localidades contrastantes.
Esta investigación se desarrolló en Ecuador en la provincia de Pichincha, en dos sitios experimentales, en las parroquias de Machachi, Cantón Mejía y Tumbaco, Cantón Quito.
Según el censo agropecuario INEC12, las pasturas ocupan el 58.3 % de la superficie que tiene labor agropecuaria, por la que la producción ganadera se realiza en un sistema pastoril. También se menciona que el 79.5 % de la producción de leche es de la región sierra, y en ella la provincia de Pichincha abarca un 18 % del total, siendo la provincia con mayor producción nacional.
El clima en la provincia de Pichincha es variable de acuerdo con la altura, el de la localidad Tumbaco se clasifica como mesotérmico seco, mientras que Machachi como mesotérmico húmedo13. Machachi se encuentra a 0°30'36.4'' S; 78°34'1.6'' O, 1,043 mm de precipitación, temperatura media de 12 0C; mientras que Quito se encuentra a 0°13'52.5'' S; 78°11'0.3'' O,
954 mm de precipitación y temperatura media de 16 0C.
El origen de los suelos en la región interandina es volcánico y el clima es el factor más importante en su desarrollo, por lo que las condiciones ambientales específicas de cada sitio han dado lugar a diferentes procesos que han influido en la formación del suelo14. Basado en ello, se tomaron muestras de suelos de cada localidad, en las cuales se determinaron: carbono orgánico (por combustión húmeda, Método Walkley-Black), pH (con potenciómetro, en solución acuosa), conductividad eléctrica (utilizando conductímetro con extracto de pasta saturada), N total (mediante cálculo a partir del porcentaje de materia orgánica), P disponible (con fotocolorímetro, Método Olsen modificado) y cationes intercambiables (K, Ca, Mg; espectrofotometría de absorción atómica) (Cuadro 1).
Cuadro 1 Características físico-químicas de los suelos de los sitios experimentales
| Localidad | pH | CE | COS | MOS | N total | P | K | Ca | Mg | |
|---|---|---|---|---|---|---|---|---|---|---|
| (dS/m) | /%) | (ppm) | (cmol/kg) | |||||||
| Machachi | 7.56 | 0.56 | 4.05 | 7.67 | 0.38 | 73.5 | 1.02 | 16.46 | 2.7 | |
| Tumbaco | 6.7 | 0.59 | 1.56 | 2.95 | 0.15 | 31.4 | 1.5 | 9.79 | 4.72 | |
CE= conductividad eléctrica; COS= carbono orgánico del suelo; MOS= materia orgánica en el suelo; dS=decisiemens; ppm=partes por millón; cmol= centimoles.
Experimento 1: Efecto de diferentes fuentes nitrogenadas sobre monocultivo de raigrás perenne (R). Se utilizó un diseño de bloques al azar (n=3, parcelas de 7 x 4 m) 30 kg ha-1 como densidad de siembra y fertilización con fuentes nitrogenadas con las fuentes especificadas en el Cuadro 2.
Cuadro 2 Tipo y concentración de fertilizantes utilizados en monocultivo de raigrás perennes en los dos sitios experimentales
| Tratamiento | Fertilizante | kg N ha-1 corte-1 | kg fertilizante ha-1 corte-1 |
Composición química |
|---|---|---|---|---|
| T0 | Sin fertilizante | 0 | 0 | Control |
| T1 | Urea | 20 | 43.5 | 46 % N, urea |
| T2 | Urea protegida | 20 | 50 | 40 % N, urea recubierta de PSCU 1 |
| T3 | Nitrato de amonio | 20 | 59.7 | 33.5 % N, 50 % en forma nítrica y 50 % en forma amoniacal |
| T4 | Nitrato de amonio + N foliar | 20 | 61-2 | 33.5 % N, 50 % en forma nítrica y 50 % en forma amoniacal + 18.7% p/v óxido de calcio; 25.5 % de p/V de N |
| T5 | N Foliar | 0.3 | 1.5 | 18.7% p/v óxido de calcio; 25.5 % de p/V de N |
(1)= polímero rico en azufre que permite una liberación controlada de urea, limitando la lixiviación.
Experimento 2: Efecto de mezclas forrajeras, raigrás con trébol blanco y trébol rojo a diferentes densidades de siembra. Se utilizó un diseño de bloques al azar (n=3, parcelas de 7 x 4 m) y mezclas de gramíneas y leguminosas, como se detalla en el Cuadro 3. Se seleccionaron estas dos especies de tréboles por sus diferentes hábitos de crecimiento: el trébol rojo tiene un crecimiento más erecto, mientras que el trébol blanco es más rastrero. Los tréboles no fueron inoculados con bacterias del género Rhizobium, ya que esto no es una práctica común en Ecuador puesto que existen cepas nativas aunque poco estudiadas15. Las densidades de siembra de trébol se ajustaron según León et al16 quienes consideran que deben oscilar entre 2.5 y 5 kg por hectárea.
Cuadro 3: Especies forrajeras utilizadas en el experimento 2 y sus densidades de siembra
| Tratamientos | Especies | Gramíneas | Leguminosas |
|---|---|---|---|
| (kg ha-1) | (kg ha-1) | ||
| T0 | Raigrás perenne (control) | 30 | 0 |
| T1 | Raigrás perenne + trébol blanco | 25 | 2.5 |
| T2 | Raigrás perenne + trébol blanco | 25 | 5 |
| T3 | Raigrás perenne + trébol rojo | 25 | 2.5 |
| T4 | Raigrás perenne + trébol rojo | 25 | 5 |
| T5 | Raigrás perenne + trébol blanco + trébol rojo | 25 | 5 (2.5 + 2.5) |
En función de la información suministrada por un tensiómetro, las parcelas experimentales de ambos experimentos se mantuvieron a capacidad de campo, mediante el uso de un sistema de riego por aspersión. Al inicio de los experimentos, se realizó una fertilización con 80 kg P ha-1 (superfosfato triple más microelementos) y 60 kg K ha-1 (muriato de potasio). Ambos experimentos se condujeron en cada sitio experimental, se sembraron en agosto 2021 mediante el método de siembra al voleo. Durante el año 2022 se evaluó mensualmente el crecimiento aéreo de los experimentos en las dos localidades, y en febrero del 2023, la biomasa subterránea.
Biomasa radicular (g MS L suelo-1): Se tomaron seis muestras al azar de cada tratamiento, se lavaron en bolsas plásticas con perforaciones tipo diamante de 3 mm, se separaron manualmente las raíces del suelo, se secaron con papel de filtro, se determinó el peso total de las raíces sin separación por cultivo (peso fresco), y finalmente se las deshidrató en una estufa con ventilación forzada, a 70 °C por 24 h; se pesaron y se calculó el porcentaje de materia seca17.
Número de nódulos (N° nódulos L suelo-1): Se tomaron seis muestras de cada tratamiento, con trébol rojo o blanco y el número de nódulos se determinó separando manualmente las raíces y nódulos18.
Peso de nódulos (mg MS L suelo-1): se tomaron seis muestras de cada tratamiento, con trébol rojo o blanco; los nódulos lavados se deshidrataron en una estufa con ventilación forzada, a 70 °C por 24 h, para determinar el peso seco19.
Todas las mediciones se realizaron en febrero 2023 sobre muestras de 20 x 20 x 20 cm20; esta profundidad de muestreo se usó porque en raigrás perenne y tréboles, más del 80 % de las raíces crece a una profundidad menor a los 20 cm21.
Análisis estadísticos. Para cada variable analizada, se determinó la distribución normal con la prueba de Shapiro- Wilks y homogeneidad de la varianza con la prueba de Levene. El análisis de los datos se realizó mediante análisis de varianza y las variables que presentaron diferencias estadísticas (P<0.05) se compararon con una prueba de Tukey. Se utilizó el programa estadístico INFOSTAT22.
El modelo matemático usado para el experimento 1 (monocultivo de ryegrass perenne) fue:
Siendo:
μ= efecto medio total,
Li= efecto de la Localidad i,
Bj (Li)= efecto del bloque j anidado en la localidad i,
Fk= efecto de la fuente de fertilización causado por el nivel k,
Eijk= Error experimental en nivel i del corte, nivel j del bloque y nivel k de la fuente.
El modelo matemático usado para el experimento 2 (mezcla de forrajes) fue:
Siendo:
μ= Efecto medio total
Li= efecto de la localidad i
Bj (Li)= efecto del bloque j anidado en la localidad i
Mk= efecto de la mezcla de raigrás con trébol causado por el nivel k
Eijk= Error experimental en nivel i del corte, nivel j del bloque y nivel k de mezcla de raigrás con trébol.
En la Figura 1 se presentan los datos de la biomasa radicular (Br) del experimento 1, expresados como gramos de MS de raíces por unidad de volumen (L) de suelo. En la sección (1A), se muestran las diferencias entre localidades sobre la cantidad de Br, siendo Tumbaco la que tuvo un mayor valor 4.04 g MS raíz L suelo-1 mientras que Machachi registró 3.22 g. En 1B, figuran los datos por tratamientos, el tratamiento N foliar tuvo la mayor Br 5.13 g, seguido de la urea, nitrato de amonio más N foliar y control (T0) (4.09; 3.58; 3.07 g), en menor cantidad el nitrato de amonio y urea protegida (2.99 y 2.92 g). En 1C se exponen la interacción (localidad x fuente), el N foliar tuvo la mayor Br en las dos localidades 4.64 g MS raíz L suelo-1 en Machachi y 5.62 g en Tumbaco, mientras que el control y el nitrato de amonio obtuvieron los menores valores de Br en Machachi (2.34 y 2.15 g).
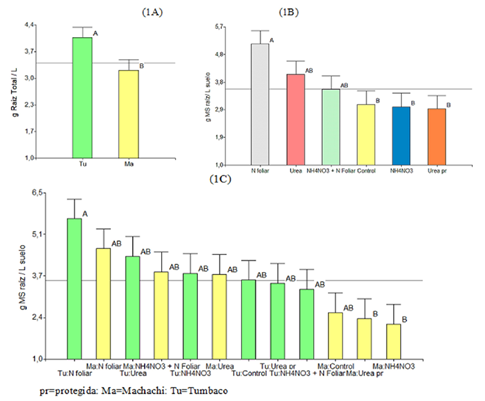
Los valores son medias + 1 error estándar. Letras diferentes indican diferencias significativas entre tratamientos (P<0.05). En cada figura, las medias generales están representadas por líneas continuas.
Figura 1 Efecto de fuentes de fertilizantes nitrogenados sobre la Biomasa radicular (g MS raíces L-1): (1A) efecto de localidades Machachi y Tumbaco; (1B) efecto de los tratamientos de las fuentes evaluadas; (1C) interacción localidad x tratamientos
En la Figura 2 se muestra la biomasa radicular (Br) de las diferentes mezclas forrajeras de raigrás perenne (R) con/sin trébol blanco (Tb) y con/sin trébol rojo (Tr). No hubo diferencias significativas entre localidades. Mientras que en 2A se observan diferencias (P<0.05) entre tratamientos, R + 2.5 Tr tuvo la mayor biomasa radicular (4.76 g MS raíz L suelo-1), el menor valor se registró en R + 2.5 Tb (2.35 g). En 2B se presentan la interacción localidad x mezcla, mostró que el R + Tr 2.5 kg tuvo la mayor Br en ambas localidades, en Machachi 4.98 g y Tumbaco 4.53 g. El control fue uno de los más altos Br en Tumbaco (4.79 g) y el valor más bajo de Br se observó en Machachi, en las parcelas R+ Tb 2.5 kg (1.37 g). Así mismo, la biomasa radicular en mezclas de raigrás con tréboles varió en función de la especie, observándose que las mezclas con trébol rojo tuvieron una mayor biomasa radicular 4.76 g, comparada con la del raigrás con trébol blanco, 2.35 g MS raíces L-1.
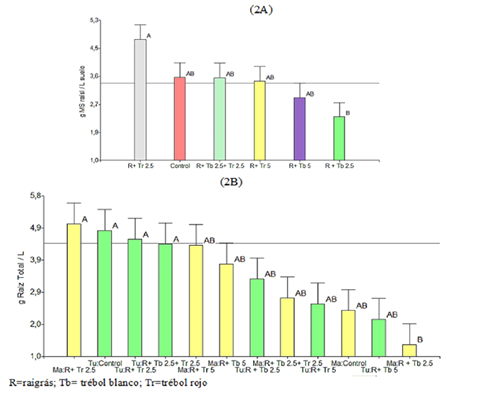
Los valores son medias + 1 error estándar. Letras diferentes indican diferencias significativas entre tratamientos (P<0.05). La media general está representada por línea continua en eje Y.
Figura 2 Efecto de las mezclas raigrás con trébol blanco o rojo sobre la biomasa radicular (g MS raíces L-1) (2A) diferencias entre mezclas; (2B) interacción localidad x mezcla
En la Figura 3A se muestran las diferencias estadísticas (P<0.05) para el número de nódulos (Nd) en la interacción localidad x mezcla. En Machachi la mezcla de R + Tb 5 kg tuvieron 90 Nd L suelo-1, así como la mezcla de R+ Tb 2.5 kg + Tr 2.5 kg 7 tuvieron 70 Nd, el mayor Nd, mientras que en Tumbaco R + Tr 5 kg tuvo 64 Nd. El peso de nódulos (Pn) presentó diferencia en la interacción localidad x mezcla (P<0.05). En 3B se observa que en Machachi la mezcla de R + Tb 5 kg tuvo 62 mg nódulos MS L suelo-1, siendo el mayor Pn, mientras que en Tumbaco la mezcla R + Tr 5 kg tuvo 41 mg nódulos.
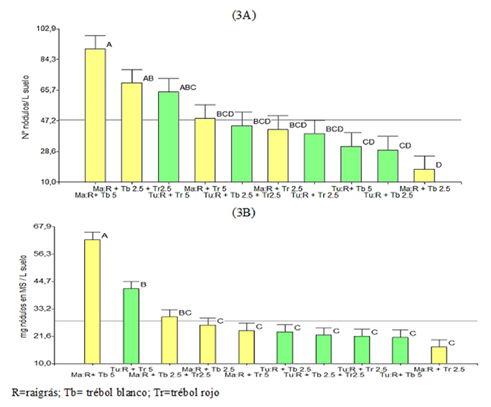
Los valores son medias + 1 error estándar. Letras diferentes indican diferencias significativas entre tratamientos (P<0.05). La media general está representada por línea continua en eje Y.
Figura 3 (3A) Efecto de la mezcla de raigrás con trébol blanco o rojo sobre el número de nódulos (N° nódulos/ L suelo) en la interacción localidad x mezcla. (3B) Efecto de la mezcla de raigrás con trébol blanco o rojo sobre el peso de nódulos (mg nódulos en MS/ L suelo) y de la interacción localidad x mezcla
Las diferencias de temperaturas, 16 °C en Tumbaco y 12 °C en Machachi, podrían ser las responsables de la mayor biomasa radicular en la primera respecto de la segunda localidad (4.04 vs 3.02 g MS raíces Lsuelo-1, respectivamente). Estos resultados guardan relación con Walne y Reddy23), quienes determinaron que la temperatura es un factor ambiental crítico que regula el crecimiento y el rendimiento de los cultivos. Por ejemplo, en el cultivo de maíz (Zea mays) al aumentar las temperaturas, detectaron raíces más largas, gruesas y más densas. De manera similar, en el cultivo de forrajeras perennes, el crecimiento de la planta se activaba con la temperatura24. En forrajeras megatérmicas, establecieron que las especies se adaptaban al ambiente al modificar su desarrollo radicular en profundidad y longitud25. Esto es corroborado por Cougnon et al26 quienes al estudiar pasturas de clima templado como el raigrás perenne y festuca (Festuca arundinacea Schreb), determinaron que tienen una mayor biomasa radicular cuando las temperaturas del suelo aumentan, como en la primavera.
La biomasa radicular en mezclas de raigrás con tréboles varió en función de la especie, observándose que las mezclas con trébol rojo tuvieron una mayor biomasa radicular 4.76 g MS raíces L-1, comparada con la del raigrás con trébol blanco, 2.35 g. Un factor importante en el desarrollo y crecimiento de las raíces del trébol blanco, según Nichols et al27, es la muerte de la raíz principal que se da entre los 12 y 18 meses después de la formación de la planta, luego de lo cual la planta depende únicamente de las raíces nodales. Las raíces nodales son más pequeñas y poco profundas, lo que limita la búsqueda de agua y nutrientes, lo que hace al trébol blanco más vulnerable28.
La nodulación de las leguminosas es un factor importante en la capacidad de fijar N, como lo aseguraron Echeverría y Sainz Rosas29, al mencionar que las bacterias de los nódulos podrían fijar entre el 25 y 80 % del N requerido por la planta, y que esta variabilidad obedecía a factores ambientales, edáficos y cepas de rizobios. También se debe tener presente que la transferencia de nitrógeno entre leguminosas y gramíneas en praderas mixtas jugaba un papel importante en el ciclo del nitrógeno de los sistemas agrícolas sostenibles30. Reilly et al31 afirmaron que la fijación biológica del N por las leguminosas aumentaba con el tiempo; también que la combinación de gramíneas y leguminas aumentaban el rendimiento total de biomasa, en comparación con monocultivos.
El número promedio de nódulos fue mayor en Machachi, 53.82 nódulos L-1 suelo, mientras que en Tumbaco fue de 41,86. Si bien el número de nódulos podría indicar la capacidad de fijar N por la leguminosa, la fijación de N2 por rizobios tiene un alto costo energético para la planta. Según Dicenzo et al32, para fijar una molécula de N2 atmosférico se requiere la inversión de 16 moléculas de ATP, aunque otros investigadores33 afirmaron que si se consideran todos los procesos asociados a la fijación biológica, el costo energético asciende a 30 ATP. En todo caso, el alto costo energético obligaría a la leguminosa a controlar el número de nódulos, evitando un excesivo gasto energético que comprometiera su desarrollo y supervivencia34. Por otro lado, si en el suelo existen zonas ricas en nitrógeno asimilable, las leguminosas obtienen este nutrimento por una vía no simbiótica, evitando un gasto energético extra35.
Así mismo, la planta provee al nódulo cantidades constantes de fosfato para el desarrollo del nódulo, por lo que las deficiencias de fosfato activan a un proceso de autoregulación de nódulos en leguminosas35,36. La disponibilidad de P en sus suelos tiene un efecto regulador en la nodulación37, por lo que la mayor disponibilidad de P en el suelo de Machachi podría explicar el mayor número de nódulos en esta localidad, puesto que deficiencias de P reducen el proceso de infección rizobial.
El peso promedio de los nódulos fue mayor en Machachi que en Tumbaco, 30.24 vs 25.97 mg de nódulos en base seca L-1 suelo. Según Dubach y Russelle38, al comparar el peso de nódulos en alfalfa (Medicago sativa) y trébol pata de pájaro (Lotus corniculatus), el peso de los nódulos estaba relacionado con la mayor concentración de N. En otro reporte39 al evaluar guisantes (Pisum sativum ssp. sativum), afirmaron que el peso de los nódulos estaba relacionado positivamente con el rendimiento de materia verde del cultivo. Por otro lado, en el cultivo de maní (Arachis hypogaea L.) la presencia de micorrizas tuvo influencia en el peso de los nódulos40.
Se ha sugerido que los nódulos de las raíces de las leguminosas establecen un nicho ecológico para la supervivencia y el crecimiento de otras bacterias41,42. Wigley et al43 concluyeron que los nódulos contienen diversas especies bacterianas en alfalfa (Medicago sativa) y que la densidad de población de estas bacterias están en el rango de 104 bacterias viables por gramo de tejido de nódulo de leguminosa fresco44.
Se ha denominado consorcio de microorganimos (CM) a la mezcla de dos o más especies o cepas microbianas, que viven juntas simbióticamente; generalmente un CM funciona mejor que la inoculación de una sola especie45. Ye et al46 también encontraron una mayor abundancia de moléculas derivadas de microbios en la plantación de leguminosas. Al evaluar el impacto de la co-inoculación de Rhizobium sp. y Azospirillum sp. en el crecimiento trébol rojo y obtuvieron una mayor desarrollo de los nodulos que al inocular Rhizobium solo47. La interacción de estas cepas forma un CM que potencializan el crecimiento radicular y rendimientos de los cultivos48. Por otro lado, se afirma49 que el contenido de carbono orgánico del suelo mejora las actividades microorganismos, y que actúa como un depósito de nutrientes del suelo y biológicamente aumenta el suministro de energía a los microbios50.
Por lo expuesto, el mayor peso de los nódulos en la localidad Machachi pudo deberse a la mejor disponibilidad de fósforo y carbono orgánico en suelo, permitiendo el desarrollo de microorganismos en general, y potencializaron la asociación leguminosa-Rhizobium.
La inoculación de leguminosa forrajeras debe ser una estrategia para mejorar la fijación de N, ya que los suelos pueden ser deficientes en número y calidad de rizobios autóctonos para mejorar la productividad de las plantas51. Trabajos realizados en Ecuador inoculando cepas nativas de Bradyrhizobium japonicum en el cultivo de soya (Glycine max L.), evidenciaron un mayor crecimiento del cultivo52. Granda-Mora et al15seleccionaron cepas nativas de Rhizobium sp. para frijol (Phaseolus vulgaris L.) en Ecuador, asegurando que el inoculante bacteriano obtenido estimulaba el crecimiento y rendimiento del frijol. Esto abre un puerta al uso potencial de cepas nativas para forrajeras, como en Argentina, donde obtuvieron mejoras de un 73 % en Desmanthus virgatus una forrajera nativa inoculada con rizobios nativos53 o Brasil, donde identificaron cepas nativas para Leucaena leucocephala y obtuvieron una mayor producción de biomasa y acumulación de N54.
El potenciar la capacidad de fijación de N en las leguminosas es una herramienta que permite reducir el uso de fertilizante N en la producción de pasturas55. Las asociaciones forrajeras de gramíneas y leguminosas aumentan la producción y calidad de forraje para el ganado56. Además presentan ventajas frente a la fertilización nitrogenada, que tiene efectos colaterales adversos: contaminación de agua por NO3-57y producción de N2O, un gas de efecto invernadero58.
La temperatura tiene un rol importante en el monocultivo de raigrás. Se detectaron diferencias entre especies respecto a la acumulación de biomasa radicular: mayor en el trébol rojo. En suelos de mayor fertilidad como Machachi, se observó un mayor número y peso de nódulos. La capacidad de nodulación fue diferente entre las leguminosas; en términos generales el trébol blanco tuvo un mayor número y peso de nódulos que el trébol rojo. Las especies pudieron adaptarse a los diferentes ambientes, el trébol rojo tuvo una mejor nodulación en las condiciones de Tumbaco, mientras que el trébol blanco fue mejor en Machachi. La cantidad de semilla de trébol a utilizar en la mezcla con raigrás perenne más aconsejable es 5 kg por hectárea, que permite lograr un mayor número y peso de nódulos, también realizar mezclas con tréboles blanco y rojo en 2.5 kg de cada uno.











 texto em
texto em 


