Introducción
El uso de aguas residuales en la región del Valle del Mezquital, en el estado de Hidalgo, ha impulsado el desarrollo agrícola al proporcionar aguas residuales a los distritos de riego: 003-Tula, 100-Alfajayucan y 112-Ajacuba, desde la construcción del gran canal de desagüe en 1856, permitiendo la producción de cultivos (García, 2019; Rosas y García, 2024).
Esta práctica ha enriquecido los suelos con materia orgánica favoreciendo el crecimiento de los cultivos (Guédron et al., 2014); sin embargo, ha generado la contaminación de fuentes de agua, degradación de suelos y exposición a sustancias tóxicas (González et al., 2015; Hernández et al., 2016; Leeser et al., 2018; Luneberg et al., 2018; Chamizo et al., 2020) propiciando problemas ambientales y de salud pública.
Entre los contaminantes más peligrosos se encuentran los metales pesados, debido a su alta movilidad en el medio y su capacidad de bioacumulación (Garduño et al., 2023). La exposición prolongada a plomo (Pb) y cadmio (Cd) representa un grave riesgo para la salud, con límites permisibles de 0.2 mg L-1 para Pb y Cd en aguas residuales y para uso y consumo humano los límites son de 0.01 mg L-1 y 0.005 mg L-1 para Pb y Cd, respectivamente, de acuerdo con las (NOM-001-SEMARNAT-2021; NOM-127-SSA1-2021; SCFI, 2022 a, b).
Los metales pesados generan radicales libres específicos del metal que causan estrés oxidativo en células que ocasiona daño al ADN, inactivación de proteínas enzimáticas, agregación de proteínas, cambios conformacionales que afectan su estructura, función y causan daño celular (Wu et al., 2016), lo anterior se ve reflejado en efectos sistémicos crónicos y aumento en la incidencia de cáncer cuando se encuentran en concentraciones elevadas en el agua de consumo humano (Contreras et al., 2017; Izquierdo et al., 2022).
A pesar del impacto ambiental y a la salud pública, la contaminación por metales pesados en el Valle del Mezquital ha sido poco analizada, siendo una de las regiones más afectadas ambientalmente en México. El objetivo del trabajo fue medir los niveles de plomo y cadmio en distintas fuentes de agua del Valle del Mezquital, Hidalgo, para determinar si exceden los límites permisibles establecidos por la normatividad mexicana.
De manera específica, se buscó cuantificar las concentraciones de estos metales en aguas residuales, naturales y potables de la región, así como comparar estadísticamente los niveles entre los distintos tipos de fuentes hídricas para identificar zonas de riesgo. La hipótesis planteó que dichas concentraciones superaron los valores normativos, lo que representó un riesgo potencial para la salud pública y el medio ambiente, derivado del uso prolongado de aguas residuales en actividades agrícolas.
Materiales y métodos
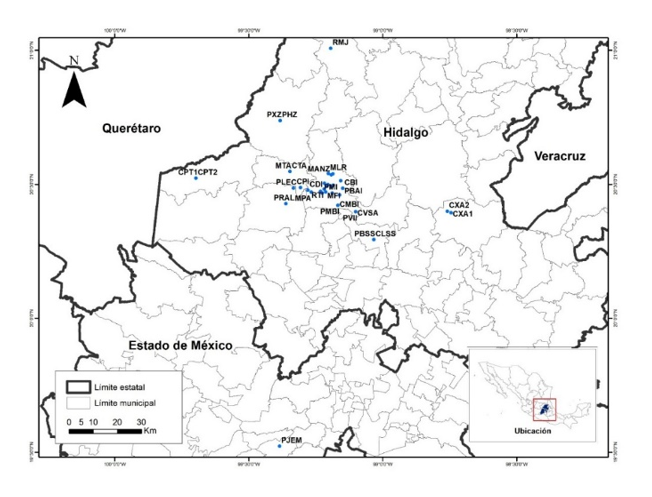
El análisis de aguas se realizó en la Universidad Tecnológica del Valle del Mezquital. Se colectaron 29 muestras de aguas residuales procedentes de canales de riego, presas y ríos, las aguas potables y purificadas se obtuvieron, seis de manantiales, cuatro de pozos y 16 de fuentes potables, en total de 54 muestras del estado de Hidalgo y una del Estado de México como control (Cuadro 1).
Cuadro 1 Muestras de aguas residuales, naturales y potables colectados en el estado de Hidalgo.
| Clave | Origen | Ubicación | Altitud (msnm) | Clave | Origen | Ubicación | Altitud (msnm) |
|---|---|---|---|---|---|---|---|
| CPT1 | Canal | Tecozautla | 1 733 | PMI1 | Presa | El Maye, Ixmiquilpan | 1 720 |
| CPN1 | Canal | Pueblo Nuevo, Ixmiquilpan | 1 781 | MTA | Manantial | Arbolado, Tasquillo | 1 704 |
| CLJI | Canal | La Joya, Ixmiquilpan | 1 772 | MFI | Manantial | El Fitzi, Ixmiquilpan | 1 798 |
| CSM1 | Canal | San Miguel, Ixmiquilpan | 1 714 | MPA | Manantial | Panales, Ixmiquilpan | 1 780 |
| CLSS | Canal | Lagunilla, San Salvador | 1 979 | MLR | Manantial | Remedios, Ixmiquilpan | 1 767 |
| CPT2 | Canal | Pañhe, Tecozautla | 1 733 | MAN1 | Manantial | Remedios, Ixmiquilpan | 1 757 |
| CPN2 | Canal | Pueblo Nuevo, Ixmiquilpan | 1 781 | MAN2 | Manantial | Remedios, Ixmiquilpan | 1 762 |
| CBI1 | Canal | Bangandho, Ixmiquilpan | 1 795 | PLRI | Pozo | Reforma, Ixmiquilpan | 1 738 |
| CNI1 | Canal | El Nith, Ixmiquilpan | 1 751 | PXZ | Pozo | Xindho, Zimapan | 1 779 |
| CMLI | Canal | Media Luna, Ixmiquilpan | 1 738 | PJEM* | Pozo | Santa Ana, Jilotzingo | 2 739 |
| CSM2 | Canal | San Miguel, Ixmiquilpan | 1 714 | CNI2 | Pozo | Panales, Ixmiquilpan | 1 751 |
| COBI | Canal | La Otra Banda, Ixmiquilpan | 1 738 | RSNI | Potable | Sn Nicolás, Ixmiquilpan | 1 719 |
| CTA1 | Canal | Tasquillo | 1 704 | PBAI | Potable | Bangando, Ixmiquilpan | 1 795 |
| CXA1 | Canal | San Nicolás, Atotonilco | 2 012 | PEC | Potable | El Carrizal, Ixmiquilpan | 1 774 |
| CPN3 | Canal | Pueblo Nuevo, Ixmiquilpan | 1 781 | PLJI | Potable | La Joya, Ixmiquilpan | 1 772 |
| CPI1 | Canal | Portezuelo, Ixmiquilpan | 1 784 | PUTV | Potable | UTVM, Ixmiquilpan | 1 772 |
| CDI1 | Canal | El Deca, Ixmiquilpan | 1 762 | PVII | Potable | Villagran, Santiago de A. | 1 941 |
| CXA2 | Canal | Xathé, Atotonilco el Grande | 2 049 | PLEC | Potable | La Vega, Alfajayucan | 1 848 |
| CLOI | Canal | Loma del Oro, Ixmiquilpan | 1 738 | PEVI | Potable | El Valante, Ixmiquilpan | 1 731 |
| CLRI | Canal | La Reforma, Ixmiquilpan | 1 738 | PMBI | Potable | Maguey B., Ixmiquilpan | 1 798 |
| CVSA | Canal | Villagrán, Santiago de A. | 1 941 | PBSS | Potable | Bóxtha, San Salvador | 1 979 |
| CMBI | Canal | Maguey Blanco, Ixmiquilpan | 1 798 | PENI | Potable | El Nith, Ixmiquilpan | 1 751 |
| CSM3 | Canal | San Miguel, Ixmiquilpan | 1 714 | PRPA | Potable | Panales, Ixmiquilpan | 1 780 |
| CCAI | Canal | Capula, Ixmiquilpan | 1 757 | PRMA | Potable | El Maye, Ixmiquilpan | 1 720 |
| RTI1 | Río | Tula | 1 773 | PLRE | Potable | La Reforma, Ixmiquilpan | 1 738 |
| RMJ | Río | Moctezuma, Jacala | 1 360 | PRPO | Potable | Portezuelo, Ixmiquilpan | 1 784 |
| CPAI | Canal | Panales, Ixmiquilpan | 1 780 | PRAL | Potable | Alfajayucan | 1 871 |
| PHZ | Presa | Hidroeléctrica, Zimapan | 1 779 |
*= muestra colectada en el Estado de México.
El muestreo se realizó de acuerdo con la NMX-AA-003-1980 (SCFI, 1980). Se colectaron 500 ml de las muestras en envase de polietileno. Se preservaron añadiendo ácido nítrico hasta un pH de 2, se refrigeraron a 4 °C por un periodo no mayor a seis meses.
La determinación de metales totales se realizó por el método de flama con espectrofotómetro de absorción atómica (modelo Buck Scientific AAS VGP 216, UAS.), por triplicado de acuerdo con la NMX-AA-051-SCFI-2001 (SCFI, 2001). La digestión se realizó en parrilla de calentamiento, se homogenizó verificando que no existieran sólidos adheridos al fondo, se tomó una alícuota de 50 ml y se transfirió a un vaso de precipitados.
Se añadieron 3 ml de ácido nítrico concentrado y se calentó en placa de evaporación, evitando el hervor, hasta obtener de 2 a 5 ml y se dejó enfriar. Se adicionaron 5 ml de ácido nítrico concentrado, se cubrió con vidrio de reloj y se pasó a parrilla, elevando la temperatura hasta reflujo de vapores, concluida la digestión, se retiró y se dejó enfriar.
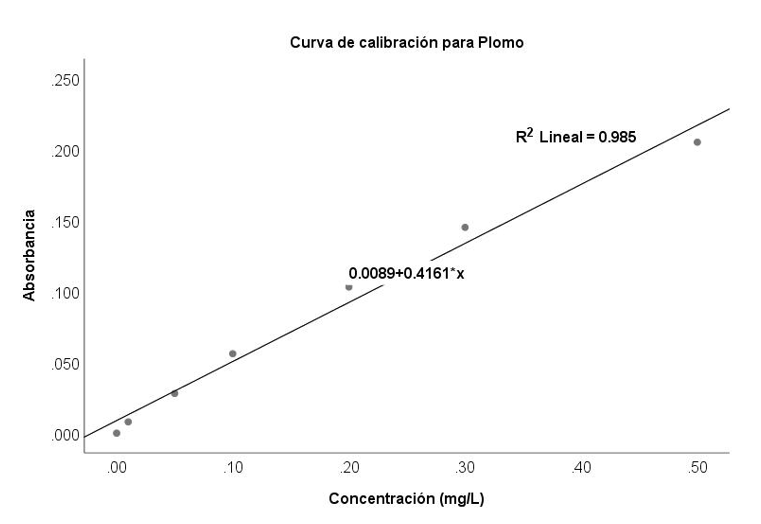
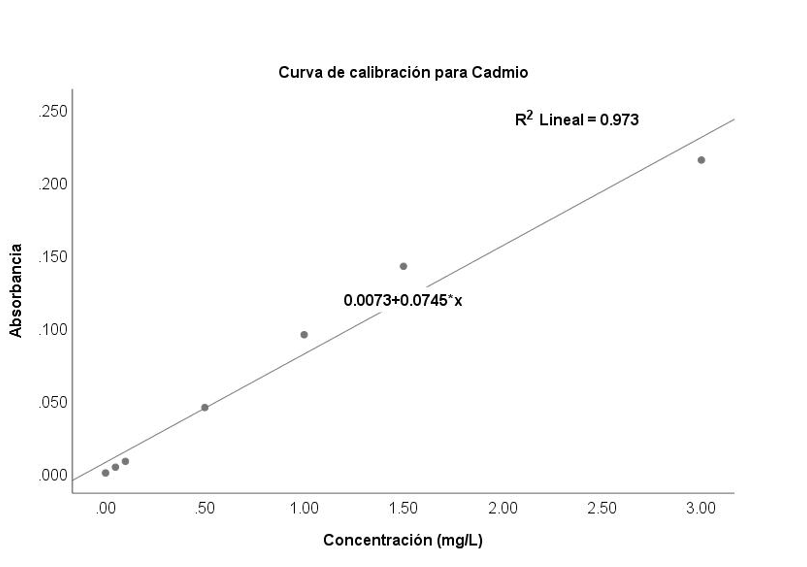
Por cada 100 ml de volumen de disolución final, se adicionaron 10 ml de ácido clorhídrico (1:1) y 15 ml de agua. Posteriormente, la muestra se calentó durante 15 min sin alcanzar el punto de ebullición y se aforó a 100 ml. Para la toma de lecturas, se calibró el espectrofotómetro de acuerdo con el inciso 9.3 de la norma NMX-AA-051-SCFI-2001, finalmente, se realizaron los cálculos, de acuerdo con la ecuación 1 de la recta, así como el coeficiente de determinación R2, con valores de 0.985 para Pb y 0.973 para Cd.
Ecuación 1.
Análisis estadísticos
Con los valores de concentraciones de Pb y Cd de los sitios de muestreo, se realizó un análisis de varianza (Anova) y post-hoc para realizar las comparaciones múltiples entre medias, se utilizó la prueba de rangos múltiples de Scheffe, con α= 0.05 para indicar la significancia estadística debido a la homogeneidad de varianzas, lo anterior se realizó con el paquete estadístico SPSS Statistics Versión 25.
Resultados y discusión
Curvas de calibración. Se prepararon soluciones patrón con concentraciones conocidas de Pb: 0.01, 0.05, 0.1, 0.2, 0.3 y 0.5 mg ml-1, y de Cd: 0.005, 0.01, 0.05, 0.1, 0.15 y 0.3 mg ml-1, incluyendo un blanco como referencia. Las mediciones se realizaron mediante espectroscopía de absorción atómica, a longitudes de onda de 283.3 nm para Pb y 326.1 nm para Cd, con un ancho de banda de 0.1 nm. Se utilizó acetileno como combustible y óxido nitroso como gas soporte, optimizando la atomización de los analitos (Figura 1).
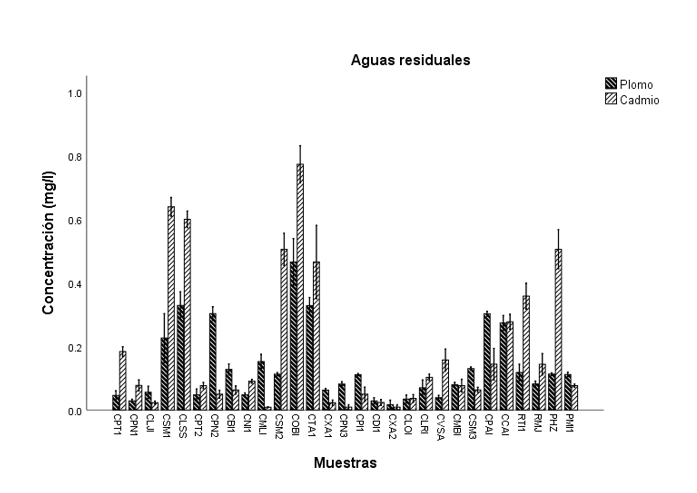
Concentraciones de Pb y Cd en aguas residuales. El análisis de las muestras de aguas residuales reveló que el 26% de ellas superaron los límites permisibles de Pb, establecidos en 0.2 mg L-1, con concentraciones que oscilaron entre 0.017 mg L-1 y 0.466 mg L-1 (Figura 2).
En el caso de Cd, el 30% de las muestras excedieron dicho límite, registrando concentraciones entre 0.009 mg L-1 y 0.774 mg L-1. Los valores obtenidos para ambos metales presentaron diferencias estadísticamente significativas (p= 0) en todos los análisis de varianza realizados, bajo condiciones de homogeneidad (Cuadro 2). Resultados similares fueron reportados por Oloruntoba et al. (2022), quienes identificaron concentraciones elevadas de Pb y Cd en aguas residuales.
Cuadro 2 Concentraciones de Pb y Cd en aguas residuales, naturales y potables.
| Clave | Plomo (mg L⁻¹) | Cadmio (mg L⁻¹) | Clave | Plomo (mg L⁻¹) | Cadmio (mg L⁻¹) |
|---|---|---|---|---|---|
| CPT1¹ | 0.046 ±0.006ᵃ⁻ᵇ | 0.184 ±0.006ᶠ | PMI1¹ | 0.111 ±0.003ᶜ⁻ᶠ | 0.077 ±0.002ᵃ⁻ᵈ |
| CPN1¹ | 0.029 ±0.002ᵃ⁻ᵇ | 0.077 ±0.007ᵃ⁻ᵈ | MTA² | 0.022 ±0.021ᵃ⁻ᵇ | 0.009 ±0.002ᵃ |
| CLJI¹ | 0.056 ±0.008ᵃ⁻ᶜ | 0.023 ±0.023ᵃ⁻ᵇ | MFI² | 0.007 ±0.017ᵃ | 0.023 ±0.001ᵃ |
| CSM1¹ | 0.226 ±0.031ᵍ | 0.64 ±0.012ʲ | MPA² | 0.015 ±0.006ᵃ⁻ᵇ | 0.036 ±0.006ᵃ⁻ᵇ |
| CLSS¹ | 0.329 ±0.017ʰ | 0.6 ±0.011ʲ | MLR² | 0.005 ±0.003ᵃ | 0.05 ±0.003ᵃ⁻ᵇ |
| CPT2¹ | 0.048 ±0.008ᵃ⁻ᵇ | 0.077 ±0.004ᵃ⁻ᵈ | MAN1² | 0.031 ±0.005ᵃ⁻ᵇ | 0.009 ±0.001ᵃ |
| CPN2¹ | 0.303 ±0.009ʰ | 0.05 ±0.005ᵃ⁻ᶜ | MAN2² | 0.147 ±0.007ᶜ⁻ᵈ | 0.023 ±0.005ᵃ |
| CBI1¹ | 0.128 ±0.007ᵉ⁻ᶠ | 0.063 ±0.005ᵃ⁻ᶜ | PLRI² | 0.029 ±0.006ᵃ⁻ᵇ | 0.009 ±0.001ᵃ |
| CNI1¹ | 0.048 ±0.003ᵃ⁻ᵇ | 0.09 ±0.003ᵇ⁻ᵉ | PXZ² | 0.113 ±0.002ᶜ | 0.506 ±0.024ᵉ⁻ᶠ |
| CMLI¹ | 0.152 ±0.009ᶠ | 0.009 ±0.001ᵃ | PJEM² | 0.178 ±0.007ᵈ | 0.372 ±0.021ᶜ⁻ᵈ |
| CSM2¹ | 0.113 ±0.002ᶜ⁻ᶠ | 0.506 ±0.02ⁱ | CNI2² | 0.012 ±0.002ᵃ | 0.063 ±0.009ᵃ⁻ᵇ |
| COBI¹ | 0.466 ±0.03ⁱ | 0.774 ±0.024ᵏ | RSNI² | 0.329 ±0.03ᵉ | 0.466 ±0.015ᵉ⁻ᶠ |
| CTA1¹ | 0.329 ±0.01ʰ | 0.466 ±0.047ⁱ | PBAI² | 0.005 ±0.001ᵃ | 0.533 ±0.008ᶠ⁻ᵍ |
| CXA1¹ | 0.063 ±0.002ᵃ⁻ᵈ | 0.023 ±0.004ᵃ⁻ᵇ | PEC² | 0.149 ±0.009ᶜ⁻ᵈ | 0.452 ±0.036ᵈ⁻ᶠ |
| CPN3¹ | 0.082 ±0.003ᵇ⁻ᵉ | 0.009 ±0.003ᵃ | PLJI² | 0.017 ±0.003ᵃ⁻ᵇ | 0.6 ±0.049ᵍ |
| CPI1¹ | 0.111 ±0.002ᶜ⁻ᶠ | 0.05 ±0.009ᵃ⁻ᶜ | PUTV² | 0.015 ±0.002ᵃ⁻ᵇ | 0.426 ±0.009ᶜ⁻ᵈ |
| CDI1¹ | 0.029 ±0.004ᵃ⁻ᵇ | 0.023 ±0.004ᵃ⁻ᵇ | PVII² | 0.022 ±0.008ᵃᵇ | 0.493 ±0.008ᵉ⁻ᶠ |
| CXA2¹ | 0.017 ±0.006ᵃ | 0.009 ±0.003ᵃ | PLEC² | 0.056 ±0.007ᵇ | 0.479 ±0.011ᵉ⁻ᶠ |
| CLOI¹ | 0.034 ±0.005ᵃ⁻ᵇ | 0.036 ±0.005ᵃ⁻ᶜ | PEVI² | 0.015 ±0.004ᵃ⁻ᵇ | 0.452 ±0.003ᵈ⁻ᶠ |
| CLRI¹ | 0.07 ±0.01ᵃ⁻ᵈ | 0.103 ±0.004ᶜ⁻ᵉ | PMBI² | 0.022 ±0.013ᵃ⁻ᵇ | 0.09 ±0.001ᵃ⁻ᵇ |
| CVSA¹ | 0.039 ±0.003ᵃ⁻ᵇ | 0.157 ±0.014ᵉ⁻ᶠ | PBSS² | 0.012 ±0.001ᵃ | 0.077 ±0.003ᵃ⁻ᵇ |
| CMBI¹ | 0.08 ±0.003ᵇ⁻ᵉ | 0.077 ±0.008ᵃ⁻ᵈ | PENI² | 0.015 ±0.003ᵃ⁻ᵇ | 0.023 ±0.001ᵃ |
| CSM3¹ | 0.13 ±0.002ᵉ⁻ᶠ | 0.063 ±0.003ᵃ⁻ᶜ | PRPA² | 0.005 ±0.002ᵃ | 0.332 ±0.002ᶜ |
| CCAI¹ | 0.274 ±0.01ᵍ⁻ʰ | 0.278 ±0.01ᵍ | PRMA² | 0.007 ±0.002ᵃ | 0.533 ±0.017ᶠ⁻ᵍ |
| RTI1¹ | 0.118 ±0.011ᵈ⁻ᶠ | 0.358 ±0.017ʰ | PLRE² | 0.024 ±0.007ᵃ⁻ᵇ | 0.009 ±0.004ᵃ |
| RMJ¹ | 0.082 ±0.004ᵇ⁻ᵉ | 0.144 ±0.014ᵈ⁻ᶠ | PRPO² | 0.027 ±0.005ᵃ⁻ᵇ | 0.117 ±0.002ᵃ |
| CPAI¹ | 0.303 ±0.003ʰ | 0.144 ±0.02ᵈᵉᶠ | PRAL² | 0.017 ±0.001ᵃ⁻ᵇ | 0.774 ±0.029ʰ |
| PHZ¹ | 0.113 ±0.002ᶜ⁻ᶠ | 0.506 ±0.025ⁱ | |||
| x̅ ±SD | 0.135 ±0.004 | 0.194 ±0.008 | x̅ ±SD | 0.049 ±0.003 | 0.268 ±0.009 |
| CV (%) | 2.92 | 3.9 | CV (%) | 5.75 | 3.46 |
Resultados expresados como la media ± la desviación estándar, letras diferentes en la misma columna indican diferencias significativas con p= 0.05. x̅= media; SD= desviación estándar; CV= coeficiente de variación; 1= aguas residuales; 2= aguas naturales y potables.
Asimismo, Kinuthia et al. (2020) documentó que los niveles de Pb en aguas residuales utilizadas para riego agrícola superaban los límites establecidos por la Organización Mundial de la Salud (OMS) y la Agencia de Protección Ambiental (EPA) de los Estados Unidos de América. En más del 30% de los estudios revisados se han identificado concentraciones de metales pesados como cromo (Cr), cadmio (Cd), plomo (Pb), cobre (Cu) y zinc (Zn) por encima de los límites permisibles establecidos por la normatividad ambiental vigente.
Esta situación resalta la necesidad urgente de tratar adecuadamente los afluentes de aguas residuales antes de su descarga en cuerpos de agua superficiales, a fin de prevenir la contaminación de los mantos acuíferos subterráneos (Arti y Mehra, 2023). En la región del Valle del Mezquital, el uso de aguas residuales para el riego agrícola es una práctica común. Diversas investigaciones han evidenciado que los metales pesados presentes en estas aguas pueden ser absorbidos por las plantas.
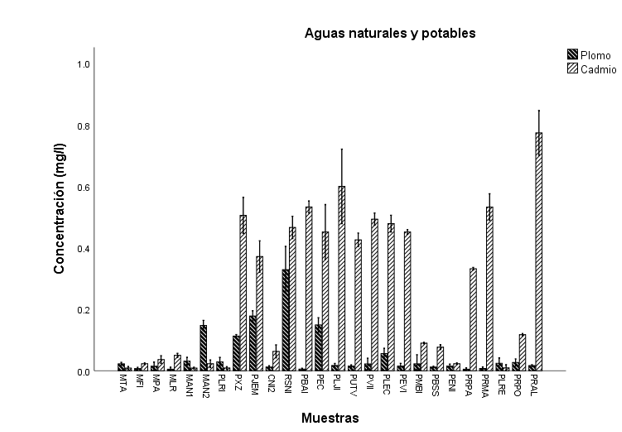
En este sentido, Lara et al. (2015) reportaron la presencia de Cd y Pb en cultivos de maíz, alfalfa y girasol, con concentraciones que variaron de 0.001 a 0.096 mg kg-1 para Cd y de 0.05 a 0.613 mg kg-1 para Pb. Las concentraciones de Pb y Cd registradas en muestras de aguas naturales y potables superaron los límites permisibles en un 70% y 100% de los casos, respectivamente. Además, se observaron diferencias estadísticas entre los valores obtenidos (Cuadro 2, Figura 3 y Figura 4).
Estos hallazgos coinciden con lo reportado por Balli y Leghouch (2018); Oloruntoba et al. (2022), quienes documentaron concentraciones elevadas de Pb y Cd en agua potable proveniente de pozos y manantiales. En ambos estudios, los niveles detectados exceden los valores establecidos por la Organización Mundial de la Salud (OMS) para agua apta para consumo humano, lo que representa un riesgo potencial para la salud pública.
Al respecto Sansom et al. (2019) reportaron que el 30.8% de los hogares analizados presentaban concentraciones de Pb en agua potable entre 0.6 y 2.4 g L-1, excediendo los límites permisibles y evidenciando la necesidad de proteger la salud pública. La contaminación de aguas subterráneas por metales pesados ya sea por causas geogénicas o antropogénicas, representa un riesgo significativo para la salud humana, especialmente mediante la ingesta de agua contaminada (Oloruntoba et al., 2022).
Mejorar su calidad antes del consumo es esencial, aunque las plantas de tratamiento no generan efectos inmediatos debido a la acumulación de materia orgánica, microorganismos y metales pesados. En el Valle del Mezquital, las aguas residuales utilizadas para riego también recargan los acuíferos, contaminando las fuentes de agua potable. A nivel global, más del 20% del agua dulce disponible ya no satisface la demanda, y se estima que la mitad de la población enfrentará escasez severa (Mancosu et al., 2015).
Esto resalta la urgencia de una gestión integral y un monitoreo continuo de los afluentes (Chamizo et al., 2020), dada la toxicidad acumulativa en organismos vivos y su relación con enfermedades como el cáncer (Arti y Mehra, 2023). El agua es la principal vía de exposición humana a metales pesados. El Cd genera estrés oxidativo, daños en pulmones, riñones, huesos y es considerado carcinogénico (Bernhoft, 2013; Rinaldi et al., 2017) El Pb, por su parte, afecta el sistema nervioso, presión arterial y el desarrollo cognitivo, especialmente en niños (Gidlow, 2004).
En el Valle del Mezquital, la contaminación del agua es el resultado del uso histórico de aguas residuales no tratadas para el riego agrícola, el vertido de residuos urbanos e industriales, así como el escurrimiento de agroquímicos desde suelos cultivados. Esta recarga contaminada de los acuíferos compromete las fuentes de abastecimiento.
Los resultados obtenidos en este estudio abren la puerta al desarrollo de investigaciones complementarias que incluyan parámetros fisicoquímicos y microbiológicos, fundamentales para la toma de decisiones en el diseño de políticas públicas y estrategias de intervención. El uso de aguas residuales debe estar sujeto a estricta vigilancia, priorizando siempre la seguridad humana (Vázquez et al., 2020).
De acuerdo a la zona de muestreo (Figura 5), no se observó una relación directa entre la concentración de Pb y Cd y la cercanía a los puntos de descarga. Aunque se esperaba una disminución en zonas más alejadas, los resultados no reflejan esta tendencia, sugiriendo una dispersión más compleja de los contaminantes.
Conclusiones
El análisis de aguas realizado en la región del Valle del Mezquital, en el estado de Hidalgo, evidenció que las concentraciones de Pb y Cd exceden los límites permisibles establecidos por la normatividad mexicana vigente. En aguas residuales, los niveles de Pb y Cd superan dichos límites en un 26% y 30%, respectivamente. En el caso de aguas naturales y potables, las concentraciones rebasan los valores normativos en un 70% para Pb y hasta en un 100% para Cd. Estos resultados reflejan las consecuencias de más de un siglo de uso continuo de aguas residuales para el riego agrícola en la región.
Ante esta situación, es indispensable fortalecer y dar continuidad a estudios científicos orientados a la evaluación periódica y específica de contaminantes en cuerpos de agua. Asimismo, resulta fundamental implementar estrategias integrales para el manejo adecuado de residuos y el tratamiento eficiente de aguas, con miras a su reutilización segura en la agricultura. Para lograrlo, es crucial fomentar la colaboración entre los distintos sectores: académico, gubernamental, industrial y social, promoviendo un enfoque interdisciplinario que garantice la protección de la salud pública, la seguridad alimentaria y la sustentabilidad ambiental en la región.











 texto em
texto em