Introducción
El esteviósido (Stv) y rebaudiósido-A (Reb-A) son los metabolitos secundarios de mayor importancia en las hojas de Stevia rebaudiana Bertoni (Asteraceae), se clasifican como glucósidos diterpénicos y son responsables de la propiedad edulcorante en las hojas y extractos derivados de las mismas (Brandle y Telmer, 2007; Libik-Konieczny et al., 2021), la particularidad de estos glucósidos es que pueden alcanzar una dulzura entre 143 y 320 veces mayor a la sacarosa y son libres de calorías, por tanto, no causan efectos secundarios dañinos en el cuerpo humano (Perrier et al., 2018; Libik-Konieczny et al., 2021). Actualmente, el Stv y Reb-A presentan alta demanda en países con problemas de salud pública como diabetes y obesidad por tratarse de edulcorantes naturales que sustituyen al azúcar y a edulcorantes sintéticos (Marcinek y Krejpcio, 2016; Ahmad et al., 2020). Con el fin de aumentar la concentración de Stv y Reb-A en el cultivo de S. rebaudiana, los estudios se han centrado en gran medida en la biomasa total producida (Mamta et al., 2010; Mandal et al., 2013), sin embargo, para mejorar la productividad en términos de metabolitos secundarios, se está impulsando la aplicación de agrotecnologías como la gestión del fotoperiodo (Alvarado-Orea et al., 2020; Rivera-Avilez et al., 2021), cultivo de tejidos (Aguilar-Jiménez et al., 2019; Sharma et al., 2023), uso de alcoholes y sales (Gupta et al., 2014) y gestión del estrés hídrico (Fronza y Folegatti, 2003; Karimi et al., 2019). No obstante, es indispensable explorar en la manipulación de macronutrientes como el fósforo (P) que son indispensables en los procesos de biosíntesis de compuestos de interés (Maniruzzaman et al., 2017; Libik-Konieczny et al., 2021).
Es necesario identificar los principales factores que afectan la concentración de Stv y Reb-A, la eficiencia en la traslocación de P en la planta es clave para mejorar la producción de metabolitos (Tavarini et al., 2018). Además, se conoce ampliamente que las micorrizas translocan P del suelo a las plantas y favorecen su crecimiento, asimismo, pueden mejorar la producción de metabolitos secundarios como resultado de una mejor absorción de agua y nutrientes por la planta (Sbrana et al., 2014; Sarmiento-López et al., 2020), no obstante, la nutrición mejorada con P es probablemente el beneficio más conocido y documentado de los hongos micorrícicos arbusculares (HMA) para las plantas (Zimmerman et al., 2009; Bagyaraj et al., 2015; Gao et al., 2020; Higo et al., 2020). El efecto beneficioso de los HMA se atribuye a una extensa red micelial capaz de explorar el suelo más allá de la zona de influencia de las raíces (Roy-Bolduc y Hijri, 2011; Spatafora et al., 2016;). También se sabe que los consorcios de HMA nativos suelen ser más efectivos que los productos a base de especies exóticas o una sola especie, debido a que los HMA se adaptan a ciertas condiciones ambientales específicas y su introducción en diferentes ambientes puede causar desbalance al medio (Lima et al., 2015).
Por otra parte, en el campo del análisis, el enfoque más popular para la cuantificación de Stv y Reb-A es la cromatografía líquida de alto rendimiento (HPLC), este método se basa en la separación y cuantificación de los glucósidos, sin embargo, tiene limitaciones como la necesidad de compuestos estándar, tiempos de análisis relativamente largos y reproducibilidad deficiente a medida que el rendimiento de la columna empeora con el tiempo. A diferencia de los métodos basados en cromatografía, la resonancia magnética nuclear (1H-RMN) ha demostrado ser una herramienta rápida y eficiente para cuantificar los glucósidos de esteviol en hojas de S. rebaudiana (Tangpaisarnkul et al., 2018).
La 1H-RMN se basa directamente en los átomos (espines nucleares) de las moléculas, por lo que tiene, en principio, capacidad cuantitativa y se puede aplicar al análisis de cuantificación. Además, representa un enfoque completamente diferente que no depende de la separación de analitos y es considerada como una alternativa factible al HPLC, ya que permite un análisis significativamente más rápido y con una excelente reproducibilidad y robustez (Pieri et al., 2011). Por lo anterior, el objetivo de este estudio fue cuantificar mediante H1 RMN el contenido de Stv y Reb-A en plantas de S. rebaudiana inoculadas con consorcios de HMA en interacción con niveles de P.
Materiales y métodos
Condiciones experimentales
Se trasplantaron a nivel invernadero plantines de S. rebaudiana Bert. variedad Morita II de 15 cm aproximadamente, provenientes del INIFAP-C.E. Uxmal, Yucatán, México. Los consorcios de HMA evaluados provenían de localidades diferentes del estado de Yucatán y se determinaron como 1) RC; proveniente de Reserva Cuxtal (integrado por Funneliformis geosporum, Claroideoglomus claroideum, Glomus ambisporum), 2) TZ; proveniente de Tizimín (Integrado por Gigaspora spp. y Glomus spp.) y CY; Colonia Yucatán (integrado por Funneliformis spp., Glomus spp. y Ambispora spp.). Los tres consorcios fueron extraídos por Cauich-Cauich et al. (2023). Los tratamientos (RC, TZ, CY y el control) se aplicaron directamente en el sustrato en concentración de 110 esporas. Los niveles de P evaluados fueron 0, 25, 50, 75 y 100 % suministrado como; 0, 79, 158, 237 y 316 mg de P2O5 kg-1 suelo respectivamente, con base en la fertilización convencional (Ramírez-Jaramillo y Lozano-Contreras, 2017). Se utilizó sustrato estéril compuesto de suelo y bagazo de henequén en proporción 2:1 v/v y bolsas negras de poliestireno de 25 x 25 cm. Se aplicó riego por goteo con el 80 % de la ETo (Cauich-Cauich et al., 2018). Las temperaturas promedio registradas fueron 39 °C máxima y 24 °C mínima.
Diseño experimental
Se utilizó un diseño completamente al azar donde se distribuyeron 20 tratamientos con 4 repeticiones que resultaron de la combinación de RC, TZ, CY, Control y 0, 25, 50, 75 y 100 % de P.
Colonización micorrícica total
Al final del experimento se estimó el porcentaje de colonización, para ello, las raíces se tiñeron siguiendo la técnica de Phillips y Hayman (1970). La colonización micorrícica total se calculó según el método de intersección de líneas (Giovannetti y Mosse, 1980). Se evaluaron 100 segmentos de raíces de cinco plantas para cada tratamiento.
Fósforo foliar
El contenido de P a nivel foliar de se realizó al final del experimento mediante µ-Fluorescencia de Rayos X (μ-XRF), con las metodologías descritas por Chí-Sánchez et al. (2021) en un equipo M4Tornado 100 (Bruker, Alemania). El haz colimador fue de 2 mm, el tubo de rayos X fue operado a 50kV y 200 μA y con un área sensible de 30 mm2. Se cuantificó P en g kg-1 de materia seca. Las mediciones fueron realizadas al vacío a 20 mbar directamente a los porta muestras que contenían hoja seca y molida.
Preparación de muestras para 1H-RMN
Las hojas de S. rebaudiana se secaron en una estufa de aire forzado a 70 °C hasta peso constante y se pulverizaron en un molino de laboratorio SV-MO-300T. Posteriormente, se liofilizaron para eliminar la humedad residual. Por cada repetición se tomaron 50 mg de muestra molida y se le colocó 1 mL de dimetilsulfóxido deuterado (DMSO-d6) (Sigma-Aldrich 99.9 atom %) como disolvente de grado espectroscópico con desplazamiento químico (δ) de 2.5, se adicionó 5 mg mL-1 de nicotinamida como referencia interna con δ de 7.5, 8.0, 8.5, 8.9, la cual se utiliza ampliamente y es aceptable como patrón de referencia (Dona et al., 2016). Posteriormente, se homogeneizo la solución por sonificación durante 60 minutos y se filtró para separar los residuos y partículas grandes.
Análisis por 1H-RMN
Los espectros se registraron en un espectrómetro Varian 600 MHz AR Premium Compact (Santa Clara, California U.S.) utilizando las siguientes condiciones experimentales: tiempo de adquisición: 2.73 s, retardo de relajación: 1 s, número de transientes: 32, recopilados en 64k puntos de datos, número de puntos de la adquisición: 28,846 y 4 bloques de barrido (Biswapriya et al., 2019). Los espectros fueron procesados en el programa MestReNova, incluyendo ajuste de fase manual, ajuste exponencial con LB: 0.3 Hz, corrección de línea base automática y referencia con respecto a la nicotinamida (7.5, 8.0, 8.5, 8.9 ppm). Se eliminaron las señales relacionadas con la saturación de la resonancia del agua con δ 3.4 y se integraron las regiones bajo las señales seleccionadas, normalizando la integración respecto a la señal de la nicotinamida. Los espectros 1H-RMN de las muestras se registraron con parámetros constantes para garantizar la precisión de los resultados.
Análisis cuantitativo de Stv y Reb-A
La aplicación de 1H-RMN cuantitativa requiere que al menos una señal no superpuesta para que cada molécula a cuantificar esté disponible para la integración, conocer el número de hidrógenos o núcleos que proyectan la señal y la concentración de la referencia. La cuantificación se realizó según Malz y Jancke (2005) de acuerdo con la siguiente ecuación:
Donde:
Cm = Concentración en la muestra (mg mL-1).
Href = Número de hidrógenos (protones) de la referencia.
Iref = Intensidad de la señal (integral) de la referencia.
Cref = Concentración de la referencia (mg mL-1).
Hm = Número de hidrógenos (protones) de la muestra.
Im = Intensidad de la señal (integral) de la muestra.
Análisis estadísticos
Los datos obtenidos en porcentaje se transformaron para homogeneizar varianzas mediante la función arco seno, con los datos obtenidos se realizó análisis de varianza y se aplicó como comparador de medias el método de Tukey (P ≤ 0.05) mediante el paquete estadístico InfoStat versión 2014 (Universidad Nacional de Córdova, Argentina).
Resultados y discusión
Porcentaje de colonización micorrícica total
El mayor porcentaje de colonización se obtuvo en el tratamiento RC+0 %P, seguido de RC+25 %P con 80 y 76 % respectivamente. Mientras mayor fue la cantidad de P aplicado, el porcentaje de colonización disminuyó. Es decir, se vio afectado con dosis altas de P, lo que sugiere que, a niveles altos de P en la rizosfera, la simbiosis micorrícica se interrumpe y se vuelve irrelevante para las plantas (Smith et al., 2011). Por tanto, la cantidad de P considerado en el plan de fertilización puede limitar el efecto de HMA en plantas inoculadas.
Contenido de fósforo foliar
La inoculación de los consorcios RC y CY permitió un aumento significativo (P ≤ 0.05) en el contenido de P a nivel foliar en S. rebaudiana. Los tratamientos RC+25 %P y CY+25 %P estimularon la mayor acumulación de P en las hojas con 1.39 y 1.34 g kg-1 de materia seca respectivamente, superando al control (control + 25 %P) en un 89 % (Tabla 1).
Tabla 1 Efecto de la inoculación de consorcios de HMA nativos y diferentes concentraciones de P2O5 en el contenido de fósforo en hojas S. rebaudiana.
Table 1: Effect of native HMA consortia inoculation and different P2O5 concentrations in phosphorous content in S. rebaudiana leaves.
| Contenido (g kg-1 materia seca) | P adicionado (%) | Consorcios de HMA | ||||
| RC | TZ | CY | Control | Media | ||
| P | 0 | 0.41 ± 0.05 c | 0.54 ± 0.11 bc | 0.37 ± 0.07 c | 0.08 ± 0.01 f | 0.35 D |
| 25 | 1.39 ± 0.20 a | 0.79 ± 0.10 b | 1.34 ± 0.21 a | 0.15 ± 0.03 d | 0.92 A | |
| 50 | 1.12 ± 0.18 a | 0.65 ± 0.13 b | 0.97 ± 0.17 ab | 0.24 ± 0.02 e | 0.75 A | |
| 75 | 0.81 ± 0.03 b | 0.71 ± 0.09 b | 0.64 ± 0.09 b | 0.36 ± 0.09 c | 0.63 AB | |
| 100 | 0.53 ± 0.07 bc | 0.47 ± 0.06 bc | 0.52 ± 0.01 bc | 0.35 ± 0.04 c | 0.47 C | |
| Media | 0.85 A | 0.63 B | 0.77 A | 0.24 C | ||
| Significancia: HMAxP= **; HMA= **; P= ** | ||||||
Medias (n= 4) ± desviación estándar. Letras minúsculas indican el efecto de la interacción HMA*P. Letras mayúsculas en la fila indican el efecto de consorcios HMA. Letras mayúsculas en la columna indican el efecto de niveles de fósforo. La significancia se indica como: **: significativo a P ≤ 0.01.
En plantas sin micorriza el contenido de P foliar mostró un comportamiento directamente proporcional al P adicionado, es decir, mientras mayor fue la dosis de P, hubo mayor contenido de P en las hojas. Por el contrario, en plantas micorrizadas se observó una tendencia diferente, a medida que aumentó la dosis de P adicionado, el contenido de P foliar disminuyó, esta respuesta puede atribuirse a la disminución del porcentaje de colonización observada en esta condición, lo que afectó la respuesta de la micorrización.
Los consorcios HMA tuvieron efectos significativos en el contenido de P foliar. Se obtuvieron aumentos considerando la sola inoculación de los HMA en comparación a plantas no inoculadas. No obstante, el consorcio TZ mostró menor desempeño en los resultados, esto sugiere que, probablemente, las especies que lo integran no tienen afinidad en la traslocación de P en plantas de S. rebaudiana como lo tendrían en otras variables u especies vegetales. Es importante tener en cuenta que las especies de HMA pueden tener diferentes tipos de interacción con las plantas, y esta condición se puede ver reflejado en su efectividad (Eun-Hwa et al., 2013).
El efecto sinérgico de RC+25 %P y CY+25 %P superó a la fertilización convencional. Estos resultados van de acuerdo con el estudio previo realizado por Mandal et al. (2015), quienes observaron aumentos hasta del 56 % en el contenido de P en plantas micorrizadas en comparación a plantas control. Por su parte, Tavarini et al. (2018) informaron que en plantas micorrizadas de S. rebaudiana el contenido de P foliar fue significativamente más alto cuando se aplicaron dosis bajas de P (25 mg de P2O5 kg-1 suelo).
La eficiencia de los consorcios RC y CY en la traslocación de P aumentó cuando los niveles de P aplicado en el suelo fueron menores a 158 mg de P2O5 kg-1 suelo, sin embargo, además de un adecuado nivel de P, también influye la afinidad con la que las especies que conforman el consorcio capturan P en el suelo, incluso cuando sea escaso (Smith et al., 2011; Jansa et al., 2019). Este sentido, este resultado puede atribuirse a que los géneros Funneliformis y Glomus spp. presentes en los consorcios RC y CY han sobresalido en otros estudios por su afinidad en la toma de P (Hoseini et al., 2015; Sahodaran et al., 2019). El consorcio TZ no tuvo efectos significativos, lo que supone, que las especies que lo integran no tienen afinidad sobre esta variable.
Los resultados son consistentes con el papel conocido de los HMA en la nutrición de las plantas, el aumento en el contenido de P foliar por efecto de la simbiosis micorrícica también se asocia principalmente a la actividad de las hifas extraradicales que proporcionan una vía adicional para la captación de P (Ezawa y Saito, 2018).
Intensidad de señales Stv y Reb-A en espectro 1H-RMN
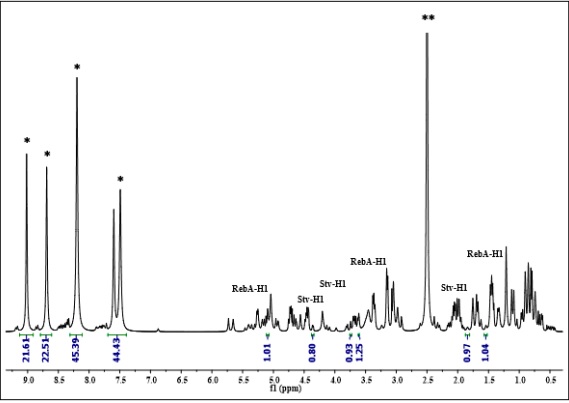
Se adquirieron 80 espectros, en cada uno se identificó la señal del disolvente DMSO-d6 (δ 2.5 ppm), y se integraron las señales de referencia interna (nicotinamida) (δ 7.5, 8.0, 8.5, 8.9 ppm), así como, las señales del Stv y Reb-A. La identificación correcta de las señales en los espectros fue respaldada con los estándares (ver información de soporte). En la figura 1 se observa un espectro 1H-RMN representativo de las muestras procesadas de S. rebaudiana.
Figura 1 Espectro 1H-RMN (DMSO-d6, 600 MHz) representativo de las muestras de S. rebaudiana mostrando las señales seleccionadas e integradas correspondientes a esteviósido (Stv-H1) y rebaudiósido-A (RebA-H1) para su cuantificación. **señal de DMSO-d6, *señales integradas de la referencia (nicotinamida).
Cuantificación
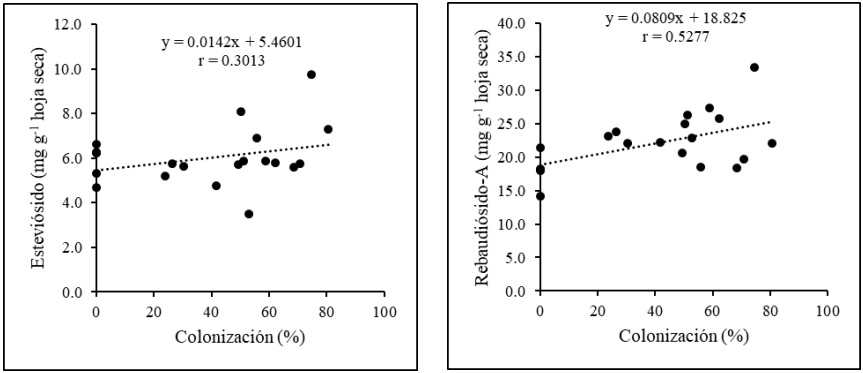
La interacción entre los consorcios de HMA y niveles de P tuvo efectos significativos (P ≤ 0.05) en la concentración de Stv y Reb-A. El tratamiento RC+25 %P mejoró la concentración tanto de Stv como de Reb-A en comparación al control, generando 9.76 y 33.46 mg g-1 de hoja seca respectivamente (Tabla 2), lo que fue consistente con la respuesta del mismo tratamiento en el contenido de P foliar. En plantas micorrizadas por RC, mientras mayor fue el nivel de P adicionado, menor fue la concentración de Stv. Por su parte, el efecto de los consorcios TZ y CY no mostró diferencias estadísticamente significativas (P ≤ 0.05) con respecto al control en la concentración de Stv, este resultado se vio reflejado en un bajo coeficiente de correlación entre el porcentaje de colonización y la concentración de Stv y Reb-A (r = 0.09 y r = 0.5 para Stv y Reb-A respectivamente (figura 2).
Tabla 2 Efecto de la inoculación de consorcios nativos de HMA y fertilización con fósforo en el contenido de esteviósido y rebaudiósido-A en hojas de S. rebaudiana Bert.
Table 2: Effect of native HMA consortia inoculation and phosphorous fertilization in stevioside and rebaudioside-A contents, in S. rebaudiana Bert leaves.
| Glucósido (mg g-1 hoja seca) | P adicionado (%) | Consorcios de HMA | ||||
| RC | TZ | CY | Control | Media | ||
| Stv | 0 | 7.29 ± 0.44 b | 5.60 ± 0.88 bc | 5.74 ± 0.26 c | 4.68 ± 1.29 c | 5.83 A |
| 25 | 9.76 ± 0.87 a | 5.77 ± 1.02 bc | 5.87 ± 0.51 bc | 5.31 ± 0.53 c | 6.68 A | |
| 50 | 8.07 ± 0.53 b | 6.91 ± 0.72 b | 5.70 ± 0.53 bc | 6.61 ± 0.76 bc | 6.82 A | |
| 75 | 4.77 ± 0.52 cd | 5.86 ± 0.60 bc | 3.50 ± 0.17 ce | 6.26 ± 0.83 bc | 5.10 AB | |
| 100 | 5.75 ± 0.91 bc | 5.19 ± 0.39 c | 5.63 ± 1.11 bc | 6.24 ± 0.85 bc | 5.70 AB | |
| Media | 7.13 A | 5.87 B | 5.29 B | 5.82 B | ||
| Significancia: HMAxP= *; HMA= **; P= ns | ||||||
| Reb-A | 0 | 22.00 ± 1.30 c | 18.38 ± 1.50 cd | 19.73 ± 0.76 cd | 14.18 ± 1.40 e | 18.57 D |
| 25 | 33.46 ± 4.41 a | 25.75 ± 0.74 b | 27.38 ± 1.25 b | 18.08 ± 2.47 cd | 26.16 A | |
| 50 | 24.91 ± 1.21 b | 18.54 ± 1.96 cd | 20.60 ± 1.29 c | 18.27 ± 2.12 cd | 20.58 C | |
| 75 | 22.15 ± 2.15 bc | 26.33 ± 0.72 b | 22.84 ± 1.00 bc | 17.97 ± 0.72 d | 22.32 B | |
| 100 | 23.75 ± 0.92 bc | 23.17 ± 1.38 bc | 22.10 ± 1.61 c | 21.38 ± 1.15 c | 22.60 B | |
| Media | 25.25 A | 22.43 B | 22.53 B | 17.98 C | ||
| Significancia: HMAxP= **; HMA= **; P= * | ||||||
Medias (n = 4) ± DE. Letras minúsculas indican el efecto de la interacción HMA*P. Letras mayúsculas en la fila indican el efecto de consorcios HMA. Letras mayúsculas en la columna indican el efecto de niveles de fósforo. La significancia se indica como: ns: no significativo, *: significativo a P ≤ 0.05, **: significativo a P ≤ 0.01.
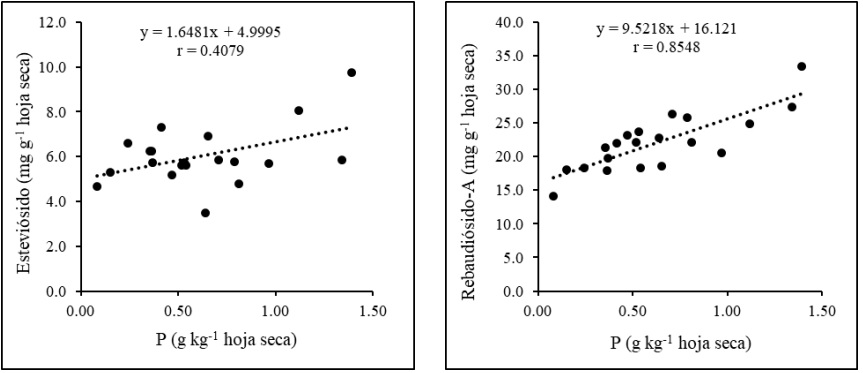
La concentración de Reb-A se vio mejorada en los tratamientos TZ y CY (22.43 y 22.53 mg g-1 de hoja seca respectivamente) en comparación al control, sin embargo, este resultado no superó la concentración que generó RC+25 %P, el cual superó en un 63 % a la fertilización convencional en la concentración de ambos glucósidos. En el presente estudio es evidente el efecto benéfico del consorcio RC, que en combinación con 25 %P permitió aumentar 63 % el rendimiento tanto de Stv como de Reb-A, lo que indica que, aportes mayores al 25 %P en la fertilización de plantas micorrizadas no siempre conlleva a un aumento en la concentración de glucósidos en S. rebaudiana. Este resultado se atribuye a que el mismo tratamiento mejoró el contenido de P foliar. A pesar de ello, esta observación no puede atribuirse a una dosis específica de P en plantas micorrícicas. Roy-Bolduc y Hijri (2011) afirman que la absorción de otros nutrientes por micorrización puede causar una disminución en la concentración de P debido a la dilución interna en la planta. Sin embargo, en este estudio, se obtuvo en general una correlación lineal positiva entre el contenido de fósforo a nivel foliar y el contenido de Stv y Reb-A en las hojas de S. rebaudiana, mostrando un coeficiente de correlación de r = 0.4 y r = 0.8 para Stv y Reb-A respectivamente, como se observa en la figura 3.
El consorcio CY también optimizó el contenido de P foliar cuando se combinó con 25 %P, sin embargo, este beneficio no se vio reflejado en la concentración de Stv. Por tanto, el aumento en la producción de metabolitos secundarios por HMA podría estar relacionado tanto por mecanismos nutricionales como no nutricionales como lo menciona Zubek et al. (2012) y Mandal et al. (2013). Probablemente, el efecto benéfico diferencial de las especies HMA que conforman el consorcio CY no tiene afinidad en la vía de glucosilación del Stv, lo que probablemente estaría relacionado con la regulación de genes involucrados en la ruta de biosíntesis de glucósidos de esteviol. Es decir, las especies de HMA pueden influir de manera diferente en la productividad de las plantas. En este contexto, Sarmiento-López et al. (2021) obtuvieron menor acumulación de Reb-A en plantas inoculadas con Rhizophagus irregularis + 200 µM de fosfato monopotásico y, por el contrario, concentraciones superiores en plantas testigo con el mismo nivel de fertilización.
Los consorcios TZ y CY aumentaron la concentración de Reb-A cuando se combinaron con 25 y 75 % P, sin embargo, no optimizaron el contenido de Stv, esto sugiere que posiblemente la combinación de los consorcios influyó en la activación de genes clave que codifican glicosiltransferasas en el proceso de biosíntesis. Mohamed et al. (2011) mencionan que las glicosiltransferasas son específicas y transfieren moléculas de azúcar de un donante activo a una molécula aceptora. Por lo tanto, la concentración de azúcar influye en la formación de cada glucósido en las hojas de S. rebaudiana (Samsulrizal et al., 2019).
Por otra parte, la concentración de metabolitos secundarios en las plantas está en función de la variedad, el lugar del cultivo, la temporada, las condiciones de cultivo y la precisión del método analítico (Pieri et al., 2011). En México se ha reportado para S. rebaudiana variedad Morita II 2.18 % de Stv y 9.12 % de Reb-A (en proporción 1:8 veces) utilizando para el análisis cromatografía líquida de alto rendimiento (HPLC) (Aranda-González et al., 2015). En este estudio, las concentraciones de Stv oscilaron entre 3.50 y 9.76 mg g-1 de hoja seca, y las de Reb-A entre 14.18 y 33.46 mg g-1 de hoja seca, utilizando para el análisis 1H-RMN. En comparación a lo reportado anteriormente, se obtuvo alrededor de 2 veces más el contenido de Stv y Reb-A en plantas micorrizadas y fertilizadas con 25 %P. En otros estudios como el de Mandal et al. (2013) reportaron en India concentraciones de Stv y Reb-A entre 35 y 40 mg g-1 de hoja seca en plantas de S. rebaudiana inoculadas con una especie de HMA (Rhizhophagus fasciculatus) + 50 mg P2O5 kg-1 suelo, sin embargo, utilizaron la variedad Cimmeethi.
Conclusiones
En este trabajo, se hace énfasis de la utilización de consorcios HMA como una estrategia para eficientizar la traslocación de P en la planta y mejorar la concentración de Stv y Reb-A. Los resultados mostraron que las plantas de S. rebaudiana inoculadas con el consorcio RC en combinación con 25 % P (con base en la dosis fertilización convencional) presentaron 76 % de colonización, mayor contenido de P a nivel foliar y se mejoró la concentración de Stv y Reb-A en comparación a las plantas fertilizadas de manera convencional. Esto indica que la nutrición vegetal, especialmente la fertilización con P en plantas micorrícicas optimiza y desempeña un papel importante en la biosíntesis de glucósidos de esteviol. Además, la aplicación del consorcio RC como biofertilizante, es válido para este cultivo, ya que mejora la concentración de Stv y Reb-A. Por otro lado, los consorcios TZ y CY solo optimizaron la concentración de Reb-A en comparación al control, esto puede explicarse por la interacción entre diferentes simbiontes presentes en cada consorcio, lo cual resulta en respuestas diferenciales en la producción de compuestos específicos. Adicionalmente, la 1H-RMN permitió la cuantificación de los principales glucósidos de S. rebaudiana sin basarse en el uso de compuestos estándar y sin la necesidad de una calibración externa, esto da como resultado un análisis más rápido. La 1H-RMN puede ser una alternativa factible al HPLC para la cuantificación de Stv y Reb-A en S. rebaudiana.
Información suplementaria
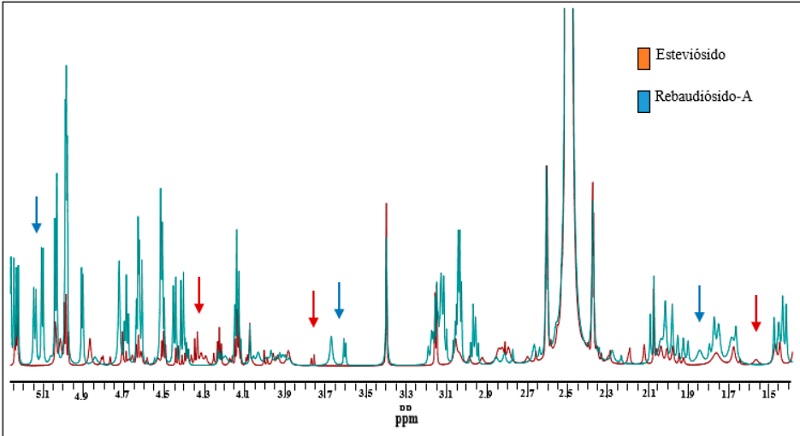
Se detectaron por 1H-RMN las señales correspondientes al esteviósido (Stv) y rebaudiósido-A (Reb-A) para lo cual, se utilizaron los estándares comerciales: stevioside hydrate (98 %) y rebaudioside A (96 %) (Sigma-Aldrich). Los espectros de los estándares se superpusieron y se compararon para seleccionar aquellas señales que no mostraran traslape, con la finalidad de identificar la diferencia y particularidad de señales de cada glucósido (Stv y Reb-A). Ambos espectros se caracterizaron por mostrar tres grupos distintos de señales que corresponderían a los protones (H-1) de la aglicona y de los azúcares unidos de acuerdo con su estructura química.
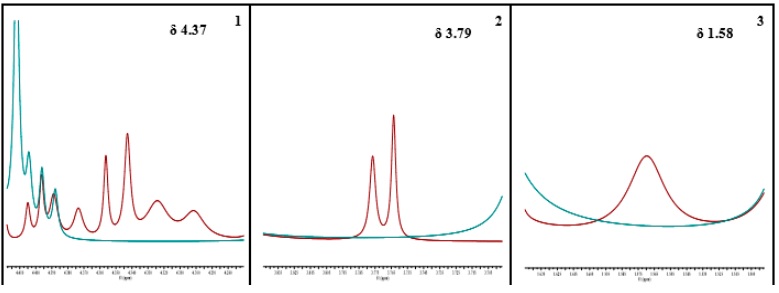
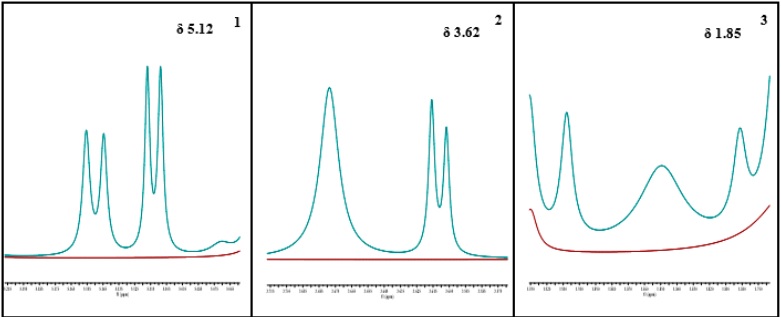
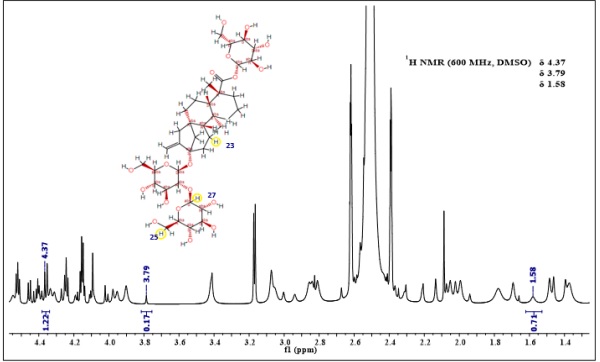
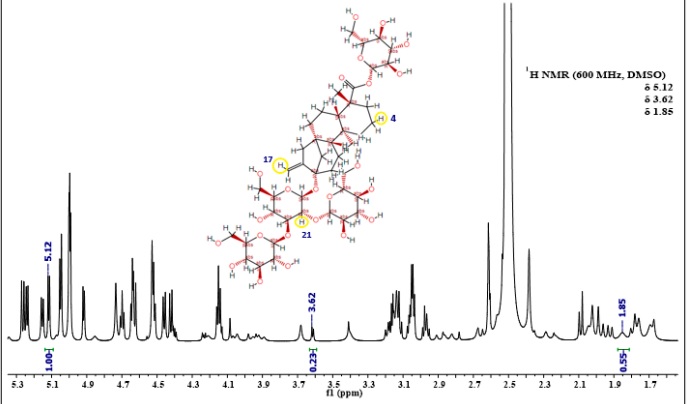
En la figura soporte 1 se observan los tres grupos distintos de señales no traslapadas que mostraron los estándares Stv y Reb-A. En el caso del Stv, se seleccionaron las señales con desplazamiento químico (δ) a 4.37, 3.79 y 1.58 ppm (Figura soporte 2, imagen amplificada que corresponde a las flechas rojas), para el caso del Reb-A se integraron las señales con δ 5.12, 3.62 y 1.85 ppm (Figura soporte 3, imagen amplificada que corresponde a las flechas azules).
En cada espectro, se identificó las señales no traslapadas, la intensidad de la señal y la posición de los H-1 de acuerdo con su estructura química. En el espectro de Stv, las señales correspondientes a los H-1 se encontraron en las posiciones 25, 27 y 23 (Figura soporte 4). En el espectro de Reb-A, las señales correspondientes a los H-1 se encontraron en las posiciones 17, 21 y 4 de acuerdo con su estructura química (Figura soporte 5).











 nova página do texto(beta)
nova página do texto(beta)