Introducción
La comunicación interauricular (CIA) tipo ostium secundum es un defecto congénito cardiaco frecuente y el tratamiento percutáneo ha demostrado ser efectivo en estos pacientes como alternativa menos invasiva al tratamiento quirúrgico1-3.
Algunas características anatómicas de la CIA como la ausencia o deficiencia de borde aórtico u otras inherentes al procedimiento, como el sobredimensionamiento del dispositivo implantado, se han relacionado con el riesgo eventual de erosión4. Esta complicación es muy poco frecuente, pero clínicamente relevante, pudiendo incluso causar taponamiento cardiaco y muerte.
Las troponinas que integran el aparato contráctil de las células musculares cardiacas son los biomarcadores utilizados en la práctica clínica para la determinación de lesión miocárdica, principalmente como criterio principal para el diagnóstico de síndromes coronarios agudos5. Sin embargo, es conocido que enfermedades cardiacas no relacionadas con trombosis coronarias como taquicardias u otras pueden provocar también elevación plasmática de troponinas.
En estudios previos, el 40-100% de los pacientes sometidos a tratamiento percutáneo de cierre de CIA presentaron elevación de troponinas en las horas posteriores a la intervención. Pocos estudios han investigado la influencia del déficit de borde aórtico en el metabolismo de las troponinas. Adicionalmente, otros autores han sugerido que intervenciones más complejas definidas como procedimientos más prolongados en tiempo, determinan la elevación de estas en plasma6.
El objetivo de nuestro estudio fue determinar la relación entre la elevación de troponina T cardiaca de alta sensibilidad (hs-cTnT) posterior al tratamiento percutáneo de una CIA con el déficit de borde aórtico, así como con otras variables anatómicas y con maniobras propias y específicas de la intervención.
Material y métodos
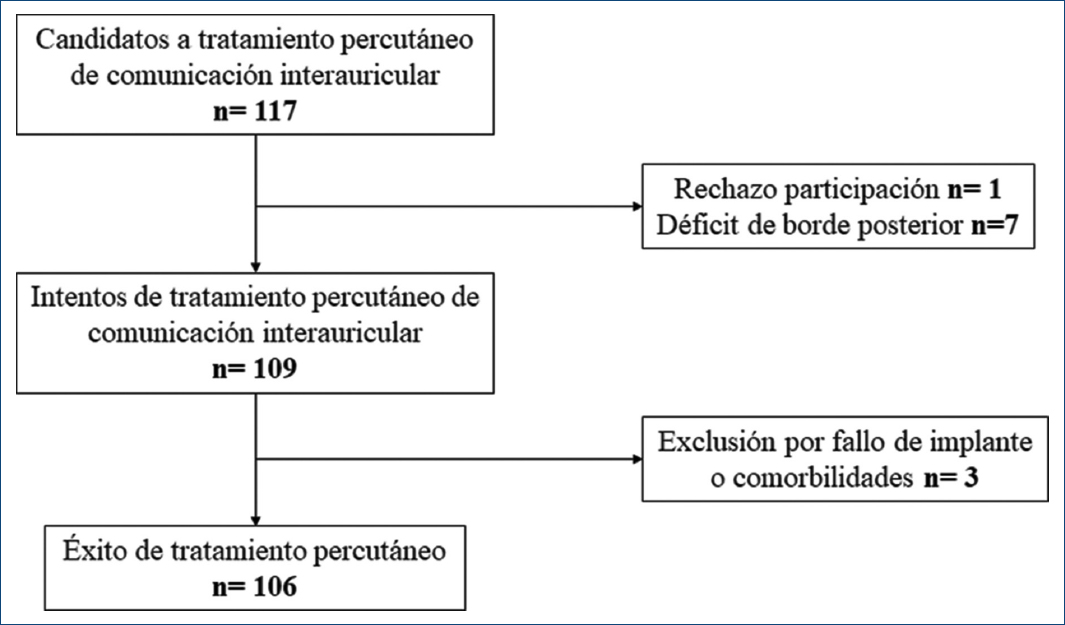
Estudio observacional, prospectivo y comparativo de mediciones repetidas. Desde julio de 2020 a noviembre de 2023, se evaluaron 117 pacientes con CIA tipo ostium secundum programados para tratamiento percutáneo. De ellos, 106 pacientes fueron finalmente incluidos en el estudio. Las causas de exclusión de los 11 pacientes restantes fueron rechazo a participar en un caso (0.85%) y en los otros 10 casos debido a falta de implante del dispositivo durante el procedimiento (8.5%) (Fig. 1). Las indicaciones de tratamiento percutáneo fueron dilatación de cavidades derechas y/o síntomas clínicos de insuficiencia cardiaca derecha. Todos los pacientes o sus tutores autorizaron mediante firma de consentimiento la participación en el estudio, el cual fue aprobado por el comité de investigación y de ética institucional.
Los datos demográficos y del procedimiento fueron obtenidos de todos los pacientes. El tratamiento percutáneo fue realizado bajo anestesia general con asistencia respiratoria mecánica en todos los casos. Los parámetros hemodinámicos fueron registrados previamente al tratamiento percutáneo. Se utilizó ecocardiografía transesofágica (ETE) para el monitoreo durante la intervención con equipo GE Vivid S5 y sonda transesofágica (GE 6Tc). El defecto fue evaluado con el paciente anestesiado y previo a comenzar con el tratamiento percutáneo. La anatomía de los bordes se clasificó según seis bordes7 y el déficit de borde aórtico fue determinado cuando este fue menor a 5 mm en tres vistas consecutivas8.
Se utilizaron dispositivos Nit-Occlud ASD-R (PFM Medical, Alemania) y Memopart ASD (Lepu Medical, China). El tamaño del dispositivo que implantar se determinó según el diámetro máximo del defecto. Se implantaron dispositivos con cintura de 2 a 4 mm mayor que el diámetro máximo medido del defecto o 2 mm mayor en caso de haber realizado medición con balón elastomérico.
El método de oclusión percutánea se realizó según los estándares actuales. En resumen, bajo guía fluoroscópica y ecocardiográfica se desplegó el disco izquierdo del dispositivo en aurícula izquierda, posteriormente tensionando el cable liberador, se apoyó el disco izquierdo sobre el septum interauricular controlando dichas maniobras con ETE. Luego se desplegó el disco derecho del dispositivo del lado derecho del septum interauricular. Después de observar la correcta posición del dispositivo, se realizó la maniobra de tirar/empujar para evaluar el anclaje y estabilidad del dispositivo. En casos de posición incorrecta o prolapso de alguno de los discos, se procedió a la recaptura, remoción y reposicionamiento del dispositivo. Previamente se reevaluó el defecto y en algunos casos fue preciso implantar un dispositivo de un tamaño mayor en diámetro.
Se definió como sobredimensionamiento cuando la cintura del dispositivo implantado fue mayor al 50% del máximo diámetro medido. Se consideró como deformación de senos de Valsalva cuando algunos de los discos del dispositivo provocaban un colapso (indentación) mayor a 1 mm de la curvatura del seno con respecto a la curvatura original de este9.
Antes de la intervención se midieron los niveles de hs-cTnT y se repitió la medición 6 horas después de la finalización del procedimiento. Las mediciones de troponinas fueron realizadas usando un autoanalizador Cobas® (EE.UU.) y Electrochemiluminescence Ultrasensitive Troponin T Assay (Roche®, Alemania). El límite de referencia superior (LRS) fue 14 pg/ml.
Los datos son presentados como número de observaciones y porcentaje para variables categóricas y media con desviación estándar (DE) o mediana y rango intercuartílico (RIC) para las variables continuas de acuerdo con su distribución.
Las diferencias entre grupos fueron analizadas con test de Chi cuadrado para variables categóricas y test U de Mann-Whitney o test t para variables continuas de acuerdo con su distribución. Se realizó test de correlación de Pearson para las variables cuantitativas con el valor de hs-cTnT a las 6 horas posteriores al procedimiento.
Para determinar la influencia de variables independientes con la variable dependiente (cambio en la hs-cTnT) se utilizó un modelo lineal generalizado mixto. El modelo final se eligió de acuerdo con el mejor máximo likelihood fit y al menor score de criterio de información de Akaike.
Se utilizó el paquete estadístico SPSS 24.0 y se consideró un valor de p menor a 0.05 como estadísticamente significativo.
Resultados
Se incluyeron 106 pacientes, de sexo femenino 65 de ellos (61.3%). La mediana de edad fue 8 años (RIC: 11 años) y 22 pacientes (21%) fueron mayores de 18 años. Todos los pacientes presentaban cavidades cardiacas derechas dilatadas y la presión arterial pulmonar media fue 21.3 mmHg (± 5.8 mmHg). La hs-cTnT antes del procedimiento fue 3.7 pg/ml (RIC: 3 pg/ml) (Tabla 1).
Tabla 1 Características clínicas y anatómicas basales, así como propias del procedimiento, en los 106 pacientes incluidos
| Variable | Población |
|---|---|
| Edad - mediana (RIC), años | 8 (11) |
| Sexo femenino, n (%) | 65 (61.3) |
| Superficie área corporal - mediana (RIC), kg/m2 | 0.98 (0.94) |
| Presión arterial pulmonar media - media (DE), mmHg | 21.3 (5.8) |
| Diámetro máximo CIA - mediana (RIC), mm | 14 (8) |
| CIA única, n (%) | 85 (80.2) |
| Borde aórtico deficiente, n (%) | 41 (38.7) |
| Borde posterior fláccido, n (%) | 46 (43.4) |
| Medición CIA con balón, n (%) | 31 (29.2) |
| Diámetro cintura de dispositivo - mediana (RIC), mm | 18 (8) |
| Sobredimensionamiento de dispositivo, n (%) | 16 (15.1) |
| Deformación senos de Valsalva, n (%) | 15 (14.2) |
| Inestabilidad del dispositivo, n (%) | 9 (8.5) |
| Necesidad de reposicionamiento del dispositivo, n (%) | 26 (24.5) |
| Tiempo de fluoroscopia - mediana (RIC), minutos | 5.3 (3.8) |
CIA: comunicación interauricular; DE: desviación estándar; RIC: rango intercuartílico.
Durante el procedimiento, 85 pacientes (80.2%) tenían CIA única. El diámetro máximo del defecto fue 14 mm (RIC: 8 mm). Presentaban deficiencia de borde aórtico 41 pacientes (38.7%) y 46 casos (43.4%) mostraban borde posterior fláccido. En 31 pacientes (29.2%) se realizó medición con balón elastomérico. En todos los casos se implantó al menos un dispositivo y en dos pacientes (1.9%) se implantaron dos dispositivos. El diámetro de la cintura de los dispositivos implantados fue 18 mm (RIC: 8 mm).
En 16 casos (15.1%) el dispositivo fue sobredimensionado. En 15 casos (14.2%) hubo deformación de los senos de Valsalva ocasionada por interacción de algún disco del dispositivo. Previo a la liberación del oclusor, en nueve casos (8.5%) hubo prolapso de este y en 26 casos (24.5%) se debió reposicionar el dispositivo. El tiempo de fluoroscopia del procedimiento fue 5.3 minutos (RIC: 3.8 minutos).
Todos los pacientes tuvieron elevación de hs-cTnT después de la intervención. La mediana de tiempo entre la culminación del procedimiento y la medición de hs-cTnT de control fue 360 minutos (RIC: 12 minutos). La hs-cTnT a las 6 horas del procedimiento fue 72.5 pg/ml (RIC: 75.6 pg/ml), lo que corresponde a 5.1 veces (RIC: 5.4 veces) sobre el LRS. A todos los pacientes se les otorgó el alta médica a las 24 horas y ningún paciente tuvo complicaciones.
Los pacientes con deformación de los senos de Valsalva tuvieron mayor hs-cTnT a las 6 horas del procedimiento (117.3 vs. 67.6 pg/ml; p = 0.03), así como aquellos pacientes en los cuales fue necesario reposicionar el dispositivo (102.2 vs. 63.4 pg/ml; p < 0.01). En los casos con déficit de borde aórtico, la hs-cTnT a las 6 horas fue similar a aquellos pacientes con borde aórtico suficiente. Tampoco hubo diferencias en los casos de sobredimensionamiento del dispositivo (Tabla 2) (Fig. 2).
Tabla 2 Comparación de troponina T cardiaca de alta sensibilidad a las 6 horas de la culminación del procedimiento entre características anatómicas y del procedimiento presentes o ausentes en los 106 pacientes. Mediana y rango intercuartílico, en pg/ml
| Variable | n | Presente | n | Ausente | p |
|---|---|---|---|---|---|
| CIA única | 85 | 67.2 (74.3) | 21 | 82 (97.6) | 0.32 |
| Medición CIA con balón | 31 | 75.7 (85.5) | 75 | 67.2 (79.9) | 0.32 |
| Borde posterior fláccido | 46 | 79.5 (89) | 60 | 59.5 (77.7) | 0.06 |
| Sobredimensionamiento dispositivo | 16 | 67.1 (77.6) | 90 | 73.6 (76.2) | 0.97 |
| Borde aórtico deficiente | 41 | 74.5 (98.6) | 65 | 71.6 (70.6) | 0.48 |
| Deformación senos de Valsalva | 15 | 117.3 (99.1) | 91 | 67.6 (73.5) | 0.03 |
| Inestabilidad del dispositivo | 9 | 119.3 (208.8) | 97 | 69.8 (73.2) | 0.13 |
| Reposicionamiento de dispositivo | 26 | 102.2 (104.5) | 80 | 63.4 (63.7) | < 0.01 |
CIA: comunicación interauricular.
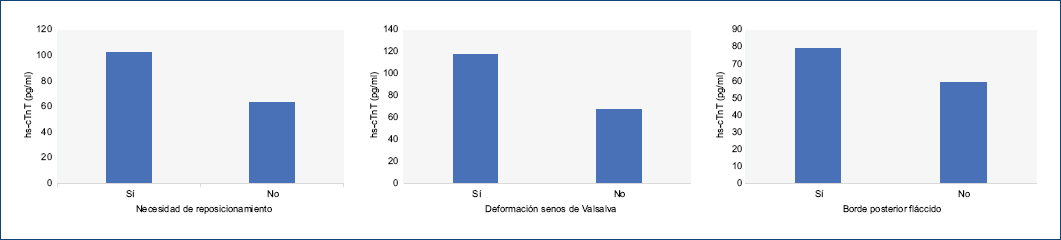
Figura 2 Gráfico de barras comparando mediana de hs-cTnT a las 6 horas del procedimiento entre variables categóricas. Necesidad de reposicionamiento del dispositivo 63.4 pg/ml vs. 102.2 pg/ml (p < 0.01) (izquierda). Deformación de senos de Valsalva 67.6 pg/ml vs. 117.3 pg/ml (p = 0.03) (centro). Borde posterior fláccido 59.5 pg/ml vs. 79.5 pg/ml (p = 0.06) (derecha). Test U de Mann-Whitney. hs-cTnT: troponina T cardiaca de alta sensibilidad.
La edad (r: –0.20), el peso (r: –0.25), el diámetro de la CIA (r: 0.17) y el tiempo de radioscopia (r: 0.34) se correlacionaron significativamente con el valor de hs-cTnT a las 6 horas de culminado el procedimiento (Tabla 3) (Fig. 3).
Tabla 3 Correlación entre variables cuantitativas y valor de troponina T cardiaca de alta sensibilidad a las 6 horas de culminado el procedimiento
| Variable | r | p |
|---|---|---|
| Edad | –0.20 | 0.03 |
| Peso | –0.25 | < 0.01 |
| PMAP | 0.15 | 0.11 |
| Diámetro CIA | 0.20 | 0.03 |
| Diámetro cintura de dispositivo | 0.17 | 0.07 |
| Tiempo de fluoroscopia | 0.34 | < 0.001 |
CIA: comunicación interauricular; PMAP: presión media de arteria pulmonar.
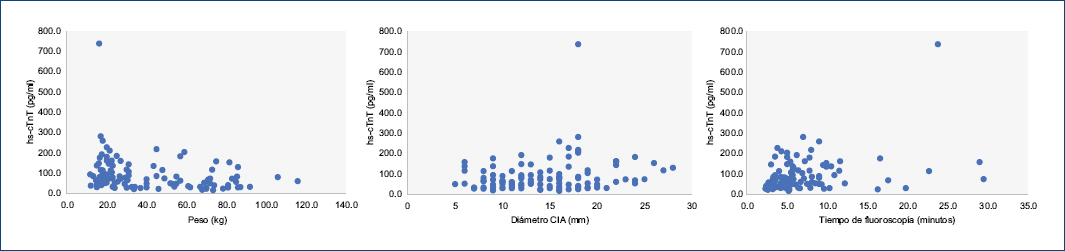
Figura 3 Gráfico de dispersión correlacionando valor de hs-cTnT y variables continuas. Correlación entre peso y hs-cTnT (r: –0.25; p < 0.01) (izquierda). Correlación entre diámetro de CIA y hs-cTnT (r: 0.20; p = 0.03) (centro). Correlación entre tiempo de fluoroscopia y hs-cTnT (r: 0.34; p < 0.001) (derecha). Test de correlación de Pearson. CIA: comunicación interauricular; hs-cTnT: troponina T cardiaca de alta sensibilidad.
Un modelo lineal mixto generalizado demostró una relación directa entre el cambio hs-cTnT y el diámetro de la CIA (β: 2.8; IC: 0.8 a 4.9; p < 0.01) y el tiempo de fluoroscopia (β: 2.7; IC: 0.6 a 4.7; p < 0.01) y una relación inversa entre el cambio de hs-cTnT y el peso (β: –0.7; IC: –1.1 a –0.3; p < 0.01) (Tabla 4).
Tabla 4 Análisis multivariante. Modelo lineal generalizado mixto teniendo en cuenta la variable dependiente cambio de troponina entre basal y a las 6 horas de culminado el procedimiento y las variables independientes
| Variable | β | IC95% | p |
|---|---|---|---|
| Deformación senos de Valsalva | 3.8 | –24.5 a 32.1 | 0.79 |
| Reposicionamiento de dispositivo | –12.1 | –36.3 a 11.9 | 0.32 |
| Borde posterior fláccido | –11.6 | –32.1 a 8.8 | 0.26 |
| Peso | –0.7 | –1.1 a –0.3 | < 0.01 |
| Diámetro CIA | 2.8 | 0.8 a 4.9 | < 0.01 |
| Tiempo de fluoroscopia | 2.7 | 0.6 a 4.7 | < 0.01 |
CIA: comunicación interauricular; IC95%: intervalo de confianza del 95%.
Discusión
El cierre percutáneo de un defecto interauricular tipo ostium secundum es la estrategia de elección por su alta eficacia y baja invasividad, aunque poco se conoce acerca del metabolismo de la troponina relacionado con este procedimiento. Nuestro estudio demostró que todos los pacientes sometidos a esta intervención tienen una elevación de hs-cTnT a las 6 horas de finalizado el procedimiento. El déficit de borde aórtico no se relacionó de forma independiente con esta elevación y el hallazgo sobresaliente fue que la variación de hs-cTnT se relacionó de forma directa con el diámetro del defecto y el tiempo de fluoroscopia y de forma inversa con el peso del paciente.
Ha sido reportado que entre el 40 y el 100% de los pacientes que requirieron tratamiento percutáneo de una CIA tipo ostium secundum presentan elevación de troponinas en las horas posteriores a la intervención6. La mayoría de las experiencias publicadas utilizaron troponina I o T de generaciones previas al kit de alta sensibilidad utilizado como referencia en la actualidad. En la práctica clínica se designa como alta sensibilidad a la capacidad de cuantificar el valor de troponinas por debajo del valor de personas sanas10. Es posible que el uso de kit de alta sensibilidad sea el motivo por el cual hallamos incremento de troponina en todos los casos.
En estudios previos se ha correlacionado la elevación de troponinas con el tamaño de dispositivo implantado o con el tamaño del defecto11-14. Otra experiencia ha correlacionado la elevación de troponinas con defectos complejos de tratar como aquellos defectos múltiples, con deficiencia de borde posterior o subrogantes de defectos complejos como prolongación del procedimiento15.
Actualmente es insuficientemente conocido el mecanismo por el cual se liberan troponinas por parte de las células musculares cardiacas en casos no relacionados con isquemia miocárdica o necrosis. Se ha descripto que otros mecanismos pueden estar implicados, como la muerte celular programada o la liberación del pool citosólico de troponinas secundario a la alteración de la membrana celular por daño mecánico16,17. Hipotetizamos que la elevación de troponinas en el contexto del cierre percutáneo de CIA podría ser secundario a un mecanismo similar a la alteración de la membrana. Otros procedimientos que involucran manipulación en las aurículas como la ablación debido a fibrilación auricular provocan también lesión miocárdica demostrada por biomarcadores18.
En el mismo sentido, es posible que defectos más complejos, como aquellos con déficit de bordes, defectos de mayor diámetro o necesidad de implantar dispositivos más grandes, requieran mayor manipulación y trauma por catéteres/dispositivos. De acuerdo con esta línea de razonamiento, Hlebowics et al. han sugerido que el trauma mecánico podría ser la explicación de la elevación de troponinas en el tratamiento percutáneo de CIA13. Una elevación de troponina I se ha observado en procedimientos pediátricos intervencionistas, mientras que no se ha detectado esa misma elevación en casos puramente diagnósticos. La ablación de arritmias mediante aplicación de radiofrecuencia causa mayor elevación que otras intervenciones19.
La mayoría de las erosiones de estructuras miocárdicas en relación con la oclusión percutánea de CIA, ocurren en las primeras 72 horas posteriores al implante de dispositivos. Un tercio de estas erosiones pueden tener un final fatal y los hallazgos de autopsia o cirugía de emergencia revelan perforaciones posiblemente causadas durante el cateterismo4.
Luego de la publicación del estudio pivote de Amin et al.4 se recomendó tener especial precaución en el caso de oclusión de defectos con déficit de borde aórtico o aquellos dispositivos con cintura mayor a 1.5 veces con respecto al defecto basal, recomendando un seguimiento estricto en estos casos. A pesar de que en general la presencia de erosiones se ha observado en pacientes con déficit de borde aórtico, los operadores no involucran al déficit de este borde como principal causa de la erosión20. El déficit de borde aórtico no se encuentra asociado a mayores eventos adversos cuando se compara con pacientes con bordes suficientes21. En línea con estos hallazgos, nuestra experiencia no evidenció cambios en la troponina luego del procedimiento en aquellos pacientes con déficit de borde aórtico, borde posterior fláccido o dispositivo sobredimensionado.
El presente estudio tiene limitaciones. Se llevó a cabo en un único centro y podrían existir sesgos de selección o de referencia. Sin embargo se evaluaron de forma consecutiva todos los pacientes con diagnóstico de CIA y menos del 10% de los pacientes tamizados no fueron incluidos. Así mismo, no se puede determinar si la elevación de troponina se relaciona con eventos adversos serios a mediano o largo plazo ya que para contestar ese interrogante sería necesario incluir un número mayor de pacientes y hacer un seguimiento más prolongado. Hasta el momento de la publicación y con un seguimiento disímil entre los pacientes incluidos (1 a 30 meses) no se han reportado eventos adversos serios. El dispositivo más utilizado fue el Nit Occlud ASD-R (pfm Medical, Alemania) y la mayor experiencia publicada en la literatura con respecto al cierre percutáneo, así como con complicaciones, ha sido con otros dispositivos, aunque el diseño y materiales componentes de los dispositivos utilizados son similares y no exentos de eventos adversos22. El equipo interviniente cuenta con experiencia previa en el uso del dispositivo, por lo que no creemos que se pueda relacionar el incremento de troponina con impericia en el implante de este23,24. La principal fortaleza del estudio es el uso de troponina de alta sensibilidad, la cual se recomienda en la actualidad, con un protocolo estricto de medición en el seguimiento y escasa variabilidad en el tiempo transcurrido entre la culminación del procedimiento y la medición de control. Existe evidencia de una variabilidad circadiana en la liberación de troponina25, sin embargo en nuestra experiencia todos los casos de extracción basal fueron durante la mañana y los de control en horas nocturnas. Al no existir una definición clara de lesión miocárdica posterior al tratamiento percutáneo de CIA consideramos que el uso de un modelo lineal generalizado mixto es el método estadístico multivariante adecuado para evaluar la variación en la hs-cTnT.
Finalmente, consideramos que el rol de la medición de hs-cTnT no parece ser necesaria como parte del seguimiento de los pacientes, ya que hasta el momento no ha demostrado estar relacionada con eventos adversos serios y no sería costo-efectivo su utilización sistemática. Por otro lado, pensamos que podría ser útil como forma de estudiar casos más complejos que demandan mayor manipulación durante el procedimiento y/o presentan factores de riesgo de erosión en donde el resultado del biomarcador podría funcionar como método de alerta adicional para un seguimiento más estricto.
Conclusión
Luego de transcurridas 6 horas del cierre percutáneo de una CIA, existe invariablemente una elevación de la hs-cTnT. La medición con balón elastomérico del defecto, la presencia de déficit de borde aórtico y/o un borde posterior fláccido y el sobredimensionamiento del dispositivo no se relacionaron con un incremento mayor de niveles de hs-cTnT. El diámetro de la CIA y el tiempo de fluoroscopia, así como el peso del paciente, se relacionan con la variación en los niveles de hs-cTnT en el seguimiento.











 nova página do texto(beta)
nova página do texto(beta)