Introducción
La Organización Mundial de la Salud (OMS) define a las reacciones adversas a medicamentos (RAM) como aquellas nocivas, no intencionadas y originadas a dosis habituales para la profilaxis, diagnóstico o tratamiento médico, independientemente del órgano afectado o el método de administración1-3. Las reacciones adversas cutáneas a medicamentos o farmacodermias constituyen la forma más común de las RAM3. Se definen como cualquier cambio indeseable en la estructura o función de la piel, sus apéndices o membranas mucosas3.
En la patogenia de las farmacodermias se involucran mecanismos inmunológicos y no inmunológicos. Los primeros ocurren como resultado de una reacción de hipersensibilidad (HS), principalmente tipo I mediada por IgE, y por la tipo IV mediada por linfocitos T4. Entre los mecanismos no inmunológicos se encuentran aquellos farmacológicos-tóxicos, comúnmente dependientes de la dosis y/o del tiempo5. Las reacciones cutáneas adversas a medicamentos pueden simular otras enfermedades de la piel, representando un problema de salud pública al ser subdiagnosticadas6. En el mundo, del 2 al 3% de estas dermatosis requieren hospitalización y se estima que 1 de cada 1,000 pacientes hospitalizados en el mundo tiene una farmacodermia grave, como el síndrome de Stevens-Johnson (SSJ), necrólisis epidérmica tóxica (NET), pustulosis exantemática aguda generalizada (PEAG) y el síndrome de hipersensibilidad a fármacos (SHF)7. Los pacientes con polifarmacia son los más susceptibles a desarrollar dichas entidades, ocurriendo en entre el 1 y el 3% de los pacientes multimedicados8.
En México se realizó un estudio en el año 2006 en el Instituto Nacional de Ciencias Médicas y Nutrición Salvador Zubirán (INCMNSZ) en la Ciudad de México, que reportó una prevalencia de farmacodermias en pacientes hospitalizados del 0.7% y una tasa de mortalidad del 16.6% en aquellos con reacciones mucocutáneas graves. Reportaron un predominio en pacientes inmunosuprimidos y mayor riesgo en aquellos con diagnóstico previo de lupus eritematoso sistémico (LES)9.
En el año 2011, Hernández-Salazar et al. reportaron una prevalencia del 0.6% de las reacciones cutáneas adversas a fármacos en el Departamento de Dermatología del Hospital General Dr. Manuel Gea González, también en la Ciudad de México, con predominio en mujeres (65.1%), al igual que el reporte de Chávez-Lemus del 2014 en el Centro Médico Nacional de Occidente del Instituto Mexicano del Seguro Social (IMSS) en Guadalajara, Jalisco. Los fármacos responsables del primer informe fueron la trimetoprima con sulfametoxazol (12.3%), piroxicam (10.7%), carbamazepina (7.6%), y las dermatosis comúnmente encontradas, fueron los exantemas morbiliformes (25%), eritema pigmentado fijo (16%) y fotosensibilidad (16%), con comorbilidades tipo hipertensión arterial sistémica (28.5%) y diabetes mellitus tipo 2 (12.5%) sin reportar ningún deceso10,11. En este último estudio se informó que el 34.4% de los pacientes hospitalizados a cargo del departamento de dermatología en el periodo de ocho años, presentó una farmacodermia y se reportó que la reacción más prevalente fue el síndrome de Brocq-Lyell o NET (32%), seguida del SSJ (14%), con una tasa de mortalidad del 24%, por ser farmacodermias graves. Dentro de las comorbilidades reportadas, destacaron la epilepsia (16.1%) y la diabetes mellitus (15%)11.
A partir de un estudio epidemiológico del año 2021 en un hospital privado en el país, Moreno-López et al. reportaron que las farmacodermias representaron el 0.67% de la consulta dermatológica general y el 2.9% de las interconsultas en pacientes hospitalizados. En este mismo estudio, la prevalencia reportada fue de 5.28 por cada 1,000 pacientes hospitalizados, con predominio en el sexo femenino (65%) y una edad promedio de 49 años, siendo las cefalosporinas y las fluoroquinolonas los medicamentos mayormente asociados, seguidos por ranitidina, paracetamol y omeprazol12. En población pediátrica, Hernández-Rosales et al. encontraron que la prevalencia de las farmacodermias en un hospital de tercer nivel en México fue el 1.7% de las consultas dermatológicas, la mayoría relacionadas con las penicilinas y sulfonamidas, siendo el sexo masculino el más afectado en este grupo etario9.
En los últimos años se ha incrementado la prevalencia de las farmacodermias debido a la polifarmacia, autoprescripción, la complejidad química de los medicamentos y la incorporación de otros a la industria. En este trabajo nos centramos en la prevalencia de las farmacodermias en los pacientes de la consulta externa y hospitalizados interconsultados al Departamento de Dermatología en el Instituto Nacional de Cardiología Ignacio Chávez (INCICh), con la intención de conocer los medicamentos causales más frecuentes en esta población de pacientes bajo polifarmacia de uso frecuente y estar alerta a las reacciones potenciales.
Como hemos comentado, la población de pacientes estudiada en el INCICh fue de alto riesgo debido a que una gran proporción contaba con polifarmacia. Definir el fármaco causal siempre es un reto en estos casos, sin embargo los grupos farmacológicos frecuentemente asociados fueron los esteroides, antipalúdicos y antiarrítmicos.
Objetivo
Establecer la frecuencia de reacciones adversas asociadas a medicamentos que afectan a la piel y las mucosas e identificar el fármaco causal en pacientes de la consulta externa y hospitalizados interconsultados al Departamento de Dermatología en el INCICh en la Ciudad de México en un periodo de 10 años.
Método
Estudio observacional, descriptivo, retrospectivo y transversal, en el que se incluyeron a todos los expedientes de pacientes de la consulta externa y hospitalizados interconsultados al Departamento de Dermatología en el INCICh, de cualquier edad y sexo, que presentaron efectos adversos o sospecha de reacción a fármacos con manifestaciones cutáneas o mucocutáneas en el periodo del 1 de enero de 2012 al 31 de diciembre de 2022.
Se obtuvo información de los pacientes desde los expedientes electrónicos y una base de datos con registro de las consultas por dermatología en el INCICh, seleccionando a los que presentaron sospecha o diagnóstico clínico y/o histológico de alguna reacción cutánea o mucocutánea medicamentosa. Las biopsias de piel se realizaron en los pacientes con diagnóstico clínico sospechoso de farmacodermia u otros diagnósticos diferenciales. Se realizó una base de datos con el programa de hojas de cálculo de Google, incluyendo el número de registro, sexo, edad, comorbilidades, fármacos administrados y un estudio histopatológico. Los criterios de inclusión fueron expedientes de pacientes con lesiones cutáneas o mucocutáneas compatibles con reacción a fármacos de cualquier edad y sexo, y pacientes ambulatorios de la consulta externa de dermatología e interconsultados de cualquier servicio del INCICh en el periodo del 1 de enero de 2012 al 31 de diciembre de 2022. Se excluyeron los expedientes de pacientes con diagnóstico diferente al de farmacodermia y se eliminaron expedientes a los que no se pudo acceder para la recolección de datos, expedientes clínicos incompletos y expedientes con diagnóstico indefinido o no concluyente. Se utilizó estadística descriptiva para el análisis de datos. Al ser este un estudio transversal, no se establecieron criterios de seguimiento y sus resultados.
Resultados
Desde el periodo del 1 de enero del 2012 al 31 de diciembre del 2022, con un total de 2,072 consultas correspondientes a 1,290 pacientes, se seleccionaron 96 expedientes con diagnóstico de RAM o farmacodermia, de los cuales se excluyeron 35; de estos, se eliminaron seis por imposibilidad de acceso al expediente clínico, nueve por expediente clínico incompleto y 20 por diagnóstico indefinido o no concluyente.
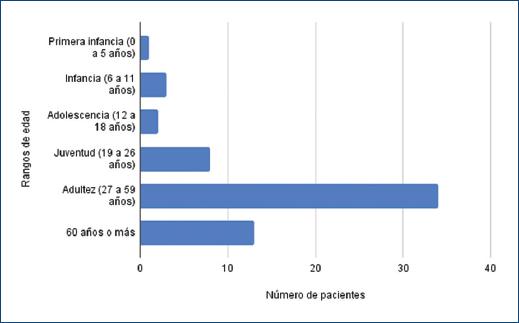
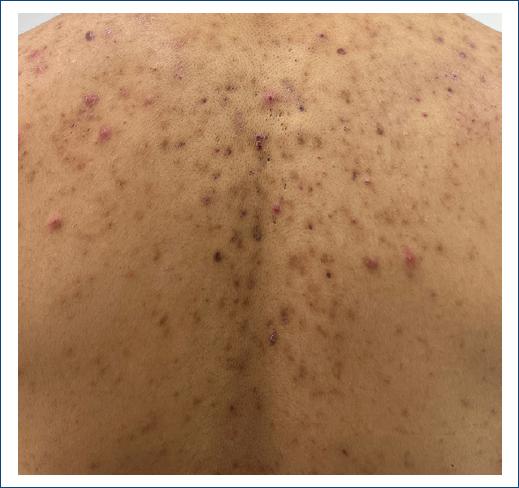
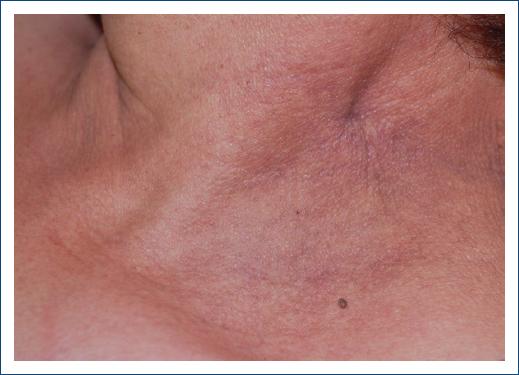
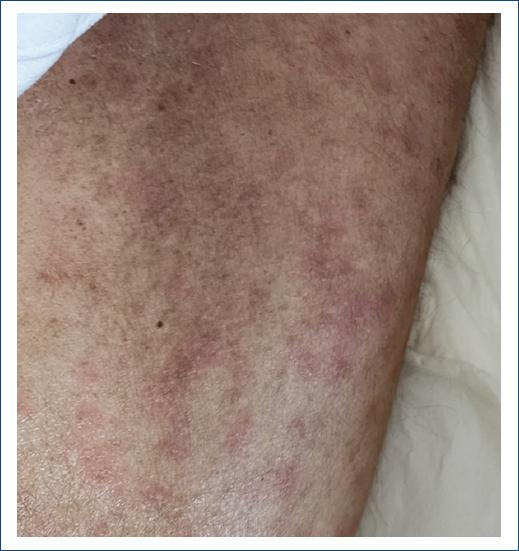
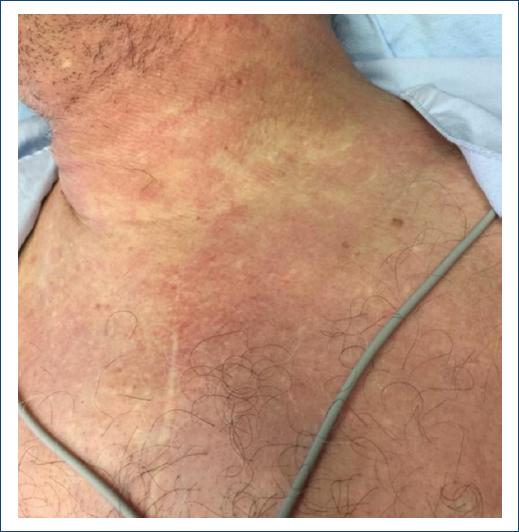
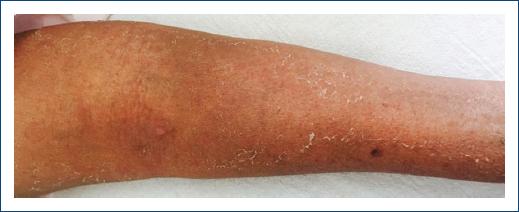
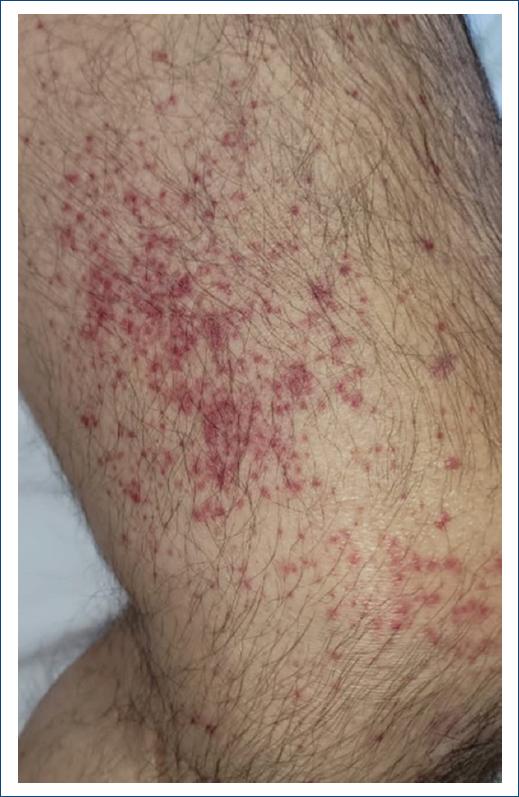
Finalmente, se incluyeron 61 expedientes de pacientes, 35 de estos fueron mujeres (57.37%) y 26 hombres (42.62%). El grupo de edad más afectado fue la adultez (27-59 años); los niños y adolescentes representaron el 9.83% del total de los expedientes de pacientes, la infancia (6-11 años) representó el 6.55% y la adolescencia (12-18 años) el 2.27%. La edad promedio global fue de 41.8 años (Figs. 1 y 2). El diagnóstico clínico se confirmó con estudio histopatológico en 12 pacientes. La farmacodermia más frecuente fue la dermatitis acneiforme (Figs. 2 y 3), diagnosticada a 17 pacientes (27.86%) seguida de la hiperpigmentación medicamentosa (Figs. 2 y 4) con siete pacientes y exantema súbito maculopapular (Fig. 5) con seis pacientes (9.83%). Los principales fármacos asociados a estos padecimientos fueron los esteroides, los asociados en polifarmacia, los antibióticos, los antipalúdicos de uso reumatológico, complejo B y los antiarrítmicos. Los 13 pacientes con polifarmacia (22.4%) se encontraban en tratamiento principalmente con antiinflamatorios no esteroideos (AINE), antihipertensivos, anticoagulantes, hipoglucemiantes y estatinas (Tabla 1), y las reacciones asociadas fueron eritema fijo pigmentado (EFP), reacciones urticariforme (Fig. 6) y maculopapular, eritema multiforme, eritrodermia (Fig. 7), vasculitis leucocitoclástica (Fig. 8) y NET. De los seis pacientes pediátricos (9.83%), el sexo más afectado fue el masculino (66.66%), con edad promedio de 9.33 años, la farmacodermia más frecuente fue el EFP diagnosticado en dos de ellos (33.33%) y un caso respectivamente de pustulosis exantemática aguda generalizada (PEAG), eritema multiforme, reacción de tipo urticariforme y eritematoescamosa. Los medicamentos mayormente asociados en la infancia (0-5 y 6-11 años) fueron el ácido acetilsalicílico y la cefalotina; durante la adolescencia (12-18 años) se asociaron la espironolactona y concentrados plaquetarios (Fig. 1).
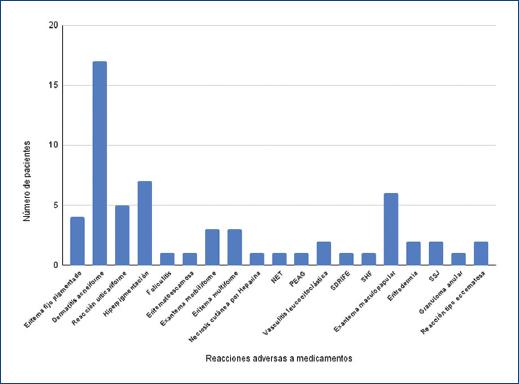
Figura 2 Número de pacientes por farmacodermia. NET: necrólisis epidérmica tóxica; PEAG: pustulosis exantemática aguda generalizada; SDRIFE: exantema intertriginoso y flexural simétrico por fármacos; SHF: síndrome de hipersensibilidad a fármacos; SSJ: síndrome de Stevens-Johnson.
Tabla 1 Medicamentos asociados a las farmacodermias
| Farmacodermias | Medicamentos asociados |
|---|---|
| Dermatitis acneiforme M:13 H:4 | Prednisona, furosemida, levonorgestrel/etinilestradiol, complejo B, clobetasol, betametasona tópica |
| Hiperpigmentación M:7 H:0 | Hidroxicloroquina, amiodarona |
| Exantema maculopapular M:3 H:3 | Polifarmacia, teicoplanina, levofloxacino, amiodarona |
| Reacción urticariforme M:1 H:4 | Polifarmacia, sulfonamidas, quinidina |
| Exantema fijo pigmentado M:2 H:2 | Polifarmacia, espironolactona, AAS |
| Exantema morbiliforme M:1 H:2 | Carbapenémicos, enoxaparina |
| Eritema multiforme M:2 H:1 | Sulfonamidas, polifarmacia, concentrado plaquetario, |
| Eritrodermia M:1 H:1 | Polifarmacia, anfotericina B |
| Síndrome de Stevens-Johnson M:1 H:1 | Difenilhidantoína, sulfasalazina |
| Vasculitis leucocitoclástica M:1 H:1 | Polifarmacia, betametasona IM |
| Reacción tipo eccematosa M:0 H:2 | Polifarmacia, alopurinol |
| Pustulosis exantemática aguda generalizada M:0 H:1 | Cefalotina |
| Exantema intertriginoso y flexural simétrico por fármacos M:0 H:1 | Vancomicina |
| Síndrome de hipersensibilidad a fármacos M:1 H:0 | Alopurinol |
| Reacción eritematoescamosa M:0 H:1 | Cefalotina |
| Necrólisis epidérmica tóxica M:0 H:1 | Polifarmacia |
| Granuloma anular M:1 H:0 | Metotrexato |
| Foliculitis M:0 H:1 | Prednisona |
| Necrosis cutánea M:1 H:0 | Heparina |
Para considerar a un paciente bajo polifarmacia se tomó como referencia la definición de la Organización Mundial de la Salud: uso de cuatro o más fármacos simultáneamente de diferentes grupos. En polifarmacia, los grupos farmacológicos fueron los antiagregantes plaquetarios, anticoagulantes, carbapenémicos, betabloqueadores, inhibidores de la enzima convertidora de angiotensina, estatinas, bloqueadores de canales de calcio, antihistamínicos, glucósidos cardiacos, nitratos, corticosteroides, diuréticos de asa, antagonistas de receptor H2, inhibidores de la bomba de protones, inhibidores selectivos de la recaptación de serotonina, hormonas, antagonistas de receptores adrenérgicos, antibióticos polipeptídicos, hipoglucemiantes orales, antipalúdicos de uso reumatológico, insulinas, analgésicos y antiarrítmicos.
Se analizaron las comorbilidades en los pacientes del INCICh, encontrando el LES como la más frecuente afectando a ocho pacientes (13.11%), seguida de cardiopatía isquémica en siete pacientes (11.47%), hipotiroidismo y dislipidemia cada uno con seis pacientes (9.83%), enfermedad renal crónica (ERC), diabetes mellitus tipo 2 e hipertensión arterial sistémica (HAS), cada una con cinco pacientes (8.19%).
También se evaluó la gravedad de la dermatosis tomando en cuenta el riesgo-beneficio respecto a la suspensión del medicamento asociado. En la mayoría de los pacientes se tomó la decisión de continuar con el tratamiento por ser indispensable para sus comorbilidades. En quienes se identificó el fármaco causal, este fue suspendido y sustituido, en su caso, por otro. En todos los casos se indicaron medidas generales del cuidado de la piel y en los necesarios se emplearon antihistamínicos o esteroides tópicos y/o sistémicos.
Discusión
Las farmacodermias son erupciones en la piel debido a drogas o medicamentos2. Algunas causan daños menores y aproximadamente el 2% ponen en riesgo la vida7.
De acuerdo con la literatura, los antibióticos, AINE, anticonvulsivos, antihipertensivos, agentes biológicos y quimioterapéuticos son los principales responsables13, sin dejar de considerar que un fármaco puede producir diferentes manifestaciones cutáneas adversas. En este estudio, fueron los esteroides, los antibióticos, los antipalúdicos de uso reumatológico, los antiarrítmicos y el complejo B los principales causantes.
De acuerdo con la clasificación de Gell y Coombs, los fármacos tienen la capacidad de inducir los cuatro tipos de reacciones inmunitarias, en las que los metabolitos actúan como haptenos a través de uniones covalentes a péptidos, modificándolos para convertirse en inmunogénicos para la inducción de una respuesta inmunitaria celular o humoral4.
La HS tipo I o mediada por inmunoglobulina (Ig) E se manifiesta con urticaria y angioedema. En las reacciones tipo II, los anticuerpos IgG o IgM interactúan con los antígenos en la membrana celular causando daño de esta con manifestaciones de tipo ampollosas. Las reacciones tipo III (causadas con frecuencia por antibióticos) son mediadas por inmunocomplejos, los cuales se depositan en el tejido causando daños como vasculitis y exantema. Por último, en las reacciones de tipo IV intervienen los linfocitos Th1 y Th2 activados manifestándose como una reacción tardía (como el exantema maculopapular, reacciones liquenoides, EFP, SJJ y NET)4.
Los mecanismos no inmunitarios son resultado de factores como toxicidad acumulativa, sobredosis, interacciones fármaco-fármaco, fototoxicidad y alteraciones metabólicas, sin dejar de considerar las reacciones de idiosincrasia5.
Tras la ingestión del fármaco asociado, las erupciones cutáneas pueden aparecer en horas (p. ej., urticaria y angioedema, reacciones de fotosensibilidad, PEAG, EFP, exantema intertriginoso y flexural simétrico relacionado con medicamentos [SDRIFE]), días (como las maculopapulosas, exantemáticas, exfoliativas, las vasculitis, la necrosis cutánea inducida por anticoagulantes, eritema multiforme, SSJ y NET), semanas o meses (como el SHF, las dermatitis acneiformes, granuloma anular y las pigmentaciones cutáneas) o en años, lo que dificulta establecer la relación causa-efecto y el diagnóstico14-27. En las reacciones de HS tipo I, después de la administración oral del fármaco, las manifestaciones cutáneas tienen una latencia de hasta 2 horas, sin embargo, en la administración parenteral su aparición es inmediata. El cuadro clínico se puede presentar o exacerbar de días a semanas después de su administración5.
Las manifestaciones en la HS tipo IV pueden iniciar tras 1 a 4 semanas de la ingesta o aplicación del fármaco. En la fase inicial existe un incremento en la expresión de marcadores de activación CD69, CD29, DR y antígeno cutáneo linfocitario de la piel en los linfocitos T de la sangre periférica4,28,29. Por métodos de inmunohistoquímica se ha estudiado el perfil de citocinas expresado durante los primeros días de estas reacciones y se ha determinado que la perforina, el factor de necrosis tumoral alfa (TNF-α) y la granzima B muestran una correlación positiva con la gravedad del padecimiento. En casos más complicados, a este grupo de citocinas se le agrega la expresión de Fas-L (CD95L)7.
Dentro de los factores de riesgo implicados para desarrollar una reacción cutánea adversa a fármacos se encuentran el sexo femenino, infecciones virales (virus de la inmunodeficiencia humana [VIH], virus de Epstein-Barr, citomegalovirus y herpes virus 6 y 7), fotoexposición, enfermedades renales, hepáticas o autoinmunes, neoplásicas, predisposición inmunogenética específica, metabolismo alterado de los fármacos, edad pediátrica debido a la alta frecuencia de automedicación y la edad geriátrica por las comorbilidades en este grupo etario y la polifarmacia asociada. Se han determinado como factores de riesgo para el síndrome de hipersensibilidad con eosinofilia y síntomas sistémicos (DRESS, o SHF), la combinación de la superficie corporal total afectada > 35%, con la cuenta de eosinófilos > 6% y con los niveles de la proteína C reactiva de alta sensibilidad > 5 mg/l30,31. De la misma manera, como los niveles de elafina (que puede elevarse en respuesta a la degradación tisular por los infiltrados neutrofílicos y en respuesta a interleucina [IL] 1 y TNF-α), IL-6 y TNF-α persistentemente elevados a los seis meses de la consulta dermatológica para pacientes oncológicos con erupciones morbiliformes que murieron en comparación con aquellos que permanecían vivos en el mismo periodo de tiempo. En el mismo estudio, la IL-6 y la IL-10 se asociaron con compromiso sistémico31. A pesar de que la atopia no se considera un factor de riesgo, se relaciona con un cuadro más grave. Respecto al fármaco, la dosis y su administración intermitente o prolongada son factores que favorecen la sensibilización a este2,29.
En este reporte el sexo femenino fue el más afectado, representando al 57.4% de los casos encontrados, lo cual concuerda con la literatura32,33. Una de las teorías que explican este predominio es la interrelación entre los sistemas endócrino e inmunitario debido al efecto hormonal dado por los estrógenos, los cuales favorecen la presentación antigénica al aumentar la expresión de moléculas del complejo mayor de histocompatibilidad. Otro efecto de estas hormonas es la liberación de IL-4, IL-13 e IL-15, las cuales polarizan a las células T hacia un perfil Th2, dando paso a la producción de IgE29.
En cuanto a la edad, en los casos descritos en el INCICh encontramos un predominio en la adultez (27 a 59 años), lo que coincide con los resultados de otros estudios, que reportan un promedio de 49 años12. En una serie de 51 pacientes con reacciones cutáneas adversas graves en un hospital de tercer nivel en Jamaica, las décadas más afectadas fueron la cuarta, la quinta y la sexta33. Si bien la adultez no representa por sí misma un grupo etario de riesgo, en nuestro estudio la mayor parte de la muestra eran adultos, factor que pudo influir en los resultados obtenidos.
En un estudio realizado a nivel mundial en niños y adolescentes la prevalencia se reportó en hasta del 10.9% de pacientes hospitalizados y del 1.5% en pacientes ambulatorios34, mientras que la prevalencia en el INCICh en estas edades fue del 9.83% de la muestra.
Dentro de la población estudiada, el 21.31% representó a los pacientes polimedicados, cuyo fármaco causal no pudo precisarse. A pesar de que las normas de tratamiento incluyen como primer paso la suspensión del medicamento del que se sospecha, esta medida podría ser riesgosa para estos pacientes, ya que cada uno puede ser imprescindible para el control de sus comorbilidades32.
En el estudio realizado en el INCMNSZ por Hernández-Salazar et al. se observó que las comorbilidades más frecuentemente relacionadas con las farmacodermias fueron el LES (14.6%), la infección por VIH (7.3%) y el linfoma no Hodgkin (7.3%)9. Al compararlos con nuestros resultados el LES continuó siendo la comorbilidad más frecuente (13.11%). En menor medida reportamos otros padecimientos como cardiopatía isquémica (11.47%), hipotiroidismo (9.83%), dislipidemia (9.83%), ERC (8.19%), HAS (8.19%) y diabetes tipo 2 (8.19%), lo que se explica por el tipo de pacientes que concentra cada instituto.
En este estudio las farmacodermias más frecuentes fueron la dermatitis acneiforme (27.86%), hiperpigmentación medicamentosa (11.47%) y el exantema maculopapular (9.83%). El predominio de la dermatitis acneiforme lo atribuimos a que un gran número de pacientes es referido por el servicio de reumatología y generalmente se encuentran en tratamiento con prednisona u otros esteroides, los cuales resultaron ser los principales causantes de esta farmacodermia. Otros medicamentos responsables fueron el complejo B, la furosemida y el levonorgestrel con etinilestradiol. Por otro lado, el caso del SDRIFE se asoció a vancomicina, hecho que no encontramos reportado previamente en la literatura.
En otras poblaciones, como la francesa, los tipos de reacciones más habituales contrastan con nuestros resultados, puesto que en estas las farmacodermias reportadas con mayor frecuencia son las exantemáticas (57%) y la eritrodermia (8%), en las que los fármacos implicados fueron los de uso cardiovascular y los AINE33-36. En el reporte de McNish et al., las reacciones más graves (SSJ, NET, sobreposición de SSJ/NET y SHF) se relacionaron con antibióticos y anticonvulsivantes33.
Para el manejo inicial se debe realizar una historia clínica completa indagando sobre otros antecedentes de HS y medicamentos utilizados; deben considerarse la fecha de inicio, dosis, tiempo de vida media del fármaco y duración del tratamiento. No se debe dejar de lado el uso de suplementos, productos de medicina alternativa o de los considerados como «naturistas». Una vez identificado el agente causal, se deberá averiguar la fecha de inicio de su administración y el tiempo de aparición de la dermatosis3,5.
El objetivo es identificar el fármaco causal y retirarlo, con excepción de los casos en los que este sea imprescindible para el tratamiento de las comorbilidades, monitorizando la evolución de la farmacodermia1. En caso de que se sospeche una reacción grave como SSJ, NET, SHF o PEAG se recomienda realizar una evaluación general en busca de daño o compromiso a otros órganos por medio de estudios de laboratorio que nos permitan identificar eosinofilia periférica, y monitorizar urea, electrolitos séricos, pruebas de función hepática y pruebas de coagulación, así como descartar causas infecciosas35.
La biopsia cutánea será de utilidad para la identificación de ciertos hallazgos histopatológicos que apoyen los diagnósticos. En las reacciones cutáneas adversas a medicamentos se han identificado diversos cambios histológicos, entre los que se encuentran múltiples focos de inflamación y superposición de patrones (patrón inflamatorio perivascular, espongiótico, psoriasiforme, fibrosante, granulomatoso, vasculítico y tipo paniculitis). Asimismo, las células características encontradas en la epidermis y la dermis corresponden a los eosinófilos, mientras que los neutrófilos se ubican en la luz de capilares dérmicos con ectasia. Como hallazgos adicionales se incluyen la vacuolización basal, queratinocitos apoptósicos en la epidermis, daño vascular que resulta en la extravasación de eritrocitos y edema dérmico papilar. En caso de que el daño sea prolongado se podría alterar la maduración de los queratinocitos15.
Entre los cambios correspondientes a NET generalmente se encuentran células necróticas que darán lugar a necrosis epidérmica y separación de la epidermis de la capa subepidérmica, espongiosis y vacuolización de células basales, así como una escasa infiltración de células mononucleares en la dermis. En el caso de SHF lo más característico es la presencia de eosinofilia y aunque la histopatología no representa un dato de alta fiabilidad, se puede acompañar de linfocitos atípicos en el frotis de sangre periférica e infiltrado en la dermis. Los cambios presentados con la PEAG incluyen neutrofilia y leucocitosis, acompañada de pústulas subcórneas, edema e infiltrado polimorfo perivascular. La necrosis fibrinoide, polvo nuclear y el infiltrado neutrofílico perivascular e intravascular corresponden a los hallazgos histológicos que pueden identificarse en vasculitis.
Además de la histopatología, existen pruebas diagnósticas de utilidad tales como el ensayo de toxicidad de linfocitos (p. ej., para SHF), pruebas de parche (para PEAG), inmunofluorescencia (depósitos de IgM, C3 y fibrina en vasculitis), así como detección de anticuerpos anticitoplasmáticos, anticuerpos anticardiolipina, anticuerpos antinucleares y anticuerpos antihistona, que son apoyo para el diagnóstico7,29.
A lo largo de los años se han hecho asociaciones entre diferentes polimorfismos del antígeno leucocitario humano (HLA) y la predisposición a presentar una farmacodermia, entre los que destacan HLA-B*1502 para SSJ/NET, HLA-B*58:01 para SHF, HLA-A30, B13 y Cw6 para EFP y HLA-DQB1*0301 asociado a eritema multiforme14,29,36-38.
Se ha llevado este conocimiento a la práctica realizando pruebas genéticas con el objetivo de identificar individuos portadores de HLA de riesgo. Se realizó un estudio en pacientes con VIH para demostrar la utilidad de estas pruebas antes de iniciar un tratamiento con abacavir con la finalidad de prevenir reacciones cutáneas graves. Sin embargo, este estudio se calificó de calidad moderada, por lo que serían necesarios más ensayos clínicos que aporten evidencia suficiente para justificar la realización de estos exámenes como tamizaje36.
Como se ha mencionado, las farmacodermias se consideran simuladoras de otras enfermedades de la piel, por lo que durante su abordaje se deben tomar en cuenta otros diagnósticos dependiendo de la entidad sospechada. Por ejemplo, en el caso de PEAG se deberá descartar psoriasis pustular (psoriasis de von Zumbusch), pustulosis subcórnea (enfermedad de Sneddon-Wilkinson), foliculitis infecciosa, exantema viral con pústulas secundarias, síndrome de Sweet o dermatosis subcórnea por IgA29. Cuando se sospeche de SSJ, este deberá diferenciarse de eritema fijo generalizado con ampollas. Por otra parte, con la NET deberán considerarse la enfermedad injerto contra huésped y el síndrome de piel escaldada asociado a Staphylococcus aureus. Tomando en cuenta que este padecimiento puede acompañarse de xerostomía residual o queratoconjuntivitis, el síndrome de Sjögren será otro diagnóstico diferencial que considerar5. Los linfomas y pseudolinfomas, el síndrome de hipereosinofilia, el LES, la infección por micoplasma y los exantemas virales (hepatitis viral y mononucleosis infecciosa) son padecimientos que descartar para el diagnóstico de SHF37.
Como parte del tratamiento, se evalúa la gravedad de las lesiones. Si se opta por continuar la administración del fármaco, se indican antihistamínicos y esteroides tópicos o sistémicos5.
En las reacciones graves, el tratamiento se basa en tres puntos: a) retiro del fármaco en cuestión; b) terapia de soporte, y c) tratamiento específico. La terapia de soporte consiste en utilizar apósitos que prevengan el traumatismo de la piel (gasas con petrolato o nitrato de plata), que conserven la humedad y que favorezcan el proceso de reepitelización. Asimismo, se recomienda el uso de un antibiótico tópico. En conjunto con estas medidas se deberá controlar el dolor, prevenir infecciones e hipotermia, así como tener un monitoreo nutricional como parte del síndrome de insuficiencia cutánea aguda, si se presentara. El tratamiento específico consiste en la administración de corticosteroides, inmunosupresores, ciclosporina e Ig intravenosa según se requiera6,35.
Actualmente las estrategias terapéuticas están evolucionando al uso de biológicos y moléculas anti-TNF, diferentes citocinas o aquellas moléculas que actúan en las vías de señalización de las cinasas Janus, considerando las características individuales de cada paciente38.
Conclusiones
El enfoque de esta investigación fue determinar la frecuencia y los principales fármacos involucrados en las farmacodermias en el INCICh en la Ciudad de México, obteniendo resultados semejantes a la información reportada en la literatura de los estudios realizados en diferentes instituciones hospitalarias públicas y privadas en el país e internacionales, mencionados a lo largo del presente artículo. Una de las limitaciones de esta investigación es que, al tratarse de un estudio retrospectivo y transversal, no se establecieron criterios de seguimiento ni sus resultados. Por supuesto también limitaron el estudio los datos incompletos en los expedientes. Por otro lado, los resultados obtenidos no se pueden generalizar.
Es importante el desarrollo de habilidades que permitan identificar de manera temprana la presentación clínica de las farmacodermias con la finalidad de proporcionar el tratamiento adecuado.
Insistimos también en la importancia que tienen las notificaciones de sospechas de reacciones adversas a medicamentos a los programas permanentes de farmacovigilancia de la Comisión Federal para la Protección contra Riesgos Sanitarios (COFEPRIS).











 nova página do texto(beta)
nova página do texto(beta)