Introducción
La COVID-19, causada por el SARS-CoV-2, ha supuesto un desafío crítico para la salud pública y la comunidad médica en todo el mundo. Debido a su rápida propagación y la falta de preparación contra enfermedades causadas por patógenos emergentes, se ha convertido en la segunda pandemia del siglo xxi, acumulando 760,360,956 casos confirmados hasta el 16 de marzo de 2022, con 6,873,477 fallecimientos1. En México, el Sistema Nacional de Vigilancia Epidemiológica (SINAVE) notificó el primer caso de SARS-CoV-2 en febrero de 2020, lo que condujo a la implementación de nuevas directrices sanitarias para la población2.
En abril de 2020, la Secretaría de Salud de México estableció lineamientos para la reconversión hospitalaria COVID-19, con el objetivo de asegurar el acceso oportuno y la calidad de la atención para los pacientes con esta enfermedad. Durante ese mismo mes, el Instituto Nacional de Cardiología Ignacio Chávez (INC) orientó su atención médica hacia pacientes con COVID-19 debido a la demanda sobrecargada de hospitales en medio de la emergencia internacional2,3. El INC se reestructuró en función de la gravedad de los casos clínicos, habilitando la terapia intensiva cardiovascular para los casos más graves de COVID-19, mientras que en el Octavo Piso de Cardiología Adultos se organizó una terapia intermedia para pacientes con COVID-19 moderada a leve, sin requerimiento de soporte ventilatorio invasivo4.
La necesidad de personal de salud para enfrentar los estragos de la pandemia llevó a la implementación de nuevas políticas sanitarias, que incluyeron medidas preventivas tanto para pacientes cardiacos que buscaban atención inmediata como para aquellos que dejaron de asistir por temor al contagio, lo que empeoró sus patologías de base. La prolongación de la pandemia hizo que la mayoría de los hospitales se centraran exclusivamente en atender a pacientes con COVID-19, descuidando otras patologías y sus complicaciones. Sin embargo, en noviembre de 2021, debido al empeoramiento de los padecimientos cardiovasculares, el INC retomó la atención integral de los pacientes cardiacos. A partir de ese momento, los pacientes con COVID-19 y enfermedad cardiaca fueron ubicados en el Octavo Piso de Hospitalización, convirtiéndose en el único sector destinado a estos pacientes. El impacto positivo generado por la inmunización contra la COVID-19 proporcionó una mayor seguridad a los enfermos y tranquilidad a los médicos, convirtiendo a los pacientes con COVID-19 en hallazgos incidentales5,6.
Conforme se fueron atendiendo más pacientes con COVID-19 se observó que los que padecían alguna enfermedad cardiovascular presentaban más complicaciones, como elevación de troponinas, miocardiopatías, mal pronóstico y hasta muerte7,8.
El objetivo de este reporte de casos es describir el curso clínico de la infección por SARS-CoV-2 en pacientes con enfermedad cardiaca preexistente a partir de la experiencia con 17 casos hospitalizados en el INC durante la cuarta ola de COVID-19 en 2022.
Método
Estudio de serie de casos de pacientes adultos con diagnóstico confirmado de COVID-19 mediante prueba de reacción en cadena de la polimerasa (PCR) o prueba de antígenos, con antecedente de enfermedad cardiovascular con o sin comorbilidad, y vacunación previa para COVID-19. Esta serie de casos incluye pacientes durante la cuarta ola epidemiológica de COVID-19 en la Ciudad de México, específicamente en el periodo entre el 30 de diciembre de 2021 y el 17 de marzo de 2022, en el INC. El diagnóstico se realizó durante la hospitalización por diversas causas cardiovasculares, y en algunos casos fue el motivo de ingreso. Se excluyeron los pacientes con diagnóstico de COVID-19 por PCR o prueba de antígenos que no tuvieran antecedentes de enfermedad cardiovascular. Los datos clínicos y demográficos, y los resultados de laboratorio y de tomografía computarizada (TC) de tórax, se recopilaron a partir del expediente clínico electrónico del INC.
Los datos recopilados incluyeron edad, antecedentes de vacunación (tipo de vacuna y número de dosis hasta el momento de la atención médica), diagnóstico al ingreso, enfermedades subyacentes, fecha de inicio de los síntomas, diagnóstico por PCR o antígenos, y estudios de laboratorio al ingreso al área COVID-19 del hospital y durante su estancia hospitalaria, lo que permitió hacer la comparación de datos. Estos estudios incluyeron leucocitos totales, proteína C reactiva, plaquetas, linfocitos, creatinina, PaFi (PaO2/FiO2) calculada, anticoagulación, días de estancia hospitalaria y motivo de alta.
Para los análisis estadísticos, las variables continuas se presentan como media y desviación estándar o como mediana y rango intercuartílico (RIC), según se determine mediante la prueba de normalidad de Anderson-Darling. Las variables categóricas se presentan como frecuencias y proporciones absolutas. El análisis estadístico se realizó en el programa estadístico R y RStudio, versión 4.2.2 y 2023.06.1+524, respectivamente. Los comités de ética y de investigación clínica del INC autorizaron el reporte de este estudio.
Definiciones
Arritmias: fibrilación auricular, flutter auricular, taquicardia supraventricular con bloqueo de rama derecha, taquicardia supraventricular paroxística y taquicardia ventricular monomórfica.
Cardiopatía isquémica: infarto agudo al miocardio con elevación del segmento ST anterior, infarto agudo al miocardio con elevación del segmento ST inferior, infarto agudo al miocardio sin elevación del segmento ST y cardiopatía isquémica crónica.
Insuficiencia cardiaca: insuficiencia cardiaca con fracción de eyección del ventrículo izquierdo reducida e insuficiencia cardiaca con descompensación aguda.
Enfermedad valvular: enfermedad de las válvulas mitral y aórtica.
Cardiopatía congénita: comunicación interauricular y conducto arterioso persistente.
Trombótico: tromboembolia pulmonar, trombosis de vena cava superior y evento vascular cerebral.
Infeccioso: hepatitis C y sífilis.
Resultados
Características generales
Se incluyeron 17 pacientes adultos con diagnóstico confirmado de COVID-19, con una mediana de edad de 58 años (RIC: 49-64) y una mediana de días de estancia hospitalaria de 10 días (RIC: 4-14). En el 53% (n = 9) de los pacientes, la infección por SARS-CoV-2 fue detectada durante la hospitalización, mientras que en el 47% (n = 8) fue detectada al ingreso al hospital. Las características individuales de los pacientes se describen en la tabla 1.
Tabla 1 Características individuales de los pacientes del estudio
| Patologías | Fármacos | Gasometría | Complicaciones | Desenlace | TC |
|---|---|---|---|---|---|
| Endocarditis infecciosa | Acenocumarol | pH ↕ | Ninguna | Mejoría | CO-RADS 4 |
| Hepatitis C | pO2↓ | ||||
| Sífilis | pCO2↓ | ||||
| Lactato↕ | |||||
| HCO3↓ | |||||
| FiO2↕ | |||||
| PaFi↕ | |||||
| Cardiacas | Apixabán | pH↕ | Ninguna | Mejoría | CO-RADS 5 |
| Diabetes mellitus | Furosemida | pO2↓ | |||
| ERC KDIGO 3 | Atorvastatina | pCO2↓ | |||
| Tromboembolia pulmonar | HCO3 | Lactato↕ | |||
| O2 | HCO3↓ | ||||
| FiO2↕ | |||||
| PaFi↕ | |||||
| Diabetes mellitus | Heparina | pH↕ | Falla renal | Trasplante | CO-RADS 6 |
| Hipertensión arterial | pO2↓ | Hemorragia de | renal por | ||
| PCO2↓ | tubo digestivo | ERC | |||
| Lactato↑ | bajo | ||||
| HCO3↓ | |||||
| FiO2↕ | |||||
| PaFi↕ | |||||
| Endocarditis infecciosa | O2 | pH↑ | Ninguna | Mejoría | CO-RADS 4 |
| Flutter auricular atípico | Enoxaparina | pO2↓ | |||
| pCO2↓ | |||||
| Lactato↕ | |||||
| HCO3↕ | |||||
| FiO2↕ | |||||
| PaFi↕ | |||||
| Endocarditis infecciosa | Ertapenem | pH↕ | Ninguna | Mejoría | CO-RADS 3 |
| ERC KDIGO 5 | Eritropoyetina | pO2↓ | |||
| Trombosis de vena cava superior | Alprazolam | pCO2↓ | |||
| Pregabalina | Lactato↕ | ||||
| Acenocumarol | HCO3↓ | ||||
| Enoxaparina | FiO2↕ | ||||
| PaFi↕ | |||||
| Insuficiencia cardiaca | Ácido acetilsalicílico | pH↓ | Ninguna | Mejoría | CO-RADS 6 |
| Hipertensión arterial | Clopidogrel | pO2↓ | |||
| Diabetes mellitus | Carvedilol | pCO2↕ | |||
| Furosemida | Lactato↕ | ||||
| Enalapril | HCO3↓ | ||||
| Enoxaparina | FiO2↕ | ||||
| Acenocumarol | PaFi↓ | ||||
| IAMCEST | Enoxaparina | pH↕ | Infección | Mejoría | Sin TC |
| Insuficiencia cardiaca | Bisoprolol | pO2↓ | asociada a | ||
| Obesidad grado II | Espironolactona | pCO2↕ | catéter | ||
| Dapagliflozina | Lactato↕ | ||||
| Bumetanida | HCO3↕ | ||||
| FiO2↕ | |||||
| PaFi↓ | |||||
| Hipertensión arterial | Levotiroxina | pH↓ | Ninguna | Mejoría | CO-RADS 6 |
| Diabetes mellitus | Enoxaparina | pO2↑ | |||
| Insuficiencia cardiaca | Metoprolol | pCO2↓ | |||
| Fibrilación auricular | Furosemida | Lactato↑ | |||
| Hipotiroidismo | Enalapril | HCO3↕ | |||
| O2 | FiO2↑↑ | ||||
| PaFi↓ | |||||
| Taquicardia supraventricular aberrada con | Enoxaparina | pH↑ | Ninguna | Mejoría | CO-RADS 4 |
| bloqueo de rama derecha | pO2↕ | ||||
| Aneurisma de aorta abdominal infrarrenal | pCO2↓ | ||||
| IAMSEST | Lactato↕ | ||||
| HCO3↕ | |||||
| FiO2↕ | |||||
| PaFi↕ | |||||
| Diabetes mellitus | Enoxaparina | pH↕ | Choque séptico | Defunción | Sin TC |
| Hipertensión arterial | pO2↑ | Mediastinitis | |||
| IAMSEST | pCO2↓ | ||||
| Lactato↕ | |||||
| HCO3↓ | |||||
| FiO2↑ | |||||
| PaFi↕ | |||||
| Cardiopatía isquémica | Enoxaparina | pH↕ | Cetoacidosis | Mejoría | CO-RADS 6 |
| Hipertensión arterial | Amiodarona | pO2↑ | diabética | ||
| Diabetes mellitus | Insulina NPH | pCO2↓ | ERC KDIGO 3 | ||
| Enfermedad vascular cerebral | Dexamatasona | Lactato↑ | |||
| HCO3↓ | |||||
| FiO2↑ | |||||
| PaFi↕ | |||||
| CIA | Apixabán | pH↕ | Ninguna | Mejoría | CO-RADS 3 |
| Tromboembolia pulmonar | O2 | pO2↓ | |||
| Taquicardia supraventricular paroxística | Levotiroxina | pCO2↓ | |||
| HAP | Lactato↕ | ||||
| HCO3↓ | |||||
| FiO2↑↑ | |||||
| PaFi↓↓ | |||||
| IAMCEST | ASA | pH↑ | Ninguna | Mejoría | Sin TC |
| Diabetes mellitus | Enoxaparina | pO2↑ | |||
| Enalapril | pCO2↓ | ||||
| Atorvastatina | Lactato↕ | ||||
| Bisoprolol | HCO3↓ | ||||
| FiO2↕ | |||||
| PaFi↕ | |||||
| Miocardiopatía dilatada/TVMS | Digoxina | pH↓ | Ninguna | Mejoría | CO-RADS 6 |
| Fibrilación auricular | Alopurinol | pO2↑ | |||
| Diabetes mellitus | Espironolactona | pCO2↓ | |||
| Enalapril | Lactato↑ | ||||
| Apixabán | HCO3↓ | ||||
| Dapaglifozina | FiO2↕ | ||||
| PaFi↕ | |||||
| IAMCEST inferior + trombólisis | ASA | pH↕ | Ninguna | Mejoría | CO-RADS 6 |
| CAP | Clopidogrel | pO2↕ | |||
| Atorvastatina | pCO2↓ | ||||
| Metoprolol | Lactato↕ | ||||
| Enalapril | HCO3↕ | ||||
| FiO2↑ | |||||
| PaFi↕ | |||||
| CAP CIA Síndrome de Down | Cefalotina | PaFi↕ | Ninguna | Mejoría | Sin TC |
| Mixoma auricular izquierdo | Metoprolol | pH↑ | Ninguna | Mejoría | CO-RADS 5 |
| Fibrilación auricular | Dexametasona | pO2↓ | |||
| Furosemida | pCO2↑ | ||||
| Lactato↕ | |||||
| HCO3↑ | |||||
| FiO2↑ | |||||
| PaFi↓ |
ASA: ácido acetilsalicílico; CAP: conducto arterial persistente; CIA: comunicación interauricular; ERC: enfermedad renal crónica; HAP: hipertensión arterial pulmonar; IAMCEST: infarto agudo al miocardio con elevación del segmento ST; IAMSEST: infarto agudo al miocardio sin elevación del segmento ST; KDIGO: Kidney Disease: Improving Global Outcomes; TC: tomografía computarizada; TVMS: taquicardia ventricular monomórfica sostenida.
Enfermedad cardiaca y comorbilidad
Los antecedentes de enfermedad cardiovascular y la comorbilidad se describen en la tabla 2. Dentro de las patologías cardiacas, la arritmia fue la más prevalente, siendo la más frecuente la fibrilación auricular, la cual presentaban 3 pacientes, representando el 50% de la población con arritmias; la segunda fue hipertensión arterial sistémica 7 (41%), y por último, el infarto agudo de miocardio (29%).
Tabla 2 Estadísticos descriptivos de las características clínicas de la población de estudio (n = 17)
| Edad (años) | |
| Mediana (RIC) | 60 (47, 64) |
| Mortalidad | 1 (5.9%) |
| Vacunación | |
| Sí | 17 (100%) |
| AstraZeneca | 9 (53%) |
| Sinovac | 2 (12%) |
| Cansino | 2 (12%) |
| Sputnik | 2 (12%) |
| Pfizer | 1 (5.9%) |
| No especificada | 2 (12%) |
| Comorbilidad y enfermedades cardiacas | |
| HAS | 7 (41%) |
| Arritmia | 8 (47%) |
| Cardiopatía isquémica | 5 (29%) |
| Insuficiencia cardiaca | 4 (24%) |
| Endocarditis | 3 (18%) |
| Cardiopatía congénita | 3 (18%) |
| Aneurisma | 1 (5.9%) |
| Enfermedad valvular | 4 (24%) |
| Obesidad | 2 (12%) |
| ERC | 2 (12%) |
| Diabetes | 8 (47%) |
| Trombosis | 4 (24%) |
| Hipotiroidismo | 1 (5.9%) |
| HAP | 1 (5.9%) |
| Infeccioso | 1 (5.9%) |
ERC: enfermedad renal crónica; HAP: hipertensión arterial pulmonar; HAS: hipertensión arterial sistémica; RIC: rango intercuartílico.
Se observó que la principal comorbilidad asociada al síndrome metabólico fue la diabetes mellitus tipo 2 en 8 pacientes (47%), seguida de 2 pacientes de obesidad (12%).
Estudios de laboratorio
Los resultados, en medianas, fueron: leucocitos 7.82 células × 103 (RIC: 6.68-8.91), dímero D 0.48 (RIC: 0.23-0.61), ferritina 212 (RIC: 152-428), proteína C reactiva 49 (RIC: 12-104), plaquetas 214 (RIC: 176-273), propéptido natriurético cerebral N-terminal (NT-proBNP) 4710 (RIC: 1.824-7667), creatinina sérica 1.0 (RIC: 0.82-2.06) y PaFi 190 (RIC: 138-300). Los resultados de los exámenes de laboratorio se muestran en la tabla 1.
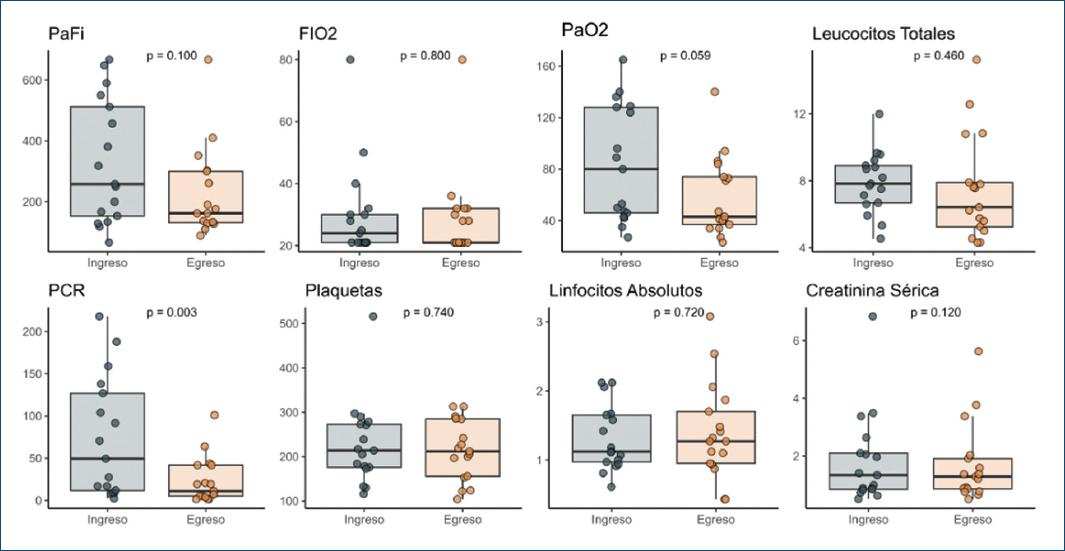
Se compararon la PaFi, la FiO2, la PaO2, los leucocitos totales, la proteína C reactiva, las plaquetas, los linfocitos y la creatinina del ingreso y del egreso de los pacientes. La figura 1 consta de ocho gráficos de cajas y bigotes que muestran la distribución de las variables bioquímicas y gasométricas de interés, al ingreso y al egreso hospitalario. Destaca que tanto la PaFi como la PaO2 disminuyeron de manera importante al egreso hospitalario; sin embargo, la diferencia no fue estadísticamente significativa (p = 0.100). En el caso de la FiO2, los leucocitos totales, las plaquetas, los linfocitos absolutos y la creatinina sérica no se observó una disminución estadísticamente significativa al egreso. Únicamente en la proteína C reactiva se observó que la mediana al egreso fue significativamente menor en comparación con la mediana al ingreso (p = 0.003).
Tomografía computarizada
La clasificación utilizada fue CO-RADS9, un sistema estandarizado que evalúa la sospecha de afección pulmonar de COVID-19 en una escala de 0 a 6 (Tabla 3). De los 17 pacientes, 4 (24%) no contaban con TC de tórax. El CO-RADS que más se encontró en los pacientes fue 6, representando el 35%; los que tuvieron menor prevalencia fueron CO-RADS 3 y 5, con solo 2 (12%) pacientes cada uno. Los datos de los demás pacientes se muestran en la tabla 1.
Tabla 3 Clasificación CO-RADS12
| Categoría CO-RADS | Nivel de sospecha de involucro pulmonar de COVID-19 | Descripción |
|---|---|---|
| 0 | No interpretable | Escaneo técnicamente insuficiente para asignar una puntuación |
| 1 | Muy bajo | Normal o sin infección |
| 2 | Bajo | Típico de otra infección, pero no de COVID-19 |
| 3 | Inseguro | Características compatibles con COVID-19, pero también con otras enfermedades |
| 4 | Alto | Sospechoso de COVID-19 |
| 5 | Muy alto | Típico para COVID-19 |
| 6 | Confirmado | PCR positiva para SARS-CoV-2 |
PCR: prueba en reacción en cadena de la polimerasa.
Vacunación
La vacuna que presentó mayor frecuencia de aplicación fue la de AstraZeneca, en 9 (53%) pacientes, y las vacunas con menor aplicación fueron las de Pfizer y Cansino, en 1 (5.88%) paciente cada una. En 2 (12%) pacientes no se especificó el tipo de vacuna que se les había aplicado. Los demás datos estadísticos se describen en la tabla 2.
Discusión
Este estudio investigó la relación entre el proceso inflamatorio y las lesiones causadas por el SARS-CoV-2 en pacientes con enfermedades cardiacas preexistentes. De los 17 pacientes, 16 mostraron un curso clínico atenuado, mientras que uno experimentó una falla multiorgánica debido a síndrome de respuesta inflamatoria sistémica que le llevó a la muerte.
Al analizar los resultados obtenidos, se observa una disminución de la proteína C reactiva, los leucocitos y los linfocitos, lo que demuestra que el proceso inflamatorio mejoró, llevando a los pacientes a una evolución favorable y por consiguiente una mejoría clínica. Además, podemos decir que la coexistencia de diabetes mellitus y cardiopatía hipertensiva pueden exacerbar la evolución de la COVID-19, condicionando la morbilidad de los pacientes. Esto se demuestra en el caso de un paciente que requirió trasplante renal 7 meses después de presentar infección por SARS-CoV-2.
En cuanto a los resultados de los parámetros gasométricos, encontramos que la mayoría de los pacientes ingresaron con una PaFi alta, indicando que el síndrome de distrés respiratorio agudo era leve y no necesitaban oxígeno suplementario. Al egreso, los valores bajaron debido a que los pacientes necesitaban una FiO2 más alta para poder llegar a los requerimientos de oxígeno. Esto puede interpretarse como que los pacientes se encontraban en un síndrome de distrés respiratorio moderado o grave.
Diversos estudios han demostrado que la hipertensión es un factor de riesgo significativo para presentar resultados desfavorables en pacientes hospitalizados por COVID-19. A pesar de que nuestra muestra fue pequeña, estamos de acuerdo en que sí es un riesgo para los pacientes, ya que confiere mal pronóstico.
El virus parece tener una predilección por el tejido cardiaco, lo que puede provocar miocarditis, miocardiopatía por estrés, arritmias e infarto agudo de miocardio7,8. La infección también puede inducir una respuesta inmunitaria inadecuada que cause una inflamación excesiva y daño al tejido cardiaco y al endotelio vascular8,9.
En una revisión realizada por Vosko et al.8 se menciona que la diabetes es una comorbilidad común en los pacientes hospitalizados por COVID-19. La posible asociación de la letalidad de la COVID-19 y la diabetes tipo 2 conlleva complicaciones vasculares asociadas y daños al endotelio. Esto podría explicar la mayor tasa de trombosis en los pacientes con diabetes hospitalizados por COVID-19, además de que la diabetes eleva los riesgos cardiovasculares que empeoran el pronóstico de los pacientes infectados8.
A medida que gracias a la vacunación aumenta el número de sobrevivientes, es necesario centrarse en los efectos cardiovasculares a largo plazo de la COVID-19. Sin embargo, faltan estudios que detallen estas manifestaciones, ya que los informes actuales se limitan a síntomas recurrentes como disnea, dolor torácico y palpitaciones10,11.
Tenemos en cuenta que una limitación del estudio es la población con la que trabajamos, ya que es pequeña y no permite realizar muchos análisis estadísticos. No obstante, al comparar nuestros resultados con los de la literatura llegamos a conclusiones similares. Otra limitación es que los pacientes solo se siguieron durante su estancia hospitalaria, y posterior a esto no se tiene información ni laboratorios, por lo que no se conocen las secuelas que pueden presentar a largo plazo.
Conclusiones
La pandemia de COVID-19 ha sido un desafío para el sistema de salud de México. A lo largo de los años se ha aprendido la importancia de adaptar rápidamente las estrategias de atención y aumentar las medidas de seguridad sanitaria. Este estudio contribuye al conocimiento de cómo la infección por SARS-CoV-2 afecta a los pacientes con enfermedades cardiacas preexistentes, demostrando que, a pesar de tener alguna enfermedad, el curso clínico es favorable en la mayoría de los casos.
Es fundamental tomar estudios de laboratorio de los pacientes al ingreso al área COVID-19, en particular la proteína C reactiva, ya que este biomarcador ayuda a determinar el curso clínico de la enfermedad.
Se debe continuar investigando y monitoreando los efectos del SARS-CoV-2 en pacientes con enfermedades cardiacas preexistentes y en aquellos con síntomas persistentes después de la infección. Esto permitirá desarrollar estrategias más efectivas para el tratamiento y la prevención de las complicaciones cardiovasculares asociadas a la COVID-19.











 nova página do texto(beta)
nova página do texto(beta)