Introducción
Esta patología se describió por primera vez en estudios de autopsia por Rokitansky, en 18751. Tiempo atrás esta cardiopatía se conoció como inversión ventricular, L-transposición o transposición corregida de las grandes arterias2,3.
La doble discordancia atrio-ventricular (AV) y ventrículo-arterial (DD) es el término adecuado para describir esta patología debido a que el mecanismo embrionario es diferente al de una transposición de las grandes arterias4.
Esta cardiopatía se forma en la etapa embrionaria por un plegamiento del giro del tubo cardiaco primitivo a la izquierda (L-asa) en vez de realizarlo en dextro torsión (D-asa) que es lo habitual, esto hace que el ventrículo izquierdo (VI) se sitúe a la derecha, mientras que el ventrículo derecho (VD) a la izquierda, lado a lado. El septo interventricular se posiciona más sagital y horizontal, con mala alineación de la cruz del corazón, por esto en un 80% de los pacientes se asocia a comunicación interventricular (CIV). El recorrido de las grandes arterias va en paralelo y no cruzadas, como es lo habitual. Es frecuente encontrar una obstrucción sub pulmonar en el VI hasta en un 40%, sobre todo si existe CIV2,5,6.
En la DD al estar conectado el VI con la arteria pulmonar hace que exista una continuidad fibrosa mitro-pulmonar; en contraparte, la conexión del VD con la aorta se caracteriza por la presencia de un infundíbulo sub aórtico, bien desarrollado por la discontinuidad fibrosa entre la tricúspide (la cual es displásica) y la arteria aorta, además de que esta se encuentra posicionada anterior y a la izquierda con respecto a la arteria pulmonar7.
Es una cardiopatía poco común. La aurícula derecha se conecta al ventrículo morfológicamente izquierdo que se encuentra a la derecha y de aquí sale la arteria pulmonar. La aurícula izquierda se conecta al ventrículo morfológicamente derecho que se encuentra a la izquierda y en ese ventrículo está conectada la arteria aorta. Se presenta en 0.02-0.07 de cada 1,000 recién nacidos vivos y menos del 0.05% del total de las cardiopatías congénitas1,8.
Se caracteriza por un VD que mantiene una circulación sistémica y bajo estas condiciones con el tiempo falla la función ventricular, mientras que el VI que está a la derecha maneja las presiones pulmonares. La mayor manifestación de disfunción del VD es la insuficiencia tricuspídea (IT), la cual se asocia a mayor morbimortalidad9.
En una forma sencilla pareciera que la alteración anatómica estuviera fisiológicamente resuelta al irse la sangre venosa sistémica al tronco pulmonar y la sangre oxigenada a la arteria aorta, sin embargo, los ventrículos están invertidos.
Las anomalías asociadas son comunes (85%) e incluyen CIV (50-60%), estenosis pulmonar (EP) o atresia (30-50%), displasia de la válvula tricúspide (tipo Ebstein) y bloqueo atrio-ventricular (BA-V). Un 25% de los casos tienen dextrocardia o mesocardia3,5,7,10.
El objetivo del estudio es describir la frecuencia, el diagnóstico, tratamiento y evolución de una serie de casos con DD.
Método
Se realizó un estudio retrospectivo y descriptivo, revisando los expedientes de pacientes con diagnóstico de DD del 1 de enero del 2000 hasta el 30 de diciembre del 2022.
Se recabaron datos de sexo, edad al momento del diagnóstico, lesiones asociadas, evolución clínica, tipo de cirugía y seguimiento clínico.
Se realizó estadística descriptiva. Las variables numéricas se obtuvieron mediante media y desviación estándar y las variables categóricas mediante frecuencias y porcentajes. Se comparan las características de nuestra población con los resultados de la literatura por medio de la prueba exacta de Fisher. La información se elaboró en una base de datos en Excel de Microsoft y el análisis estadístico se realizó con el paquete computacional Statical Package for the Social Sciences (SPPS) versión 28.
Resultados
En el periodo de los últimos 23 años estudiamos 30 pacientes. Se estima que ingresa un poco más de un paciente por año con ese diagnóstico a nuestro instituto.
Las edades al momento del diagnóstico comprendieron de recién nacido al mayor, que fue de 11 años de edad, con una media de 20.2 meses. Fueron 18 del sexo masculino, para una relación 1.5:1.
El situs fue solitus en 24/29 pacientes (82.7%), en 5/29 inversus (17.2%), un paciente poco frecuente en criss-cross (en inversus y dextrocardia), 9/24 (37.5%) presentaron dextrocardia, 15/24 (62.5%) levocardia. Con arco aórtico derecho en 16/29 (55.1%).
Dentro de las anomalías anatómicas asociadas, la CIV fue la más frecuente, en 25/29 pacientes (86.2%), de las cuales cinco fueron peri membranosas, tres musculares y cinco sub pulmonares, 12 con CIV muy amplia. Le siguieron en frecuencia 16 pacientes con EP (53.3%), 13/29 (44.8%) con comunicación interatrial (CIA), 6/28 (21.4%) con persistencia del conducto arterioso (PCA), tres Ebstein izquierdos, tres con hipoplasia del arco aórtico, dos con rama derecha pulmonar hipoplásica y dos con atresia pulmonar. Dos casos poco frecuentes con canal AV común, en situs solitus, los cuales se identificaron: el VD a la izquierda por su hipertrofia y la banda moderadora con entrada de la aurícula izquierda y emergencia de la aorta y al VI a la derecha por ser más liso y elipsoide con entrada de la aurícula derecha y emergencia de la arteria pulmonar. En cuanto al arco aórtico: 13/29 fueron derechos y 16/29 izquierdos y un paciente con doble arco aórtico. Uno con coronaria derecha emergiendo de la descendente anterior, el resto con coronarias de distribución en espejo, excepto una que no se estudió (Tabla 1). Todos los pacientes cursaron con lesiones cardiacas asociadas. Se hizo un comparativo con otras publicaciones, encontrando significancia en algunas lesiones asociadas con nuestro estudio (Tabla 2).
Tabla 1 Características clínico-quirúrgicas en pacientes con doble discordancia
| Paciente | Sexo | Edad en meses | Situs | Lesiones asociadas | Disfunción ventricular | Procedimiento | Resultado |
|---|---|---|---|---|---|---|---|
| 1 | M | 3 | SS | Ebstein, CIV, IT, IM. AAo izq | No | Bandaje, Glenn | Fallece en POP |
| 2 | M | 9 | SI | CIV, CIA, EP, AAo izq, HVD | No | Glenn, Fontan | Ross I. Alta |
| 3 | F | 18 | SI | CIA, EP, IT, IM, AAo der | Sí | Ampl. TSVD, cierre CIA | Ross II. Alta |
| 4 | M | 12 | SI | CIV, EP, AAo der, AT | No | Ninguno. En espera de cirugía | Ross I |
| 5 | M | 1 | SI | CIA, EP, IT, AAo der | No | Ampl. TSVD, cierre CIA | Ross I. BA-V-I. Alta |
| 6 | M | RN | SS | CIV, IM, IT, AAo izq | No | Ninguno | Ross I |
| 7 | M | 12 | SS | CIV, CIA, EP, AAo izq | No | Ninguno | Ross I |
| 8 | M | 84 | SS | CIV, EAo, AAo izq, IT, IM | No | Cierre CIV y DAE | Ross II, HAP, BA-V-III |
| 9 | M | 5 | SS | CIV, Ebstein, IT, IM, Ao izq | Sí | Cierre CIV, plastia T, bandaje pulmonar | Ross I, BA-V-I |
| 10 | F | 5 | SS | CIV, CIA, AP, PCA, AAo izq | Sí | Glenn-Fontan | Ross I |
| 11 | M | 16 | SS | PCA, CIV, EP, IT, AAo izq, HVD | No | Glenn-Fontan | Ross I |
| 12 | F | 5 | SS | CIV, PCA, CoAo, HAAo, IT severa, AAo der | Sí | Bandaje pulmonar, avance Ao, Glenn-Fontan | Ross II |
| 13 | M | 132 | SI | CIV, EP, EAo, AAo izq | Sí | FB-T | Fallece por osteosarcoma |
| 14 | M | 24 | SI | CIV, CIA, IT, AAo der, EP, HVD | No | Glenn | Ross II |
| 15 | M | RN | SS | CIV, Ao izq | Sí | Bandaje (no alcanzó a operarse) | Ross I, falleció |
| 16 | M | 5 | SS | CIV, AAo izq, HVD, IM | No | Bandaje/Glenn | Ross III, BA-V 3° |
| 17 | F | RN | SS | CIV, PCA, HAAo, AAo der | Sí | Bandaje, avance aórtico | Fallece en POP |
| 18 | M | RN | SS | FOP, CIV, PCA, AP, AAo der, IT, IM, coronariopatía | Sí | FB-T/Glenn | Ross I |
| 19 | M | 132 | SS | Ebstein, IT, AAo izq | No | Ninguno/ablación WPW | Ross I, WPW |
| 20 | F | RN | SS | CIV, CIA, PCA, IT, IM, HAAo, Ao izq | Sí | Cierre de defectos. Avance Ao | Ross I |
| 21 | M | 1 | SS | CIV, HAAo, CoAo, IT, IM, Ao izq | Sí | Bandaje pulmonar, plastia VT, avance Ao | Ross IV, BA-V-I POP tardío fallece |
| 22 | F | 12 | SS | CIV, IT, IP, AAo izq | No | Ninguno | Ross I |
| 23 | F | 1 | SS | Canal AV, PCA, EP, AAo derecho, insuficiencia de válvula común | No | Pendiente corrección del canal atrio-ventricular | Ross I, BA-V-III. Marcapasos |
| 24 | F | 16 | SI | PCA, CIV, CIA, EP, IT, interrupción de vena cava inferior. Doble AAo | No | Cierre de defectos | BA-V 3°, marcapasos Ross I |
| 25 | M | 6 | SS | IT, displasia de tricúspidea, AAo izq | Sí | Ninguno | Ross I, BA-V-1° |
| 26 | F | 1 | SS | Canal AV, EP, Ao der | No | Pendiente corrección del canal atrio-ventricular | Ross I, BRDHH |
| 27 | M | 15 | SI | CIA, CIV, EP, IT, AAo der | No | Ninguno | BA-V 3°, Ross I, marcapasos |
| 28 | M | 24 | SI | CIV, EP, IT, AAo izq | No | Corrección de CIV | Ross I |
| 29 | F | 34 | SS | IT, IP, AAo izq | Sí | Ablación Qx ninguno | TPSV, Ross II |
| 30 | F | 24 | SI | Criss-cross, CIV, PCA, AAo izq, ventrículos supero-inf | No | Cierre de defectos | Ross I |
Anom VT: anomalías de la válvula tricúspide; Anom VM: anomalías de la válvula mitral; CIV: comunicación interventricular; EP: estenosis pulmonar; CIA: comunicación interauricular; AP: atresia pulmonar; AT: atresia tricúspidea; EAo: estenosis aórtica; PCA: persistencia del conducto arterioso; AV: atrioventricular; CoAo: coartación de la aorta; HAAo: hipoplasia del arco aórtico; TPSV: taquicardia paroxística supraventricular; HVD: hipoplasia del ventrículo derecho.
Tabla 2 Comparativo de lesiones asociadas en pacientes con doble discordancia
| Lesiones cardiacas | Day16 (43) n (%) | Estudio actual (30) n (%) | Rutledge12 (121) n (%) | p |
|---|---|---|---|---|
| Sin lesiones | 0 | 0 | 9 (7.4) | 0.07 |
| Anomalías de la válvula tricúspide/Ebstein | 4 (9.3) | 3 (10) | 19 (15.7) | 0.5 |
| Comunicación interventricular | 29 (67.4) | 25 (86) | 88 (72.7) | 0.3 |
| Estenosis pulmonar | 14 (32.6) | 16 (53) | 61 (50.4) | 0.09 |
| Comunicación interauricular | 0 | 13 (44.8) | 44 (36.6) | < 0.001 |
| Atresia pulmonar | 0 | 2 (8) | 18 (14.8) | 0.007 |
| Estenosis aórtica | 0 | 2 (8) | 0 | 0.02 |
| Persistencia del conducto arterioso | 0 | 6 (21) | 0 | < 0.001 |
| Canal atrio ventricular | 0 | 2 (8) | 0 | 0.02 |
| Coartación de aorta/hipoplasia del arco aórtico | 4 (9.3) | 4 (16) | 16 (13.2) | 0.81 |
| Anomalías coronarias | 0 | 1 (4) | 2 (1.6) | 0.49 |
Dentro de las alteraciones funcionales asociadas, en 19/27 pacientes (70.3%) presentaron IT de diverso grado: ocho leves, seis moderadas y siete graves. Los dos con canal AV común con insuficiencia de la válvula AV única. Uno con atresia tricuspídea, otro con hipoplasia tricuspídea; cuatro pacientes con diagnóstico de hipertensión arterial pulmonar.
A 10/30 pacientes (33.3%) se les detectó disfunción VD de acuerdo con parámetros ecocardiográficos. En todos los pacientes el VI fue el anterior, excepto en un solo caso (en uno con situs inversus y arco aórtico derecho) (Tabla 1).
Respecto a las anomalías electrocardiográficas, se observaron 6/30 pacientes (20%) con BA-V: tres de ellos con BA-V de primer grado, uno de 2° grado y dos con BA-V III. Cuatro con bloqueo incompleto de rama izquierda del haz de His, tres con bloqueo incompleto de rama derecha del haz de His y uno con disfunción del nodo sinusal en un paciente, manifestado por ritmo nodal intermitente y otro con diagnóstico de síndrome de Wolff-Parkinson-White.
El tratamiento médico se administró en 19 pacientes (63%) con furosemida, espironolactona y captopril; en pacientes con fisiología uni ventricular con ácido acetilsalicílico y al paciente con Wolff-Parkinson-White, se manejó con metoprolol, propafenona y ablación de vía accesoria.
El tratamiento quirúrgico hasta el momento del corte del estudio fue en 21 (70%) de los pacientes; dos con fístula sistémico-pulmonar, dos con plastia de la válvula tricúspide, dos con cierre de CIA, tres avances aórticos, cuatro con cierre de CIV, a cinco pacientes se les realizó bandaje pulmonar previo a la paliación y hasta el momento del estudio con ocho procedimientos de Glenn (26.6%) y cuatro con cirugía de Fontan (13.3%).
En cuanto a la evolución, 25 (83.3%) continúan en seguimiento; en espera de cirugía al momento del estudio tres pacientes (10%). El seguimiento fue en algunos pacientes de un mes a 17 años.
Cinco fallecieron (16.6%): uno a los cinco años de edad, por choque séptico y cardiogénico en el posquirúrgico inmediato posterior a cirugía de Fontan; otro a los 17 años de edad, tras desarrollar un osteosarcoma y por complicación por quimioterapia, presentó un infarto inferior (paciente que no recibió tratamiento quirúrgico cardiaco); el tercer fallecido fue a los nueve días de vida en el posquirúrgico inmediato por choque cardiogénico, tras corrección de anomalías asociadas (avance aórtico, cierre de CIV y bandaje pulmonar). El cuarto fallece por una crisis de hipoxia ante una estenosis severa del anillo y ramas pulmonares a los cinco meses de edad. El quinto paciente fallece a los 3 años 8 meses por taquicardia ventricular sostenida y choque cardiogénico.
Evolución de los 25 pacientes en seguimiento hasta la última consulta: están en una clasificación de Ross de grado I 18 pacientes (72%), grado II 5 pacientes (20%) y grado III 2 (8%).
Discusión
Esta patología se puede acompañar de alteraciones del situs: con 20-30% en situs inversus y 70-80% en situs solitus2,11. De nuestros pacientes, 7 (23%) se presentaron en situs inversus (Tabla 1), sin embargo, en el reporte de Rutledge solo hubo un 8.2%, mostrando significancia estadística respecto a nuestra serie (p < 0.005)12. Nosotros encontramos un mayor número de casos con situs solitus, como en otras publicaciones12-14.
Es de las pocas cardiopatías en donde el VI casi invariablemente se encuentra anterior y en raros casos los ventrículos se acomodan supero-inferiores, con el VD superior. En nuestra casuística 29 pacientes tuvieron el VI anterior.
En la radiografía se puede presentar hipertrofia del VD que está a la izquierda por el manejo de presiones sistémicas, o sin cardiomegalia y pedículo vascular estrecho por malposición de las grandes arterias (Fig. 1).
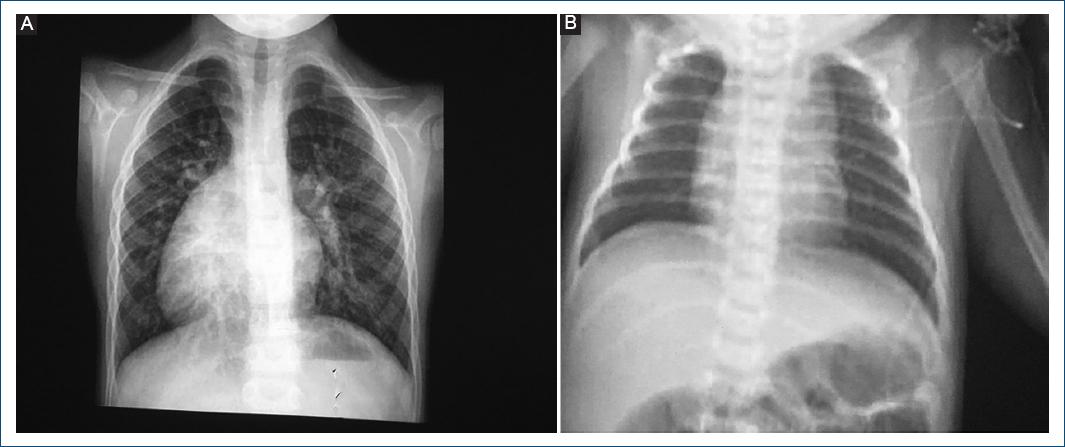
Figura 1 Imágenes radiológicas sugestivas de doble discordancia auriculo-ventricular y ventrículo-arterial. A: en mesocardia, sin cardiomegalia. B: en dextrocardia, con cardiomegalia leve y pedículo vascular angosto.
En estos pacientes existe riesgo de presentar BA-V a largo plazo por una alteración en la alineación del septum AV15. En nuestra casuística el 20% cursó con BA-V. Se puede asociar a otras lesiones: CIV 80%, EP 40-70%, insuficiencia aórtica 30%, IT 3%11. Parecido a nuestra casuística (Tabla 1).
El sistema de conducción es anormal en el asa L, por la mala alineación del tabique auricular y ventricular. Su disposición tiene valor pronóstico y significancia para el cirujano al momento de la reparación de la CIV12. El BA-V congénito se produce en el 5-10% de los casos en la adolescencia y hasta el 30% en la etapa adulta debido al crecimiento ventricular progresivo12. En nuestra casuística tuvimos 6 (20%) con BA-V, a diferencia de Rutledge, que tuvo 59 (48.7%) (p < 0.001). Se presentan taquiarritmias en el 12-38%. Cuando la válvula AV es displásica (Ebstein-like), la fibrilación auricular puede presentarse y persistir a pesar del reemplazo de la válvula tricúspide2.
De nuestros tres pacientes con Ebstein izquierdo, uno de ellos cursó con Wolff-Parkinson-White.
El realizar el diagnóstico prenatal es complicado cuando no se asocia a otras lesiones6. La ecocardiografía transtorácica es capaz de describir con precisión las características de la cardiopatía (Fig. 2) y dar las características preoperatorias y postoperatorias (gravedad de la IT, función del VD, estado actual de la CIV, EP, insuficiencia pulmonar e insuficiencia mitral, evaluación para decisión y seguimiento de doble switch, Rastelli o manejo uni ventricular)5. En una selección de pacientes se pueden incluir otros estudios de imagen como la angiografía, resonancia magnética y tomografía axial5.
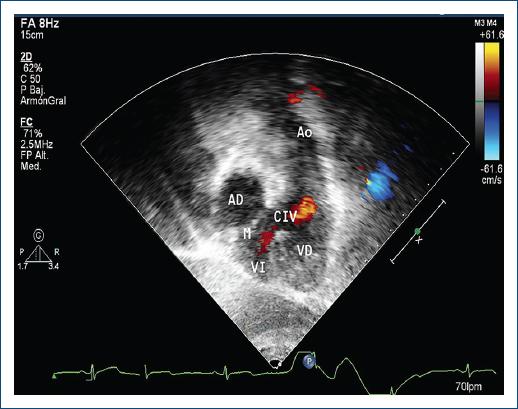
Figura 2 Ecocardiograma bidimensional-color en ventana subcostal, donde se observa a la derecha la conexión de la aurícula derecha (AD) con el ventrículo izquierdo (VI) y a la izquierda el ventrículo derecho (VD) conectado a la arteria aorta (Ao) (doble discordancia). Se observa una comunicación interventricular (CIV) como lesión concomitante.
De acuerdo con lo anterior, la presencia de una DD sin lesiones asociadas no es lo habitual11, como sucedió en nuestro estudio, siendo la CIV la más frecuente12,16.
En un gran porcentaje de los estudios tienen algún grado de estenosis o atresia pulmonar, por lo que presentarán cianosis y factor que considerar para la realización de cirugía de Rastelli junto con Senning o Mustard, requiriendo en forma previa una fístula sistémico-pulmonar14,17. Los pacientes con CIV y EP en algunos estudios mencionan que son de buen pronóstico y supervivencia a largo plazo, al no presentar disfunción del VI (que está a la derecha) posterior a la corrección anatómica16,18.
En caso de una DD y CIV sin obstrucción pulmonar, se requerirá un bandaje pulmonar previo a la corrección para evitar disfunción del ventrículo sistémico3,14.
Cuando esta patología se asocia a anomalía de Ebstein, se acompaña de hipoplasia del VD, con grados variables de desplazamiento y cabalgamiento de la tricúspide hacia el VD7. En nuestros pacientes nos llamó la atención: tres casos de anomalía de Ebstein y otros tres con cardiopatías asociadas poco frecuentes (dos con canal AV y otro en criss-cross, aunque ya descritos con anterioridad)8,19,20.
En cuanto a las características de las coronarias muestran una orientación invertida (siguen a sus ventrículos) con flujo adecuado ventricular 85% (imagen en espejo). La arteria coronaria derecha se origina del seno coronario derecho que es posterior y la coronaria izquierda que está a la derecha da origen a la arteria descendente anterior y circunfleja2,21. (Fig. 3). En ocasiones se encuentra una sola coronaria en los pacientes con DD7,22 como se presentó en uno de nuestros casos.
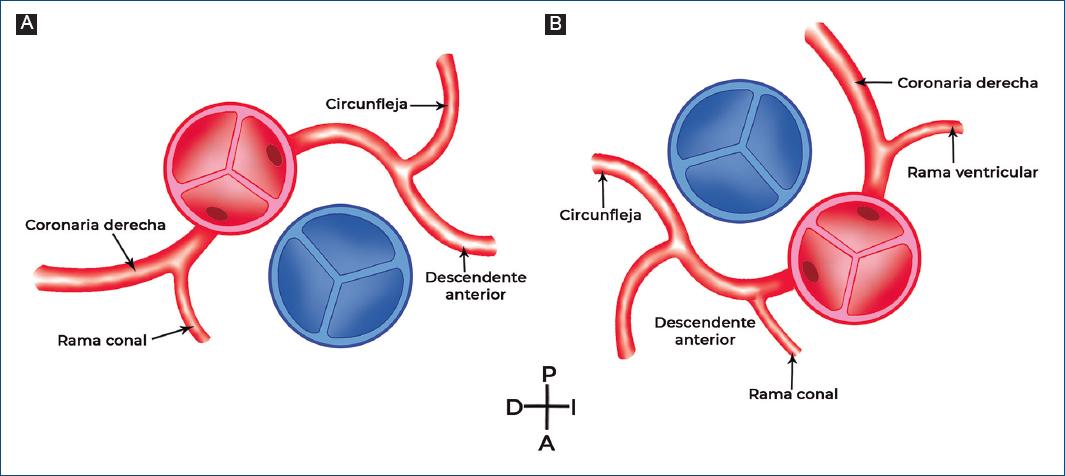
Figura 3 A: relación anatómica de arterias y coronarias normales. B: la anomalía más frecuente en arterias y coronarias en la doble discordancia auriculo-ventricular y ventrículo-arterial.
La mala evolución es debida a la sobrecarga crónica de la presión en el VD que da como consecuencia hipertrofia y una reserva limitada de la circulación de la coronaria derecha, con disminución de la oxigenación, isquemia, fibrosis progresiva e insuficiencia cardiaca1,23.
Los pacientes con DD pueden cursar asintomáticos hasta la edad de los 40 años, sin embargo, como el VD está en posición sistémica, hay una alta incidencia en ese momento de insuficiencia ventricular derecha6; las manifestaciones clínicas son reflejo de sus lesiones asociadas (la bradicardia por BA-V, la cianosis por obstrucción sub pulmonar, insuficiencia cardiaca por la arritmia o CIV o displasia de la válvula tricúspide)2,3. Es muy frecuente la insuficiencia cardiaca secundaria a la IT, con hipertrofia, seguida de dilataciones del VD y del anillo tricuspídeo. El tratamiento médico lo que busca es disminuir precarga y poscarga.
Hoy en día hay una gran variedad de técnicas quirúrgicas propuestas: técnicas paliativas (fístula sistémico pulmonar, bandaje pulmonar); corrección fisiológica de las lesiones asociadas (cierre de CIV y PCA, liberación de la obstrucción subpulmonar, reparación de la válvula AV izquierda); corrección univentricular (Glenn/Fontan) y corrección anatómica (Senning o Mustard)2.
Con el doble switch con bandaje de la arteria pulmonar previo, que se realiza desde 1990, la supervivencia se calcula en un 83.3%, requiriendo un 80% de reintervención quirúrgica7. En un estudio de pacientes con desplazamiento valvular AV (straddling) o hipoplasia del VD, se llevaron a paliación univentricular con muy baja mortalidad y con clase funcional I-II al seguimiento12, aunque experimentando arritmias, eventos embólicos e insuficiencia cardiaca a largo plazo24.
Quizá podamos resumir en el tratamiento el llevar a cabo una corrección funcional (corrección de lesiones asociadas o residuales, fístulas-sistémico pulmonar, marcapasos) o corrección anatómica Mustard + Jatene, Sening-Mustad + Rastelli25.
En la experiencia de nuestros 30 casos tuvimos 10 casos sin corrección quirúrgica por lesiones leves, uno con Ebstein asintomático; dos de estos están pendientes de corrección del canal AV. En siete pacientes se llevó a cabo cirugía paliativa, uno previo a corrección fisiológica, de estos, cuatro fallecieron en el postoperatorio. De corrección fisiológica hubo 10 pacientes, tres posteriores a una cirugía paliativa. Corrección uni ventricular: tuvimos ocho Glenn y cuatro que llegaron al Fontan, solo uno de los pacientes con Glenn falleció (Tabla 1). En esta última se restaura el VI como sistémico, y la función cardiaca se preserva mejor a mediano y largo plazo con sobrevidas de hasta el 92%, si sobrevive al trauma postoperatorio inmediato2.
Por las características morfológicas, en ningún paciente de esta serie se consideró que la alternativa de realizar doble switch ofreciera una significativa ventaja en términos de sobrevida o de calidad de vida. En estudios previos7 se ha determinado que alrededor del 80% de pacientes sometidos a doble switch requieren de reintervención quirúrgica.
Hay que llevar a cabo un seguimiento para valorar plastia de la válvula tricuspídea en caso de insuficiencia importante, falla de la función del VD, bloqueo AV y obstrucción del conducto que se haya colocado en el tracto de salida8.
La corrección anatómica comenzó a desarrollarse a partir de 1989, siendo en pacientes con DD sin atresia o EP el procedimiento de elección junto con cierre de CIV o corrección de otras anomalías asociadas. La realización del doble switch en grandes centros a nivel mundial produce buenos resultados, gracias a su desarrollo en los últimos 10 años, con una mortalidad a corto plazo de solo el 5% y una supervivencia a 10 años por arriba del 95%14,26. La principal complicación posquirúrgica temprana del doble switch es el BA-V completo y a largo plazo alteraciones auriculares como disfunción sinusal, arritmias auriculares y obstrucción de alguno de los parches.
Las contraindicaciones al procedimiento incluyen anomalías coronarias, hipoplasia del ventrículo morfológico izquierdo, desplazamiento (straddling) o cabalgamiento importante de la válvula tricúspide y anomalías de la válvula mitral14,26,27.
La cirugía de uno y medio, la cual sustituye al Senning de un hemi-Mustard y Glenn bidireccional es otra opción, cuando hay un VD pequeño efectivo y función limítrofe o cuando hay poca experiencia con el procedimiento de Senning. La posibilidad de la operación de Fontan es en los casos de hipoplasia ventricular.
Los pacientes ideales para la reparación anatómica son los que tienen excelente función biventricular y sin obstrucción pulmonar23.
Como última opción en el tratamiento puede considerarse el trasplante cardiaco5.
Siempre existe la discusión sobre dejar la evolución natural de esta cardiopatía (por la fisiología circulatoria corregida) o realizar intervención quirúrgica correctiva. En una casuística en el hospital de niños de Boston, de 83 pacientes, 45 (54%) se llevaron a cirugía, 5 pacientes con reemplazo de la válvula tricúspide y 24 (32%) con BA-V, 4 de ellos posterior a cirugía cardiaca. De estos el 15% fallecieron en el primer año, el restante sobrevivió a 20 años, con clase funcional I-II de la NYHA8. Nosotros tuvimos una mortalidad semejante del 16%.
Con la corrección funcional, la mortalidad se ha detectado en un 5-20% y a largo plazo incremento de la IT y disfunción del VD hasta en un 67%. En cuanto a la corrección anatómica, con o sin bandaje previo de la arteria pulmonar, se ha detectado en la evolución a largo plazo la necesidad de recambio del Rastelli e insuficiencia aórtica y o estenosis supra valvular aórtica y arritmias en el Jatene11.
En forma anecdótica se conoce la sobrevida de un paciente con DD y sin lesiones asociadas, hasta los 84 años de edad8, lo cual confirma que la historia natural de esta patología empeora con las lesiones asociadas (lesiones de válvulas mitral y tricuspídea). El presentar CIV y o hipertensión arterial pulmonar hace que el VI esté mejor preparado, se conoce que pueden tener una vida satisfactoria pero que con el avance de la edad su clase funcional declina9,18. La sobrevida en la DD aislada a cinco años es del 89%, y con EP y CIV la sobrevida es del 100%. Con Ebstein y otras anormalidades cardiacas complejas la sobrevida es pobre16.
La circulación sistémica en un VD morfológico falla en un tercio de los pacientes con ninguna lesión asociada y dos terceras partes con cirugía previa y o defectos concomitantes, para la 5.ª década de la vida23.
En cuanto al tratamiento quirúrgico, depende de la experiencia de cada grupo.
En un estudio reciente de 11 años con 85 pacientes operados de Senning, Senning-Rastelli y hemi-Mustard-Rastelli-Glenn bidireccional, nueve pacientes se re operaron, cinco fallecieron en postoperatorio inmediato, siete en posoperatorio tardío, con un 85% de sobrevida a cinco años28.
La mortalidad de nuestro estudio con seguimiento de 1 mes a 17 años fue de 5 pacientes (16.6%), semejante a los comparativos de Day (20.9%) y Rutledge (16.5%) (p < 0.79)12,16.
Conclusiones
Si bien una de las limitaciones de nuestro estudio es la poca cantidad de pacientes (30) dada la rareza de la patología, las características anatómicas y la evolución de los pacientes son similares en México a otros centros de EE.UU. y Europa, incluso en la mortalidad.
La mortalidad a corto plazo y la calidad de vida de estos pacientes es cada vez mejor, existiendo aún controversia en la literatura del momento ideal para realizar el procedimiento quirúrgico anatómico o fisiológico.
Consideramos que hay gran variabilidad en las opciones del manejo quirúrgico, este debe ser individualizado, tratado de acuerdo con la experiencia del grupo quirúrgico, de la terapia intensiva cardiovascular y a todos ellos darles un seguimiento permanente.











 nova página do texto(beta)
nova página do texto(beta)


