Introducción
Los sargazos (Sargassum spp.), son un grupo sobresaliente de algas pardas que sirve de hábitat y alimento para una gran variedad de animales marinos; pertenecen al orden Fucales de la división Phaeophyta, con 356 especies reconocidas (Guiry & Guiry, 2020). La mayoría son especies bentónicas que habitan zonas subtropicales y tropicales formando “bosques” en ambientes costeros submareales (Yip, Quek & Huang, 2020). Sargassum sinicola es la especie predominante en el Golfo de California, México; en Sonora se le encuentra desde el Golfo de Santa Clara hasta las bahías de Kino y Guaymas (Aguilar-Rosas, Aguilar-Rosas, Mateo-Cid & Mendoza-González, 2002; Andrade-Sorcia et al., 2014).
Entre los polisacáridos que componen la pared celular de las algas pardas se encuentra el fucoidan, un heteropolímero constituido principalmente por fucosas unidas mediante enlaces α (1 → 3), α (1 → 2) y en algunas especies también pueden encontrarse uniones α (1 → 4), (Jiao, Yu, Zhang & Ewart, 2011). Algunos de los residuos de fucosa del fucoidan están sulfatados (SO3 -) en los carbonos C-2 o C-4, y raramente en el carbono C-3. El grado de sulfatación es especie dependiente; esta modificación le imparte a la molécula de fucoidan una carga neta negativa (Ale, Mikkelsen & Meyer, 2011). Otros monosacáridos presentes en pequeñas concentraciones son las galactosas unidas a las fucosas mediante enlaces β (1 → 6) y ramificaciones con moléculas de manosas, unidas por enlaces β (1 → 2). De acuerdo a la especie también se encuentran pequeñas cantidades de glucosa, ácidos urónicos y xilosa (Ale et al., 2011; Jiao et al., 2011). El interés por el fucoidan se ha centrado en sus efectos anticoagulantes, antivirales, antinflamatorias, antitumorales, inmunomoduladores y antioxidantes (Pradhan et al., 2020).
Actualmente, el fucoidan se obtiene de las algas pardas de los géneros Ascophyllum, Fucus y Laminaria y se utiliza para estudios dirigidos a aplicaciones farmacéuticas y como suplemento nutracéutico (Li et al., 2021). Al ser una fuente de fucosas, el fucoidan también podría actuar como carbohidrato receptor para diferentes patógenos (Mousavifar & Roy, 2018).
La fucosa (6-desoxi-L-galactosa), es una desoxihexosa funcional que predomina en diversos organismos. Es única por tener una configuración L, diferente al resto de los monosacáridos presentes en los organismos vivos, que es en su forma D (Vanhooren & Vandamme, 1999). La fucosilación consiste en la adición de fucosas, en general terminales, a una cadena de oligosacáridos; la reacción es catalizada por enzimas denominadas fucosiltransferasas (Pekdemir & Karav, 2024). Estos oligosacáridos se conjugan con proteínas y lípidos para formar diferentes glicanos (glicoproteínas, proteoglicanos y glicolípidos) que se expresan en la superficie de las células eucariotas formando una estructura llamada glicocálix (Möckl, 2020).
El glicocálix se relaciona con una serie de eventos celulares fundamentales en la que los carbohidratos actúan como moléculas receptoras para mediar interacciones célula-célula, desarrollo embriogénico, transducción de señales, reconocimiento inmunológico y adhesión celular, entre otros (Möckl, 2020). Además, una gran cantidad de virus, protozoarios y bacterias patógenas de humanos, utilizan el reconocimiento lectina-carbohidrato para infectar a sus hospederos (Behren et al., 2023).
El término lectina se utiliza para definir a una familia heterogénea de proteínas que reconocen y se unen reversiblemente a epítopos estructurales de carbohidratos específicos, sin modificarlos (Lis & Sharon, 1986; Nilsson, 2007). Las lectinas están presentes en todos los reinos biológicos y en los virus. Se encuentran libres o unidas a las superficies celulares y al reconocer a los carbohidratos, también están involucradas en vías de señalización, control de calidad en la biosíntesis de glicoproteínas, desarrollo y crecimiento celular, fertilización e interacciones célula-célula, entre otras (Sharon, 2007; Raposo, Canelas & Barros, 2021).
Algunas lectinas, denominadas adhesinas tipo lectinas, son componentes de las proteínas de adhesión que se expresan en la superficie microbiana. Estas adhesinas son factores de virulencia clave que median la unión de las bacterias a las células hospederas (Abraham, Sharon, Ofek & Schwartzman, 2015). En algunos patógenos, esta unión adhesina-hospedero es el primer paso para la infección (Ielasi et al., 2016; Cho, Park & Kim, 2022). En particular, Pseudomona aeruginosa y Helicobacter pylori expresan adhesinas tipo lectina que reconocen y se unen a los glicoconjugados fucosilados de las mucinas y de las células epiteliales de los tejidos que infectan (Chahal et al., 2022; Mała et al., 2022). En Campylobacter jejuni, se han documentado adhesinas que reconocen carbohidratos complejos, entre los que se encuentran las moléculas fucosiladas (Mahdavi et al., 2014).
Uno de los primeros trabajos que documenta la unión de C. jejuni al intestino a través del reconocimiento de fucosas, es el trabajo de Cinco, Banfi, Ruaro, Crevatin & Crotti (1984), quienes probaron la adhesión de 14 cepas de C. jejuni a líneas celulares intestinales, demostrando que la incubación previa del microorganismo con diferentes cantidades de L-fucosa, inhibe significativamente la adhesión de la bacteria. Esto es un indicio de la presencia de adhesinas específicas para fucosas, en la superficie celular del patógeno.
C. jejuni es el agente etiológico de la campilobacteriosis, la primera causa de diarrea bacteriana a nivel mundial. La incidencia de campilobacteriosis aumenta en el orbe día con día. A pesar de que la infección es autolimitante, puede llegar a causar la muerte de niños de dos años o menores, ancianos y personas inmunocomprometidas (OMS, 2024). Incluso la enfermedad puede complicarse en enfermedades como: la colecistitis, la pancreatitis, la peritonitis y la hemorragia gastrointestinal; también en complicaciones neurológicas, como los síndromes de Guillain-Barré (SGB) y Miller Fisher (Kaakoush, Castaño-Rodríguez, Mitchell & Man, 2015). Aunque la frecuencia de las complicaciones por el SGB es baja, en México se han vinculado las epidemias de esta enfermedad a los brotes de C. jejuni. (Jackson et al., 2014). La más reciente se presentó en el estado de Tlaxcala, con 34 casos clasificados como SGB (Gobierno de México, 2024).
En el futuro próximo, el problema de la campilobacteriosis se agravará debido a la aparición de resistencia y multirresistencia de C. jejuni a los antibióticos, al grado de que la OMS ha clasificado a esta bacteria como un patógeno de alta prioridad, debido a su elevado nivel de resistencia (Portes, Panzenhagen, Pereira dos Santos & Junior, 2023). Por tanto, es importante buscar alternativas a estos tratamientos.
El principio de la glicoterapia se basa en bloquear la unión de las adhesinas tipo lectinas de naturaleza proteica, cuya función aparente es iniciar la infección. La estrategia, como se muestra en la Figura 1, es utilizar moléculas que mimeticen a los receptores celulares y que actúen como anclas o anzuelos para la bacteria, ocupando sus sitios de reconocimiento e impidiendo de esta manera que se unan a las células de su hospedero; estas moléculas se conocen también como antagonistas glicomiméticos (Mousavifar & Roy, 2018). El fucoidan, al ser una estructura fucosilada, tiene potencial de actuar como antagonista glicomimético. Sin embargo, hay que probarlo y una fuente potencial de este polisacárido es S. sinicola, el sargazo mexicano más abundante en el Golfo de California. Por lo anterior, el objetivo de este trabajo fue aislar y realizar un análisis químico al fucoidan de S. sinicola para probar que es reconocido in vitro por Campylobacter jejuni.
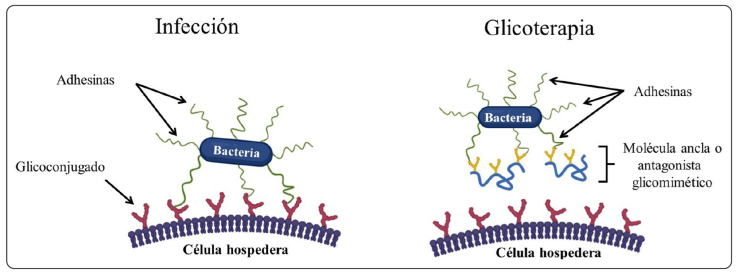
Figura 1 Principio de la glicoterapia para prevenir la infección por bacterias. Modificado de Mahdavi et al. (2014).
Materiales y métodos
Materiales
La cepa utilizada en el presente estudio fue Campylobacter jejuni subsp. jejuni (ATCC 43442) aislada de heces de humano obtenida de la American Type Culture Colection (ATCC) (https://www.atcc.org/products/43442). Se utilizaron fucoidanes grado reactivo de Ascophyllum nodosum, Fucus serratus y Laminaria japonica comprados en Carbosynth (Biosynth, UK). El caldo Brucella para el cultivo de C. jejuni se adquirió en Becton, Dickinson & Company (BD), (Franklin Lakes, NJ, EUA). El sistema generador de gas, las bolsas CampyGen, anaerogen y los clips de sellado para el cultivo de C. jejuni, se obtuvieron en Hardy Diagnostics (Santa María, CA, EUA). El resto de las substancias fueron de grado reactivo y se consiguieron en Sigma-Aldrich (St. Louis, MO, USA).
Recolección y preparación de las algas
Las algas se colectaron durante el mes de junio de los años 2022 y 2023 en dos puntos de la Bahía San Francisco, coordenadas 27.9591° N, 110.9857° O. En cada punto se muestrearon de 20-25 kg de algas a la deriva, se eliminaron epífitas y se identificaron con base en las claves taxonómicas de McCourt (1983) y Norris (2010), se lavaron sumergiéndolas en agua dulce varias veces y se secaron a la sombra durante varios días, hasta que la humedad llegó a ≤ 4 % (método 945.09 de la AOAC, 2000). La presencia de arena remanente se eliminó al tamizar con un colador. En seguida, las algas se molieron en un molino de aspas (Nutribulet Serie 900, Homeland Housewares, LLC, China) y se pasaron por un tamiz de malla 60 para uniformar el tamaño de la partícula. Finalmente se envasaron en recipientes plásticos a 25 °C, hasta su posterior análisis.
Obtención del extracto crudo de fucoidan
El fucoidan se extrajo a partir de 50 g de polvo de alga con el método de Foley, Szegezdi, Mulloy, Samali & Tuohy (2011), con las siguientes modificaciones. Los pigmentos y lípidos se separaron por doble extracción con etanol al 80 % (v/v) durante 12 h a 25 °C. Al término de este periodo se separó la parte sólida mediante centrifugación a 1210 x g durante 20 min, a 4 °C (Sorvall ST 16R, Thermo Scientific, Waltham, MA, USA). El precipitado se utilizó para la extracción de fucoidan, alginato y proteína; el procedimiento se realizó en dos pasos. En el primer paso, se añadieron 100 mL de agua desionizada a 25 °C en agitación moderada, durante 12 h. Posteriormente se centrifugó a 1210 x g durante 20 min, a 4 °C, recuperando el sobrenadante. Al precipitado se le añadieron 100 mL de agua desionizada para realizar la segunda extracción a 70 °C durante 12 h, con agitación moderada, se volvió a centrifugar (1210 x g durante 20 min, a 4 °C) y se recuperó el sobrenadante. Los sobrenadantes de ambas extracciones se mezclaron con agitación leve durante 10 min y posteriormente se precipitaron secuencialmente en el siguiente orden: proteínas, alginato y fucoidan.
Las proteínas se precipitaron con cristales de ácido tricloroacético a concentración final del 10 % (p/v). Después de incubar a 25 °C durante 4 h, fueron separadas por centrifugación a 1210 x g durante 20 min a 4 °C. El alginato presente en el sobrenadante se precipitó con CaCl2 3M, hasta ajustar la concentración final a 2M. La mezcla para su reacción estuvo en agitación moderada a 25 °C durante 5 h, lo siguiente fue separarla a 1210 x g durante 20 min y se liofilizó a -54 °C y 0.1 mbar (Virtis Benchtop, Modelo 2312, NY, USA). El fucoidan contenido en el sobrenadante se obtuvo por precipitación con etanol absoluto frío (4°C), ajustando la concentración al 80 % (v/v) y dejando reaccionar a 4°C durante 12 h. Después se separó por centrifugación a 1210 x g durante 20 min a 4 °C. Al fucoidan obtenido se le estimó el contenido de la proteína para saber qué cantidad no precipitó con el ácido tricloroacético. Esta determinación se hizo por triplicado con el método de Bradford (1976), empleando una curva estándar de albúmina de suero bovino. A continuación, el fucoidan precipitado se liofilizó para producir un extracto crudo de fucoidan (a -54 °C y 0.1 mbar). Los rendimientos se calcularon a partir del peso seco del polvo de alga. Se realizaron diez extracciones independientes.
Características del extracto crudo de fucoidan
El extracto crudo de fucoidan liofilizado se caracterizó analizando el color y los contenidos de carbohidratos totales, fucosa, sulfatos y ácidos urónicos. Además, se llevaron a cabo estudios de dispersión dinámica de la luz (DLS, por sus siglas en inglés), para determinar tamaño de partícula y potencial zeta, y de espectroscopía de infrarrojo con transformada de Fourier en modo de reflectancia total atenuada (FTIR-ATR), para conocer los grupos químicos presentes en la molécula.
Color y carbohidratos totales
El examen de color se hizo por triplicado con un colorímetro Konica Minolta, Modelo CR40/4100 (Konica Minolta, inc., Tokio, Japón). Para cada réplica se realizaron 10 mediciones. Se utilizó el sistema CIELAB, para medir la luminosidad o brillo superficial (*L) y las coordenadas cromáticas (*a y *b); a* es una medida de intensidad del color que va del color rojo +a* (positivo) al verde -a* (negativo); y b* es una medida de la intensidad del color amarillo +b* (positivo) al azul -b* (negativo) (Kumar, Tarafdar, Kumar & Badgujar, 2019).
Los carbohidratos totales se obtuvieron por triplicado con el método colorimétrico del fenol-sulfúrico de DuBois, Gilles, Hamilton, Rebers & Smith (1956), y una curva estándar de glucosa (0-100 µg • mL-1); la absorbancia de las muestras al mezclarlas con fenol al 5 % y H2SO4 concentrado se midió 490 nm en un espectrofotómetro UV-V (CECIL CE 1020, UK).
Concentración de fucosa, sulfatos y ácidos urónicos
La concentración de L-fucosa presente en el extracto de fucoidan se obtuvo a 340 nm con el kit de Megazyme (K-FUCOSE, Megazyme, Bray, Dublín, IE) (https://www.megazyme.com/l-fucose-assay-kit). Se hidrolizaron 5 mL de extracto añadiendo 1 mL de HCl 4M, incubando durante 60 min a 105 °C. En seguida se neutralizó con una solución de NaOH 4 M y se dejó enfriar en baño de hielo para posteriormente hacer la determinación de L-fucosa siguiendo el protocolo del proveedor. La presencia de grupos sulfatos se detectó con el método turbidimétrico de Dodgson & Price (1962), y una curva standard de Na2SO4 (0-10 mg/mL). Previamente el fucoidan liofilizado se disolvió en una solución de HCl 1M ajustando la concentración a 2.5 mg. mL-1 para dejarlo hidrolizar durante 5 h a 105 °C. El hidrolizado (50 µL), se mezcló con 250 μL de reactivo de cloruro de bario-gelatina [0.5% (p/v) de gelatina y 0.5 % (p/v) de BaCl2] y 950 μL de ácido tricloroacético al 3% (p/v) y se incubó 15 min a 25 °C para formar BaSO4. Posteriormente se midió la turbidez a una absorbancia de 360 nm. Como control se utilizó solución de gelatina (0.5% (p/v) en ausencia de BaCl2.
El contenido de ácidos urónicos se obtuvo por colorimetría, con base en Blumenkrantz & Asboe-Hansen (1973), empleando una curva estándar de ácido galacturónico (0- 80 µg/mL). En un baño de hielo se agregaron 3 mL de solución 50 mM de Na2[B4O5(OH)4]·8H 2O en H2SO4 concentrado, en seguida se añadió un mL de extracto de fucoidan frío a concentración de 100 µg • mL-1 y se incubó a 100 °C por 5 min para promover su hidrólisis. Posteriormente se generó la reacción colorimétrica al agregar 100 μL de 3-fenilfenol al 0.15% (p/v) en NaOH al 0.5% (p/v), se incubó por 4 min para posteriormente detectar la señal a una absorbancia de 520 nm. Las pruebas se realizaron por triplicado.
Dispersión dinámica de la luz y espectroscopía de infrarrojo
Los estudios de DLS se efectuaron en el extracto crudo liofilizado de fucoidan disuelto en agua desionizada a una concentración de 1 mg/mL, se midió el tamaño de la partícula (dm; diámetro medio) y el potencial zeta (z, mV) con un ángulo de dispersión de 90° en un equipo Zetasizer Nano ZS 90 (Malvern instruments Ltd., Malvern RU. Los ensayos se realizaron por triplicado a 25 °C y un índice de refracción de 1.33.
Los estudios de FTIR-ATR se realizaron en un espectroscopio de infrarrojo Cary 630 FTIR (Agilent, Santa Clara, CA, USA) en un rango espectral de 4000 a 650 cm-1 con una resolución de 4 cm-1. Se tomaron tres lecturas independientes para cada tratamiento y el aparato programado para realizar 40 corridas por réplica. Los espectros de cada tratamiento se adquirieron graficando el número de onda (cm-1) contra el promedio de las absorbancias (unidades arbitrarias), empleando el software SigmaPlot versión 11.0 (Systat, software, Inc., San José, CA, USA).
Cultivo de Campylobacter jejuni
La cepa de C. jejuni (ATCC 43442) se sembró en caldo Brucella (Franklin Lakes, NJ, EUA). Después, se incubó a 37- 42 °C durante 48 h en las siguientes condiciones de microaerobiosis: 10% CO2, 5% O2, 85% N2 (Erkmen, 2022). Para crear la atmósfera adecuada se empleó un sistema generador de gas, bolsas de cierre hermético CampyGen, anaerogen y clips de sellado para el cultivo de C. jejuni (Santa María, CA, EUA).
Las células bacterianas de Campylobacter jejuni, se recuperaron centrifugando a 1210 × g durante 15 min a 4 °C y se lavaron dos veces con solución salina amortiguadora de fosfatos (PBS; pH 7.4 ± 0.2 M). En seguida, la cepa se suspendió en PBS con el ajuste de la absorbancia a 0.6 (~ 1 x 10 8 UFC/mL) a 600 nm.
Biotinilación de fucoidan
Con este procedimiento se conjugó al fucoidan de S. sinicola con la molécula de biotina como un paso previo a los experimentos de reconocimiento de C. jejuni. Para efectos de comparación, también se conjugaron fucoidanes de: Ascophyllum nodosum, Fucus serratus y Laminaria japonica. La biotinilación se llevó a cabo de acuerdo con Sostaric, van de Lest, Colenbrander & Gadella (2005) y Miyazaki et al. (2019). Para ello, se disolvieron 10 mg de fucoidan en 200 μL de agua desionizada, se agregaron 50 μL de NaIO4 (100 mM, CH3COONa, pH 5.5) incubándose durante 15 min a 25 °C, en seguida se eliminó el exceso de NaIO4 pasando la mezcla en una columna de desalación PD-10 (Cytiva) acondicionada con CH 3COONa, 100 mM, pH 5.5. Al fucoidan eluido de la columna, se le agregó biotina-hidrazida (Sigma-Aldrich, B7639) hasta una concentración final de 5 mM y se incubó durante 2 h a 25 °C en oscuridad; al término, se eliminó la biotina-hidrazida no conjugada en una columna de desalación PD-10. El fucoidan-biotinilado se congeló a -40 °C y se liofilizó a -54 °C y 0.1 mbar (Virtis Benchtop, Modelo 2312, NY, EUA) para análisis posteriores.
Ensayo con lectinas similar a ELISA
El reconocimiento del fucoidan de S. sinicola por C. jejuni ATCC 43442 se analizó mediante ensayos con lectinas similares a ELISA (ELLAS, por sus siglas en inglés), de acuerdo con Sandoval-Larios et al. (2023), con las siguientes modificaciones: se ajustó una suspensión bacteriana de C. jejuni en PBS a 0.6 unidades de absorbancia a 600 nm (~108 UFC/mL), seguida de una inmovilización de las bacterias con glutaraldehído al 1 % durante 1 h a 25 °C, en placas de ELISA de 96 pozos (Costar, 3590, Corning, EUA). Se realizaron tres lavados con PBS pH 7.4 con CaCl2 y MgCl2 para eliminar a las bacterias no inmovilizadas. A continuación, se bloquearon las interacciones no específicas con albúmina sérica bovina al 1.5% durante 24 h a 4 °C. Al término de este tiempo, se hicieron tres nuevos lavados con PBS (CaCl2 y MgCl2, pH 7.4), para eliminar la albúmina que no reaccionó. Posteriormente las bacterias se incubaron individualmente con 40 μg/mL de los diferentes fucoidanes-biotinilados durante 2 h a 25 °C en oscuridad. Después de tres nuevos lavados con PBS (CaCl2 y MgCl2, pH 7.4), las placas se incubaron con avidina-peroxidasa (1:1000, v/v) durante 1 h a 25 °C y se lavaron nuevamente con PBS (CaCl2 y MgCl2, pH 7.4). A continuación, se usó O-fenilendiamina (OPD sigmafast, P9187 Sigma Aldrich, EUA) para detectar la adhesión bacteriana a los diferentes fucoidanes leyendo las absorbancias a una longitud de onda de 450 nm, en un lector de ELISA (Anthos Zenyth 340ST, ESP). En la Figura 2 se presenta el principio del ensayo. Los análisis se hicieron por duplicado con 16 observaciones por réplica.
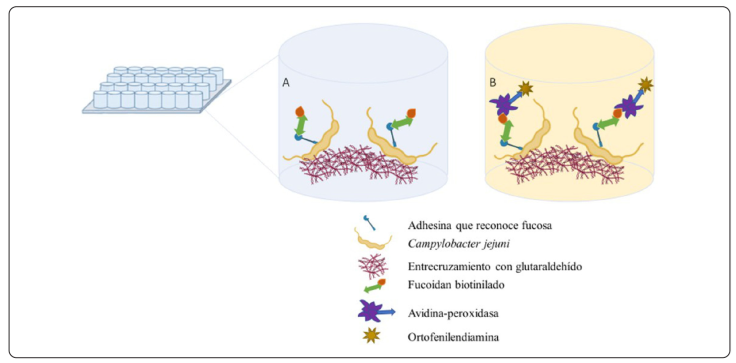
Figura 2 Principio del ensayo con lectinas similar a ELISA. A). la bacteria se entrecruza con la superficie utilizando glutaraldehído. Esto evita su desprendimiento de la caja. Posteriormente se incuba con el polisacárido biotinilado. B). Después de eliminar el polisacárido que no interaccionó, se incuba con avidina-peroxidasa, se lava y se revela la interacción con diaminobencidina midiendo la intensidad de la reacción a 450 nm.
Análisis estadístico
Los análisis fisicoquímicos y de dispersión dinámica de la luz se llevaron a cabo por triplicado reportándose la media y desviación estándar de los mismos. Los ensayos de ELLA se hicieron por duplicado con 16 observaciones por réplica. Se les aplicó un análisis de varianza utilizando la prueba de Tukey-Kramer para detectar diferencias significativas (p>0.05).
Resultados y discusión
Obtención y caracterización del extracto crudo de fucoidan
El fucoidan de S. sinicola se obtuvo por extracción acuosa a diferentes temperaturas. Posteriormente, las moléculas que se solubilizaron durante el procedimiento se precipitaron con etanol frío y se volvieron a suspender en agua para precipitar a las proteínas con ácido tricloroacético, al alginato con cloruro de calcio y al fucoidan con etanol frío. El contenido de alginato fue del 20.3 ± 1.6 %; estos valores son similares (~18- 21.4 %) a los obtenidos por Di Filippo-Herrera, Hernández-Carmona, Muñoz, Arvizu-Higuera & Rodríguez-Montesinos (2018) para S. horridum de Bahía de la Paz, Baja California, entre los meses de mayo y junio y mayores a los reportados (~ 13.7 %) por Rodríguez-Montesinos, Arvizu-Higuera & Hernández-Carmona (2008), para S. sinicola, colectado en Bahía de la Paz durante la primavera. De acuerdo con Rodríguez-Montesinos et al. (2008) la mejor estación para tener una mayor cantidad de alginato de S. sinicola es durante la primavera. En este periodo se lleva a cabo la maduración del alga, aumenta el contenido de este polisacárido, tanto en la matriz como en la pared celular. Sin embargo, las condiciones geográficas y ambientales varían en los diferentes puntos del Golfo de California, por lo que es necesario realizar un estudio sobre las variaciones estacionales y otros factores ambientales, que influyen en el contenido de alginato en S. sinicola de las playas de Sonora. La cantidad de fucoidan crudo fue de 3.1 ± 0.29 %; ésta varía de acuerdo a la especie de sargazo, según lo reportado, desde 1.35 % para S. wightii hasta 26 % para S. filipendula (Sharmila, Sheba & Ilakkia, 2019; García-Ríos, Ríos-Leal, Robledo & Freile-Pelegrin, 2012). No se encontraron datos para S. sinicola, aunque los resultados son similares a los encontrados para S. hystrix, S. vulgare y S. ilicifolium (Turan, 2017; Tsou, Lee, Wu, Lee & Lin, 2022) . Otras variaciones en composición son estacionales, como lo establecieron Di Filippo-Herrera et al. (2018), al encontrar contenidos de fucoidan de 6.8 a 13.5 % para S. horridum. El método de extracción también influye; por lo general se obtienen menores rendimientos con el método acuoso que se utilizó en nuestro trabajo, aunque el contenido de impurezas es menor (Sharmila et al., 2019; Husni, Izmi, Ayunani, Kartini, Husnayain & Isnansetyo, 2022). Uno de los contaminantes que puede estar presente en el extracto crudo es la proteína que no precipitó, a pesar del tratamiento con ácido tricloroacético. En este estudio se estimaron 15.7 mg de proteína (1.02 %) presentes en el extracto crudo de fucoidan, con el método de Bradford (1976). Esta concentración es menor a los valores encontrados por Wang & Chen (2016), quienes al analizar el fucoidan extraído de diferentes especies de sargazos encontraron concentraciones de proteína muy cercanas al 3 %.
Caracterización del fucoidan crudo
Color
La Figura 3 muestra el aspecto del fucoidan extraído y liofilizado; éste coincide en apariencia con diferentes extractos comerciales. El color marrón se debe a la presencia residual de pigmentos presentes en el alga, específicamente fucoxantina y compuestos polifenólicos, como los florotaninos de tipo floroglucinol, que están fuertemente unidos de forma no covalente al fucoidan (Zayed, El-Aasr, Ibrahim & Ulber, 2020). Los valores de L* se encontraron en el rango de 55.57 a 59.53; L* mide la luminosidad del producto en un rango de 0 (negro) a 100 (blanco). Por ejemplo, el color del polvo de cocoa muestra valores de L* entre 22.0 y 33.8, dependiendo del método de alcalinización respecto al de azúcar de coco, entre 53.4 y 63.6 (Trinidad et al., 2015; Puchol-Miquel et al., 2021). El parámetro a* presentó valores positivos, indicativo del predominio de los colores rojos sobre los verdes; los valores de b* también fueron positivos, con prevalencia de las tonalidades amarillas sobre los colores azules.
Características fisicoquímicas
La Tabla I muestra las características fisicoquímicas del fucoidan de S. sinicola. En este trabajo se encontró una concentración de carbohidratos de 32.1± 2.25, menor a la reportada para otros sargazos colectados en la Península de Baja California como S. horridum y S. herphorizum y similar a la encontrada para S. wightii (Di Filippo-Herrera et al., 2018; Kumar, Sahoo & Levine, 2015). El contenido de carbohidratos en el fucoidan de sargazo varía entre 23 y 43 % (Husni et al., 2022). Estas diferencias se ven influidas por la especie, la etapa de crecimiento del alga y, el método de extracción utilizado. Husni et al. (2022) y Sharmila et al. (2019) obtuvieron mayores contenidos de carbohidratos en S. hystrix y S. wightii, al aplicar extracciones acuosas y precipitación con etanol (como es el caso de este estudio), en comparación con los métodos en presencia de ácidos o de diferentes sales. Esto se debe a la gran solubilidad del fucoidan en agua y a la capacidad de los carbohidratos de precipitar en presencia del etanol.
Tabla I Rendimiento y características fisicoquímicas del extracto de fucoidan obtenido de S. sinicola. (Media ± Desv. Std.).
| Análisis | (%) |
|---|---|
| Contenido de fucoidan | 3.1 ± 0.29 |
| Carbohidratos | 32.1± 2.25 |
| Fucosa | 16.8 ± 0.46 |
| Sulfatos | 14.2 ± 1.2 |
| Ácido urónico | 6.8 ± 0.02 |
Los contenidos de fucosa (16.8 ± 0.46 %) y de sulfatos (14.2 ± 1.2 %), encontrados en nuestro estudio, fueron similares a los de S. wightii y menores a los de S. hystrix, con el mismo método de extracción para obtener al fucoidan. El fucoidan de otros géneros y especies de algas pardas presenta mayor contenido de fucosa y de sulfatos. Por ejemplo, el contenido de fucosa varía entre 18.0-28.0 %, 26.0-39.0 % y 35.0-46.0 % en peso y el contenido de sulfato entre 30.0-40.0 %, 9.0-35.0 % y 6.0-22.0% en peso para Fucus serratus, F. vesiculosus y Ascophyllum nodosum, respectivamente (Fletcher, Biller, Ross & Adams, 2017).
La cantidad de ácidos urónicos presentes en el fucoidan fue cercana al 7 %. Esto es importante debido a que contenidos muy altos pueden evidenciar una contaminación con alginato, que está compuesto por los ácidos manurónico y gulurónico. Sin embargo, algunos fucoidanes, además de fucosas, contienen pequeñas cantidades de ácidos urónicos y de otros monosacáridos como galactosa, xilosa, glucosa o ramnosa. El tipo de monosacáridos y su concentración, depende de la especie de alga de donde se extrae el fucoidan (Ponce & Stortz, 2020). En el género Sargassum se ha cuantificado la presencia del ácido urónico en S. henslowianum (10.8-14.5 %) y S. ilicifolium (11. 7%); además de la evidencia de su presencia en S. hystrix, utilizando FTIR (Husni et al., 2022; Li et al., 2021; Lakshmanan et al., 2022).
Dispersión dinámica de la luz y espectroscopía de infrarrojo
La Tabla II muestra el potencial z, el tamaño de partícula y el índice de polidispersidad del fucoidan de S. sinicola, comparándolo con otros fucoidanes comerciales grado reactivo. La carga superficial de este fucoidan fue menor a la del resto de los fucoidanes. Esto puede deberse al grado de sulfatación de la molécula, que varía entre géneros y aun entre especies Blanco-Pascual, Montero & Gómez-Guillén, 2014). El tamaño de partícula fue similar al de los otros fucoidanes. Sin embargo, en todos los casos se observaron diferentes poblaciones con tamaños mayores, lo que explica su alto índice de polidispersidad.
Tabla II Potencia zeta, tamaño de partícula e índice de polidispersidad de S. sinicola. (Media ± Desv. Std.)
| Especie | Potencial zeta (mV) | Tamaño (nm) | Índice de polidispersidad |
|---|---|---|---|
| Sargassum sinicola | -23.5 ± 0.10 | 117.3 ± 34.7 | 0.80 ± 0.21 |
| Ascophyllum nodosum | -66.6 ± 0.48 | 99.87 ± 0.91 | 0.32 ± 0.04 |
| Fucus serratus | -52.9 ± 3.60 | 101.1 ± 20.44 | 0.44 ± 0.03 |
| Laminaria japonica | -62.1 ± 2.54 | 105.5 ± 3.50 | 0.40 ± 0.08 |
La diversidad de tamaños puede deberse tanto a los métodos de obtención del polisacárido como a las funciones biológicas de este carbohidrato. El fucoidan participa en la síntesis de la pared celular de las algas pardas, al impartir soporte y estructura a este organismo y lo protege de la desecación (Ponce & Stortz. 2020; Zayed et al., 2020). Además, es componente de las esporas y previene la liberación prematura de los gametos femeninos; cuando estos se encuentran listos, las fucosidasas los degradan en diferentes tamaños de partículas (Skriptsova, 2015). No se encontraron datos publicados, para comparar estos resultados.
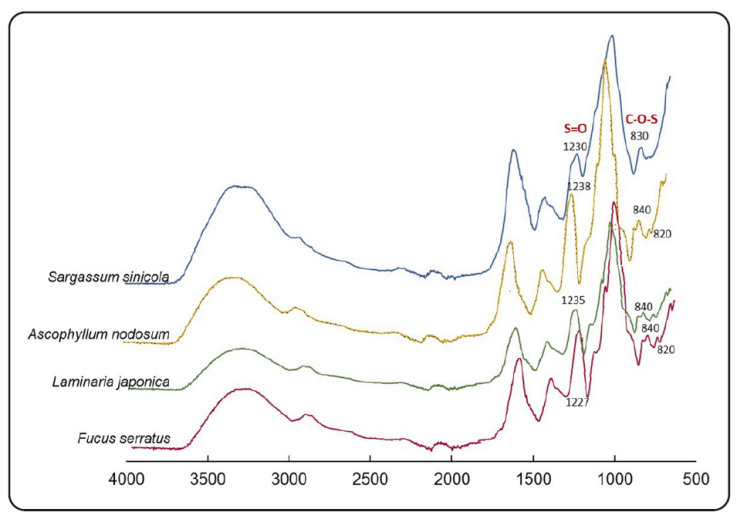
En la Figura 4b se muestra el espectro típico del extracto crudo del fucoidan de S. sinicola. El patrón del espectro fue similar al reportado para Sargassum binderi por Saepudin, Sinurat & Suryabrata (2018). Se observó una banda ancha entre los 3000 y 3500 cm-1 con valor máximo a los 2395 cm-1. Esta señal corresponde a los grupos OH, que en los polisacáridos son muy abundantes por ser moléculas de naturaleza polihidroxílica. El pico observado a los 2890 cm-1 se atribuye a los grupos C-H, provenientes de estructuras carbonadas. La sección más interesante corresponde a la huella dactilar de los carbohidratos cuyas señales estructurales están presentes en la región de 2000 a los 800 cm-1. La banda a 1610 cm-1 se asocia con el grupo C=O, del ácido urónico presente en pequeñas cantidades en algunos fucoidanes (Cid, Ortiz, Pizarro & Moreno-Piraján, 2020). Lo anterior concuerda con el análisis fisicoquímico. La banda en el número de onda 1419 cm-1 corresponde a los grupos carboxilo (COOH), mayoritariamente disociados en forma de carboxilato simétrico (-COO-) (Blanco-Pascual et al., 2014). La señal detectada a los 1230 cm-1 es característica del fucoidan, ya que se asocia a la extensión del enlace S=O de los grupos sulfatados que modifican a algunas de sus fucosas. La señal cercana a los 1000 cm-1 se atribuye a los enlaces glucosídicos típicos de los polisacáridos; la vibración de flexión del enlace C-O-S registrada a los 830 cm-1 indica que la modificación con grupos sulfato se encuentra principalmente en el C4 (Marais & Joseleau, 2001).
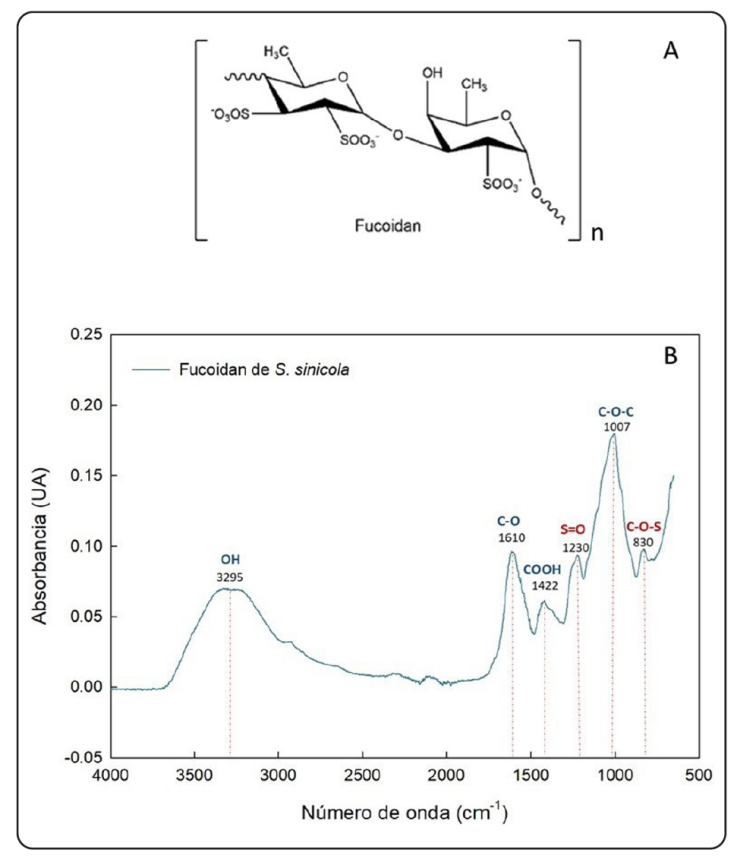
Figura 4 Espectro infrarrojo típico con transformada de Fourier del fucoidan de Sargassum sinicola. A). Unidades repetidas del fucoidan (fucosas) que muestran la presencia de grupos sulfatos característicos de esta molécula. B). Espectro FTIR-ATR del fucoidan, en color rojo se resaltan los grupos sulfatos.
La Figura 5 muestra los espectros del fucoidan y del alginato obtenidos en este estudio. La principal diferencia entre estos, es que en el alginato no se observa la señal característica de los grupos S=O (1230 cm-1) y C-O-S (830 cm -1). Por otro lado, la señal del alginato, emitida a los 812 cm-1, se atribuye al ácido poligulurónico (Mollah, Faruque, Bradley, Khandaker & Assaf, 2023). En la Figura 6 se aprecia una comparación entre los espectros de los diferentes fucoidanes. Aunque en los espectros se ven las diferencias relacionadas con su composición, en todos se observa la señal producida por los grupos S=O, si bien, con diferentes corrimientos. Para el caso de los fucoidanes comerciales la vibración de flexión del enlace C-O-S quedó registrada en los 820 y los 840 cm-1. Esto sugiere un patrón complejo de sustitución, mayoritariamente en la posición en C-4 (sustitución axial del ligando α de L-fucopiranosa) con otras sustituciones en C-2 o/y C-3 (posiciones ecuatoriales) en menor cantidad. Esta característica ha sido observada con anterioridad en el fucoidan de A. nodosum (Marais & Joseleau, 2001).
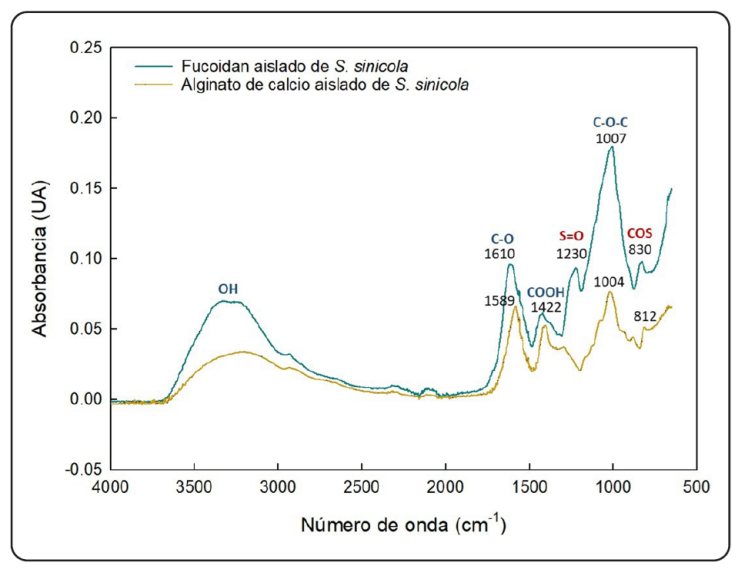
Figura 5 Comparación entre los espectros de infrarrojo del alginato y fucoidan, extraídos de Sargassum sinicola.
Reconocimiento del fucoidan de Sargassum sinicola por Campylobacter jejuni
Las bacterias enteropatógenas representan un problema de salud pública a nivel mundial, principalmente aquellas que son zoonóticas, se transmiten por el consumo de alimentos contaminados y causan diarrea. De acuerdo con la Organización Mundial para la Salud las enfermedades diarreicas, entre las que se encuentra la campilobacteriosis, producen alrededor de 550 millones de casos anuales, la mitad afecta a niños menores de cinco años, con riesgo a su vida. Debido a su alcance mundial, las enfermedades diarreicas representan una carga económica y social importante, causando una pérdida global de 33 millones de años de vida saludable (OMS, 2024). El problema se agrava con la aparición de resistencia bacteriana a los antibióticos, debida al mal uso de estos fármacos. Lo anterior nos lleva a la búsqueda de otras estrategias, además del uso de antibióticos, para combatir a los patógenos. Una de estas estrategias es el uso de moléculas anclas o antagonistas glicomiméticos (Figura 1).
La adhesión de los patógenos entéricos a las células intestinales es un requisito previo a la infección y en muchos casos está mediada por reconocimientos proteína-carbohidrato. En este tipo de interacciones las adhesinas tipo lectina, expresadas en la superficie microbiana se unen específicamente a “carbohidratos complementarios”, presentes en la membrana plasmática de las células que van a infectar (Kato & Ishiwa, 2015). La adhesión de C. jejuni a las células de su hospedero es fundamental para la persistencia y colonización de los enterocitos y posiblemente para la posterior invasión de estos, por tanto, es fundamental conocer las interacciones que se establecen entre el patógeno y su hospedero, para poder controlarlo (Sabotič, Janež, Volk & Klančnik, 2023). A la fecha no se ha encontrado una adhesina tipo lectina específica para fucosa en C. jejuni (Sabotič et al., 2023). Sin embargo, existe evidencia de su presencia. Cinco et al. (1984) probaron que la presencia de fucosa inhibe la unión de C. jejuni a líneas celulares intestinales en modo de concentración dependiente. Ruiz-Palacios, Cervantes, Ramos, Chavez-Munguia & Newburg (2003) demostraron que los oligosacáridos fucosilados de la leche humana inhiben la adhesión de C. jejuni a células epiteliales humanas Hep-2, a células de ovario de hámster chino transfectadas con fucosiltransferasas y a tejido de íleon humano ex vivo. Por otro lado, Day et al. (2009) descubrieron que C. jejuni se une a glicanos fucosilados, cuando se cultiva en condiciones que imitan a los hospederos mamíferos y a los aviares. Con base en lo anterior se realizó una prueba in vitro para determinar si esta bacteria reconoce a las estructuras fucosiladas del fucoidan de S. sinicola.
Como se observa en la Figura 7, el fucoidan de S. sinicola fue reconocido con mayor afinidad (p < 0.05) que el resto de los fucoidanes probados. Estos resultados pueden deberse a un menor grado de sulfatación en el fucoidan del sargazo. Una evidencia de lo anterior es la menor carga eléctrica negativa que presentan con respecto a la carga de los otros fucoidanes (Tabla II). Por otro lado, la interacción lectina-carbohidrato es muy específica y la presencia de grupos sulfatos de los otros fucoidanes puede interferir en el sitio de reconocimiento. Este es un hallazgo importante, ya que la mayoría de las otras bioactividades del fucoidan (antinflamatorias, antihipertensivas, anticancerígenas) están relacionadas con la carga que imparten los grupos sulfato a su molécula (Ale et al., 2011). Para el caso del fucoidan de S. sinicola una alternativa de uso podría ser el diseño de antagonistas glicomiméticos para aprovechar sus estructuras fucosiladas no sulfatadas.
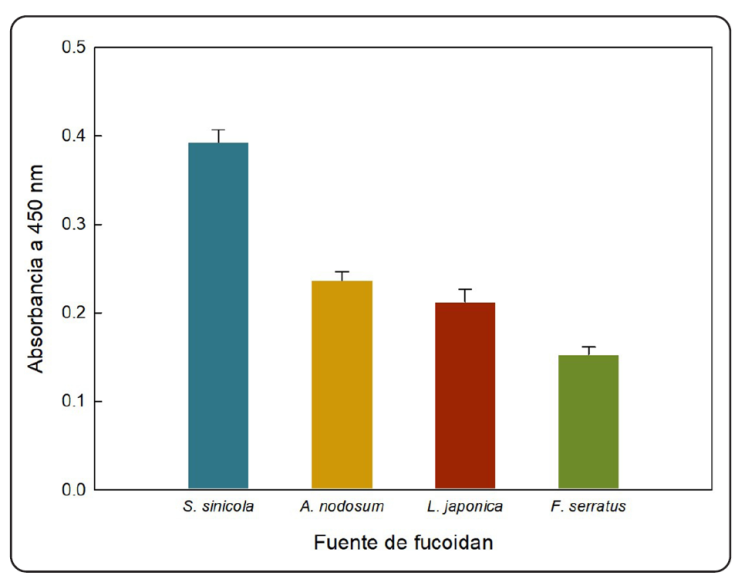
Figura 7 Comparación del reconocimiento biológico de diferentes fuentes de fucoidan por Campylobacter jejuni.
El fucoidan certificado de alta pureza es un ingrediente generalmente reconocido como seguro (GRAS, por sus siglas en inglés), soluble en agua y fácil de formular. Puede incluirse en tabletas, geles, aerosoles, cápsulas y polvos a granel. Actualmente se utiliza en suplementos alimenticios y nutracéuticos encaminados a la promoción de la salud y el bienestar (Mensah, Kanwugu, Panda & Adadi, 2023). Al ser reconocidas por C. jejuni, las moléculas de fucoidan actuarían como “trampas señuelo” para evitar la adhesión del patógeno al intestino, ya sea a través de interacciones lectina-carbohidrato, o de otros mecanismos relacionados con la utilización de la fucosa por C. jejuni. Por ejemplo, los monómeros de fucosa y los glicanos fucosilados servirían como quimio-atrayentes para dirigir a la bacteria a su sitio de infección (Hugdahl, Beery & Doyle, 1988). Por tanto, también es probable que las proteínas de C. jejuni involucradas en la quimiotaxis de la fucosa sean, al menos en parte, responsables de la unión de C. jejuni a las estructuras fucosiladas presentes en el glicocálix (Hugdahl et al., 1988; Stahl et al., 2011; Kemper & Hensel, 2023) . Este sistema quimiosensorial es un componente esencial de la motilidad dirigida de la bacteria hacia sus sitios de unión en el intestino (Kemper & Hensel, 2023). En este sentido, el patógeno también sería atraído hacia el fucoidan, por tener enzimas quimio-receptoras que detectan la fucosa. Otra posibilidad en estudio es que la molécula señuelo sea atraída hacia enzimas relacionadas con el metabolismo de la fucosa (Garber, Hennet & Szymanski, 2021).
C. jejuni ha sido considerada durante mucho tiempo una especie asacarolítica, que utiliza principalmente aminoácidos como fuente de carbono (Stahl et al., 2011) Sin embargo, está documentado que varias cepas de esta bacteria metabolizan a la fucosa (van der Hooft et al., 2018; Muraoka Wayne & Zhang, 2011). Basado en lo anterior, el fucoidan podría actuar como molécula señuelo para las enzimas responsables del metabolismo de la fucosa. Sin embargo, son necesarios estudios complementarios para conocer si estas enzimas degradan al fucoidan a fucosas libres, ya que se ha observado una supervivencia mejorada y una morfología pro-infectiva espiral prolongada en las cepas que utilizan la fucosa (van der Hooft et al., 2018; Middendorf, Jacobs-Reitsma, Zomer, den Besten & Abee, 2022).
La fucosa es un componente común presente en las mucinas y los enterocitos a las que se une el patógeno; existe evidencia de una ventaja en la colonización intestinal de lechones neonatales por el uso de fucosa (Muraoka Wayne & Zhang, 2011; Stahl et al., 2011). Day et al. (2009) descubrieron que C. jejuni se une a glicanos fucosilados cuando se cultiva en condiciones que imitan a los hospederos mamíferos y aviares. En contraste, la unión a fucosas disminuye considerablemente cuando la bacteria se cultiva en condiciones que simulan el estrés ambiental al que el patógeno se enfrenta fuera de los organismos que infecta. Lo anterior sugiere la posible expresión de una lectina que reconoce fucosas durante el proceso de infección (Jug et al., 2024; Day et al., 2009).
Los estudios realizados al momento muestran que el reconocimiento de fucosas por C. jejuni representa un factor central para la colonización efectiva, la invasión posterior y la persistencia de la bacteria. A pesar de que se requieren estudios posteriores para comprender mejor los mecanismos de reconocimiento bacteria-fucosa, queda claro que el uso de moléculas señuelo que mimeticen a la fucosa tiene gran potencial en el tratamiento temprano de la campilobacteriosis.
Conclusiones
El rendimiento del fucoidan extraído de Sargassum sinicola fue de 3.1 ± 0.29, similar al contenido encontrado en otras especies del mismo género. La afinidad con que este fucoidan fue reconocido por Campylobacter jejuni fue mayor, comparada con la afinidad con que fueron reconocidos los fucoidanes de Ascophyllum nodosum, Fucus serratus y Laminaria japonica, lo que destaca su potencial como antagonista glicomimético para combatir la campilobacteriosis.











 nova página do texto(beta)
nova página do texto(beta)