Introducción
En México, los bosques de pino-encino tienen alta importancia ecológica para los ecosistemas templados debido a su alta diversidad y amplia distribución de especies (Méndez Osorio et al., 2018). Los encinos son un componente que destacan en los ecosistemas forestales por la gran cantidad de funciones ecosistémicas que desempeñan, como la conservación del suelo y el agua, regulación del clima, provisión de alimento y hábitat a una amplia variedad de fauna silvestre; además, son especies adecuadas para recuperar sitios degradados (Sánchez-González, 2008). También, ocupan el segundo lugar nacional en aprovechamiento forestal, principalmente para la producción de carbón y la construcción de vivienda (Hernández Quiroz & Badano, 2017); sin embargo, se carece de programas integrales para su aprovechamiento.
La Sierra Madre Occidental posee una de las mayores riquezas de diversidad biológica, los bosques de encino cubren casi el 14 % de la superficie, y alberga 54 especies del género Quercus (34 % del total nacional) (González-Elizondo et al., 2012). En los últimos 15 años se han realizado diversos estudios sobre la ecología de encinos, enfocados principalmente a investigar su diversidad, estructura, caracterización, distribución y composición florística (Aguilar-Romero et al., 2016; Block & Meave, 2015; Bravo-Bolaños et al., 2020; Encina-Domínguez et al., 2011; Olvera-Vargas & Figueroa-Rangel, 2012; Rosaliano Evaristo et al., 2022; Rubio-Licona et al., 2011; Ruiz-Aquino et al., 2015; Sabás-Rosales et al., 2015), pero existen otros campos del conocimiento pocos explorados, como su fenología.
La fenología de las plantas describe los periodos de aparición y duración de las diferentes etapas en el ciclo de vida, como brotación, floración, fructificación y foliación durante el año (Saveanu & Murray, 2014), procesos relacionados directamente con los factores ambientales, esenciales para entender las interacciones entre las plantas, los animales y el medio ambiente (Maldonado, 2011). La temporalidad y distribución de la floración y fructificación de las plantas son importantes, porque favorecen la biodiversidad, la disponibilidad de alimento para la fauna, la regeneración de la vegetación, la adaptación y la permanencia de las especies (Zárate Cuevas et al., 2022).
Las especies arbóreas han implementado estrategias de adaptación a las variaciones climáticas a través del desarrollo de sus estructuras vegetativas y reproductivas (Zárate Cuevas et al., 2022); por ejemplo, la temperatura, la irradiancia, la precipitación y el fotoperiodo son desencadenantes de la brotación en algunas especies de árboles, las cuales pueden variar dependiendo de las especies, provocando que se adelante o se atrase alguna fenofase (Tang et al., 2016), como sucede en el género Quercus, sensible a las señales ambientales en los patrones fenológicos, como la formación de hojas, la floración y el crecimiento vegetativo (Gerst et al., 2017); por ello, son considerados como un grupo altamente susceptible al cambio climático (Hernández Quiroz & Badano, 2017).
En encinos, la formación de frutos está relacionada con aves y mamíferos que se alimentan de ellos a través de las bellotas y las dispersan, por lo que es importante conocer el periodo que comprenden esta fase (Ramírez-Martínez & Mondragón Chaparro, 2020), debido a que la duración de la fructificación varía ampliamente entre especies y entre años (Gallinat et al., 2018), es importante conocer con precisión cuándo existe suficiente disponibilidad de semillas en cantidad y calidad para su recolección, antes de que sean consumidas por la fauna silvestre, ya que aproximadamente el 99 % son depredadas (Díaz-Pontones & Reyes-Jaramillo, 2009). Lo anterior permite planificar de mejor manera su colecta para reproducirlas en vivero con el fin de cubrir programas de restauración, reforestación y conservación forestal (Rivas Romero et al., 2021).
El objetivo de la presente investigación fue describir la fenología inicial de Quercus durifolia Seemen ex Loes., especie que se distribuye principalmente en zonas de transición de la Sierra Madre Occidental. La generación de información en este ámbito contribuirá a la recolección oportuna de semilla, para su posterior propagación en viveros y así obtener plantas de calidad para programas de reforestación y restauración forestal.
Materiales y métodos
Área de estudio
El estudio se realizó en el ejido Otinapa, municipio de Durango, Durango, México, en las coordenadas 24°03’27” N y 105°00’54” O, a una altitud de 2.397 m. La vegetación que predomina está compuesta por especies del género Pinus (P. engelmannii Carr., P. leiophylla Schiede ex Schltdl. & Cham., P. cooperi C.E. Blanco y P. teocote Schltdl. & Cham.), Quercus sp., Juniperus sp., así como Arbutus sp. (González-Elizondo et al., 2012); el sitio se ubica en medio de un bosque de transición de zonas semiáridas a un bosque de clima templado (Figura 1).
El clima es marcadamente estacional, con una estación fría que comprende los meses de octubre a marzo, y una estación calurosa de abril a septiembre, con un período con precipitación baja o escasa de diciembre a junio; la temporada de lluvias ocurre entre julio y septiembre, y en ocasiones se alarga hasta noviembre, con su pico máximo en julio. Para el presente estudio los datos de temperatura y precipitación, correspondiente al período 2010 a 2023, fueron obtenidos de la página web Climate Explorer (https://climexp.knmi.nl/start.cgi) y extraídos a una resolución de 0.5° de la base de datos CRU TS v. 4.04.
Selección de árboles monitoreados
En un rodal natural se seleccionaron al azar seis árboles de Quercus durifolia, buscando que existiera una distancia mínima de 50 m entre sí; los mismos se numeraron del uno al seis, a cada uno se les escogieron seis ramas con presencia de yemas, ubicadas entre la parte media y baja de la copa, por la facilidad del seguimiento del proceso fenológico y considerando que los encinos tienen estructuras reproductivas en toda la copa del árbol (Figura 2). En promedio, los árboles tenían una altura de 12.5 m y un diámetro a la altura del pecho de 36.3 cm.
Las observaciones del estadío fenológico se realizaron cada 15 días, a partir de la visualización de las estructuras reproductivas en las yemas (inicio de la floración), las observaciones se hicieron cada cinco días hasta que las estructuras femeninas dejaron de recibir polen e inició el crecimiento de la bellota; lo anterior, se realizó mediante observaciones directas y toma de imágenes fotográficas; esto permitió que de cada árbol se pudiera determinar: periodo de caída de hojas, de brotación y de floración masculina y femenina, fecha de inicio y desarrollo de bellotas, tiempo durante el cual ocurrió el crecimiento de las hojas y ramas, y período de aparición de nuevas yemas y de dispersión de bellotas.
El trabajo se realizó mediante una descripción de las etapas fenológicas señalando el tiempo de inicio y el final de cada fenofase de los árboles monitoreados; además, se realizó una comparación del desarrollo de las fenofases con relación a los elementos climáticos a través del tiempo (Mejía Gutiérrez, 1990). El periodo de seguimiento se hizo de marzo a noviembre de 2023. Debido a que este trabajo fue descriptivo, solo se registraron observaciones directas en forma periódica, mediante imágenes y registro de los tiempos en que ocurrió cada fenofase; además, se cuidó que el registro de la información fuera representativo de la especie evaluada.
Resultados y discusión
Calendario fenológico
Durante el periodo 2010 a 2023, el promedio en la precipitación anual fue 616 mm, siendo el año 2011 el de menor precipitación (251 mm) y 2021 el que tuvo la mayor cantidad de lluvia (839 mm); la temperatura promedio máxima fue 32.2 °C y la mínima -6.4 °C (Figura 3a). Durante el periodo de observaciones fenológicas (marzo a noviembre de 2023) el promedio anual de precipitación fue 408 mm, la temperatura media 18.0 °C, la mínima promedio 4.2 °C y la máxima promedio 31.0 °C (Figura 3b).
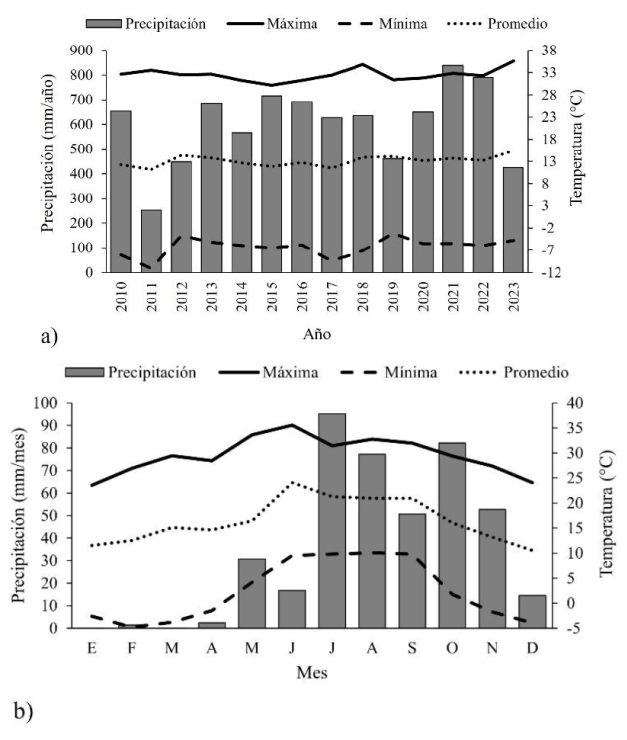
Figura 3 Temperatura y precipitación anual promedio registradas en el área de estudio: a) en un período de más de 10 años; b) durante el período de estudio.
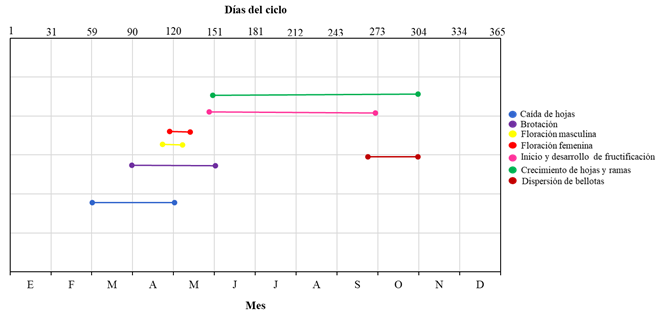
La caída de hojas ocurrió en los meses de marzo y abril, quedando los árboles totalmente defoliados, donde las condiciones promedio de temperatura máxima fueron de 28.9 °C, de temperatura media de 14.9 °C y de temperatura mínima de -2.7 °C, con una precipitación de 2.53 mm. El inicio de la brotación ocurrió en los meses de abril y mayo, con temperatura máxima promedio de 30.0 °C, de temperatura mínima de 4.5 °C y precipitación de 33.2 mm. También, en los mismos meses se presentó la fase fenológica de floración masculina, en tanto que la floración femenina solo ocurrió en el mes de mayo. El inicio y desarrollo de las bellotas ocurrió en los meses de junio a septiembre con condiciones promedio de temperatura máxima de 32.3 °C, de temperatura mínima de 10.0 °C y con una precipitación de 322 mm; en este mismo período se presentó la fase fenológica de crecimiento de hojas y ramas. La dispersión de bellotas ocurrió entre finales de septiembre y durante el mes de octubre, cuando las temperaturas empezaron a descender (1.0 °C); con esas mismas condiciones comenzaron a producirse yemas indicando el cese de crecimiento (Figura 4).
Los factores ambientales como la temperatura, la luz y la humedad influyen en la floración, ya sea acelerándola o retrasándola (Pérez López et al., 2013). Por ejemplo, las temperaturas bajas pueden inhibir la floración o ralentizar el desarrollo de los granos de polen (Rodríguez-Rajo et al., 2000). En ese sentido, Gerst et al. (2017) mencionan que las temperaturas máximas de primavera influyeron en el inicio de las fenofases de brotación y floración de Q. alba L. y Q. rubra L., mientras que en Q. agrifolia Née y Q. lobata Née influyeron las temperaturas mínimas. La duración de cada fenofase puede variar entre las mismas especies a lo largo de temporadas de crecimiento, como sucedió en este estudio.
Descripción de cada fase fenológica
Caída de hojas
El periodo de esta etapa fenológica comprendió de marzo a abril; al inicio del mismo los árboles aún conservaban sus hojas con un tono verde amarillento, las ramillas presentaban yemas mixtas, yemas axilares (entre las hojas) y terminales (al final de la rama); sin embargo, para el mes de abril las hojas adquirieron un color amarillo-café y se desprendieron por completo en 50 % de los árboles monitoreados (Figura 5).

Figura 5 a) hojas de color verde oscuro con presencia de yemas axilares (flecha amarilla) y yema terminal (flecha azul), b) hojas amarillentas, c) hojas de color café y, d) ramas sin hojas con presencia de yemas vegetativas más grandes (flecha amarilla).
A pesar de que todos los árboles pertenecían a la misma especie y se encontraban en áreas cercanas, la variabilidad fue significativa en la temporalidad y secuencia del desprendimiento de hojas. Este proceso comenzó a finales de marzo, primero en los árboles que florecieron y, posteriormente, en aquellos que solo generaron brotes (Figura 6).
Brotación
Esta etapa fenológica se observó de abril a mayo; después de la caída de hojas las yemas quedaron expuestas y presentaron un mayor crecimiento, Meger et al. (2024) mencionan que en Quercus robur el momento de la brotación está fuertemente relacionado con los regímenes de temperatura. Además, las yemas eran mixtas ya que dieron origen a hojas y a flores de manera conjunta o por separado. Aunado a esto, solo 50 % de los árboles florecieron y el resto solo exhibió crecimiento de brotes; en el primer caso, existió una coincidencia temporal entre el desprendimiento de las hojas y la floración, lo que sugiere una interacción estrecha entre ambos procesos; en particular, típicamente en las especies anemófilas, la floración ocurre antes de la foliación, de modo que el follaje no interfiere en la polinización (Cortés-Flores et al., 2011). En contraste, en el segundo caso, el brote de hojas nuevas tuvo lugar una vez que los árboles se encontraban completamente desprovisto de follaje, donde se observó que la pérdida de hojas se extendió hasta finales de mayo, teniendo un proceso de brotación más lento, caracterizado por la aparición de nuevas hojas únicamente en las yemas terminales, con 4 a 10 hojas, de color verde claro, tanto en la superficie adaxial como abaxial, con color rosado en el borde (Figura 7).

Figure 7 Sprouting of branches: a) branches with axillary and terminal buds, b) swollen terminal bud in development, c) opening of terminal bud, d) beginning of leaf unfolding, e) leaf unfolding.
En el caso de los árboles que florecieron, durante esta etapa, las yemas comenzaron a abrirse para generando flores masculinas y nuevos brotes de hojas, que presentaban un tono verde claro en la superficie adaxial y un tono grisáceo en la superficie abaxial con los bordes rosados y blandas al tacto, en todas las ramas del árbol. Para mayo, ya se habían formado las nuevas ramillas con hojas en crecimiento, algunas con hasta 12 hojas; además, se observó un crecimiento simultáneo de hojas y flores. Algunas ramas emitidas de las yemas terminales tuvieron un considerable crecimiento, llegando a generar hasta 21 hojas (Figura 7).
Crecimiento de hojas y ramas
Esta etapa fenológica comprendió un periodo de cinco meses (junio-octubre), el crecimiento se limitó principalmente a las hojas, con la aparición de algunas ramas que aún no habían madurado completamente. Las ramas crecieron entre 2 y 26 cm de largo, portando entre 5 y 21 hojas de 4 a 5.5 cm de largo. En julio y agosto se produjo el crecimiento mayor, en las hojas el color verde se intensificó a un tono más oscuro en la superficie adaxial y la superficie abaxial se puso blanquecino. Dichos meses coinciden con el valor más alto de precipitación (Figura 3b), aumentando la disponibilidad de recursos, lo que asegura grandes cantidades de fotosintatos disponibles para, a su vez, generar tejido fotosintético (Garcia-Barreda et al., 2021). Después de estos meses no se registró un aumento significativo en su tamaño, sólo se intensificó el color verde en la superficie adaxial de las hojas, mientras que el color grisáceo continuó en la superficie abaxial y estaban duras al tacto. Finalmente, en septiembre y octubre, todas las ramas nuevas presentaban yemas axilares y terminales más pronunciadas de 2 a 4 mm, indicando el cese del crecimiento (Figura 8).

Figure 8 Growth and development of leaves with shades from light green to dark green: a) 2.5 GY 5/4, b) 5 GY 6/6, c) 5 GY 4/8, d) 7.5 GY 5/2 and, e) abaxial surface (2.5G 7/8) and adaxial surface (7.5 GY 8/2), according to the Munsell notation system.
Un estudio en varias especies arbóreas reporta que la temperatura está fuertemente correlacionada con la fecha de inicio de la brotación (Basler & Körner, 2012). En Quercus robur se encontró que la relación entre la temperatura primaveral y las primeras hojas fue significativa (Askeyev et al., 2005). Asimismo, Gerst et al. (2017) indican que el inicio de las hojas y la floración en cuatro especies de Quercus se produce antes en los últimos años, aparentemente en respuesta a temperaturas más altas en invierno y primavera. Entre individuos de una misma población de Quercus se encontraron diferencias en las fechas de comienzo de la brotación y floración (Chesnoiu et al., 2009); en este caso algunos árboles brotaron al inicio de la primavera, mientras que otros lo hicieron en el verano. Bertin (2008) menciona que la aparición de hojas y la floración en los encinos se llega adelantar varias semanas, debido a las altas temperaturas en primavera.
Floración
Los encinos son árboles monoicos, producen flores masculinas en amentos, encargadas de la producción de polen y las femeninas emergen en brotes axilares en las hojas de la nueva rama. El desarrollo floral masculino y femenino siguió patrones similares en 50 % de los árboles monitoreados. Esta etapa fenológica ocurrió a finales del mes de abril y principios de mayo, inició cuando se cayeron las hojas de los árboles, quedando las yemas cerradas y expuestas, no pudiendo diferenciarse de las reproductivas. El desarrollo de flores y ramas ocurrió de manera simultánea; durante este proceso los árboles se cubrieron primero de flores masculinas y ramillas jóvenes. La floración tuvo un inicio muy incipiente en cada árbol, extendiéndose después a toda la copa. De las mismas yemas múltiples brotaron tanto flores masculinas como hojas, siendo común que la mayoría de las yemas primero produjeran las flores y luego la rama, aunque en algunos casos se presentaron exclusivamente flores o ramas. La floración masculina duró aproximadamente 15 días, período en el cual las flores liberaron polen (dehiscencia de las anteras), mientras que la floración femenina duró tres semanas. Las yemas reproductivas masculinas desarrollaron de dos a seis amentos. Hacia finales de mayo las flores comenzaron a marchitarse después de la liberación de polen, cambiando de color amarillo claro a un tono más blanco, señalando el final de la etapa de floración. Mientras las flores masculinas emergían directamente de las yemas, las femeninas se desarrollaban entre el crecimiento de las nuevas hojas, haciéndose evidentes una vez que estaban fecundadas (mes de mayo) (Figura 9).

Figure 9 Flowering: a) catkins beginning to develop, b and c) catkins in successive stages of growth, with the anthers not yet dehiscent, d) pollen dispersion (anther dehiscence), e) wilting of the catkins (withered and dry catkin, prior to abscission), f) detail of male flowers with some anthers closed and others open, g) male flowers with all anthers open, h) receptive female flowers in the axils of new twigs, i) female flower with fertilized ovary and withered stigmas (dry and blackish), and j) female flower with receptive, turgid and reddish stigmas.
La floración se produjo en época de escasa precipitación y aumento de la temperatura en el área de estudio. En este período los brotes de las hojas son pequeños; por lo tanto, la polinización se beneficia debido a que ocurre mediante el viento, favoreciéndose durante estos meses (Coombes, 2020). Cortés-Flores et al. (2011) reportaron periodos de un mes de floración en especies como Quercus candicans Née, Q. castanea Née, Q. crassipes Bonpl., Q. obtusata Bonpl., y Q. rugosa Née.
El inicio del periodo de floración está ligado al desarrollo de brotes vegetativos, es decir, el retraso o adelanto en la brotación conlleva un retraso o adelanto en la floración (Bogdziewicz et al., 2020). En este caso, aunque existió una abundante cantidad inicial de flores masculinas, no necesariamente existió una alta producción de semilla. Gómez-Casero et al. (2004) mencionan que las condiciones climáticas del invierno y primavera influyen en la dehiscencia y la densidad de las flores, también en la cantidad de polen producido. También, Schermer et al. (2020) indican que temperaturas altas en primavera favorecen la sincronización fenológica entre árboles; es decir, se reduce el período de floración, lo que a su vez aumenta el éxito de la polinización por la cantidad de polen en el aire que puede movilizarse y las flores femeninas reciban el polen y sean fecundadas, produciéndose las bellotas.
Fructificación y dispersión de bellotas
La fructificación ocurrió a finales de mayo y el tamaño mayor de los frutos se alcanzó en el mes de julio y agosto, coincidiendo con los meses más cálidos (Figura 3b) y el desarrollo de la temporada de lluvias. La producción de bellotas puede variar año tras año, fenómeno conocido como masting (Coombes, 2020): los encinos producen muchas semillas cada dos años o más de manera sincronizada con otros árboles; este patrón de fructificación alternado puede tener implicaciones importantes para la ecología del bosque y para las comunidades de animales que dependen de los encinos como fuente de alimento.
De los seis árboles monitoreados, sólo la mitad produjo bellotas, de los cuales uno tuvo una producción escasa. El principio de la formación de las bellotas indicó que a finales del mes de mayo había tenido lugar la fecundación de las flores femeninas; para el mes de junio las bellotas ya tenían la forma redonda, entre 3 y 5 mm de longitud (Figura 10). En julio, la nuez comenzó a emerger de la cúpula, y durante agosto y septiembre ocurrió un crecimiento tanto en el diámetro como en la longitud de la cúpula y la nuez; en ese periodo, aproximadamente el 50 % de la nuez ya se encontraba fuera de la cúpula (Figura 10). Para el mes de octubre las bellotas alcanzaron 1.5 a 2 cm de longitud, con 0.81 cm de diámetro, llegando a su madurez, indicada por el cambio de tonalidad de verde a café, tanto en la cúpula como en la nuez; además, la nuez se desprendía de la cúpula con facilidad, iniciando su liberación, facilitada por el movimiento de las ramas debido a la acción del viento. La fecha de inicio de la caída de la bellota ocurrió al mismo tiempo en los tres árboles evaluados que produjeron bellotas.

Figure 10 Acorn growth process: a) fertilized female flower, b and c) developing green ovary, d and e) small rounded scaly dome with brown ovary, f) nut emerging from the dome, g) acorn length equal to dome length, h) acorn length greater than dome length, still green, i) acorn about to mature, green-brown tone, and j) mature acorn, brown color.
Un aspecto a destacar es que, pese a que los árboles estuvieron cubiertos con flores masculinas, la producción de bellotas fue notablemente escasa. Se han reportado pérdidas previas a la dispersión debido al aborto causado por condiciones climáticas desfavorables durante la etapa de floración y desarrollo de bellotas (Díaz-Fernández et al., 2004). La producción de bellotas se correlaciona con la lluvia o la temperatura en primavera (Bogdziewicz et al., 2017a); por lo tanto, en gran parte el aborto de bellotas se debe a la escasez de agua. Gręda et al. (2022) mencionaron el aborto de bellotas en Q. rubra L., debido a eventos climáticos extremos que inhibieron la reproducción. Otro factor adverso que influye es el consumo de bellotas por insectos, aves y especialmente roedores antes de desprenderse del árbol (Aguilar-Peralta et al., 2016). En el área se observaron algunos pájaros carpinteros y ardillas, quienes pudieron haber consumido las bellotas previo a su liberación de los árboles, en general se observó una baja producción de bellotas en los encinos cercanos al área de estudio.
Otra causa del déficit de bellotas es el consumo de las flores femeninas por orugas de lepidópteros, lo cual tiene un impacto directo y significativo en la producción de frutos (Pulido, 2002). La pérdida de flores femeninas de Quercus suber L. durante el verano fue atribuido a una intensa sequía (Díaz-Fernández et al., 2004). La floración temprana en las especies de encinos de zonas templadas da como resultado que normalmente se libere polen durante condiciones climáticas desfavorables y, con frecuencia, resulta en fallas reproductivas (Schermer et al., 2020). Sin embargo, la capacidad de fructificación entre especies del género Quercus es variable, independientemente de las condiciones ambientales (Díaz-Pontones & Reyes-Jaramillo, 2009).
Según Coombes (2020), la variación anual en la producción de bellotas, de manera sincronizada y masiva cada dos años, se debe a que el polen es escaso en los intervalos bianuales; en contrapartida, se considera una estrategia reproductiva común en poblaciones de encino, debido a que producen más semillas de las que pueden ser consumidas por los depredadores (Cortés-Flores et al., 2011), como se ha registrado en Quercus ilex L. (Bogdziewicz et al., 2017b). Incluso existen marcadas variaciones en la producción de bellotas entre individuos dentro del mismo año, las cuales oscilan entre 0.5 y 150 kg/árbol (García-Mozo et al., 2007). Quercus robur L. mostró fluctuaciones anuales, tendiendo a alternarse años de mayor producción con años de baja producción (Askeyev et al., 2005). Al parecer este comportamiento está asociado con la variación anual en las condiciones climáticas y la capacidad de los árboles para almacenar recursos después de la última producción de bellotas (García-Mozo et al., 2007).
Garcia-Barreda et al. (2021) menciona tres hipótesis que vinculan el clima y las reservas almacenadas con la producción de bellotas; la primera es que la alta producción de bellotas ocurre en los años en que existen más recursos disponibles, prediciendo así una relación positiva entre reproducción y crecimiento. La segunda es que la producción de bellotas no puede ocurrir todos los años porque la reproducción es costosa y el árbol debe acumular recursos más allá de un cierto umbral, con grandes esfuerzos reproductivos que agotan las reservas. Y la tercera es que un árbol invierte una cantidad relativamente constante de recursos del año en curso en crecimiento o reproducción, prediciendo así compensaciones de asignación entre reproducción y crecimiento.
El comportamiento fenológico varía de un año a otro, ya que las condiciones climáticas varían (Gómez-Casero et al., 2007); por lo tanto, las observaciones fenológicas deben llevarse a cabo a lo largo de varios años, con el fin de obtener una visión general del comportamiento de este fenómeno.
Conclusiones
Quercus durifolia tuvo fases fenológicas definidas durante el periodo de evaluación (nueve meses), pese a que existieron diferencias entre los individuos evaluados. La defoliación comenzó a finales de marzo, primero en los árboles que florecieron y, posteriormente, en aquellos que solo generaron brotes. El crecimiento vegetativo se inició durante la época seca del año (abril y mayo). Las yemas dieron origen a ramas y flores de manera simultánea, y en algunos casos solo generaron ramas o flores. El 50 % de los árboles monitoreados produjeron bellotas, las cuales se desarrollaron de mayo a septiembre y culminaron su dispersión en octubre. Futuros estudios deberían abordar variaciones interanuales, en el contexto del cambio climático y de las variaciones típicas periódicas en este género.











 nova página do texto(beta)
nova página do texto(beta)