Introducción
En el estado de Durango, México, existe diversidad importante en especies de plantas del género Phaseolus. Particularmente, puede encontrarse un número alto de poblaciones nativas de frijol en varios municipios (Wallander-Compean et al., 2022), por lo que ésta entidad debe ser considerada como un centro importante de diversidad genética y domesticación del frijol, sobretodo cuando se consideran los antecedentes históricos (Chacón-Sánchez, 2009; Punzo-Díaz & Ramírez-Luna, 2008) y los requerimientos para hacer frente a los escenarios de calentamiento global (Mourice et al., 2016; Rosales-Serna, R., C. M. Reyes-Rodríguez, N. Almaraz-Abarca, D. Sierra-Zurita, J. L. Becerra-López, S. Santana-Espinoza., 2024). La adaptación del frijol en condiciones adversas requerirá la incorporación de genes relacionados con mecanismos de adaptación al estrés hídrico, temperaturas altas y organismos patógenos. Varias clases comerciales de frijol, como bayo y pinto, se originaron dentro del Complejo Poblacional de la Raza Durango y muestran grado alto de tolerancia al estrés hídrico (sequía), temperaturas altas (29 a 33 °C) y enfermedades (Chaves-Barrantes et al., 2018; Rosales-Serna et al., 2004). Sin embargo, es necesario explorar, colectar y caracterizar colectas nativas provenientes de áreas de origen, para ampliar la gama de posibilidades en la selección de fuentes de resistencia al estrés hídrico, variaciones de temperatura y efectos negativos de organismos patógenos. Con ello, se podrá realizar mejoramiento genético para dichos factores en diferentes países del mundo donde se cultiva frijol en forma intensiva y extensiva.
La tolerancia a la sequía del frijol de la Raza Durango se debe principalmente a su fenología precoz, que le permiten el escape al estrés hídrico terminal y recuperación de la planta, después de periodos de escasez de agua (Rosales-Serna et al., 2004). El escape implica la transición rápida a la etapa reproductiva y la removilización acelerada de fotoasimilados a las vainas y granos en formación; mientras que, la recuperación requiere el fortalecimiento del crecimiento vegetativo y ajuste de la fenología (plasticidad fenológica) (Labastida et al., 2023). El estrés hídrico, registrado en múltiples países a nivel mundial donde se cultiva frijol, se agrava con la presencia de temperaturas altas (>35 °C), por lo que cuando se presentan ambos factores por periodos prolongados, causan problemas fisiológicos y caída de flores y frutos en formación (Hernández et al., 2015).
En la localidad de La Ferrería, Durango, México, crecen poblaciones nativas y formas intermedias (recombinantes genéticos) de frijol. La Ferrería, es considerada como la zona arqueológica más importante del Valle del Guadiana (Durango) en la época Chalchihuites, 600 a 1,300 d.c. [INAH (Instituto Nacional de Antropología e Historia, 2024]. La población Chalchihuites fomentó el consumo de frijol (Punzo-Díaz & Ramírez-Luna, 2008); mientras que, la confluencia y movilización de las poblaciones humanas y el intercambio de semillas, favorecieron la recombinación genética del Complejo Poblacional de la Raza Durango (Singh et al., 1991) con el germoplasma de frijol de otras áreas de México. Lo anterior, favoreció la diversidad genética que puede ser utilizada para la solución de problemas derivados del cultivo de frijol en áreas sujetas a sequía y presión de diversos patógenos que reducen el rendimiento y calidad del grano en varios países del mundo.
El análisis de la variabilidad genética, recombinación y flujo génico entre estas poblaciones vegetales contribuiría al esclarecimiento del proceso de evolución paulatina que les ha permitido adaptarse a los cambios ocasionados por el calentamiento global (Köstner et al., 2013); así como, la identificación de genes relacionados con la tolerancia a la sequía, temperaturas altas y enfermedades. La caracterización morfológica y morfométrica de las colectas de frijol nativo puede brindar información esencial sobre la diversidad genética que persiste en el Complejo Poblacional de la Raza Durango. Las directrices para la ejecución del examen de la distinción, la homogeneidad y la estabilidad, para judía común, alubia, Phaseolus vulgaris [SNICS (Servicio Nacional de Inspección y Certificación de Semillas), 2017; UPOV (Unión Internacional para la Protección de las Obtenciones Vegetales, 2012], relacionadas con los descriptores de la especie [IBPGR (International Board for Plant Genetic Resources, 1982)], son aceptadas internacionalmente y pueden utilizarse en la determinación de la diversidad genética del frijol nativo y cultivado del Complejo Poblacional de la Raza Durango.
Los ISTR son marcadores genéticos moleculares que detectan polimorfismos entre regiones del genoma que separan retrotransposones, los cuales son los elementos móviles más abundantes y activos de los genomas vegetales y la principal fuente de variación en este tipo de organismos (Orozco-Arias et al., 2022; Paszkowski, 2015). Los diferentes tipos de retrotransposones han formado linajes en diferentes grupos de plantas (Yu et al., 2024), por lo que se consideran marcadores útiles, para el estudio de la diversidad genética en germoplasma de frijol. Los resultados obtenidos favorecerán el conocimiento y uso eficiente de la diversidad genética de frijol para el mejoramiento de las variedades usadas en la alimentación humana, en respuesta a los efectos del calentamiento global. El objetivo del presente estudio fue estimar la diversidad genética en el Complejo Poblacional de la Raza Durango de frijol nativo y cultivado.
Materiales y métodos
Germoplasma. En el año 2022, se colectaron al azar semillas de plantas individuales de poblaciones nativas de frijol, en La Ferrería, Durango, Dgo., México. También, se obtuvieron variedades criollas en la zona de cultivo de Los Llanos, Guadalupe Victoria e Ignacio Allende, Dgo. Se generó una base de datos sobre la ubicación de los sitios donde se obtuvieron las colectas nativas y variedades criollas de frijol. Se utilizó un grupo de 27 colectas, de las cuales 26 son de frijol (18 nativas, 4 variedades criollas y 4 variedades mejoradas, producidas en Durango, Dgo.) y una variedad criolla de Phaseolus coccineus, como testigo de referencia.
Las variedades criollas son poblaciones de plantas cultivadas tradicionalmente, por los productores, mediante su reproducción constante por más de 30 años (Herrera-Cabrera et al., 2002) y algunas de ellas (Río Grande), fueron generadas en las primeras etapas de mejoramiento genético de frijol [1960-1976 (Rosales et al., 2004)]. Durante dicho proceso, se aplicó selección masal en variedades locales, heterogéneas y ocasionalmente heterócigotas, las cuales, aún en la actualidad, muestran variación intrapoblacional considerable y se adaptan a las condiciones locales de cultivo. Las variedades mejoradas son poblaciones desarrolladas mediante la recombinación genética entre progenitotres sobresalientes y la aplicación de un esquema de mejoramiento genético, principalmente el método de pedigrí (genealógico) (Rosales et al., 2020).
La descripción de las colectas utilizadas en el presente estudio se muestran en la Tabla 1, donde se consideró como colecta la muestra obtenida de las semillas de cada una de las plantas individuales, en el caso de Phaseolus nativo, y de muestras masales obtenidas en el caso de las variedades criollas y mejoradas de frijol cultivado. Phaseolus coccineus L. (patol o ayocote) se colectó y caracterizó de la misma manera (morfo-agronómica y molecular) para su uso con fines comparativos. Las colectas y variedades se sembraron en condiciones de campo en Durango (INIFAP-C. E. Valle del Guadiana, Durango, Dgo., México) para realizar la caracterización morfo-agronómica y molecular.
Tabla 1 Colectas de frijol utilizadas para la caracterización de la diversidad genética en el Complejo Poblacional de la Raza Durango.Table 1. Common bean accessions used for the characterization of the genetic diversity in the Durango Race Population Complex.
| Colecta | Forma | Color de semilla | Colecta | Forma | Color de semilla |
|---|---|---|---|---|---|
| 1LF 1 | Nativa | 2FM Negro | LF 27 | Nativa | Café |
| LF 2 | Nativa | Bayo (crema) | LF 29 | Nativa | Negro |
| LF 3 | Nativa | Café | LF 30 | Nativa | Bayo (crema) |
| LF 5 | Nativa | BY-PT Negro | LF 35 | Nativa | Café |
| LF 7 | Nativa | FM Rosa | Borroso | Criolla | Café-Gris |
| LF 12 | Nativa | Café | BY Madero | Mejorada | Bayo (crema) |
| LF 13 | Nativa | FM Negro | NG San Luis | Criolla | Negro |
| LF 16 | Nativa | FM Morado | Patol | Criolla | Negro, Pinto |
| LF 19 | Nativa | Negro | PT Burro | Criolla | Pinto |
| LF 21 | Nativa | Negro | PT Nacional | Criolla | Pinto |
| LF 23 | Nativa | Bayo (crema) | PTSaltillo | Mejorada | Pinto |
| LF 24 | Nativa | Crema-Gris | PT Villa | Mejorada | Pinto |
| LF 25 | Nativa | Crema-Gris | Querétaro | Mejorada | Bayo (crema) |
| LF 26 | Nativa | FM Morado |
1LF = La Ferrería, 2FM= flor de mayo, rosa, violeta, morado, o jaspeado de negro sobre fondo amarillo-pálido; PT= pinto moteado de café o negro, sobre fondo blanco o beige; NG= negro brillante.
Condiciones de cultivo. La siembra se realizó el 10 de julio de 2023 y se aplicó el manejo agronómico, recomendado en Durango, para el cultivo del frijol en condiciones de riego [INIFAP (Instituto Nacional de Investigaciones Forestales, 2017)]. La parcela experimental estuvo situada en la carretera Durango-El Mezquital km 4.5 (23° 59’ 21” N, 104° 37’ 33” O, 1,877 m). La parcela útil estuvo compuesta por un surco de 5 m de largo, con un espaciamiento de 0.81 m y 80 plantas. Se colocaron estacas cerca de cada planta para ayudar a las guías a trepar en secciones de carrizo (Arundo donax) colocadas verticalmente y con una altura de 2 m sobre la superficie del suelo.
El suelo predominante es de sitio es de tipo franco-arcilloso (Kastañozem), el cual tiene capacidad intermedia para la retención de humedad, profundidad media, pendiente de 0 a 4%, pH de 7.9 y es pobre en contenido de materia orgánica, fósforo y nitrógeno. El clima predominante es templado semiárido [BS1 kw (w) (e)], con régimen de lluvias en verano, variación fuerte de temperatura con una media anual de 17.4 °C (García, 1987). La lluvia acumulada durante el año alcanza un promedio de 476 mm, con valores altos entre junio y septiembre (Medina-García, 2005).
Caracterización morfo-agronómica. En una población > 60 plantas de cada colecta se registraron 48 atributos morfo-agronómicos incluidos en las guías publicadas por [UPOV (Unión Internacional para la Protección de las Obtenciones Vegetales), 2012] y [SNICS (Servicio Nacional de Inspección y Certificación de Semillas), 2017]. En dichas variables se consideran mayoritariamente variables cualitativas (46) y únicamente dos cuantitativas. Las observaciones para cada atributo se realizaron conforme a las recomendaciones incluidas en las guías [UPOV (Unión Internacional para la Protección de las Obtenciones Vegetales), 2012]. El registro del número de días a floración se realizó cuando más del 50% de las plantas mostraron una flor abierta; mientras que, la maduración se evaluó cuando la mayoría de las plantas presentaron las vainas y hojas amarillas, típicas de la madurez fisiológica [CIAT (Centro Internacional de Agricultura Tropical), 1986].
Extracción de ADN. La extracción de ADN se realizó de acuerdo a Coelho et al. (2009), a partir de 100 mg de tejido foliar de 3 plantas de frijol para cada colecta y variedad.
Cuantificación del ADN. La cuantificación y estimación de la pureza del ADN obtenido se determinó a partir de los registros de absorbancia a 260 y 280 nm, de acuerdo a Chan (1992). La determinación de la cantidad de ADN obtenido se realizó de manera espectrofotométrica. Se tomaron 4 μL de cada solución individual de ADN y se combinaron con 996 μL de agua inyectable (dilución 1/250). Se determinaron los valores de absorbancia a 260 nm (A260). La concentración de ADN en cada muestra se estimó considerando que una solución de ADN de 50 ng μL-1 tiene un valor de A260 de 1 (Chan, 1992). La determinación de la pureza de las soluciones de ADN se realizó de manera espectrométrica de acuerdo a Sambrook J. (1989). De manera individual se registraron los valores de A280 y se calcularon los valores de la relación A260/A280, considerando las lecturas previas de A260. Valores de esas proporciones iguales o mayores de 1.7 indicaron que el ADN se encontraba lo suficientemente libre de proteínas para su ampliación por PCR (Reyes-Martínez et al., 2011).
Amplificación. Se emplearon cuatro pares (combinaciones) de iniciadores B1/F10, B6/F10, B8/F9 y B1/F10, los cuales fueron seleccionados por la facilidad de implementación en el CIIDIR-IPN Unidad Durango; así como, por su eficiencia en la discriminación de especies y detección de variabilidad genética intrapoblacional en Agavaceas (Torres-Morán et al., 2008) y capacidad para separar germoplasma silvestre y cultivado de frijol; así como, para establecer el grado de similitud entre colectas (Castellanos-Hernández et al., 2017). Las secuencias de cada uno de los iniciadores se muestran en el Tabla 2.
Tabla 2 Secuencia de los iniciadores ISTR utilizados en la caracterización molecular de 27 colectas de frijol (Phaseolus spp.).Table 2. Primer sequences for ISTR used in molecular characterization of 27 accessions of common bean (Phaseolus spp.).
| Iniciador | Secuencia (5’→3’) |
|---|---|
| F9 | TTA CCT CCT CCA TCT CGT AG |
| F10 | TAA GCA AGC ATC TCG GAG |
| B1 | ATC AGG AAG GTC TGT AAA GC |
| B6 | GGT TCC ACT TGG TCC TTA G |
| B8 | ATA CCT TTC AGG GGG ATG |
Caracterización molecular. Los perfiles de amplificación ISTR se obtuvieron mediante la técnica de la reacción en cadena de la polimerasa (PCR), de acuerdo a (Osorio et al., 2006). La concentración inicial de ADN fue 1,490 ng μL-1 y con base en ello, se prepararon 1.5 μL de una solución de ADN (25 ng μL-1) se combinaron con 2 µL de regulador de la enzima (1X), 3 mM de MgCl2, 0.3 μM de cada iniciador ISTR, 0.25 mM de dNTP, 1U de Taq polimerasa (Promega®) y la cantidad de agua (ultrapura) necesaria para que el volumen final de reacción fuera de 20 µL. Las condiciones de amplificación fueron, un primer ciclo de desnaturalización de 3 min a 95 °C, seguida por 40 ciclos de desnaturalización a 95 °C por 3s, alineación a 45 °C por 1 min y extensión a 72 °C por 2 min. Se incluyó un paso de extensión final de 10 min a 72 °C.
Los fragmentos amplificados se separaron y visualizaron en geles de poliacrilamida (5%), de acuerdo con (Sanguinetti & Simpson, 1994), teñidos con Sybr Green. Los fragmentos amplificados en cada muestra representaron su perfil de amplificación. Las bandas resueltas en los geles de poliacrilamida se seleccionaron y cuantificaron con ayuda del programa de cómputo GelAnalyzer 23.1.
Análisis de la información. Los datos fenotípicos, resultantes de la caracterización morfo-agronómica, se analizaron mediante estadística descriptiva (promedios) y se sometieron a análisis de componentes principales (ACP) y análisis de agrupamiento o conglomerados (cluster analysis). Los perfiles de amplificación se usaron para construir matrices binarias (una para cada tipo de datos) de presencia/ausencia (1/0) de bandas amplificadas (caracteres fenotípicos). Con los datos moleculares se estimó el porcentaje de polimorfismo y se sometieron a análisis de agrupamiento. En los análisis de agrupamiento se utilizó el método UPGMA (Agrupación de Pares no Ponderados con Promedios Aritméticos). Los análisis de datos se hicieron con los programas R ver.2023.12.0+369 y Past 4.14 (Hammer & Harper, 2001).
Resultados
Caracterización morfo-agronómica. Las colectas de frijol nativo mostraron precocidad para el desarrollo de las guías (29 días después de la siembra; DDS); aunque resultaron tardías para el número de días a floración (59 DDS) e intermedias a la madurez (107 DDS), al mismo tiempo que presentaron semillas pequeñas (15 g 100 semillas-1). Las variedades criollas y mejoradas de frijol mostraron valores entre 34 y 35 DDS para el inicio del desarrollo de la guía, 49 DDS para el inicio de la floración, entre 93 a 97 días a madurez fisiológica y 31 a 44 g para el peso de 100 semillas. El testigo mostró 33 DDS para el inicio del desarrollo de las guías, floración a los 44 DDS, madurez 125 DDS y peso de 100 semillas 127 g. Se observaron diferencias considerables para los rasgos morfo-agronómicos evaluados en el presente estudio, en colectas nativas y cultivadas de frijol; así como, con respecto al testigo de referencia.
El Análisis de Componentes Principales (ACP) generado a partir de la caracterización morfo-agronómica mostró una proporción baja de la varianza explicada por el CP 1 (15.2%) y CP 2 (10.1%), por lo que se requirieron 26 CP para alcanzar un valor cercano a 100%. La diferencia (altura) más pronunciada en el dendrograma generado a partir del análisis de la información de atributos morfo-agronómicos se observó para P. coccineus (frijol patol), la cual formó un grupo independiente del resto de las colectas, lo que está en concordancia con el hecho de que es una especie diferente (Figura 2). La variabilidad disminuyó entre las colectas con semillas pequeñas y típicamente de frijol nativo, las cuales formaron dos subgrupos (IIa y IIb), que incluyeron colectas con semillas de color bayo (crema-beige), café, negro y rayadas negras (IIa1). El subgrupo IIa2 incluyó colectas con semillas pequeñas de color beige, conocidas como frijol bayo y flor de mayo, incluyendo coloración abigarrada negra y rosada en la testa de la semilla.
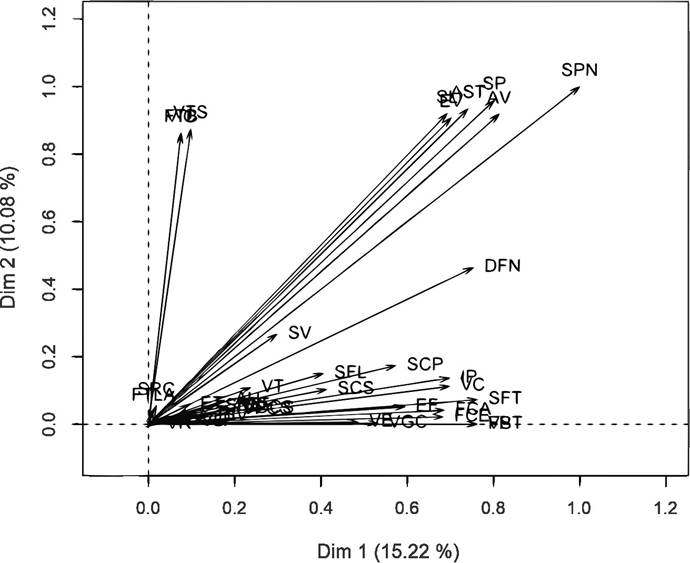
Figura 1 Resultado bidimensional del análisis de componentes principales para variables morfo-agronómicas de frijol nativo y cultivado del estado de Durango (SPN = semilla peso numérico, AV = anchura de la vaina, SP = tamaño de la semilla, AST = anchura de la semilla, en sección trasversal).
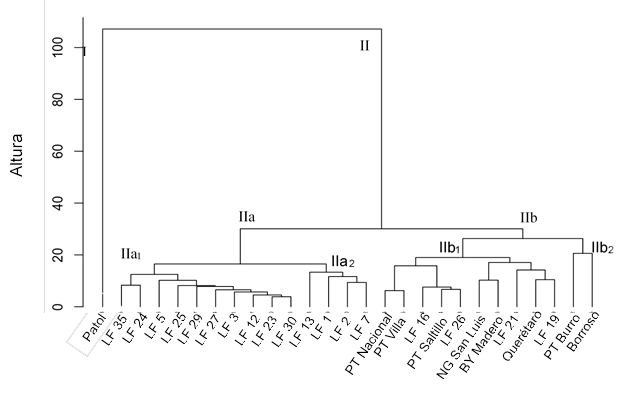
Figura 2 Dendrograma basado en características morfo-agronómicas evaluadas en colectas de frijol del Complejo Poblacional de la Razas Durango y Jalisco.
El grupo IIb incluyó dos subgrupos, que englobaron variedades criollas y mejoradas con semillas de color pinto y formas intermedias (regresivas) con semillas grandes de color flor de mayo (rosado). También, se observó grado alto de diferenciación en el subgrupo IIb1 de variedades criollas (Negro San Luis) y variedades mejoradas (Río Grande y Bayo Madero); así como, para colectas recombinantes con semillas flor de mayo. Otro subgrupo (IIb2) estuvo compuesto por dos variedades criollas con grado alto de segregación (recombinantes), conocidas como Pinto Burro y Borroso (Rebocero), que probablemente se originaron a partir de cruzamientos naturales de tipo interracial.
Caracterización molecular. Las cuatro combinaciones de marcadores moleculares ISTR, produjeron un total de 69 bandas (Tabla 3). El nivel de polimorfismo varió entre 56% para la combinación B1/F10 y 86% para la combinación B8/F9, por lo que esta última fue más informativa. El dendrograma generado por los perfiles de amplificación, con cuatro combinaciones ITSR incluidas en el análisis, mostraron una separación clara de las colectas bajo estudio, revelando dos grupos principales (I y II) (Figura 3). El grupo I incluyó colectas principalmente nativas (subgrupos Ia y Ib) y únicamente se mezcló en el subgrupo (Ib) la variedad criolla de la Sierra de Durango, conocida como Borroso (Rebocero), la cual puede ser resultado de la recombinación genética entre colectas criollas y nativas.
Tabla 3 Variables evaluadas en 27 colectas de frijol sembradas en Durango, México.Table 3. Traits evaluated in 27 common bean accessions sown at Durango, México.
| Colectas | DDG | DIF | P100S (g) | DMF |
|---|---|---|---|---|
| Nativas | 29 | 59 | 15 | 107 |
| Criollas | 34 | 49 | 44 | 97 |
| Mejoradas | 35 | 49 | 31 | 93 |
| Testigo | 33 | 44 | 127 | 125 |
| Total/Promedio | 33 | 50 | 54 | 106 |
DDG = días para el desarrollo de guías, DIF = Días a inicio de floración, P100S= peso de 100 semillas y DMF = días a madurez fisiológica.
Tabla 4 Parámetros genéticos obtenidos en la evaluación de la diversidad genética en colectas de frijol de la Raza Durango mediante cuatro combinaciones de ISTR.Table 4. Genetic parameters obtained in the evaluation of the genetic diversity in common bean accessions of the Durango Race by using four ISTR combinations.
| Iniciador ISTR | Total de Bandas | Bandas Polimórficas |
Polimorfismo (%) |
|---|---|---|---|
| Combinación 1 (B1/F10) | 32 | 18 | 56 |
| Combinación 2 (B6/F10) | 17 | 12 | 71 |
| Combinación 3 (B8/F9) | 14 | 12 | 86 |
| Combinación 4 (B8/F10) | 6 | 4 | 67 |
| Total | 69 | 46 | -- |
| Promedio | 17 | 12 | 70 |
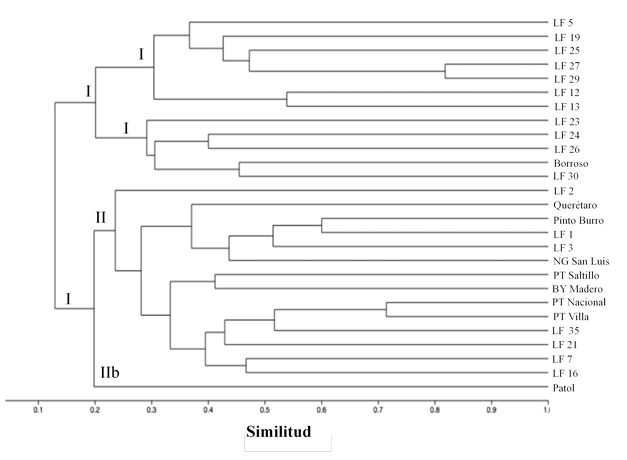
Figura 3 Dendrograma basado en cuatro pares de iniciadores de marcadores moleculares ISTR evaluados en colectas de frijol de las razas genéticas Durango y Jalisco.
El grupo II se subdividió en dos subgrupos (IIa y IIb), el grupo IIa incluyó principalmente frijol cultivado (criollo y mejorado) y una colecta de frijol nativo, con grano de color bayo y tamaño pequeño (LF 2), la cual, formó un clado independiente del resto de las muestras de frijol cultivado (Figura 3). En el mismo subgrupo IIa, se formó un clado separado de variedades criollas de la Raza Jalisco (Río Grande, Negro San Luis) y formas intermedias, como Pinto Burro, lo que sugiere que éstas pueden ser el resultado de la recombinación genética entre razas (Jalisco y Durango).
En otra división del subgrupo IIa se incluyeron variedades criollas y mejoradas provenientes de la raza Durango, la cual incluye las clases comerciales bayo (Bayo Madero) y pinto (Pinto Saltillo). También, englobó colectas recombinantes y granos medianos-grandes de color café, negro y flor de mayo, éstos últimos con diferentes tonalidades del color primario y secundario de la testa (Figura 3). Phaseolus coccineus (patol) fue el único elemento del subgrupo IIb, lo cual era esperado por ser una especie diferente. Los perfiles ISTR permitieron la diferenciación clara de cada grupo de colectas y variedades cultivadas, ya que cada una formó un clado individual, lo que sugiere perfiles genéticos diferentes. La mayor similitud genética se estableció entre la población LF 27 y LF 29 (Figura 3).
Discusión
Caracterización morfo-agronómica. Las plantas de las colectas de frijol nativo mostraron hábito de crecimiento trepador, lo que favorece su crecimiento en ecosistemas con competencia intra e interpoblacional fuerte con especies arbustivas y arbóreas (Kwak et al., 2012), lo cual contrastó con las variedades criollas y mejoradas; así como con el testigo de comparación. Lo anterior, provocó retraso en la floración y madurez de las colectas silvestres, por la necesidad de asignar la biomasa producida hacia el crecimiento vegetativo de la planta. Además, mostraron semillas pequeñas, testa gruesa y brillante; así como vainas dehiscentes de forma explosiva, lo que les permite adaptarse y reproducirse en ambientes adversos y contrastó con el resto de las colectas incluidas en el estudio (Acosta‐Gallegos et al., 2007).
Los resultados del Análisis de Componentes Principales (ACP) difirieron de lo observado en otros estudios con frijol, en los cuales se requirieron entre dos y cuatro Componentes Principales para explicar 40 a 84% de la variación total observada (Espinosa-Pérez et al., 2015; Long et al., 2020). El requerimiento de un número alto de Componentes Principales se relacionó con la diversidad alta para las colectas y variables incluidas en la caracterización realizada en el presente estudio, entre las que sobresalieron el tamaño de la semilla (Blair et al., 2009) y anchura de vainas y granos (Lépiz-Ildefonso et al., 2010) (Figura 1), las cuales estuvieron asociadas al CP 1 y al proceso evolutivo del frijol en la región bajo estudio. En estudios previos realizados en Durango, México, se encontró también una variación importante en las características de semillas y vainas entre cinco poblaciones nativas de frijol (Wallander-Compeán et al., 2022). Lo anterior, permite determinar que Durango es un centro importante para la diversidad y domesticación del frijol en México debido a la variación para diferentes atributos de la vaina y las semillas detectada en las colectas de frijol nativo, lo cual persiste en las variedades criollas y mejoradas cultivadas actualmente.
Los resultados mostraron qué el estudio de atributos morfo-agronómicos de la planta de frijol reveló variabilidad abundante, lo que sugiere que estos rasgos representan una herramienta importante para la caracterización del frijol y los estudios de diversidad genética. A pesar de lo anterior, se consideró necesaria la depuración de las variables incluidas en la caracterización morfo-agronómica, debido a la falta de variabilidad intra e interpoblacional en algunas de ellas, para incrementar la precisión y reducir tiempos y costos de evaluación en estudios posteriores.
La separación clara de P. coccineus (frijol patol), estuvo en concordancia con el hecho de que es una especie con morfología, fenología y adaptación diferente a P. vulgaris (Giurcă, 2008). La diversidad genética disminuyó entre las colectas que producen semillas pequeñas y típicamente nativas, las cuales formaron un subgrupo que incluyó colectas con semillas de color bayo (crema-beige), café, negro y rayadas negras (IIa1), pero con similitud para otros caracteres morfo-agronómicos. Los colores de la semilla, se observan en algunas de las variedades cultivadas tradicionalmente en Durango, Chihuahua y Zacatecas (López et al., 2021), por lo que se pudo establecer un vínculo entre colectas nativas y cultivadas de frijol. En otro subgrupo (IIa2) se acumularon colectas con semillas pequeñas de color beige, conocidas como frijol bayo y flor de mayo, incluyendo coloración abigarrada negra y rosada en la testa de la semilla. Este subgrupo fue generado por la recombinación genética con colectas de la raza Jalisco, o bien estas colectas son la fuente de la variabilidad presente en la raza Durango y las clases comerciales cultivadas localmente (bayo y flor de mayo) (Singh et al., 1991).
El grupo alterno (IIb) se formó con variedades criollas y mejoradas con semillas de color pinto (Raza Durango) y recombinantes genéticos interaciales, así como con semillas grandes de color flor de mayo (rosado). Los resultados mostraron continuidad geográfica para algunas clases comerciales de frijol (flor de mayo) tanto en las colectas de frijol nativo, como las variedades cultivadas. Lo anterior, pudo estar relacionado con la movilización de semillas y el intercambio genético interacial; así como, entre las clases comerciales de frijol de las razas Durango y Jalisco. También, se observó grado alto de diferenciación en el subgrupo IIb1 de variedades criollas (Negro San Luis) y variedades mejoradas (Río Grande y Bayo Madero); así como, para las colectas nativas con semillas flor de mayo. Se apreció separación entre clases comerciales de frijol, especialmente entre las colectas nativas y cultivadas de grano pinto y por otro lado las variedades con grano negro y bayo. Se ha observado que algunas variedades (Durango 222) con grano bayo (bayo blanco, bayo rata) muestran características típicas de las variedades con semillas negras (flores y guías moradas), lo que se asoció con la cercanía genética. Además, se observó que las colectas y variedades de grano flor de mayo comparten características con la mayoría de las colectas nativas y variedades cultivadas que fueron incluidas en el estudio. Otro subgrupo (IIb2) estuvo compuesto por dos variedades criollas con grado alto de segregación (recombinantes), conocidas como Pinto Burro y Borroso (Rebocero), que probablemente se originaron a partir de cruzamientos naturales de tipo interracial (Raza Durango y Raza Jalisco).
El uso de caracteres morfo-agronómicos permitió la separación entre colectas nativas y variedades cultivadas de frijol, las cuales se relacionan principalmente con la raza Durango y sus interacciones con la raza Jalisco. Además, pudo determinarse que algunas colectas nativas y variedades cultivadas han mantenido una identidad genética propia, asociada a su origen genético y geográfico. Los resultados obtenidos permiten suponer que las formas cultivadas de frijol (variedades criollas y mejoradas), pertenecientes a las razas Durango y Jalisco, descienden de poblaciones nativas de frijol con semillas pequeñas que presentan los colores siguientes: beige, café, bayo rata (beige veteado de gris) y pinto (café y rayado negro). Dichos resultados serán corroborados, mediante un análisis filogenético que establezca con precisión las relaciones genéticas entre colectas pertenecientes al Complejo Poblacional de la Raza Durango y su dispersión a otras áreas de México.
Las colectas nativas de La Ferrería, Dgo., mostraron presencia de semillas de color negro brillante y flor de mayo (de color negro y rosa), las cuales predominan en la Raza Jalisco (Singh et al., 1991) y en la actualidad están presentes en la Raza Durango. Lo anterior, pudo ser ocasionado por la dispersión del germoplasma de frijol originado en Durango, hacia una zona con condiciones más favorables para su crecimiento. También, influyó el flujo genético entre las poblaciones de frijol nativo y las variedades cultivadas (criollas y mejoradas) (Zizumbo-Villarreal et al., 2005), que se introdujeron en áreas cercanas a la zona arqueológica de La Ferrería, Dgo. Se ha detectado variación en el nivel de entrecruzamiento entre germoplasma nativo y cultivado de frijol [0.0 - 66.8% (Chacon-Sanchez et al., 2021)]. Con base en los resultados obtenidos, pudo establecerse la importancia del germoplasma de la raza Durango debido a que las colectas nativas obtenidas en La Ferrería, Dgo., fueron similares a las variedades cultivadas en Durango, Chihuahua y Zacatecas.
Caracterización molecular. Los niveles de polimorfismo encontrados en el presente estudio fueron inferiores (B1/F10, B6/F10, B8/F10) y en algunos casos similares (B8/F9) a los obtenidos, con el mismo tipo de marcadores moleculares, para frijol nativo, cultivado e intermedio de Jalisco, que fluctuaron entre 85 y 89% (Castellanos-Hernández et al., 2017). Los iniciadores incluidos en el presente estudio resultaron útiles para separar las colectas de frijol con base en su diversidad genética y nivel evolutivo (nativo, criollo, mejorado y testigo). En cada uno de los grupos se observaron colectas que representan recombinantes genéticos entre razas y niveles evolutivos, aunque se desconoce el sentido del intercambio, es decir se pueden tratar de avances y retrocesos desde el nativo hasta las colectas mejoradas, o bien desde éstas hacia el frijol nativo. En el grupo de colectas nativas se mezcló la variedad criolla de la Sierra de Durango, conocida como Borroso (Rebocero), la cual puede ser resultado de la recombinación genética entre germoplasma nativo y criollo, de las razas Durango y Jalisco, lo que dio lugar a esta colecta de crecimiento indeterminado, guía de longitud media y grano grande.
Otro de los grupos (II) incluyó principalmente frijol cultivado (criollo y mejorado) y una colecta de frijol nativo, con grano de color bayo y tamaño pequeño (LF 2), que mostró grado alto de diferenciación. En el mismo subgrupo, se formó un clado independiente de variedades criollas de la raza Jalisco (Río Grande y Negro San Luis) y variedades de origen interacial, como Pinto Burro, lo que sugiere que éstas pueden ser el resultado de la recombinación genética entre razas (Jalisco y Durango). Pinto Burro es una variedad que puede ubicarse en la raza Durango debido a que tiene granos de color crema y moteado de color café; aunque difiere de los pintos tradicionales, debido a que presenta tamaño grande y forma redondeada, que son atributos comunes en los granos observados en la raza Jalisco (Singh et al., 1991).
En el grupo predominante de variedades cultivadas, se incluyeron colectas de frijol criollo y mejorado de la raza Durango, con grano bayo (Bayo Madero) y pinto (Pinto Saltillo). Además, se englobaron colectas con formas intermedias y granos medianos-grandes de color café, negro y flor de mayo, éstos últimos con diferentes tonalidades del color primario y secundario de la testa. La colecta de Phaseolus coccineus (patol) fue el único elemento del subgrupo IIb, lo cual era esperado por ser una especie diferente. Los perfiles ISTR permitieron la diferenciación de cada grupo de colectas (nativas y cultivadas de las razas Durango y Jalisco), ya que cada uno formó un clado individual, lo que sugiere un perfil genético único. La mayor similitud genética se estableció entre las colectas LF 27 y LF 29, aunque una tiene grano de color amarillo oscuro y la otra negro brillante, lo cual demostró que los caracteres morfológicos pueden mostrar cierto nivel de error en la diferenciación de colectas cercanas genéticamente. La identificación de colectas y variedades genéticamente distantes favorecerá los avances en los programas de mejoramiento genético del frijol para tolerancia a la sequía, altas temperaturas y tolerancia a las enfermedades, lo que a su vez incrementará el rendimiento y calidad del grano.
Conclusiones
Persiste variación morfo-agronómica y molecular importante en el Complejo Poblacional de la raza Durango de frijol, lo que facilitó la diferenciación entre las colectas con grado diferente de evolución y ésto fue consistente con su origen genético y geográfico. Las colectas de frijol nativo, obtenidas en La Ferrería, Dgo., se perfilaron como parte de las poblaciones originarias del frijol cultivado de la raza Durango, principalmente de aquel perteneciente a la clase comercial pinto y bayo. Los resultados obtenidos sugieren que ha habido flujo genético entre las colectas nativas y cultivadas; así como, entre las razas genéticas Durango y Jalisco. Se sugiere el estudio detallado del origen de los colores negro brillante y flor de mayo, los cuales predominan en la raza Jalisco y en la actualidad, están presentes de forma abundante en frijol nativo de la Raza Durango. Las formas intermedias que mostraron colores de grano principalmente flor de mayo (rosado y negro) puede ser el resultado del flujo genético entre colectas nativas y variedades cultivadas de frijol que fueron introducidas en Durango. Algunas colectas de frijol nativo y la mayoría de las formas intermedias colectadas en La Ferrería mostraron similitud con las variedades cultivadas en Durango, Chihuahua, Zacatecas y Jalisco.
Se observaron algunas variedades criollas con características similares a las colectas nativas y variedades recombinantes, como son Borroso y Pinto Burro, por lo que sus granos fueron grandes en comparación con el frijol nativo. La heterogeneidad intrapoblacional de los granos, observada en la mayoría de las colectas de frijol nativo y formas intermedias colectadas en Durango, dificultó la caracterización con base en los atributos de la semilla. El uso de marcadores genéticos moleculares, corroboró las diferencias genéticas entre las colectas y variedades cultivadas que fueron incluidas en el estudio. Los resultados obtenidos ayudarán a optimizar los programas de mejoramiento genético para tolerancia a sequía, temperaturas altas y enfermedades, los cuales son desarrollados en diferentes áreas productoras de frijol en México y otros países del mundo.











 nova página do texto(beta)
nova página do texto(beta)



