Introducción
Actualmente, existe mayor interés por consumir alimentos naturales, en lugar de procesados, por su valor nutritivo y nutracéutico y los aportes en beneficios de la salud, debido al alto contenido de compuestos bioactivos, que juegan un papel importante en la prevención de enfermedades crónico degenerativas en la población, lo que ha incrementado la demanda de alimentos funcionales (Tadesse & Emire, 2020). Afortunadamente, los alimentos y bebidas derivadas de plantas nativas pueden desempeñar un papel importante en la prevención de enfermedades, debido al contenido de ingredientes nutracéuticos (Sohaimy, 2012).
El aguamiel es un producto natural con atributos nutricionales (azúcares, proteínas, aminoácidos, vitaminas y minerales) y potencial nutracéutico atribuido principalmente a la presencia de compuestos fenólicos, fructooligosacáridos, saponinas y vitamina C, por lo que podría considerarse una bebida funcional o nutracéutica, con propiedades medicinales (actividad antiinflamatorio, antioxidante, anticancerígena, antimicrobiana, prebiótica, entre otras) (Castañeda-Ovando et al., 2023; Santos-Zea et al., 2012; Tovar-Robles et al., 2011). El aguamiel es la savia que se obtiene mediante el capado previo del maguey, que consiste en la eliminación del cogollo (meyolote) o meristemo del agave para evitar que brote el escapo floral, conocido también como quiote, con el fin de dejar una cavidad central denominada cajete; seguido de un periodo de maduración y concentración de las reservas de carbohidratos de la planta, conocido como añejamiento o reposo que dura entre uno a doce meses; transcurrido este periodo, se pica la cavidad central y se dejan los restos de las pencas en el centro de la planta por ocho días, con el fin de favorecer la salida de aguamiel y la acumulación en el cajete; después se inicia el raspado, esta última práctica es crucial por la cantidad y calidad del aguamiel, proceso de extracción del aguamiel que se realiza diariamente, dos veces (por la mañana y al anochecer), mediante la succión oral utilizando una calabaza grande y seca conocida como acocote (Valdivieso Solís et al., 2021; Villarreal-Morales et al., 2019).
La producción de aguamiel es principalmente reservada para la elaboración de pulque y jarabes de agave, representa una posible alternativa de consumo en regiones donde la calidad del agua no es buena y la disponibilidad de carne es limitada (Ortiz-Basurto et al., 2008); sin embargo, actualmente su consumo ha disminuido, asociado a una campaña de desprestigio hacia el pulque y a la competencia con otras bebidas, que ha repercutido en la disminución de la superficie cultivada con maguey pulquero en algunas regiones del país ( Álvarez-Ríos et al., 2020).
Por otra parte, el volumen producido de aguamiel y su composición físico-química están influenciados principalmente por la etapa de maduración de la planta, el ambiente o condiciones edafoclimáticas donde crece y por el tipo de especies de agave que lo producen (Villarreal-Morales et al., 2019; Leal-Díaz et al., 2015; Ortiz-Basurto et al., 2008). En este sentido, es importante señalar que México es considerado centro de origen del género Agave, con más de 200 especies (Narváez Suárez et al., 2016); aunque, no todas las especies de agave son adecuadas para la extracción de aguamiel, destacando como las principales especies pulqueras A. mapisaga y A. salmiana (Santos-Zea et al., 2012). De acuerdo con Mora-López et al. (2011), dentro de estas especies pulqueras, el mayor número de variedades y cultivares corresponde a A. salmiana con alrededor de 47 variantes con amplia variabilidad morfológica. Respecto a A. mapisaga, esta especie presenta menor variación morfológica, cultivado en condiciones agronómicas.
Actualmente, existen estudios referentes al valor nutricional y contenido de ingredientes nutracéuticos del aguamiel (Castañeda-Ovando et al., 2023; Peralta-García et al., 2020; Leal-Díaz et al., 2015; Santos-Zea et al., 2012; Tovar-Robles et al., 2011; Ortiz-Basurto et al., 2008); sin embargo, a pesar de la diversidad de especies y cultivares de agave en México, no existen estudios sobre sus propiedades en los diferentes cultivares de agave pulquero. Por tanto, es importante ampliar las investigaciones de la calidad nutricia y nutracéutica del aguamiel, para seleccionar aquellas especies y cultivares de agave por sus atributos antioxidantes y nutricionales, información que podría ayudar a revalorizar el consumo del aguamiel, así como, el cultivo del maguey pulquero, patrimonio natural y cultural de México. Con base en lo anterior, el objetivo de la presente investigación fue determinar las características fisicoquímicas, nutricionales y nutracéuticas del aguamiel de diferentes cultivares de A. salmiana y A. mapisaga.
Materiales y métodos
Material de estudio
Se recolectaron nueve muestras de aguamiel de dos especies de maguey pulquero (Agave mapisaga Trel y A. salmiana Otto ex Salm-Dyck), ubicadas en diferentes localidades de Hidalgo y del Estado de México de la República Mexicana.
Las muestras fueron recolectadas de diferentes cultivares xamini, cerro, penca ancha y cimarrón (A. salmiana) de magueyales de Durango, Daboxtha, El Cardonal, Hidalgo, en la región del Valle de Mezquital (Figura 1), de clima BS1kw(w) semiseco templado con lluvias en verano; otras muestras de aguamiel se obtuvieron de los cultivares manso (cultivar dominante, por lo que se recolectó en tres localidades), cenizo y carrizo (A mapisaga) recolectados de magueyales de diversas localidades de los municipios de Otumba, Teotihuacan, Axapusco y Texcoco, Estado de México, con clima C(w1) (w) b(i’) templado subhúmedo y semifrío, con lluvias en verano.

Figura 1 Agaves pulqueros utilizados para la obtención de aguamiel: A. mapisaga Trel (cultivar cenizo y carrizo) y A. salmiana (cultivar xamini, penca ancha, cerro, corriente o cimarrón y manso). Cultivar manso: 1Santa Ma. Aticpac, Axapusco, Edo. de México; 2Santiago Zacualupan, Teotihuacan, Edo. de México; 3San Marcos, Otumba, Edo. de México.
El aguamiel (aproximadamente 10 L) de cada cultivar (Cuadro 1) se obtuvo de plantas en madurez comercial, en el tercer mes del periodo de cosecha (tiempo de raspado), raspadas entre 7 y 9 de la mañana, con muestras de 1 L para su análisis; el muestreo se realizó durante 5 días. Las muestras de aguamiel fueron colocadas en botellas de polipropileno, etiquetadas y refrigeradas para disminuir el metabolismo fermentativo. Inmediatamente fueron trasladadas al laboratorio para su congelación a -22 ºC hasta su análisis.
Cuadro 1 Identificación y localización geográfica de las especies de agave pulquero utilizadas para la obtención de aguamielTable 1. Identification and geographical location of the pulquero agave species used to obtain aguamiel
| Especie | Cultivar | Lugar de recolecta | Localización | Herbario y número de registro |
|---|---|---|---|---|
| A. salmiana | Xamini | El Cardonal, Hgo. | 20°32'39.42"N, 99° 4'43.80"O 2022 msnm | MEXU, UNAM: 1388318,1388332 y 1388333 |
| A. salmiana | Cerro | El Cardonal, Hgo. | 20°32'29.40"N, 99° 4'24.54"O 2015 msnm | Preparatoria Agrícola, UACh: 31460 |
| A. salmiana | Cimarrón | El Cardonal, Hgo. | 20°32'27.00"N, 99° 4'27.42"O 2007 msnm | MEXU, UNAM: 1388337 y 1388338 |
| A. salmiana | Penca ancha | El Cardonal, Hgo. | 20°32'45.06"N, 99° 4'40.20"O 2015 msnm | MEXU, UNAM: 1388339 y 1388343 |
| A. salmiana | Manso | Otumba, Edo. de México | 19°41'49.92"N, 98°45'33.88"O 2364 msnm | Preparatoria Agrícola, UACh: 31392 |
| A. salmiana | Manso | Teotihuacan, Edo. de México | 19°42'12.09"N, 98°56'4.91"O 2280 msnm | Preparatoria Agrícola, UACh: 31391 |
| A. salmiana | Manso | Axapusco, Edo. de México | 19°52'34.96"N, 98°44'26.13"O 2379 msnm | MEXU, UNAM: 1388320 y 1388345 |
| A. mapisaga | Cenizo | Teotihuacan, Edo. de México | 19°42'56.82"N, 98°54'49.12"O 2328 msnm | Preparatoria Agrícola, UACh: 31390 |
| A. mapisaga | Carrizo | Texcoco, Edo. de México | 19°28'56.35"N, 98°50'52.61"O 2365 msnm | Preparatoria Agrícola, UACh: 30189 |
Herborización e identificación de los agaves pulqueros
De las plantaciones donde se obtuvo el aguamiel, se recolectó el material vegetal de los agaves encontrados en floración o fructificación para la preparación de un ejemplar de herbario por cultivar para su posterior identificación taxonómica y registro de ejemplares (Cuadro 1). De cada ejemplar se registró su ubicación con coordenadas geográficas, altitud, tipo de vegetación y abundancia relativa del taxón. La identificación taxonómica se realizó en el Herbario Jorge Espinosa Salas (JES) del Departamento de Preparatoria Agrícola de la Universidad Autónoma Chapingo y en el Herbario Nacional de México (MEXU) del Instituto de Biología de la UNAM.
Caracterización fisicoquímica del aguamiel
La medición de color se realizó mediante un colorímetro Hunter Lab MiniScan XE Plus (modelo 45/0-L RestonVa, USA), con un iluminante D65, un ángulo del observador de 10° y la escala CIE L*a*b*. Debido a que la determinación de esta variable se realizó en una muestra líquida, el aguamiel se colocó en una cápsula de vidrio del Hunter Lab especial para líquidos; la cápsula se situó sobre una base, la distancia entre ésta y el punto de emisión de luz del equipo estuvo previamente estandarizada. Se cubrió la cápsula con un cilindro de papel negro para evitar la incidencia de luz sobre el líquido. Se calculó el índice de saturación del color (Croma) y el ángulo de tono (Hue) de acuerdo con lo descrito por McGuire (1992).
El pH se determinó en un potenciómetro (H1 2221 Hanna Instruments, Woonsocket, RI, USA); los sólidos solubles totales (SST, ºBrix) fueron medidos con un refractómetro (PAL-3, ATAGO®, Japon); y los azúcares reductores directos (ARD), sacarosa y azúcares totales (AT) por la prueba de Lane-Eynon, mediante la solución Fehling-Soxhlet, descritó por la Asociación de Químicos Analíticos Oficiales (AOAC, 2005).
Contenido mineral
La cuantificación se realizó de acuerdo con los métodos señalados por Perkin-Elmer Corporation (1996), con modificaciones. Las muestras de aguamiel se trataron con ácido nítrico a 50% (v/v) en una digestión húmeda a 95 ºC por 45 min (Sistema de digestión Tecator, TD20 Digestion System Tubes and Racks, Foss, USA). Posteriormente, se realizó una segunda etapa de digestión/oxidación mediante la adición de peróxido de hidrógeno (30 % p/v) para su incubación a 95 ºC (15 min). Después de la digestión total, cada muestra se aforó a 50 mL con agua desionizada. Se determinaron los contenidos de Cu, Zn, Fe, Ca, Mg, K y Na mediante espectrofotometría de absorción atómica (700 AAnalyst, PerkinElmer, USA).
Análisis proximal
Los contenidos de humedad (g L-1), cenizas (g L-1), proteína cruda (g L-1) y carbohidratos (g L-1) se determinaron de acuerdo con la metodología establecida por la AOAC (2005). El valor energético (g L-1) del aguamiel se determinó mediante los factores de Atwater (AOAC, 2005).
Determinación de compuestos fenólicos solubles totales
El contenido de compuestos fenólicos se determinó por el método descrito por Joaquín-Cruz et al. (2015), con algunas modificaciones. Cada muestra de aguamiel se ajustó a una concentración de 10% en metanol acidificado a 1% con ácido trifluroacético, la mezcla se sonicó por 30 min con un equipo de ultrasonido (Cole Parmer 8892, Illinois, USA). La mezcla se dejó reposar en oscuridad por 20 min a temperatura ambiente (~22 °C). Posteriormente, las muestras se centrifugaron a 1431 x g por 15 min (Cole Parmer YV-17414-21, Illinois, USA) para facilitar la separación del sobrenadante y residuo. El sobrenadante fue recuperado y el residuo sometido a dos extracciones más, usando como disolvente de extracción metanol: ácido acético: agua en una proporción de 10:1:9 (v/v/v). Los sobrenadantes de las tres extracciones se unieron y se cuantificó el contenido de compuestos fenólicos totales por el método de Folin-Ciocalteu (Singleton & Rossi, 1965). Una alícuota de 1 mL del extracto se mezcló con 10 mL de agua y 1 mL del reactivo de Folin-Ciocalteu (2 N, Sigma - Aldrich), se dejó reposar por 2 min. Finalmente, a la mezcla se le adicionaron 4 mL de una solución de carbonato de sodio (Na2CO3) a 7.5% (p/v) y se dejó reposar en oscuridad a temperatura ambiente por 60 min; Se tomó lectura de la absorbancia a 765 nm en un espectrofotómetro (Genesys 10s, Thermo Scientific, USA). La curva de calibración (y=5.9332x−0.0375 , R 2 =0.995) se construyó con ácido gálico como referencia. El contenido total de compuestos fenólicos se expresó en mg equivalentes de ácido gálico por litro de aguamiel (mg EAG 100 L-1).
Cuantificación de flavonoides
Las muestras de aguamiel se disolvieron en metanol a 80% v/v para obtener una concentración de 40% (v/v). El contenido de flavonoides se cuantificó de acuerdo con el método Dowd, adaptado por Arvouet-Grand et al. (1994). A 2 mL del extracto metanólico se le agregaron 0.5 mL de AlCl3 (2% p/v) y agua destilada hasta un volumen final de 25 mL. La mezcla se homogeneizó en un vortex y se incubó durante 30 min a temperatura ambiente, en oscuridad. Se leyó la absorbancia a una longitud de onda de 425 nm en un espectrofotómetro (Genesys 10s, Thermo Scientific, USA). La curva estándar se construyó con quercetina como referencia (𝑦=5.4696𝑥+0.0018 , R 2 =0.996). Los resultados se expresaron en mg equivalentes de quercetina en un litro de aguamiel (mg EQ L1).
Cuantificación de vitamina C
La concentración de vitamina C (ácido ascórbico) se determinó por espectrofotometría siguiendo el método descritó por Burdurlu et al. (2006), con algunas modificaciones. Se tomó 1 mL del aguamiel y se aforó a 10 mL con ácido metafosfórico a 3% (p/v). En un matraz erlenmeyer se colocaron 2 mL de la mezcla anterior, 2 mL de regulador de acetatos (solución buffer pH = 4, ácido acético glacial: acetato de sodio a 5% p/v), 3 mL de 2,6-dicloroindofenol y 15 mL de xileno, en sucesión rápida y agitación vigorosa. La solución se transfirió a un embudo de separación para eliminar la fase acuosa. A la fase de xileno se le adicionó un gramo de cristales de Na2SO4 anhidro, para eliminar trazas de agua; posteriormente, se leyó su absorbancia a una longitud de onda de 520 nm en un espectrofotómetro (Genesys 10s, Thermo Scientific, USA). El contenido de vitamina C fue calculado mediante una curva estándar de ácido ascórbico (𝑦= −2.666𝑥+0.567 , R 2 =0.995), los resultados se expresaron en mg equivalentes de ácido ascórbico por litro (mg EAA L-1).
Evaluación de la actividad antioxidante
La actividad antioxidante se determinó por el método del radical libre DPPH (2,2-difenil-1-picrilhidrazil) descrito por Brand-Williams et al. (1995). El aguamiel fue diluido a una concentración de 40% (v/v) en metanol a 80% v/v. Para la reacción de reducción del DPPH, 0.1 mL del extracto metanólico se mezcló con 2.9 mL de solución de DPPH (6 x 10-5 M). La mezcla se mantuvo en reacción en oscuridad por 30 min a temperatura ambiente, después la absorbancia se midió a 517 nm en un espectrofotómetro (Genesys 10s). Como referencia se realizó una curva estándar de Trolox (𝑦=76.889𝑥+2.2556 , R 2 =0.997). Los resultados se expresaron en (M equivalentes de trolox por litro de aguamiel (μM ET L-1). La actividad antioxidante de cada muestra se determinó por el porcentaje de reducción de DPPH (% 𝐷𝑃𝑃𝐻 𝐼𝑛ℎ𝑖𝑏𝑖𝑑𝑜 = Abs blanco − Abs muestra ×100 Abs blanco ).
Análisis estadístico
Los resultados de la caracterización de los diferentes tipos de aguamiel se sometieron a un análisis de varianza (ANOVA) de acuerdo con un diseño completamente al azar con nueve tratamientos y comparación de medias de tratamientos (Tukey, P ≤ 0.05). La unidad experimental consistió en un litro de aguamiel. La relación entre las características físico-químicas, nutricionales y nutracéuticas del aguamiel fueron determinadas por el coeficiente de correlación de Pearson mediante el programa Statistical Analysis System (SAS 9.0 for Windows). Finalmente, se realizó un análisis de componentes principales con la finalidad de agrupar las muestras de aguamiel por sus características mediante el programa The Unscrambler X 10.3 (Camo Process AS, Oslo, Norway).
Resultados y discusión
Propiedades físico-químicas
El análisis estadístico mostró diferencias significativas (P ≤ 0.05) en los atributos de color del aguamiel entre cultivares, especies y origen (Cuadro 2). Las muestras de aguamiel presentaron valores menores (25%) de luminosidad (L*) (brillantez de color), lo que permitió formar dos grupos: 1) aguamiel de color más claro (12.5 % < L* < 25%) donde se ubicó el aguamiel de los cultivares manso, xamini, carrizo, cimarrón y penca ancha, y 2) aguamiel más oscuro (L* < 12.5%), recolectado de los cultivares cenizo y cerro (Figura 2).
Cuadro 2 Atributos de color en aguamiel de Agave salmiana (cultivares xamini, cerro, cimarrón, penca ancha y manso) y A. mapisaga (cutivares carrizo y cenizo), recolectado en diferentes localidades del Estado de México e Hidalgo, México.Table 2. Color attributes of aguamiel of Agave salmiana (cultivars xamini, cerro, cimarrón, penca ancha and manso) and A. mapisaga (cutivars carrizo and cenizo), obtained in different locations from States of Mexico and Hidalgo, Mexico.
| Especie | Cultivar* | Luminosidad (%) | Ángulo de tono (°Hue) | Índice de saturación (Croma) |
|---|---|---|---|---|
| A. salmiana | Xamini1 | 20.22 ± 0.17 bcd | 69.97 ± 5.31 abc | 1.97 ± 0.46 cd |
| A. salmiana | Cerro1 | 12.04 ± 0.17 f | 53.49 ± 4.35 d | 1.12 ± 0.14 e |
| A. salmiana | Cimarrón1 | 18.63 ± 0.18 de | 74.44 ± 1.67 ab | 2.64 ± 0.04 bc |
| A. salmiana | Penca ancha1 | 16.94 ± 0.07 e | 61.10 ± 3.98 cd | 1.07 ± 0.04 e |
| A. salmiana | Manso2 | 21.85 ± 0.04 ab | 79.90 ± 0.58 a | 4.66 ± 0.06 a |
| A. salmiana | Manso3 | 19.46 ± 0.31 cd | 74.76 ± 3.05 ab | 2.31 ± 0.16 bc |
| A. salmiana | Manso5 | 23.04 ± 0.50 a | 78.02 ± 0.99 a | 4.00 ± 0.27 a |
| A. mapisaga | Cenizo4 | 11.83 ± 0.52 f | 65.15 ± 7.49 bc | 1.15 ± 0.20 de |
| A. mapisaga | Carrizo6 | 20.95 ± 2.28 bc | 76.12 ± 5.27 a | 2.93 ± 1.00 b |
| DHS§ | 1.93 | 10.16 | 0.82 | |
*Aguamiel recolectado en: 1Durango Daboxtha, El Cardonal, Hgo.; 2San Marcos, Otumba, Méx.; 3Santa Ma. Actipac, Axapusco, Méx.; 4San Isidro del Progreso, Teotihuacan, Méx.; 5Santiago Zacualuca, Teotihuacan, Méx.; 6Tequexquinahuac, Texcoco, Méx. Los valores reportados son la media de 5 repeticiones ± desviación estándar. §DSH: Diferencia significativa honesta (Tukey, 0.05). Medias con la misma letra, en una misma columna, son estadísticamente iguales.

Figura 2 Aguamiel obtenido de Agave salmiana (cultivares xamini, cerro, cimarrón o corriente, penca ancha y manso) y A. mapisaga (cultivares carrizo y cenizo), recolectado en diferentes localidades del Estado de México e Hidalgo, México.
Los valores de Hue asociados con la percepción de color fueron menores a 80º, observándose dos grupos: aguamiel color amarillo (cultivares carrizo, cimarrón y manso) con valores de hue entre 70° y 80°; y aguamiel de color amarillo-marrón (xamini, penca ancha, cenizo y cerro) con hue menor a 70°; sin embargo, todas las muestras de aguamiel presentaron bajos valores de croma (Cuadro 2), lo que indicó poca pureza de color, es decir, que el color estuvo más cerca del gris (Figura 2).
También se encotraron diferencias significativas (P ≤ 0.05) en las características físicoquímicas (pH, SST, ARD, sacarosa y AT) del aguamiel entre los diferentes cultivares, especies y origen (Cuadro 3). El aguamiel del cultivar cenizo (A. mapisaga) fue estadísticamente superior en el contenido de SST y la concentración de AT en comparación al aguamiel de los otros cultivares, con 93.45% de sacarosa en AT. En contraste, el aguamiel obtenido del cultivar manso (Agave salmiana) de Axapusco, Estado de México, presentó el mayor contenido de ARD (76.83 g L-1). Las variaciones de SST y AT entre cultivares pueden deberse a los diferentes tiempos de añejado del maguey (reposo de la planta después de ser “capada” para inducir la producción de aguamiel), práctica agrícola que permite la maduración de las hojas centrales y aumento del contenido de azúcares totales (AT) en la savia (Lappe-Oliveras et al., 2008).
Cuadro 3 Características físicoquímicas del aguamiel de Agave salmiana (cultivares xamini, cerro, cimarrón, penca ancha y manso) y A. mapisaga (cultivares carrizo y cenizo).Table 3. Physical-chemical characterization of aguamiel of Agave salmiana (cultivars xamini, cerro, cimarrón, penca ancha and manso) and A. mapisaga (cultivars carrizo and cenizo).
| Especie | Cultivar* | pH | Sólidos solubles totales (°Brix) |
Azúcares reductores directos (g L −1 ) |
Sacarosa (g L −1) |
Azúcares totales g L −1 |
|---|---|---|---|---|---|---|
| A. salmiana | Xamini1 | 7.45 ± 0.38 ab | 11.06 ± 0.63 bcde | 22.04 ± 3.30 cd | 70.83 ± 16.18 c | 96.59 ± 13.90 bcd |
| A. salmiana | Cerro1 | 6.91 ± 0.01 b | 9.65 ± 0.17 de | 14.31 ± 0.18 ef | 77.81 ± 5.42 bc | 96.22 ± 5.53 bcd |
| A. salmiana | Cimarrón1 | 5.08 ± 0.01 cd | 12.60 ± 0.19 b | 15.50 ± 0.17 def | 98.95 ± 9.48 b | 119.66 ± 10.03 b |
| A. salmiana | Penca ancha1 | 7.09 ± 0.01 b | 11.56 ± 0.79 bcd | 8.24 ± 0.22 fg | 101.57 ± 16.40 b | 115.16 ± 17.14 bc |
| A. salmiana | Manso2 | 4.57 ± 0.01 d | 12.12 ± 0.10 bc | 49.35 ± 3.86 b | 41.74 ± 6.92 d | 93.28 ± 3.86 cd |
| A. salmiana | Manso3 | 5.19 ± 0.01 c | 10.32 ± 0.10 cde | 76.83 ± 4.19 a | 10.01 ± 3.30 e | 87.37 ± 2.20 d |
| A. salmiana | Manso5 | 5.03 ± 0.02 cd | 9.40 ± 0.10 e | 27.12 ± 0.31 c | 54.93 ± 11.62 cd | 84.93 ± 12.34 d |
| A. mapisaga | Cenizo4 | 7.77 ± 0.24 a | 16.02 ± 1.23 a | 2.67 ± 0.23 g | 143.50 ± 8.68 a | 153.72 ± 9.09 a |
| A. mapisaga | Carrizo6 | 5.24 ± 0.50 c | 11.19 ± 2.15 bcde | 20.81 ± 6.58 cde | 77.62 ± 8.41 bc | 102.52 ± 6.80 bcd |
| DSH§ | 0.55 | 2.06 | 7.42 | 25.50 | 24.15 |
*Aguamiel recolectado en: 1Durango Daboxtha, El Cardonal, Hgo.; 2San Marcos, Otumba, Méx.; 3Santa Ma. Actipac, Axapusco, Méx.; 4San Isidro del Progreso, Teotihuacan, Méx.; 5Santiago Zacualuca, Teotihuacan, Méx.; 6Tequexquinahuac, Texcoco, Méx. Los valores reportados son la media de 5 repeticiones ± desviación estándar. §DSH: Diferencia significativa honesta (Tukey, 0.05). Medias con la misma letra, en una misma columna, son estadísticamente iguales.
En general, el pH del aguamiel se encontró en el intervalo de 4.57 a 7.77, la literatura reporta que el aguamiel normalmente puede presentar un pH ácido (≤ 4.5) a ligeramente alcalino (aproximadamente 8.0), asociado al grado de fermentación, ya que principalmente a mayor concentración de ácido láctico, producto de la fermentación, menor pH (Medina Mendoza et al., 2022). De acuerdo a Escalante et al. (2012) el aguamiel Tipo I se caracteriza por un pH menor entre 6.60-7.50 y una concentración de ácido láctico menor a 0.90-1.03 mg 100 mL-1; el aguamiel Tipo II con pH < 4.5 y una concentración de ácido láctico < 4 mg 100 mL-1. El pH del aguamiel puede acidificarse por la acumulación de otros ácidos orgánicos producidos por la flora microbiana (fermentación) que se desarrolla espontáneamente desde que el aguamiel se encuentra en el cajete del maguey, asociada al medio ambiente (polvo, aire o insectos) o incorporada mediante las herramientas de raspado o extracción del aguamiel (Contreras-López et al., 2023; Escalante et al., 2012).
Por otra parte, el pH mostró correlación con el contenido de azúcares reductores directos (-0.607) y con el contenido de sacarosa (0.6379), debido a que el pH ácido es una condición que favorece la hidrólisis de sacarosa en glucosa y fructosa (Ávila Núñez et al., 2012). Por lo anterior, un pH ácido es el óptimo para la hidrólisis de sacarosa del aguamiel en el cajete, por lo que aquellas muestras de aguamiel con pH ácido presentaron mayor contenido de azúcares reductores (glucosa y frucosa) (Cuadro 3).
Contenido de minerales
Otros componentes nutritivos del aguamiel son los minerales, implicados en varias funciones vitales del cuerpo humano. El mineral predominante en el aguamiel (Cuadro 4) fue el potasio (K), con un contenido promedio de 1830 mg L-1, equivalente a 41% del potasio presente en un kilo de plátano, considerando que un plátano de tamaño mediano aporta aproximadamente 440 mg de K (Brown, 2016). El consumo de este mineral es importante debido a que una dieta rica en potasio reduce la presión arterial en personas con presión arterial elevada. Considerando que la dosis dietética recomendada de K es de 4700 mg día-1 en adultos (Brown, 2016), el consumo de un litro de aguamiel podría contribuir ha satisfacer al menos 24.2% de los requerimientos diarios, y el consumo de aguamiel de A. mapisaga cultivar cenizo podría aportar un porcentaje mayor (76.8%).
Cuadro 4 Composición mineral del aguamiel de A. salmiana (cultivares xamini, cerro, cimarrón, penca ancha y manso) y A. mapisaga (cultivares carrizo y cenizo), recolectado en diferentes localidades del Estado de México e Hidalgo.Table 4. Mineral composition of aguamiel of Agave salmiana (cultivars xamini, cerro, cimarrón, penca ancha and manso) and A. mapisaga (cutivars carrizo and cenizo), obtained in different locations from States of Mexico and Hidalgo, Mexico.
| Especie | Cultivar* | Minerales (mg L-1) | ||||||
|---|---|---|---|---|---|---|---|---|
| K | Mg | Ca | Na | Fe | Cu | Zn | ||
| A. salmiana | Xamini1 | 1650.97 ± 437.09 bc | 93.86 ± 28.51 bc | 154.68 ± 61.70 bc | 161.19 ± 26.44 a | 25.60 ± 0.33 a | 4.33 ± 1.79 cd | 0.59 ± 0.23 bc |
| A. salmiana | Cerro1 | 1944.04 ± 442.90 bc | 127.62 ± 32.29 abc | 409.97 ± 94.43 a | 162.81 ± 6.40 a | 25.91 ± 0.58 a | 1.85 ± 0.17 d | 0.87 ± 0.40 bc |
| A. salmiana | Cimarrón1 | 1442.29 ± 55.16 c | 88.03 ± 4.08 bc | 199.11 ± 26.49 b | 140.55 ± 36.64 a | 20.05 ± 0.03 cd | 4.73 ± 1.37 bcd | 0.85 ± 0.06 bc |
| A. salmiana | Penca ancha1 | 1499.68 ± 40.82 bc | 65.13 ± 5.06 c | 123.75 ± 7.59 bc | 155.49 ± 13.88 a | 11.85 ± 0.65 e | 6.22 ± 1.47 abc | 1.11 ± 0.35 ab |
| A. salmiana | Manso2 | 2300.27 ± 183.89 ab | 167.95 ± 2.69 a | 204.06 ± 13.60 b | 170.46 ± 12.86 a | 19.36 ± 1.07 cd | 8.55 ± 0.96 a | 1.53 ± 0.12 a |
| A. salmiana | Manso3 | 1993.34 ± 17.71 abc | 138.46 ± 7.08 ab | 70.22 ± 5.71 c | 167.56 ± 43.66 a | 18.34 ± 0.57 d | 2.66 ± 0.48 cd | 0.43 ± 0.15 c |
| A. salmiana | Manso5 | 1533.15 ± 66.76 bc | 112.46 ± 14.66 abc | 111.31 ± 51.11 bc | 160.62 ± 37.51 a | 21.71 ± 2.31 bc | 3.70 ± 1.38 cd | 0.68 ± 0.27 bc |
| A. mapisaga | Cenizo4 | 2813.39 ± 798.17 a | 148.09 ± 64.70 ab | 99.57 ± 18.62 bc | 186.20 ± 16.26 a | 23.17 ± 0.71 ab | 8.21 ± 2.87 ab | 0.95 ± 0.40 abc |
| A. mapisaga | Carrizo6 | 1290.86 ± 151.44 c | 84.59 ± 11.21 bc | 64.66 ± 9.30 c | 176.19 ± 14.10 a | 6.53 ± 2.54 f | 5.83 ± 2.18 abc | 0.96 ± 0.13 abc |
| DHS§ | 830.39 | 64.449 | 104.53 | 64.88 | 2.94 | 3.75 | 0.62 | |
*Aguamiel recolectado en: 1Durango Daboxtha, El Cardonal, Hgo.; 2San Marcos, Otumba, Méx.; 3Santa Ma. Actipac, Axapusco, Méx.; 4San Isidro del Progreso, Teotihuacan, Méx.; 5Santiago Zacualuca, Teotihuacan, Méx.; 6Tequexquinahuac, Texcoco, Méx. Los valores reportados son la media de 5 repeticiones ± desviación estándar. §DSH: Diferencia significativa honesta (Tukey, 0.05). Medias con la misma letra, en una misma columna, son estadísticamente iguales.
Respecto al magnesio (Mg), mineral necesario para casi todos los procesos bioquímicos del cuerpo por su participación en el control de los niveles de azúcar en sangre y en el mantenimiento del sistema inmunológico (Carrillo-López et al., 2016). En la presente investigación se encontró una concentración promedio de 114.02 ( 41.73 mg L-1 de aguamiel (Cuadro 4), con diferencias entre muestras que se pueden deber a diversas condiciones edafológicas (condiciones del suelo) propias de los sitios de recolecta. Por lo que, el consumo de un litro de aguamiel podría contribuir a satisfacer entre el 27 a 35 % de los requerimientos diarios en adultos mayores de 70 años (Ingesta dietética recomendada de 420/320 mg en hombres y mujeres, respectivamente (Brown, 2016).
Otro mineral importante en el aguamiel fue el calcio (Ca), elemento requerido principalmente durante el embarazo para el desarrollo esquelético del feto (Brown, 2016), esta bebida contiene entre 64.66 a 409.97 mg de Ca por litro. El aguamiel obtenido del cultivar cerro de A. salmiana (Cuadro 4) destaca por el mayor contenido. El consumo de un litro de esta bebida podría contribuir con hasta 50% de los requerimientos dietéticos recomendados en mujeres embarazadas de 19 a 30 años (1000 mg d-1) (Brown, 2016), por lo que el aguamiel de este cultivar es una excelente fuente de este mineral a bajo costo.
De la misma forma, es importante destacar el contenido de hierro (Fe) en el aguamiel de las especies y cultivares estudiados, el cultivar cerro de A. salmiana mostró la mayor concentración de este mineral (Cuadro 4). Actualmente, la carencia nutricional más generalizada en todo el mundo y la principal causa de anemia es por la falta de Fe, la ingesta de un litro de aguamiel podría contribuir a que una mujer embaraza adquiera de 25 a 95% de los requerimientos diarios de este mineral (ingesta dietética recomendada en mujeres embarazadas: 27 mg d-1) (Brown, 2016)). El Fe presente en el aguamiel es “no hemínico” (presente en vegetales, no en carne); sin embargo, la absorción de este tipo de Fe es favorecido por la presencia de vitamina C (Binaghi et al., 2008) y de fructanos (Castañeda-Ovando et al., 2023), el aguamiel es una fuente de estos metabolitos. Aunado a lo anterior, el aguamiel es una excelente fuente de cobre (Cu), al encontrarse en concentraciones de 1.85 a 8.55 mg L-1 (Cuadro 4), mineral que es componente de las enzimas implicadas en la utilización y movilización del Fe en el cuerpo (Brown, 2016).
Por otra parte, los contenidos de Na y Zn fueron bajos, por lo que el consumo de un litro de aguamiel solo contribuiría aproximadamente con 10 % de la ingesta diaria recomendada de estos minerales (1500-2300 mg d-1 de Na y 8-11 mg d-1 de Zn (Brown, 2016)). Es importante destacar que el contenido de Na mostró niveles bajos en todas las muestras estudiadas (Cuadro 4), lo anterior es valioso, ya que actualmente, es ampliamente conocida la estrecha relación entre la hipertensión y la ingesta dietética de Na (mayor riesgo de enfermedades cardiovasculares cuando la ingesta de Na excede los 5 g día-1 o es inferior a 3 g día-1) (Mente et al., 2021), por lo cual el aguamiel puede ser consumido por personas con hipertension sin ningun riesgo para su salud.
Finalmente, es importante señalar que las diferencias encontradas en las concentraciones de minerales en el aguamiel de las diversas especies y cultivares pueden atribuirse a las características del suelo (tipo, fertilidad, propiedades físicas y químicas) del sitio de recolecta y manejo agronómico que se realiza a las plantas (Pohl, 2009; Santos-Zea et al., 2012), principalmente fertilización por los productores del lugar con composta orgánica de estiércol de ovino (Com. personal). Con base en los resultados, el consumo de aguamiel representa una alternativa económica de ingesta de algunos requerimientos mínimos de minerales para personas de zonas rurales marginadas del país.
Análisis proximal
El contenido de humedad fue estadísticamente diferente entre las muestras de aguamiel estudiadas (Cuadro 5), el del cultivar cerro destacó con un valor mayor (90.80% p/v equivalente a 908.00 g L-1); sin embargo, los cultivares restantes se encontraron en el contenido promedio de humedad reportado (85 a 88%, equivalente a 850 a 880 g L-1) por Silos-Espino et al. (2011).
Cuadro 5 Composición proximal del aguamiel de A. salmiana (cultivares xamini, cerro, cimarrón, penca ancha y manso) y A. mapisaga (cultivares carrizo y cenizo), recolectado en diferentes localidades del Estado de México e Hidalgo.Table 5. Proximal composition of aguamiel of Agave salmiana (cultivars xamini, cerro, cimarrón, penca ancha and manso) and A. mapisaga (cutivars carrizo and cenizo), obtained in different locations from States of Mexico and Hidalgo, Mexico.
| Especie | Cultivar* | Humedad (g L-1) |
Carbohidratos (g L-1) |
Proteína (g L-1) |
Cenizas (g L-1) |
Valor energético (kcal L-1) |
|---|---|---|---|---|---|---|
| A. salmiana | Xamini1 | 870.47 ± 6.88 b | 118.20 ± 8.10 b | 7.60 ± 0.72 b | 6.72 ± 2.29 ab | 449.51 ± 32.38 b |
| A. salmiana | Cerro1 | 908.00 ± 10.21 a | 70.78 ± 9.28 c | 11.96 ± 1.09 a | 9.26 ± 1.18 a | 300.66 ± 36.58 c |
| A. salmiana | Cimarrón1 | 873.23 ± 6.40 b | 111.97 ± 5.74 b | 8.40 ± 0.73 b | 6.41 ± 1.57 ab | 440.26 ± 18.00 b |
| A. salmiana | Penca ancha 1 | 885.15 ± 1.89 ab | 104.65 ± 3.72 b | 6.13 ± 0.53 b | 4.07 ± 2.60 b | 405.69 ± 11.13 bc |
| A. salmiana | Manso2 | 871.89 ± 17.00 b | 111.08 ± 16.50 b | 7.45 ± 0.72 b | 9.58 ± 1.40 a | 433.80 ± 62.00 b |
| A. salmiana | Manso3 | 874.24 ± 1.20 b | 110.28 ± 2.80 b | 7.73 ± 0.47 b | 7.75 ± 1.75 ab | 431.80 ± 9.01 b |
| A. salmiana | Manso5 | 890.77 ± 5.70 ab | 90.42 ± 4.80 bc | 8.18 ± 0.62 b | 10.63 ± 3.10 a | 360.24 ± 18.20 bc |
| A. mapisaga | Cenizo4 | 794.30 ± 19.00 c | 190.49 ± 20.20 a | 8.54 ± 0.59 b | 6.67 ± 1.50 ab | 729.70 ± 73.80 a |
| A. mapisaga | Carrizo6 | 891.67 ± 24.20 ab | 90.84 ± 25.00 bc | 7.70 ± 2.60 b | 9.80 ± 2.80 a | 360.16 ± 89.80 bc |
| DSH§ | 29.80 | 30.70 | 2.60 | 4.90 | 111.50 |
*Aguamiel recolectado en: 1Durango Daboxtha, El Cardonal, Hgo.; 2San Marcos, Otumba, Méx.; 3Santa Ma. Actipac, Axapusco, Méx.; 4San Isidro del Progreso, Teotihuacan, Méx.; 5Santiago Zacualuca, Teotihuacan, Méx.; 6Tequexquinahuac, Texcoco, Méx. Los valores reportados son la media de 5 repeticiones ± desviación estándar. §DSH: Diferencia significativa honesta (Tukey, 0.05). Medias con la misma letra, en una misma columna, son estadísticamente iguales.
Los carbohidratos representaron el segundo componente más importante del aguamiel (Cuadro 5), el 95.3% corresponde a AT (ARD + sacarosa), la diferencia podrían ser carbohidratos complejos y/o fibra. De acuerdo con Ortiz-Basurto et al. (2008), 75% corresponde a carbohidratos como 32.4% fructosa, 26.5% glucosa, 8.8% sacarosa y 10% fructooligosacáridos, en materia seca de aguamiel. Asimismo, el aguamiel del cultivar cerro presentó los valores más bajos de AT, de acuerdo con los productores, esto podría ser una característica para considerarse de menor calidad en la elaboración de pulque y jarabes debido a la baja disponibilidad de azúcares para la fermentación o concentración de estos.
Los valores de proteína encontrados en el aguamiel de los diferentes cultivares y especies analizadas (6.13 a 11.96 g L-1) fueron superiores a lo reportado en aguamiel de Agave salmiana (6.9 g L-1) por Silos-Espino et al. (2011) y en Agave mapisaga (3.5 g L-1) por Ortiz-Basurto et al. (2008). El consumo de un litro de aguamiel de los cultivares estudiados podría cubrir entre 23 y 62% de la cantidad diaria de proteínas recomendada en infantes de 1-13 años (13 a 34 g día-1) (Brown, 2016), lo que sugiere que esta bebida podría ser una alternativa de consumo en aquellos lugares del país donde el agua y el consumo de carne son limitados. Los alimentos son fuente de proteína de diferente calidad, la cual depende de varios factores, uno de ellos es el perfil de aminoácidos esenciales; al respecto, diversos estudios señalan que el aguamiel es fuente de todos los aminoácidos esenciales, a excepción de metionina (Castañeda-Ovando et al., 2023; Ortiz-Basurto et al., 2008; Villarreal-Morales et al., 2019).
Por último, es importante referir que el aguamiel es una bebida de bajo valor energético (Cuadro 5) y alto valor nutricional, lo que le confiere atributos para considerarse como una bebida funcional. Rivera et al. (2008) señalan que las bebidas con alto aporte energético incrementan el riesgo de obesidad, por ello se deben de consumir de forma esporádica, siendo fundamental considerar consumir bebidas que tengan un equilibrio entre valor calórico y contenido de nutrientes como parte de una alimentación saludable.
Contenido de antioxidantes
Compuestos fenólicos
Los compuestos fenólicos, uno de los de mayor grupo de fitoquímicos presentes en las plantas, destacan por sus propiedades antioxidantes, actividad cardioprotectora, cancerígena, antiinflamatoria, antimicrobiana y efecto neuro-protector (Li et al., 2014). Los resultados del contenido de compuestos fenólicos demostraron que el aguamiel es una fuente de estos metabolitos (240.21 - 478.28 mg EAG L-1) (Cuadro 6). El análisis estadístico mostró diferencias significativas (P ≤ 0.05) en la concentración de compuestos fenólicos entre las muestras de aguamiel estudiadas. El valor mayor se observó en el aguamiel de Agave salmiana cultivar cerro (estado de Hidalgo), estadísticamente superior al de los otros cultivares debido a que éste presentó aproximadamente el doble de compuestos fenólicos en comparación con el aguamiel de maguey manzo. Es importante destacar que el cultivar cerro también produjo el aguamiel con el mayor contenido de proteína, Fe y Ca.
Cuadro 6 Contenido de fitoquímicos y actividad antioxidante en aguamiel de A. salmiana (cultivares xamini, cerro, cimarrón, penca ancha y manso) y A. mapisaga (cultivares carrizo y cenizo), recolectado en el Estado de México e Hidalgo.Table 6. Phytochemical content and antioxidant activity in Agave salmiana (cultivars xamini, cerro, cimarrón, penca ancha and manso) and A. mapisaga (cutivars carrizo and cenizo), obtained in different locations from States of Mexico and Hidalgo, Mexico.
| Especie | Cultivar* | Fenoles totales (mg EAG L-1) |
Flavonoides totales (mg EAG L-1) |
Vitamina C (mg EAA L-1) |
DPPH inhibido (%) |
Actividad antioxidante ((M ET L-1) |
|---|---|---|---|---|---|---|
| A. salmiana | Xamini1 | 375.35 ± 42.63 b | 2.27± 0.69 c | 598.00 ± 18.18 a | 38.38 ± 8.18 b | 1208.31 ± 249.25 b |
| A. salmiana | Cerro1 | 478.28 ± 20.94 a | 2.55 ± 0.64 c | 454.69 ± 30.89 b | 83.16 ± 0.25 a | 2576.29 ± 7.77 a |
| A. salmiana | Cimarrón1 | 347.66 ± 23.08 b | 1.39 ± 0.25 c | 239.49 ± 38.84 d | 37.84 ± 0.56 b | 1191.80 ± 17.21 b |
| A. salmiana | Penca ancha1 | 336.89 ± 18.46 b | 0.66 ± 0.39 d | 304.20 ± 58.31 cd | 31.06 ± 0.21 bc | 984.80 ± 6.41 bc |
| A. salmiana | Manso2 | 240.21 ± 33.59 c | 4.72 ± 0.53 b | 233.36 ± 18.01 d | 25.52 ± 0.59 cd | 815.31 ± 17.98 cd |
| A. salmiana | Manso3 | 247.70 ± 9.45 c | 6.42 ± 0.19 a | 351.39 ± 37.26 c | 27.96 ± 1.00 c | 892.33 ± 32.00 c |
| A. salmiana | Manso5 | 335.04 ± 22.16 b | 2.24 ± 0.82 c | 264.51 ± 41.90 cd | 29.69 ± 2.43 bc | 942.88 ± 74.34 bc |
| A. mapisaga | Cenizo4 | 318.44 ± 14.70 b | 3.95 ± 1.03 b | 230.12 ± 61.60 d | 23.65 ± 3.45 cd | 758.33 ± 105.26 cd |
| A. mapisaga | Carrizo6 | 251.37 ± 62.50 c | 1.27 ± 0.69 cd | 232.77 ± 68.19 d | 18.89 ± 6.26 d | 612.89 ± 191.08 cd |
| DSH§ | 60.44 | 1.39 | 93.05 | 8.82 | 269.47 |
*Aguamiel recolectado en: 1Durango Daboxtha, El Cardonal, Hgo.; 2San Marcos, Otumba, Méx.; 3Santa Ma. Actipac, Axapusco, Méx.; 4San Isidro del Progreso, Teotihuacan, Méx.; 5Santiago Zacualuca, Teotihuacan, Méx.; 6Tequexquinahuac, Texcoco, Méx. Los valores reportados son la media de 5 repeticiones ± desviación estándar. §DSH: Diferencia significativa honesta (Tukey, 0.05). Medias con la misma letra, en una misma columna, son estadísticamente iguales.
Se encontró que estos metabolitos mostraron una fuerte correlación negativa (-0.77) con el ángulo de tono (hue), por lo que su presencia fue mayor en las muestras de aguamiel de color oscuro (xamini, penca ancha, cenizo y cerro) de tonalidad amarillo-marrón (menor hue), causada posiblemente por la oxidación de este tipo de metabolitos, ya que tienen tendencia a autooxidarse y formar quinonas, responsables del color amarrillo-marrón, oxidación catalizada por la enzima polifenoloxidasa (Rappoport, 2003).
También es importante señalar que se encontró correlación de los compuestos fenólicos con el contenido de calcio (0.76), por lo que las muestras de aguamiel de mayor contenido de este mineral (A. salmiana cultivar cerro) presentaron el más alto contenido de estos metabolitos (Cuadro 6). Esta correlación explica que el Ca es un factor importante en la estimulación de la síntesis de compuestos fenólicos al incrementar la actividad enzimática de fenilalanina-amonioliasa (PAL), enzima clave para la síntesis e estos metabolitos (Ngadze et al., 2014).
Flavonoides
Los flavonoides son un grupo importante dentro de los compuestos fenólicos. En el Cuadro 6 se observa el bajo contenido de flavonoides reportado en aguamiel, como lo señala Ahumada-Santos et al. (2013) al encontrar trazas en varias especies de agave de Sinaloa, México. El análisis estadístico mostró diferencias significativas (P ≤ 0.05) en la concentración de flavonoides entre los nueve tipos de aguamiel estudiados. Los valores más altos de este tipo de metabolitos se encontraron en el aguamiel de A. salmiana cultivar manso (Axapusco, Estado de México), el cual fue estadísticamente diferente al resto de muestras y presentó más del triple de contenido de flavonoides en comparación con el aguamiel del estado de Hidalgo.
La concentración encontrada de flavonoides en todas las muestras de aguamiel fue menor a la de compuestos fenólicos (Cuadro 6), posiblemente por encontrarse formando procianidinas (taninos condensados) como sucede en algunos frutos. Algunos autores han reportado la presencia de taninos en las hojas de algunas especies de agave (Ahumada-Santos et al., 2013) y abundante presencia de ácidos fenólicos en el género agave (Almaraz-Abarca et al., 2013a; Almaraz-Abarca et al., 2013b).
Vitamina C (ácido ascórbico)
El contenido de vitamina C en las muestras de aguamiel estudiadas varió entre 230.12 y 598.00 mg EAA L-1 de aguamiel) (Cuadro 6), donde el aguamiel obtenido de A. salmiana cultivar xamini presentó la concentración estadísticamente superior, cercano a lo encontrado en el jugo de limón (486.1 mg EAA L-1) (Alvarez et al., 2005), mandarina y naranja (121.6 a 368.3, 325.6 a 727.2 mg EAA L-1, respectivamente) (Del Caro et al., 2004).
Se observaron diferencias significativas del contenido de vitamina C del aguamiel entre las diferentes especies, cultivares y origen (Cuadro 6). En el presente estudio, las concentraciones de ácido ascórbico de las muestras de aguamiel fueron superiores a lo descrito por (Tovar-Robles et al., 2011), 140.4 mg EAA L-1 en el aguamiel de A. salmiana de Aguascalientes.
La vitamina C se degrada fácilmente por acción de la luz, actividad de agua, presencia de oxígeno y alta temperatura (Heldman et al., 2018); sin embargo, se descarta la posible degradación de este metabolito por esas vías, debido a que todas las muestras se trasladaron en semejantes condiciones de refrigeración y se procesaron simultáneamente. Por lo tanto, las diferencias estadísticas encontradas entre los contenidos de vitamina C se podrían deber a diferencias edafoclimáticas.
De manera general, las variaciones observadas en el contenido de fitoquímicos (compuestos fenólicos, flavonoides y vitamina C) se debe a factores edafoclimáticos propios de los sitios de recolecta de aguamiel (temperatura, humedad relativa, radiación, precipitación y condiciones del suelo, entre otros), que pueden ocasionar estrés abiótico y generar una respuesta de defensa en la planta produciendo una diversidad de metabolitos secundarios para evitar daños en las células y los tejidos (Yeshi et al., 2022). Otro factor que pudo influir en el contenido de estos metabolitos fue el añejado del maguey, tiempo que permite la maduración de las hojas centrales y aumenta el contenido de azúcar de la savia (aguamiel); sin embargo, se desconoce cómo este periodo afecta la calidad nutricional y nutracéutica del aguamiel y, en el presente estudio, los magueyes muestreados no fueron añejados durante el mismo tiempo dado las diferencias en el proceso de preparación de la planta entre las diferentes regiones de estudio.
Actividad antioxidante
Se encotraron diferencias significativas (P ≤ 0.05) de la actividad antioxidante entre las diferentes especies y cultivares, aunque destacan las muestras recolectadas en el estado de Hidalgo, siendo el aguamiel de A. salmiana cultivar cerro el de mayor capacidad para neutralizar los radicales libres (Cuadro 6). Estas diferencias posiblemente se deben a las condiciones edafoclimáticas del Valle de Mezquital Hidalgo, región semiárida caracterizada por un clima semiseco y precipitaciones anuales menores a 400 mm, condiciones de estrés que pudieron favorecer la síntesis de algunos antioxidantes. La síntesis de algunos metabolitos secundarios en los vegetales se favorece como mecanismo de defensa o para contrarrestar los factores de estrés (sequía, condiciones climáticas adversas, patógenos) (Iriti & Faoro, 2006).
En general, las muestras de aguamiel presentaron una actividad antioxidante promedio de 1109.21 μM ET L-1 similar a lo reportado por Tovar-Robles et al. (2011) (1096.8 μM ET L-1); actividad antioxidante moderada (menos de 20%) en comparación con algunas bebidas comerciales como café (6299.2 μM ET L-1) y jugo de uva (6444.8 μM ET L-1); pero superior (más de 50 %) en actividad antioxidante al pulque (567.2 μM ET L-1) y jugo de naranja con nopal de la marca Nutriva® (311.6 μM ET L-1) (Tovar-Robles et al., 2011). De acuerdo con el análisis de correlación de Pearson, la actividad antioxidante observada en el aguamiel mostró una alta correlación significatica con el contendio de compuestos fenólicos (0.88).
Es importante destacar que A. salmiana cultivar cerro, a diferencia de los cultivares xamini, cimarrón y penca ancha de la misma especie, también localizada en El Cardonal, Hidalgo, es un agave más silvestre que no se cultiva y aprovechado por los productores debido a que consideran que el aguamiel es de baja calidad (poco contenido de azúcares) y color oscuro, no apto para la elaboración de pulque o jarabe de agave; por lo que los resultados de esta investigación podrían contribuir a revalorizar su aprovechamiento y cultivo por su alto contenido de compuestos fenólicos, compuestos con potencial actividad antioxidante.
Análisis de componentes principales
Una vez que se estudió el comportamiento individual de cada metabolito del aguamiel, se realizó un análisis de componentes principales (ACP) para agrupar las muestras de aguamiel de acuerdo con sus características físicoquímicas, nutricionales y nutracéuticas (Figura 3). La gráfica de proyecciones del primer componente (CP1) y segundo componente (CP2) permitieron separar en cuatro grupos a las muestras de aguamiel (Figura 3). El CP1 presentó asociación positiva con hue y azúcares reductores directos (ARD). El CP2 tuvo asociación positiva con azúcares totales, Cu y K.
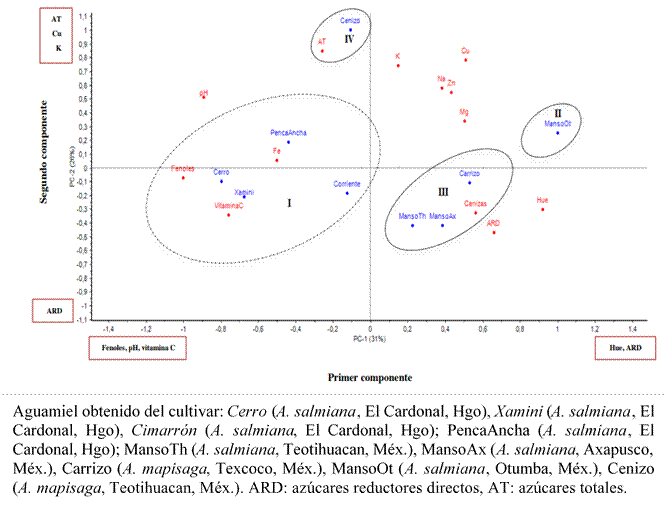
Figura 3 Agrupación de muestras de aguamiel de Agave salmiana (cultivares xamini, cerro, cimarrón o corriente, penca ancha y manso) y A. mapisaga (cultivares carrizo y cenizo), recolectado en el Estado de México e Hidalgo, con base en características físico-químicas, nutricionales y nutracéuticas.
Las muestras de aguamiel obtenidas de los cultivares cerro, xamini, cimarrón y penca ancha (A. salmiana) recolectadas en el Estado de Hidalgo, conformaron el Grupo I; se caracterizó por agrupar muestras de aguamiel de tonalidad amarillo-marrón (bajo valor de hue), alto contenido de Fe (11.85-25.91 mg L-1), mayor valor nutracéutico y actividad antioxidante. El aguamiel del cultivar manso (A. salmiana) de Otumba, Estado México, conformó el Grupo II, se caracterizó por su elevado contenido de azúcares reductores directos. El Grupo III estuvó conformado por el aguamiel de los cultivadares manso (Teotihuacan y Axapusco, Estado de México) y carrizo (A. mapisaga, Texcoco, México), muestras de mayor hue (tono amarillo) y mayores valores de luminosidad; pero menor contenido de compuestos fitoquímicos y actividad antioxidante. El aguamiel del cultivar cenizo de A. mapisaga (Teotihuacan, Estado de México) formó el Grupo IV, destacando por su mayor contenido de K, Cu y mayor concentración de AT, por lo cual podría ser de alta calidad para la elaboración de pulque; pero menor contenido de ARD, es decir, mayor contenido de sacarosa, que podría aprovecharse igualmente para elaborar jarabes de agave.
En general, las diferencias observadas entre las muestras de aguamiel podrían deberse a prácticas de manejo agronómico (principalmente aplicación de composta orgánica de estiercol de ovino) que se le da al agave y a factores edafoclimáticos (diferentes tipos de suelo y condiciones climáticas entre los sitios de estudio que ocasionan variación en la síntesis de fitoquímicos en plantas bajo diversos tipos de estrés abiótico). Los resultados de esta investigación pueden contribuir a identificar los cultivares con mayor valor nutracéutico y nutricional; así como, el tipo de uso que se le puede dar al aguamiel (bebida, elaboración de pulque o jarabe de maguey) con el fin de realizar un aprovechamiento agroindustrial eficiente. Actualmente, el aguamiel es poco consumido y muchas especies y cultivares de maguey pulquero están en peligro de extinción, por lo que esta información podría contribuir a la revalorización del cultivo de maguey y a su consumo, como parte de la identidad cultural México.
Conclusiones
Las muestras de aguamiel de color más oscuro (menor hue, tonalidad amarillo-marrón) y mayor pH presentaron mayor actividad antioxidante, asociada al mayor contenido de compuestos fenólicos y vitamina C. Los compuestos fenólicos contribuyeron en mayor medida a la actividad antioxidante del aguamiel, en comparación con los otros nutracéuticos. El aguamiel obtenido de A. salmiana cultivar cerro (Hidalgo) presentó el mayor contenido de proteína, Ca, Fe y compuestos fenólicos; así como, la mayor actividad antioxidante, tres veces superior al aguamiel de Agave mapisaga y el doble que las muestras obtenidas de los otros cultivares de A. salmiana que se estudiaron en el presente estudio. El aguamiel es una bebida subvalorada de buena calidad nutricional y funcional. El aguamiel de A. salmiana cultivar cerro es considerado de baja calidad para la elaboración de pulque y jarabe de agave por los productores, dado su menor contenido de azúcares totales; sin embargo, los resultados obtenidos en el presente estudio permiten afirmar que este fue el cultivar con mayor potencial para obtener aguamiel de mayor calidad nutricional y nutracética con posibles beneficios a la salud.











 nova página do texto(beta)
nova página do texto(beta)



