ANTECEDENTES
Los fibroadenomas son la patología mamaria benigna más común en mujeres de 14 a 35 años.1 Se estima que el 10% de la población femenina ha tenido un fibroadenoma alguna vez en su vida.2,3 Estos tumores son dependientes del estrógeno y afectan el tejido epitelial y estromal.4 Las mutaciones del gen MED12 también se han implicado en su fisiopatología.5 Los fibroadenomas se caracterizan por ser masas firmes y elásticas, con bordes regulares, de tamaño variable, de larga evolución, localizadas en el cuadrante superior externo de la mama.6 Desde el punto de vista histológico se clasifican en cinco tipos.6 Su diagnóstico no constituye un reto y su tratamiento dependerá de factores de riesgo: edad, antecedentes familiares de cáncer de mama, tamaño del fibroadenoma, entre otros.7 Gran parte de los fibroadenomas involucionan y desaparecen con el tiempo.8 A largo plazo, su pronóstico es bueno.
En los estudios al respecto se reporta que entre el 0.002 y el 0.125% de los casos malignizan.9 A partir de 1949 comenzaron a reportarse casos aislados y series de casos de lesiones de alto riesgo, lesiones precancerosas y cáncer de mama en el contexto de los fibroadenomas mamarios.10 Entre las lesiones de alto riesgo están: hiperplasia ductal atípica, hiperplasia lobulillar atípica, carcinoma ductal in situ, carcinoma lobulillar in situ y carcinomas mamarios invasivos.9,11-15 Hoy día, pocos estudios han recopilado información de las causas de la transformación maligna de esta afección mamaria benigna, el riesgo de malignidad de cada subtipo histológico, los factores de riesgo implicados, su diagnóstico y tratamiento.
Por lo anterior, con base en una revisión bibliográfica, se busca caracterizar a los fibroadenomas conforme a su epidemiología, etiología, diagnóstico y tratamiento; además, describir su relación con el cáncer de mama.
METODOLOGÍA
Revisión narrativa de la bibliografía de los fibroadenomas y cáncer de mama con base en la información más reciente y relevante. Para ello se efectuó una búsqueda bibliográfica exhaustiva en PubMed-Medline, Scopus, SciELO y LILACS. Se revisaron artículos en español e inglés, publicados entre enero del 2019 y abril del 2024. Los tipos de artículo seleccionados fueron: originales, revisiones narrativas y sistemáticas, casos clínicos y extractos de libros. Se buscaron, también, de forma independiente, estudios históricos relacionados con el tema.
Se seleccionaron los estudios más relevantes según su aporte y pertinencia. Se evaluó la calidad metodológica de los estudios de forma independiente; las discrepancias se discutieron y resolvieron en conjunto. Se excluyeron artículos duplicados, trabajos poco claros, de bajo rigor científico y literatura gris. En total, se incluyeron 50 estudios. Por tratarse de un estudio de bases secundarias no se requirió la aprobación de un comité de bioética.
Características de los fibroadenomas
Los fibroadenomas son los tumores benignos de la mama más comunes.1 Desde el punto de vista clínico se caracterizan por ser móviles, con una textura firme, gomosa y bordes bien definidos. Estos tumores fibroepiteliales generalmente surgen de los tejidos glandulares y estromales de la mama, con una relación entre estroma y glándulas que suele ser constante y homogénea a lo largo de toda la lesión.6 Desde la perspectiva microscópica son tumores bifásicos, de contornos circunscritos, que producen un efecto ocupativo, compuestos por una mezcla de elementos epiteliales y estromales, con pérdida de la arquitectura lobulillar debido a la expansión del estroma entre los elementos epiteliales.7 Lo normal es que sean de naturaleza benigna y tengan un bajo riesgo de malignidad; sin embargo, pueden generar un grado significativo de preocupación e inquietud entre las pacientes debido a que en la mayoría de los casos son fácilmente palpables.8 Además, se consideran un factor de riesgo a largo plazo de padecer cáncer de mama.16
Por su patrón de crecimiento, los fibroadenomas se clasifican en: patrón intracanalicular, pericanalicular y adenoma. El estroma comprime y distorsiona las glándulas en espacios similares a hendiduras en el patrón intracanalicular, mientras que en el patrón pericanalicular el estroma rodea las glándulas, sin distorsionarlas, y las glándulas mantienen sus luces abiertas.2 En el adenoma predomina el crecimiento tubular con escaso estroma.17
Por sus variantes histológicas, los fibroadenomas se clasifican en: simples, complejos, juveniles, gigantes, mixoides, hialinizados y celulares.4,7,18 Las características de cada uno se muestran en el Cuadro 1.
Cuadro 1 Clasificación y características de los fibroadenomas mamarios
| Tipos | Características epidemiológicas | Hallazgos histopatológicos de la evaluación macroscópica: | Riesgo de cáncer |
|---|---|---|---|
| Simples | Variante más común. Representan el 86% de todos los casos. Edad media 28 años. | Lesiones circunscritas. Celularidad: conservada, similar a la del estroma perilobular. Actividad mitótica: ausente o poca. Atipias estromales: ausentes. | El riesgo de cáncer de mama invasivo se incrementa en 1.89 veces. |
| Complejos | Variante rara y la más importante relacionada con el cáncer de mama. Representan del 16 al 22% de todos los fibroadenomas. Edad media de 47 años. | Lesiones circunscritas, quistes mayores de 3 mm. Celularidad: metaplasia apocrina papilar. Actividad mitótica aumentada. Atipias estromales. | El riesgo de cáncer de mama invasivo se incrementa en 3.1 veces. |
| Juveniles | Variante rara. Representen del 7 al 8% de todos los fibroadenomas. En pacientes de 10 a 18 años. Más comunes en afroamericanos. | Lesiones circunscritas. Celularidad: hiperplasia estromal y epitelial. Actividad mitótica aumentada. Atipias estromales ausentes. | Riesgo de cáncer de mama invasivo muy bajo. Sin estudios. |
| Gigantes | Variante rara. Representen del 0.5 al 2% de todos los casos. En pacientes menores de 30 años. Más comunes en afroamericanos y asiáticos. | Lesiones circunscritas, mayores de 5 cm, de más de 500 g. Celularidad: hiperplasia estromal y epitelial. Actividad mitótica aumentada. Atipias estromales: ausentes. | Riesgo de cáncer de mama invasivo muy bajo. Sin estudios. |
| Mixoides | Variante rara. Asociados con el complejo de Carney. Edad media a la aparición 26 años. | Lesiones circunscritas. Celularidad: abundante matriz mixoide y estroma hipocelular. Actividad mitótica aumentada. Atipias estromales ausentes. | Riesgo muy bajo de cáncer de mama invasivo. Sin estudios. |
| Celular | Variante rara. Representan del 4 al 7% de todos los fibroadenomas. Más común en adolescentes. | Lesiones circunscritas. Celularidad: aumentada, uniforme, focal o leve. Actividad mitótica aumentada. Atipias estromales ausentes. | Riesgo de cáncer de mama invasivo muy bajo. Sin estudios. |
| Hialinizado | Variante rara. Aparece en mujeres de edad avanzada. | Lesiones circunscritas. Celularidad: disminuida, esclerosis, hialinización y atrofia epitelial. Actividad mitótica: disminuida, necrosis. Atipias estromales ausentes. | Riesgo de cáncer de mama invasivo muy bajo. Sin estudios. |
Elaborado por los autores. Fuente: Basara Akin I & Balci P, 2021.
A pesar de los patrones y variantes histológicas de los fibroadenomas, su naturaleza suele tener un curso benigno. En raras ocasiones la hiperplasia ductal atípica, la hiperplasia lobulillar atípica, el carcinoma ductal in situ, el carcinoma lobulillar in situ y los carcinomas invasivos pueden implicar un fibroadenoma.19
Epidemiología
Los fibroadenomas suelen aparecer con más frecuencia en mujeres entre los 20 y 30 años, sin que ello implique que puedan encontrarse en cualquier edad. Se estima que alrededor del 10% de la población mundial femenina puede llegar a tener un fibroadenoma.23 Si bien pueden localizarse en cualquier parte de la mama, hay predilección por el cuadrante superior externo. Más del 70% son lesiones solitarias y el resto son masas múltiples en una o ambas mamas.3 Debido a su sensibilidad hormonal, los fibroadenomas pueden fluctuar con el ciclo menstrual, comúnmente aumentan de tamaño durante el embarazo e involucionan en la menopausia. La incidencia de fibroadenomas disminuye con la edad; por lo tanto, rara vez se encuentran después de los 40 años.2,3
Etiología, factores de riesgo y factores protectores
Está clínicamente reconocido que la actividad hormonal, sobre todo el aumento de la estrogénica, tiene un papel relevante en el origen de los fibroadenomas.4 Su crecimiento, a menudo, coincide con periodos de fluctuaciones hormonales.8 Además, la evidencia sugiere una predisposición genética hacia la aparición de fibroadenomas, respaldada por la identificación de mutaciones o variaciones genéticas específicas; por ejemplo, las variaciones genéticas en el gen MED12 son críticas y susceptibles de potencial tumorigénico que proyectan al MED12 como un potencial marcador de fibroadenomas.20 A pesar de ello, la base genética de los fibroadenomas sigue siendo en gran parte desconocida y no se comprende del todo, ello subraya la complejidad de la afección. Quizá múltiples genes y factores interactúen para influir en su aparición y crecimiento.5
Se reconocen como factores de riesgo de fibroadenomas:
Edad y género: los fibroadenomas siguen un patrón distinto en cuanto a edad y género, se diagnostican, predominantemente, en mujeres de 20 a 30 años, son excepcionales en mujeres posmenopáusicas y extremadamente poco comunes en hombres.8,21
Factores hormonales: las variaciones de la dinámica hormonal, en particular la influencia del estrógeno y la progesterona, contribuyen de manera fundamental a la aparición de los fibroadenomas. La pubertad, el embarazo y el ciclo menstrual se han relacionado con un mayor riesgo de tenerlos. La mayor actividad hormonal durante estos periodos puede estimular su crecimiento en el tejido mamario.6,8,21
Antecedentes familiares: el antecedente de fibroadenomas en familiares cercanos es un factor de riesgo elevado de aparición de un fibroadenoma. Esta predisposición familiar subraya los posibles fundamentos genéticos de la enfermedad.2,6,21
Raza y origen étnico: la raza y el origen étnico parecen influir en la prevalencia de los fibroadenomas; algunos estudios indican una mayor incidencia entre las mujeres de ascendencia africana. Sin embargo, se requieren más investigaciones para comprender estas variaciones y sus causas subyacentes.6,8,22
Peso corporal: investigaciones emergentes han explorado posibles asociaciones entre el peso corporal, la obesidad y el riesgo de fibroadenomas. Algunos estudios sugieren un vínculo entre mayor peso corporal y mayor riesgo de fibroadenomas. Esta asociación puede atribuirse a los cambios hormonales relacionados con la obesidad. Para confirmarlo hacen falta más estudios al respecto.6
Menarquia temprana y nuliparidad: la mayor exposición estrogénica y los cambios hormonales durante estas fases reproductivas contribuyen a la generación de condiciones favorables para el crecimiento de fibroadenomas, aunque su asociación es motivo de controversia.8
En la actualidad, la información registrada de factores protectores en contra de los fibroadenomas es limitada. Algunos estudios han notificado que la anticoncepción hormonal oral, durante al menos cuatro años, podría disminuir el riesgo de tenerlos en comparación con controles que no recurrieron a estos.23 También se ha investigado el efecto de la metformina en los fibroadenomas que reporta un efecto favorable en relación con el tamaño, sin que aún la evidencia sea contundente.24
Importancia clínica, técnicas diagnósticas y diagnóstico diferencial
Si bien los fibroadenomas son una lesión fibroepitelial benigna que no evoluciona, merece especial atención debido a su alta prevalencia y repercusiones en la calidad de vida y la salud mental de las pacientes.25 Los fibroadenomas suelen ser más frecuentes en mujeres de 20 años y, por lo general, surgen como una masa bien definida, móvil e indolora. Los fibroadenomas pueden diagnosticarse mediante el examen clínico de la mama, la ecografía mamaria y la citología por aspiración con aguja fina.1
Si los fibroadenomas son tumores benignos, no es factible ni necesario tomar una biopsia a todas las pacientes para establecer el diagnóstico. Las biopsias son clínicamente desafiantes e implican cargas físicas, psicológicas y financieras innecesarias. Por lo tanto, en la práctica clínica, lo más aconsejable para el diagnóstico es la ecografía.25
El tumor filodes es el principal diagnóstico diferencial porque comparte varias características histológicas con los fibroadenomas. No obstante, su diferenciación es importante porque poseen un comportamiento clínico distinto. El tumor filodes es raro y puede asociarse con recurrencias, avance en grado e, incluso, metástasis.7Los hallazgos ecográficos del tumor filodes suelen ser de una masa hipoecoica, densa, lobulada y redonda con márgenes parcialmente indistintos o circunscritos. Con frecuencia, el tumor filoides mostrará un aumento de la vascularización en el Doppler color o power. La evaluación por resonancia magnética puede resultar benéfica para evaluar la invasión y diferenciarlo de los fibroadenomas.26
Tratamiento
La mayoría de las pacientes con fibroadenomas mostrarán, clínicamente, bultos evidentes en la mama, que se detectan en el examen médico o el autoexamen y, ocasionalmente, experimentan dolor. Sin embargo, la mayoría de los casos no requiere tratamiento quirúrgico por lo que puede optarse por una conducta conservadora.2,6 Las indicaciones para la intervención quirúrgica incluyen: crecimiento rápido, tamaño superior a 2 cm y solicitud de la paciente.2
Las pacientes jóvenes pueden resultar con una cicatriz quirúrgica, con potencial de queloide y pérdida de volumen mamario, lo que resulta en un defecto estético y efectos negativos en la lactancia.27,28 Por esta razón han surgido técnicas menos invasivas, como la escisión asistida por vacío guiada por ultrasonido, ablación por radiofrecuencia, crioablación, resección transareolar y ecografía focalizada de alta intensidad, entre otras. 6,8,27,28
Relación con el cáncer de mama
Varios estudios han relacionado a los fibroadenomas con el inicio futuro de cáncer de mama.16,29,30 Román y colaboradores analizaron los datos de 778,306 mujeres en quienes compararon las tasas de incidencia de cáncer de mama en pacientes con y sin enfermedad mamaria benigna durante una mediana de seguimiento de 7.6 años. El riesgo de cáncer de mama fue 1.77 veces mayor en las mujeres con enfermedad mamaria benigna que entre las que no la padecían.29 De la misma forma, Dyrstad y su grupo llevaron a cabo un metanálisis en el que se encontró que la enfermedad mamaria proliferativa, sin atipia, entre estos el fibroadenoma, se asoció con un riesgo significativamente mayor de cáncer de mama con un riesgo relativo resumido de 1.76.30 Las mujeres con enfermedad mamaria benigna podrían beneficiarse de una vigilancia más estrecha y estrategias de detección personalizadas. Los factores implicados en esta asociación se exploran en la siguiente sección.
Fibroadenomas y cáncer de mama: ¿cuál es su relación?
Al igual que otras tumoraciones mamarias benignas, los fibroadenomas no son precursores directos del cáncer de mama. Por ello, su aparición se considera rara y su hallazgo suele ser fortuito. En general, entre el 3 y el 6% de los cambios mamarios benignos se deben a cáncer de mama.1 De estos, solo el 0.002 al 0.125% están relacionados con fibroadenomas.9 Esta asociación es más común en mujeres europeas y americanas, jóvenes, premenopáusicas, y con antecedentes familiares de cáncer de mama.21,29,31,32 Si bien los fibroadenomas son más frecuentes en las mujeres afro, el riesgo de cáncer de mama cuando hay fibroadenomas es muy bajo (SIR 0.94; IC95%: 0.75-1.18), incluso cuando hay atipia (RR 0.67; IC95%: 0.48-0.93).22 La edad al momento del diagnóstico está relacionada con la transición de los fibroadenomas a cáncer de mama a largo plazo, con una razón de riesgo que aumenta entre 1.07 (IC95%: 1.03-1.12) a 1.99 (IC95%: 1.32-2.92) veces por cada año29,31 Los factores protectores de cáncer de mama parecen disminuir ese riesgo.31
La coexistencia de ciertas características histológicas puede indicar un mayor riesgo de cáncer de mama, incluso formas más agresivas de éste, como en el caso de los fibroadenomas complejos con atipia o hiperplasia atípica.1,30,32,33 Otras variantes de los fibroadenomas, como los fibroadenomas juveniles, gigantes, mixoides, celulares y hialinizados, aunque bajo, tienen potencial de transformación maligna (Cuadro 1).4,7,18
Está reportado que la hiperplasia atípica, no especificada, aumenta tres veces más el riesgo de padecer cáncer de mama (RR 3.93; IC95%: 3.24-4.76).30 Asimismo, la pérdida de control en los genes supresores tumorales como TP53, PTEN, BRCA1, BRCA234-37 o MTUS1,38 las mutaciones de los genes asociados con las vías de señalización celular como PIK3CA-PI3K/AKT/mTOR39 y la expresión de los miARN circulantes como miR-181a y miR-25 asociados con la regulación de la expresión de los genes relacionados con la carcinogénesis,37 se han relacionado con cáncer de mama y fibroadenomas. Además, en el contexto de uno o varios fibroadenomas, la sobreexpresión de la metalotioneína 1 y las metaloproteinasas de matriz 2 y 9 también podría estar relacionada con un mayor riesgo de evolución a cáncer de mama.40,41 También se ha observado que los cambios epigenéticos relacionados con la metilación de genes, como BCSG1 y BRCA1, pueden influir en la evolución a cáncer de mama a partir de fibroadenomas.36,42 No obstante, hace falta más investigación para comprender por completo la relación y relevancia clínica del porqué de los fibroadenomas.34
Se ha observado que la interacción adipocito-epitelio mamario podría desencadenar una transformación maligna de las enfermedades mamarias benignas, especialmente en mujeres con sobrepeso u obesidad.43 Además, podría haber una relación entre FBP1 y LDHB, enzimas que participan en la gluconeogénesis, en la transformación de fibroadenomas y otras tumoraciones mamarias benignas a cáncer de mama.44 A su vez, las vías de resistencia endocrina, como ERBB2, BCL2 y CCND1, podrían desempeñar un papel importante. Los mecanismos fisiopatológicos aún no están claros.5 Se plantea que esas alteraciones endocrinológicas podrían estar relacionadas con la evolución tumoral y ser decisivas en la detección de fibroadenomas con un alto riesgo de recurrencia y mayor riesgo de cáncer de mama.5,44
Durante la exploración física y la valoración ecográfica o mamográfica los fibroadenomas asociados con cáncer de mama suelen advertirse como masas típicas y características, sin alteraciones. Cuando esos hallazgos difieren de lo esperado clínicamente, se sugiere buscar alteraciones compatibles con las variantes conocidas de los fibroadenomas o lesiones mamarias malignas.4 Además del tamaño de la masa mamaria (≥ 25 mm), el aumento consecutivo de este último, la inmovilidad y la pérdida de definición de los bordes. Puesto que el 13.50% de esas tumoraciones malignizan a largo plazo durante la evaluación y seguimiento también deben considerarse: edad, antecedentes familiares de cáncer de mama y la categoría más o menos mayor de 3 a 4 del tumor, conforme a la clasificación del Breast Imaging-Reporting and Data System (BI-RADS). 11,12,27,29,31,45Por ello, el seguimiento a corto plazo y la práctica de estudios complementarios sensibles y específicos son decisivos. Otras técnicas, como la imagen de perfusión tomográfica computada de baja dosis, han permitido explorar a detalle y diferenciar entre cáncer de mama y fibroadenomas.46
El desarrollo y validación de modelos de predicción de riesgo de cáncer de mama, con base en la densidad mamaria y el diagnóstico previo de enfermedad mamaria benigna, han demostrado su utilidad (OR 1.04; IC95%: 1.03-1.06).13 Además, los nomogramas radiómicos han expresado una eficacia diagnóstica favorable en la diferenciación de los fibroadenomas y el cáncer de mama triple negativo (AUC 0.986; IC95%: 0.975-0.997).47
Los miARNs, como biomarcadores plasmáticos, pueden ser de utilidad en la discriminación entre carcinomas ductales invasivos y fibroadenomas; entre estos el miARN-637, miARN-523-5p y miARN-490-3p.48 El estudio de las mutaciones del gen MD12, que desempeña un papel decisivo en la regulación de la transcripción génica, podría contribuir a la diferenciación de tumores fibroepiteliales benignos y malignos.34 Asimismo, la identificación de las variantes genéticas RANKL T643C, OPG G1181C, T950C, VDR BsmI, FokI, y YKL-40 G-131C podría servir de biomarcador genético para la predicción del riesgo de estas enfermedades en determinadas poblaciones.49
El estudio histológico mediante biopsia percutánea con aguja gruesa es el patrón de referencia para el diagnóstico de lesiones mamarias.1,14,50 El diagnóstico de fibroadenomas suele ser directo, aunque la diferenciación entre sus variantes histológicas citadas y el tumor filoides suele representar un reto. Su comportamiento clínico es la principal diferencia.7,18 En el contexto de los fibroadenomas y mastopatía fibroadenomatosa se ha observado la aparición de carcinoma ductal invasivo, carcinoma ductal in situ y carcinoma lobulillar in situ.9,11-15
Otros hallazgos incluyen: proliferaciones epiteliales, confinamiento del carcinoma lobulillar in situ al fibroadenoma propiamente dicho y la afectación al tejido mamario circundante en el caso del carcinoma ductal in situ.11Éste se asocia con un aumento del riesgo de cáncer de mama multifocal (OR 2.13; IC95%: 1.58-2.88).33 Los subtipos luminal, de mama triple negativo y HER2+ son los fenotipos moleculares que más se reportan.12 Con estos hallazgos es importante valorar el daño a los ganglios linfáticos subyacentes en búsqueda de metástasis;12 pues ésta suele sobrevenir en el 23.8% de los casos.9
Si bien los fibroadenomas son tumores benignos y no requieren tratamiento, la tumorectomía, cirugía conservadora de mama y mastectomía deben considerarse dependiendo de los hallazgos radiológicos e histológicos.1,9,15,45 Otras opciones de tratamiento incluyen: terapia de reemplazo hormonal, quimioterapia y radioterapia coadyuvante.9,12 A larga data, su recidiva es poco probable;9,12,15 dado el caso, se practicarán los estudios imagenológicos e histológicos correspondientes, si está indicado. En general, el pronóstico es bueno. Sin embargo, éste puede ser desfavorable en estadios avanzados del cáncer de mama identificado.9El seguimiento y valoración posterior deberá efectuarse según el tratamiento iniciado.
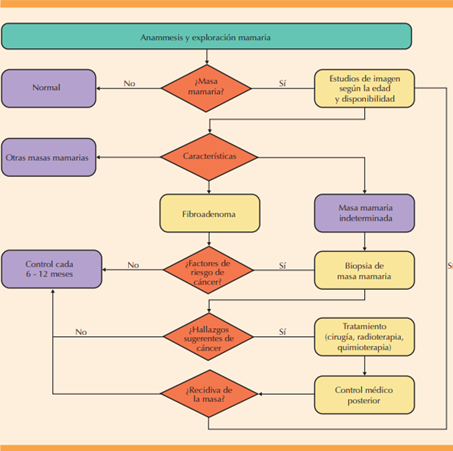
Con base en lo revisado, en la Figura 1 se propone un algoritmo para el diagnóstico y tratamiento de la asociación fibroadenomas-cáncer de mama.
CONCLUSIONES
Los fibroadenomas son los tumores mamarios benignos más comunes en mujeres en edad fértil. Están compuestos de tejido glandular y estromal, son estrógeno-dependientes y se reconocen cinco tipos. Desde el punto de vista clínico son masas firmes, elásticas, bien definidas, de tamaño variable y de larga evolución. En la actualidad, su diagnóstico y tratamiento están debidamente establecidos, motivo por el que no representan un desafío. Cuando del 0.002 al 0.125% de los fibroadenomas malignizan, el riesgo de cáncer de mama aumenta hasta 1.7 veces en comparación con mujeres sin patología mamaria. Por tanto, los cambios proliferativos en los fibroadenomas y el parénquima mamario subyacente deben considerarse señales de alerta. Los antecedentes personales y familiares de la paciente son relevantes, lo mismo que el cuadro clínico, evolución y hallazgos en los exámenes complementarios. Esto es lo que permite sospechar y, en consecuencia, determinar, el riesgo de cáncer de mama o identificar uno ya existente.











 nova página do texto(beta)
nova página do texto(beta)