INTRODUCCIÓN
Se sabe que los factores físicos de los sistemas naturales causan estrés a los organismos que los habitan (Hellawell, 1986; Hoffmann & Hercus, 2000). Esta situación de estrés es el motor en los procesos de adaptación y evolución en cada nivel de organización biológica. Normalmente, varios agentes de estrés actúan simultáneamente (Markert et al., 2003; Pirotta et al., 2022), de forma que el equilibrio de un sistema es dinámico y oscila en diferentes amplitudes (Sánchez-Pinillos et al., 2024). De esta manera, el medio ambiente influye en la diversidad y la abundancia de las comunidades que constituyen el sistema, además de incidir en la distribución de sus especies. En otras palabras, los componentes biológicos reflejan los efectos de esas variaciones en la calidad del medio fisicoquímico (Karr et al., 1986; Peck, 2011). Si el estrés induce el cambio de estado de un sistema biótico o abiótico ante los disturbios, la respuesta a dicho estrés se reflejará en la estructura y función de las comunidades y los ecosistemas (Sulmon et al., 2015). Además de la amplia gama de tensiones naturales que soportan los organismos en sus hábitats, las actividades humanas y la manipulación del medio ambiente han generado otras perturbaciones, algunas de ellas similares a las naturales, como las modificaciones en los patrones de inundación, pero en diferente grado o magnitud, y otras de un tipo completamente ajeno al entorno natural, como la descarga de contaminantes emergentes como hormonas, pesticidas y medicamentos (Chu & Karr, 2017). Sin embargo, los factores de estrés y las limitaciones que estos generan, tienen el carácter de ser señales externas y los organismos afectados registran tales señales, a fin de responder mediante las reacciones y tensiones adecuadas (Baedke et al., 2021). Los mecanismos de adaptación al estrés comprenden, por una parte, las modificaciones en las propiedades internas del organismo, que se oponen al disturbio por medio de una respuesta específica, y por la otra, el sistema de reparación que invierte esos cambios (Turner et al., 2003; Sulmon et al., 2015).
La adaptación de una especie puede ser estable, surgida a lo largo de un gran número de generaciones, o inestable, dependiendo de la etapa de desarrollo del organismo y de los factores ambientales a los que ha estado expuesto. En este contexto, las muestras de organismos individuales que se obtienen del medio ambiente alterado se pueden utilizar y analizar como posibles representaciones de entidades mayores (poblaciones, comunidades o ecosistemas) o de comportamientos ambientales similares o relacionados (Xue et al., 2019; Baedke et al., 2021). Así, se pueden definir agrupaciones de organismos que desarrollan adaptaciones similares para sobrevivir, dependiendo del medio y de las limitaciones que éste presente. La evaluación de tales características, a través de las dimensiones corporales de los individuos, lleva a clasificarlos dentro de determinados grupos, lo que se denomina el estudio de la morfología funcional.
El primero en hablar de la morfología funcional fue el botánico Christen Raunkiær, quien en 1907 aplicó el concepto de formas de vida a las plantas (Raunkiær, 1934). Según Raunkiær, dichas formas de vida son la respuesta al clima y a sus fluctuaciones. Las ideas de este autor hicieron cuestionarse a los ficólogos de la época sobre las adaptaciones del fitoplancton a las condiciones ambientales del medio acuático. Los investigadores W.H. Munk y G.A. Riley demostraron esta premisa y la relacionaron con el hundimiento y con la absorción de nutrientes por parte de las algas (Munk & Riley, 1952). A partir de ese trabajo, se han desarrollado otros estudios, como el análisis de la relación superficie/volumen de las formas de vida fitoplanctónicas y sus efectos sobre la absorción de la luz y nutrientes (Lewis, 1976; Margalef, 1978). El estudio de la plasticidad morfológica de las algas y su relación con las condiciones del medio físico muestra que, en ambientes con características abióticas similares, las formas de vida del fitoplancton son morfológicamente muy parecidas. Reynolds (1980) señala que esto implica una interacción directa del medio con los organismos que componen las comunidades de microalgas.
En diversos estudios se ha confirmado la utilidad de los análisis morfométricos o de tamaño de las algas para evaluar las condiciones de los cuerpos de agua en respuesta a los procesos ecológicos y evolutivos ocasionados por las particularidades ambientales (Salmaso & Padisák, 2007; Stanković et al., 2012; Bortolini et al., 2014; Vadrucci et al., 2017). En ecosistemas de planos de inundación neotropicales, también se han estudiado los cambios en los rasgos morfofuncionales de las algas perifíticas y planctónicas como respuestas directas a las variaciones estacionales (Dunck et al., 2015; Lobo et al., 2018). Este enfoque no se ve afectado por la heterogeneidad taxonómica que presentan las algas en los diferentes ecosistemas, lo cual hace que los estudios en distintos ambientes sean comparables (Vadrucci et al., 2007). En Colombia existen algunos trabajos sobre morfología funcional de fitoplancton, como los realizados por Muñoz-López et al. (2017) y Hernández et al. (2020), pero los estudios que tratan estos aspectos en algas perifíticas son escasos y apenas se empiezan a abordar. Una primera aproximación fue el estudio de Guerrero-Lizarazo et al. (2021), quienes hicieron un análisis preliminar de las características morfológicas del ficoperifiton de algunos ríos de la Reserva La Planada (Nariño); para las algas perifíticas del complejo cenagoso de Zapatosa, Guerrero-Lizarazo (2022) incluyó esta perspectiva morfofuncional.
Una visión general sobre la importancia de las algas perifíticas en los ecosistemas acuáticos colombianos, se puede consultar en el artículo de Montoya Moreno & Aguirre (2013) y, una perspectiva más amplia con respecto a la ecología y la biodiversidad de las ciénagas de la región de interés está disponible en el libro del Rangel-Ch. (2012). En el presente artículo se señalan algunos aspectos sobre la morfología funcional de las algas perifíticas del Complejo Cenagoso de Zapatosa (CCZ) y se contrasta la hipótesis de que la caracterización morfofuncional obtenida se relaciona con las condiciones derivadas de las variables físicas y químicas de los diferentes sistemas acuáticos estudiados en esa región. Este objetivo se enmarcó en un diseño muestral estratificado (no aleatorio) y solo para el periodo hidrológico de descenso de la inundación que se presenta en este complejo cenagoso.
METODOLOGÍA
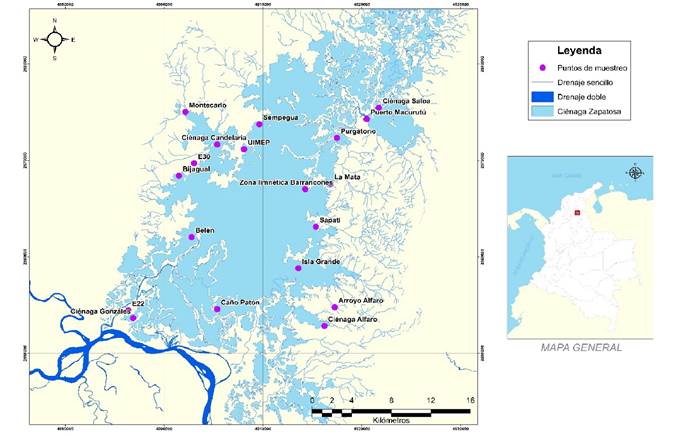
Área de estudio. La ciénaga de Zapatosa es una depresión cóncava con una profundidad máxima de 12 metros (Fig. 1). Por su ubicación geográfica, es el mayor reservorio de agua dulce de Colombia y la trampa de sedimentos más grande de la planicie inundable de los ríos Cesar y Magdalena. Estacionalmente, es una zona de amortiguamiento del río Magdalena (Rangel-Ch., 2012), pero su origen principal es el río Cesar, el cual nace en las estribaciones de la Sierra Nevada de Santa Marta. La ciénaga de Zapatosa es responsable de buena parte de la dinámica hídrica del sistema geográfico del nororiente colombiano. En época de caudales altos, el río Magdalena irrumpe en la ciénaga y hace retroceder al río Cesar, arrastrando juveniles de especies acuáticas importantes para la repoblación natural del CCZ; en la época seca, la ciénaga se contrae porque el río Magdalena recibe el agua almacenada en la planicie de inundación por medio de canales y zonas de menor consolidación de sedimentos. El patrón climático en el CCZ es bimodal-tetraestacional, con un ciclo mayor de lluvias que se inicia en septiembre y que conduce a una fase de caudales altos en el período octubre-diciembre; el otro periodo de niveles altos de precipitación ocurre en mayo-julio, pero es notablemente menor (Rangel-Ch., 2012).
Trabajo de campo. Los muestreos de los ecosistemas acuáticos dulceacuícolas de la CCZ se realizaron entre el 15 y el 28 de julio de 2021, época de descenso de la inundación del sistema. Se empleó un diseño de muestreo estratificado en el que las zonas de colecta se seleccionaron con base en criterios del grado de conservación. Como zonas mejor conservadas por los requerimientos para el desarrollo de los peces, se ubicaron las áreas de mayor riqueza íctica, de acuerdo con el conocimiento de los pescadores locales. Se usaron herramientas cartográficas y sistemas de información geográfica (ArcGIS) para establecer los usos del suelo y las coberturas vegetales mejor y peor conservadas. También se tuvo en cuenta la cercanía o lejanía a las comunidades humanas. De esta manera, se buscó que las zonas para la toma de muestras representaran condiciones ambientales contrastantes y, por lo tanto, distintos efectos sobre la comunidad de ficoperifiton. En cada estrato o zona de muestreo, el sitio específico de colecta se ubicó aleatoriamente. La recolección de muestras se hizo en 19 zonas de muestreo dentro del CCZ, dos de las cuales (el Arroyo Alfaro y Montecarlo) se ubicaron en sistemas lóticos, pero para la época de muestreo presentaron características de ambientes lénticos. Los 17 lugares restantes se localizaron en la zona litoral de los sistemas lénticos. En la Figura 1 se muestran las localidades de muestreo y en la Tabla 1 se indican sus coordenadas y algunas características generales de las condiciones que los circundaban.
Tabla 1 Ubicación y características generales de los lugares de muestreo en el CCZ. El uso circundante se refiere a la condición observada en los alrededores del área al momento del muestreo.
| Lugar | Tipo de sistema | Coordenadas | Altitud (m.s.n.m) | Usos circundantes |
|---|---|---|---|---|
| Ciénaga González | Léntico | N 9°00’33,0” | 28 | Cobertura natural |
| W 73°56’19,2” | ||||
| Montecarlo | Lótico (léntico para el momento del muestreo) | N 9°12’10,2” | 22 | Ganadería |
| Cobertura natural | ||||
| W 73°53’28,0” | ||||
| Belén | Léntico | N 9°05’17,3” | 26 | Cobertura natural |
| Ganadería | ||||
| W 73°53’18,7” | ||||
| Bijagual | Léntico | N 9°08’44,1” | 26 | Ganadería |
| Cobertura natural | ||||
| W 73°54’01,1” | ||||
| Ciénaga Candelaria | Léntico | N 9°10’20,4” | 30 | Ganadería |
| Natural | ||||
| W 73°51’42,00” | ||||
| Sempegua | Léntico | N 9°11’29,1” | 29 | Cobertura natural |
| W 73°49’22,40” | ||||
| Ciénaga Saloa | Léntico | N 9°12’25,5” | 26 | Cobertura natural |
| W 73°42’46,5” | ||||
| Zona limnética- Barrancones | Léntico | N 9°07’50,1” | 33 | Ganadería |
| Cobertura natural | ||||
| W 73°46’49,9” | ||||
| La Mata | Léntico | N 9°08’08,60” | 23 | Ganadería |
| W 73°45’25,9” | ||||
| Ciénaga Alfaro | Léntico | N 9°01’11,00” | 35 | Cobertura natural |
| Agricultura | ||||
| W 73°45’11,4” | ||||
| Sapatí | Léntico | N 9°05’42,91” | 25 | Ganadería |
| Cobertura natural | ||||
| W 73°46’14,40” | ||||
| Estación E-22 | Léntico | N 8°59’19,2” | 28 | Cobertura natural |
| W 73°58’08,3” | ||||
| Estación E-30 | Léntico | N 09°09’16,4” | 26 | Cobertura natural |
| Otras: Balneario | ||||
| W 73°52’58,5 | ||||
| Unidad de Mejoramiento Pesquero (UIMEP) | Léntico | N 0910’4,3” | 33 | Ganadería |
| W 73°50’13,2” | Agricultura | |||
| Cobertura natural | ||||
| Arroyo Alfaro | Lótico (léntico para el momento del muestreo) | N 9°00’07,70” | 31 | Ganadería |
| W 73°45’45,34” | ||||
| Puerto Macurutú | Léntico | N 09°11’47,4” | 26 | Ganadería |
| Residencial | ||||
| W 73° 43’26,4” | ||||
| Purgatorio | Léntico | N 09°10’43,4” | 28 | Ganadería |
| Agricultura | ||||
| Natural | ||||
| W 73° 45’05,1” | ||||
| Isla Grande | Léntico | N 9°03’22,5” | 30 | Cobertura natural |
| W 73° 47’12,1” | ||||
| Caño Patón | Léntico | N 9°01’03,6” | 28 | Ganadería |
| W 73°51’40,8” |
En cada sitio se midieron las siguientes variables in situ: profundidad media, oxígeno disuelto, porcentaje de saturación de oxígeno, temperatura del agua, pH y conductividad eléctrica, para lo cual se emplearon sondas multiparamétricas HYDROLAB y HANNA. La transparencia se registró con un disco Secchi. Se tomaron muestras de agua de cada zona en recipientes que se conservaron refrigerados y se llevaron al Laboratorios Nancy Flórez García SAS, certificado por Instituto de Hidrología Meteorología y Estudios Ambientales (IDEAM) de Colombia, donde se realizaron análisis de carbono orgánico total (COT), ortofosfato, calcio, demanda biológica de oxígeno (DBO5), demanda química de oxígeno (DQO), turbiedad, hierro, magnesio, sílice, nitrógeno total, nitrato, fósforo total, fosfato, sulfato, sólidos disueltos totales (SDT), sólidos suspendidos totales (SST), dureza total, alcalinidad y coliformes fecales y totales. Las muestras de agua correspondieron a la integración de las profundidades sub-superficial, mitad de la zona fótica y aproximadamente 50 cm antes del fondo.
Para la colecta del perifiton se siguieron los procedimientos establecidos por el IDEAM & INVEMAR (2021), consistentes en seleccionar el sustrato más representativo y tomar fragmentos de este para preservarlos completamente. En el CCZ, se utilizaron principalmente trozos de madera de plantas sujetas al sustrato y expuestas al sistema hídrico a muestrear; estos fragmentos se cortaron y se preservaron directamente en un frasco plástico con solución Transeau (agua destilada, etanol 90% y formol al 40%, en proporciones 6:3:1). En algunos pocos casos, se seleccionaron hojas o tallos de plantas flotantes (cuatro sitios), o rocas (un sitio), dependiendo de la disponibilidad del sustrato en cada lugar. Para reducir en lo posible el sesgo ocasionado por el uso de estos diferentes sustratos, se tuvo cuidado en mantener similares las condiciones de profundidad e iluminación en todos los casos. Posteriormente, los fragmentos se rasparon y se midieron sus áreas.
Análisis de laboratorio. En el departamento de Biología de la Universidad Nacional de Colombia Sede Bogotá, se hizo la identificación taxonómica de los individuos hasta el nivel de género, para lo cual se utilizaron claves locales y regionales como las publicadas por Necchi (2016), Bicudo & Menezes (2006) y Dos Santos (2016), y claves más generales como las de Whitford & Schumacher (1969), Ramírez (2000) y Wehr et al. (2015). Mediante un microscopio con cámara integrada, se tomaron fotografías de las algas en cuatro láminas portaobjetos por cada sitio. Las fotografías se utilizaron para medir con el programa ImageJ (Rueden et al., 2017), en al menos 20 individuos de cada taxón, los siguientes rasgos morfológicos sugeridos por Biggs et al. (1998) y Tapolczai et al. (2016): dimensión lineal máxima, área, relación superficie-volumen ENT#091;S/VENT#093; y biovolumen. El cálculo del área superficial, la S/V y el biovolumen se basó en los trabajos de Lewis (1976), Hillebrand et al. (1999) y Sun & Liu (2003). Otros atributos funcionales de tipo nominal cualitativo (formación de colonias o de filamentos, presencia de exoesqueleto de sílice, de aerotopos, de mucílago o de flagelos), conocidos como rasgos de formas de vida (Dunck et al., 2016), se observaron directamente en los taxones colectados. El conteo de los organismos se realizó en un microscopio invertido mediante la técnica de sedimentación en cámaras de tipo Utermöhl (Lund et al., 1958; Wetzel & Likens, 2000), para lo cual se contabilizaron los organismos de cada género hasta llegar a 200 individuos del taxón más abundante en cada muestra, de acuerdo con la recomendación de Kryk et al., (2023). Los resultados se reportaron en individuos por cm2 de sustrato.
Análisis numéricos. Dado que para llevar a cabo los análisis de ordenamiento es preferible tener un número de variables igual o menor al número de lugares evaluados (Kenkel, 2006), se hizo una selección previa de las variables ambientales más representativas (tanto de las tomadas in situ como de las fisicoquímicas y microbiológicas de laboratorio). Para ello, se seleccionaron aquellas variables no redundantes que tuvieran una alta explicación y que describieran el mayor porcentaje de la varianza de los datos. Para esta selección inicial de las variables fisicoquímicas, se siguieron dos pasos: 1) cálculos de la correlación de Spearman para eliminar las variables que covariaban, es decir, cuyas correlaciones fueran mayores a 0,8; 2) cálculo del coeficiente de variación para excluir las variables con coeficientes menores al 20%. Las variables ambientales seleccionadas se emplearon para realizar otros análisis multivariados que permitieron organizar los datos y cruzar la información biótica y abiótica. Así, el análisis de componentes principales (PCA), se utilizó para identificar los agrupamientos de lugares, de acuerdo con sus condiciones ambientales; para este ordenamiento, se calculó el test de esfericidad de Bartlett (Bartlett, 1951) y la medida de Kaiser-Meyer-Olkin (Kaiser, 1970) a fin de establecer la exactitud del ordenamiento. Por su parte, el escalamiento multidimensional no métrico (NMDS) permitió explorar las relaciones entre las variables ambientales y las abundancias de los géneros del ficoperifiton. Este NMDS se basó en una matriz de distancias calculada con el índice de Morisita (Magurran, 2004) y tuvo en cuenta las variables ambientales, cuyos coeficientes de correlación con las puntuaciones del NMDS se presentan como vectores desde el origen, a fin de considerar sus direcciones y longitudes relativas (Hammer, 2024). Los taxones se incluyeron en los gráficos del NMDS como promedios ponderados de las puntuaciones de los sitios de muestreo; la ponderación utiliza los valores originales, por lo que son independientes del índice de similitud utilizado y permiten el trazado de los géneros de algas junto con los sitios (Taguchi & Oono, 2005). También se usó el NMDS, con las matrices ambientales y las matrices de rasgos somáticos, para examinar la organización de cada atributo morfológico (dimensión lineal máxima, área superficial, biovolumen, relación S/V) en el conjunto de sitios de muestreo y para ver la influencia que tuvieron los factores ambientales sobre dicha organización. Todos los análisis NMDS incluyeron el cálculo del “stress” o grado de ajuste de las ordenaciones obtenidas. Por otra parte, se elaboraron gráficas de cajas y bigotes (“box plots”) con los promedios de los atributos morfológicos (previamente estandarizados) y de las abundancias de los rasgos nominales y se calculó la correlación de Spearman entre las variables ambientales y los rasgos morfofuncionales.
Adicionalmente, para conocer el grado de deterioro del agua en los distintos sitios del CCZ, se calculó el Índice de Calidad del Agua (ICA) utilizado en Colombia por el Instituto de Hidrología Meteorología y Estudios Ambientales (IDEAM) para determinar las condiciones sanitarias de los sistemas acuáticos del país (Caho-Rodríguez & López-Barrera, 2017). Este índice emplea las variables oxígeno disuelto, demanda química de oxígeno, conductividad eléctrica, sólidos suspendidos totales, pH, relación nitrógeno total/fosforo total y coliformes fecales. Un análisis final mediante la técnica NMDS, incluyó las variables fisicoquímicas y el ICA como factores ambientales en la organización de los promedios de todo el conjunto de rasgos morfofuncionales en los sitios de muestreo del complejo cenagoso. Todos los análisis estadísticos se realizaron en el programa PAST 4.16 (Hammer et al., 2001). Las figuras de PAST se editaron con el programa INKSCAPE 1.3 (The Inkscape Project, 2022).
RESULTADOS
Caracterización ambiental. Los datos completos del conjunto de variables fisicoquímicas y bacterianas evaluadas se presentan como material suplementario (Tabla 1S). En general, se observó que la mayoría de los factores ambientales fueron similares en las distintas zonas del CCZ: la temperatura del agua fue alta y osciló entre 29,3 °C y 33,7 °C; el pH tendió a la neutralidad, con un promedio de 6,9 y variaciones de condiciones más ácidas (4,4) en el sitio E22 a más básicas (8,07) en E30; la conductividad eléctrica fue moderadamente alta, con una media de 123,36 µS/cm y con el menor valor (68 µS/cm) en el Arroyo Alfaro; la DBO5 (promedio 4,27 mg O2/L) y la DQO (promedio 20 mg O2/L) fueron bajas en todos los lugares muestreados; el fosfato y el fósforo total presentaron concentraciones casi iguales en todos los sitios, con promedios de 0,153 mg/L para los dos casos; los valores de nitrato fueron reducidos, con una concentración generalizada de 0,886 mg NO3/L, exceptuando la Ciénaga González, que alcanzó los 1,28 mg NO3/L y la Zona limnética Barrancones, que llegó a 0,896 mg NO3/L; la concentración de nitrógeno total fue baja, con 2 mg N/L en todos los lugares y los sólidos disueltos fueron moderadamente altos, con un promedio de 97,24 mg/L, un valor mínimo en el Arroyo Alfaro de 57,5 mg/L y una concentración máxima en Puerto Macurutú de 126 mg/L.
En cuanto a los sitios que mostraron diferencias notables, se observó que la mayor abundancia de coliformes totales se presentó en la Ciénaga Alfaro, pero esta a su vez registró la menor concentración de coliformes termo-tolerantes (fecales). El Caño Patón fue el lugar más turbio y por consiguiente con una mayor cantidad de solidos suspendidos; también presentó la mayor concentración de coliformes termo-tolerantes, el valor de oxígeno disuelto más elevado y, por ende, la saturación de oxígeno más alta. El Arroyo Alfaro sobresalió por su alta concentración de carbono orgánico; adicionalmente, fue el sitio de menor alcalinidad. Por el contrario, Puerto Macurutú fue la zona de alcalinidad más elevada y de baja cantidad de sólidos suspendidos totales.
Organización de los sitios de muestreo de acuerdo con las variables ambientales. Con las 11 variables fisicoquímicas y microbiológicas seleccionadas (las de mayor coeficiente de variación y que no covariaron con otras variables), se realizó el PCA que se presenta en la Figura 2.
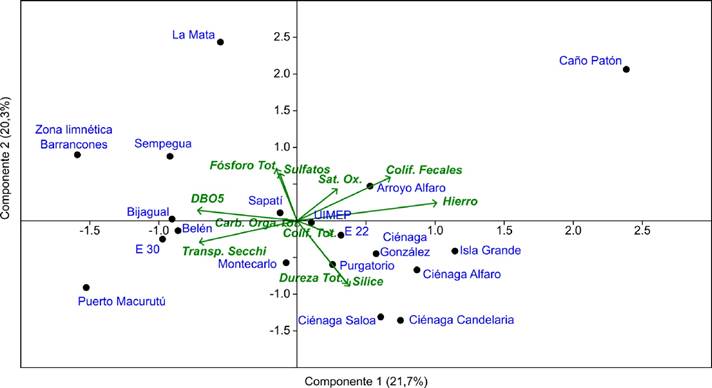
Figura 2 Análisis de componentes principales (PCA) de las variables físicas, químicas y microbiológicas del CCZ. Se alcanzó el 60,1% de explicación con los tres primeros ejes. PC1: 21,7%; PC2: 20,3%; PC3: 18,1%.
El test de esfericidad de Barlett (p = 0,05) indicó que el análisis proporcionó una reducción eficiente de la dimensionalidad de los datos, pero la medida de Kaiser-Meyer-Olkin fue 0,36 (< 0,5), lo que implica que la adecuación del muestreo fue “inaceptable”, es decir que la proporción de varianza en las variables podría ser causada por otros factores subyacentes. En consecuencia, los resultados del PCA deben asumirse con precaución. El hierro (en el componente 1) y el sílice (en el componente 2) fueron las variables más asociadas a los ejes del ordenamiento. Según este análisis, parecen existir cuatro grupos de estaciones. Un primer grupo estuvo constituido por el Caño Patón y el Arroyo Alfaro, los cuales presentaron una alta concentración de coliformes termotolerantes y de hierro. Los dos sitios de este primer grupo hicieron parte de los lugares con mayor grado de contaminación. Un segundo grupo lo conformaron las estaciones UIMEP, Purgatorio, E22, Ciénaga Alfaro, Ciénaga González, Ciénaga Candelaria, Ciénaga Saloa e Isla Grande, todas ellas con mayor dureza total, más sílice y una concentración media a alta de coliformes totales. Este conjunto de estaciones parece tener un mayor grado de mineralización del agua. Un tercer grupo asoció a los sitios La Mata, Zona limnética Barrancones y Sempegua, los cuales tendieron a una alta concentración de sulfato y a una mayor DBO5. El cuarto grupo correspondió a los lugares Montecarlo, Sapatí, Puerto Macurutú, Belén, Bijagual y E30, que se ubicaron opuestos a las mayores cantidades de hierro y coliformes fecales, con aguas más transparentes. Este cuarto grupo parece ser el de condiciones de menor contaminación del agua, aunque presentan cierta cantidad de carbono orgánico.
De acuerdo con estos resultados, los lugares que, desde el punto de vista del análisis PCA, se consideraron como localidades con el mejor estado de conservación fueron Puerto Macurutú, Belén, Bijagual y E30. Las estaciones más contaminadas fueron el Arroyo Alfaro, el Caño Patón, La Mata y Sempegua. Las demás localidades se encontraron en una posición intermedia en el gradiente de deterioro. Al considerar los resultados del cálculo del ICA (Tabla 2), se puede ver que según este índice todos los sitios del CCZ tendrían una condición de calidad del agua entre aceptable y regular, a excepción de la estación Purgatorio, que tuvo una mala calidad sanitaria del agua. Además, los sitios con mayor valor del ICA (Ciénaga Saloa, Isla Grande, Zona limnética-Barrancones) no coinciden con los de mejores condiciones ambientales detectados con el PCA.
Tabla 2 Resultados del Índice de Calidad del Agua (ICA) basado en siete variables ambientales para los sitios de muestreo del Complejo Cenagoso de Zapatosa (julio de 2021).
| Lugar | ICA | Condición según el ICA |
|---|---|---|
| Ciénaga Saloa | 0,81 | Aceptable |
| Isla Grande | 0,79 | Aceptable |
| Zona limnética-Barrancones | 0,77 | Aceptable |
| Sapatí | 0,76 | Aceptable |
| Estación E-30 | 0,76 | Aceptable |
| Ciénaga Candelaria | 0,76 | Aceptable |
| Ciénaga Alfaro | 0,74 | Aceptable |
| Belén | 0,73 | Aceptable |
| La Mata | 0,73 | Aceptable |
| Bijagual | 0,72 | Aceptable |
| Sempegua | 0,71 | Aceptable |
| Ciénaga González | 0,69 | Regular |
| Unidad de Mejoramiento Pesquero (UIMEP) | 0,69 | Regular |
| Caño Patón | 0,67 | Regular |
| Puerto Macurutú | 0,67 | Regular |
| Montecarlo | 0,63 | Regular |
| Estación E-22 | 0,62 | Regular |
| Arroyo Alfaro | 0,56 | Regular |
| Purgatorio | 0,49 | Mala |
Descripción general de la comunidad de algas perifíticas y de sus rasgos funcionales. En total, se encontraron 75 géneros, de los cuales 41 se hallaron simultáneamente en los conteos del microscopio invertido y en las fotografías para los análisis morfológicos. Los 35 taxones que no se midieron pertenecieron a géneros que aparecieron una sola vez en los sitios de muestreo o que tuvieron abundancias inferiores al 0,3 % de los individuos contados; la abundancia total de estos 35 taxones fue de 1,46 %, es decir, correspondió a algas con una representación muy baja en la comunidad. Las abundancias absolutas (ind/cm2) y las características morfofuncionales de los 41 taxones más importantes se detallan en la Tabla 2S (material suplementario) y fotografías de los organismos más abundantes se muestran en la Figura suplementaria 1. Aulacoseira (Thwaites, 1848) y Oscillatoria (Vaucher ex Gomont, 1892) estuvieron presentes en los 19 lugares de muestreo. Los géneros que mostraron la mayor variación de sus abundancias entre sitios fueron Aulacoseira, Cosmarium (Corda ex Ralfs, 1848), Eunotia (Ehrenberg, 183), Fragilaria (Lyngbye, 1819), Nitzschia (Hassall, 1845), Pinnularia (Ehrenberg, 1843) y Trachelomonas (Ehrenberg, 1834), con ocurrencia en más de la mitad de los lugares muestreados. En cambio, el género Ulnaria (ENT#091;KützingENT#093; Compère, 2001), que tuvo una gran variación en sus abundancias, solo se halló en seis de las 19 localidades. En conjunto, las comunidades evaluadas mostraron una alta heterogeneidad y una gran variabilidad en su estructura. Sin embargo, el Caño Patón y UIMEP presentaron una notoria abundancia de Nitzschia, para el primer caso, y de Aulacoseira para el segundo.
En cuanto a los rasgos funcionales cualitativos, el 53,6 % de los taxones (22 géneros) presentaron mucílago, el 44 % (18 géneros) fueron formadores de colonias, el 39 % (16 géneros) tuvieron exoesqueleto de sílice, el 19,5 % (8 géneros) se organizaron en filamentos, el 4,9 % (2 géneros) presentaron aerotopos y el 7,3 % (3 géneros) tuvieron flagelos. La presencia de aerotopos y flagelos fueron los atributos con menor abundancia de individuos en casi todos los lugares, exceptuando Sapatí y Puerto Macurutú, sitios que presentaron también una menor abundancia de organismos con exoesqueleto de sílice. La Figura 3A resume este comportamiento de los atributos nominales del ficoperifiton del CCZ.
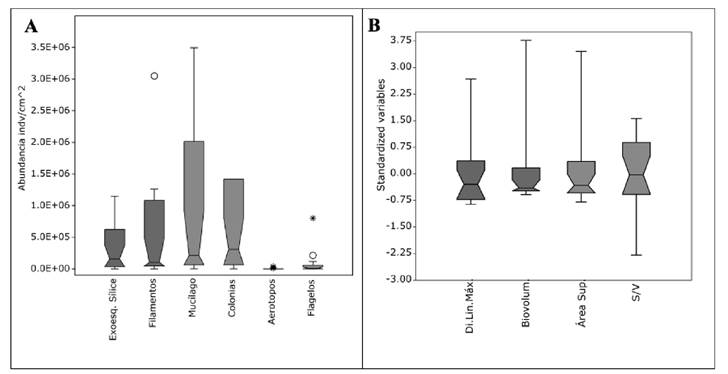
Figura 3 Análisis de cajas y bigotes (“box plots”) de los rasgos morfofuncionales de comunidad de ficoperifiton del CCZ. A. Atributos cualitativos; datos de abundancia de los organismos que presentan los rasgos (ind/cm2). B. Caracteres morfológicos estandarizados.
La presencia de individuos con aerotopos solo se dio en cinco de las 19 estaciones de muestreo. Al parecer, todas estas características cualitativas se distribuyeron de forma heterogénea en los distintos puntos de muestreo; sin embargo, en términos de abundancia, los organismos más comunes fueron aquellos con presencia de mucílago y los formadores de colonias.
De las medidas morfológicas, las algas de mayor dimensión lineal máxima promedio (25,2 µm) ocurrieron en la Ciénaga Alfaro (Melosira C.Agardh, 1824, Oedogonium Link ex Hirn, 1900), en contraposición con la estación E22, en donde los taxones tuvieron un menor promedio de esta longitud (3,54 µm) (Anabaena Bory ex Bornet & Flahault, 1886, Rhabdoderma Schmidle & Lauterborn, 1900). El punto E22 mostró una escasa variación en los datos de dimensión lineal máxima, mientras que Montecarlo fue el de mayor variabilidad en esta característica. Para el biovolumen y el área superficial, Montecarlo presentó en promedio los mayores registros, así como las medidas absolutas más altas de estos dos atributos, con datos absolutos máximos de 5796,9 µm3 (biovolumen) y 2349 µm2 (área superficial), correspondientes al género Oedogonium. En contraste, Bijagual tuvo los menores promedios, con un registro de 40,3 µm2 de área superficial y un biovolumen de 29,9 µm3, que estuvo entre los valores más bajos registrados. Consecuente con sus datos altos de biovolumen y área superficial, el índice S/V fue máximo en Montecarlo (28,7 µm-1). En promedio, este lugar alcanzó el valor más alto de este índice (algas con tendencia a ser pequeñas y esféricas), mientras que la Ciénaga Alfaro tuvo el menor registro, con 6,37 µm-1 (algas con tendencia a ser más grandes, planas y voluminosas). En síntesis, la Figura 3B (basada en las variables morfológicas estandarizadas) muestra que todos los rasgos somáticos tuvieron un comportamiento similar en el conjunto de estaciones del CCZ, con cierta tendencia a una mayor cantidad de registros superiores a la mediana. Para el biovolumen los cuartiles estuvieron más cercanos a dicha mediana (menor dispersión), mientras que la relación S/V tuvo un comportamiento opuesto.
Relaciones entre las abundancias de ficoperifiton y las variables ambientales. Para este análisis se tuvieron en cuenta las 11 variables ambientales evaluadas en el PCA y la composición y abundancia de los géneros de las algas perifíticas (Tabla 2S). El resultado del NMDS se muestra en la Figura 4, en la que se observa que algunos sitios se ubicaron alejados del origen de los datos. Así, a la Zona limnética-Barrancones, con mayor transparencia y aguas más saturadas de oxígeno, se asociaron los géneros Anabaena y Dictyosphaerium (Nägeli, 1849); en La Mata, donde el fósforo total fue alto, se destacaron Aphanocapsa (Nägeli, 1849) y Aphanothece (Nägeli, 1849); y en el Arroyo Alfaro, con predominancia de carbono orgánico total y tendencia a aguas más duras, se presentó un grupo de algas que incluyó los géneros Cocconeis (Ehrenberg, 1836), Gloeocystis (Nägeli, 1849), Oocystis (Nägeli ex A.Braun, 1855), Closterium (Nitzsch ex Ralfs, 1848), Melosira, Eudorina (Ehrenberg, 1832), Spondylosium (Brébisson ex Kützing, 1849), Eunotia, Coelastrum (Nägeli, 1849), Cosmarium y Frustulia (C.Agardh, 1821), entre otros. Otros taxones, como Phacus (Dujardin, 1841), Rhabdoderma, Gomphonema (Ehrenberg, 1832), Oscillatoria y Botryococcus (Kützing, 1849) no mostraron una asociación clara a algún sitio de muestreo específico. El “stress” de este ordenamiento fue de 0,13 (inferior a al valor límite de 0,2) y se considera como un resultado que permite hacer deducciones valederas (Clarke, 1993). Desde el punto de vista de la composición y abundancia de las algas perifíticas, se nota una dispersión de los datos y no se destacan otros patrones de agrupamiento o segregación, más allá de los casos mencionados.
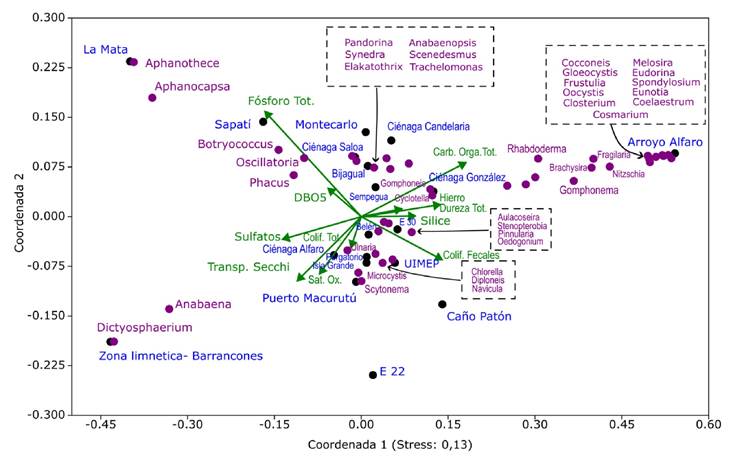
Figura 4 Análisis multidimensional no métrico (NMDS) de la comunidad de ficoperifiton del CCZ y de las variables ambientales. En el título del eje X se indica el “stress” o grado de ajuste de la ordenación.
Los rasgos funcionales del ficoperifiton en el espacio ambiental del CCZ. La técnica de ordenamiento NMDS, permitió explorar la organización de los rasgos morfológicos de las algas perifíticas en el conjunto de estaciones del CCZ y ver la posible influencia de las variables ambientales en dicha estructura. Como se observa en la Figura 5, para los cuatro rasgos morfológicos la primera coordenada estuvo principalmente asociada a la demanda biológica de oxígeno y en menor grado a lo dureza total. En cambio, la importancia de las variables ambientales de la segunda coordenada varió para cada rasgo morfológico.
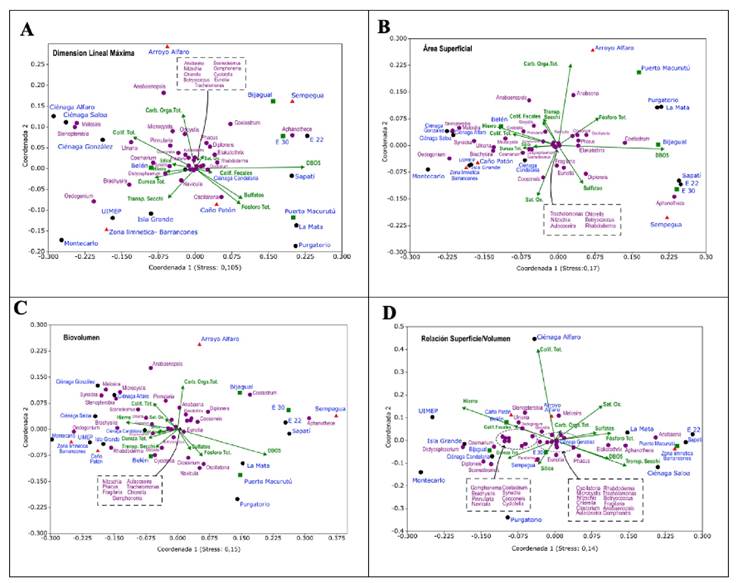
Figura 5 Análisis multidimensional no métrico (NMDS) de los rasgos morfológicos de comunidad de ficoperifiton del CCZ y de las variables ambientales. A. Dimensión lineal máxima. B. Área superficial. C. Biovolumen. D. Relación S/V. En cada caso, en el título del eje X se indica el “stress” o grado de ajuste de la ordenación. Los triángulos rojos corresponden a las estaciones probablemente más contaminadas, los cuadrados verdes a las aparentemente menos deterioradas y los puntos negros a los sitios con una degradación moderada.
Para la dimensión lineal máxima (Fig. 5A), los factores determinantes en la coordenada 2 fueron el carbono orgánico total y las coliformes totales; para el área superficial (Fig. 5B), además del carbono orgánico total, otras variables importantes fueron la saturación de oxígeno y sulfato; en el caso del biovolumen (Fig. 5C), el carbono orgánico tuvo la mayor influencia sobre esta coordenada 2; por su parte, las coliformes totales mostraron un mayor dominio en el eje Y de la relación S/V (Fig. 5D). De otro lado, los cuatro ordenamientos tuvieron un “stress” < 0,2, o, dicho de otra manera, los modelos estadísticos obtenidos fueron aceptables. Se destacó el ordenamiento de la dimensión lineal máxima (Fig. 5A), que alcanzó el menor “stress” (0,105), lo cual indica que en este caso el ajuste del modelo con la realidad fue el más preciso. Para el área superficial, el biovolumen y la relación S/V el “stress” fue de 0,17, 0,15 y 0,14, respectivamente, lo cual señala que los datos permitieron establecer algunas diferencias en el espacio de dos dimensiones del ordenamiento, por lo que se pueden considerar como modelos moderadamente aceptables (Kruskal, 1964; Clarke, 1993). Con base en lo anterior, se detallan a continuación los resultados del ordenamiento más ajustado, correspondiente a la dimensión lineal máxima.
La máxima longitud se halló en las algas de los géneros Oedogonium, Melosira y Oscillatoria, todas ellas de tipo filamentoso. La clorofícea Oedogonium se ubicó cerca de las estaciones Sempegua, UIMEP y la Zona limnética-Barrancones, mientras que Melosira y Stenopterobia (Brébisson ex Van Heurck, 1896) (una diatomea de gran tamaño) se asociaron a las Ciénagas Saloa, Alfaro y González. La cianobacteria Aphanothece, cuyas colonias alcanzan dimensiones grandes, se relacionó con las estaciones E30 y E22 que mostraron mayores registros de demanda biológica de oxígeno (Fig. 5A). El género Oscillatoria estuvo más cerca de Caño Patón, donde las características ambientales fueron opuestas, es decir, menor cantidad de coliformes totales, además de aguas más ricas en sulfato y fósforo. Por su parte, el tamaño de las algas más pequeñas (Scenedesmus, Anabaena, Anabaenopsis (V.V.Miller, 1923), Chlorella (Beyerinck ENT#091;BeijerinckENT#093;, 1890), Cyclotella (ENT#091;KützingENT#093; Brébisson, 1838) y Eunotia, entre otras) no parece estar afectado en especial por ninguna variable ambiental, como se deduce de la ubicación de estos taxones cerca del origen de los datos.
En un intento por estudiar de manera simultánea el efecto del ambiente fisicoquímico y bacteriológico sobre las variables cualitativas y morfológicas del ficoperifiton del CCZ, se realizó el NMDS que se muestra en la Figura 6. Este análisis incluyó las abundancias de las características funcionales cualitativas (formas de vida) y los promedios de los rasgos dimensionales y los relacionó con los factores fisicoquímicos, bacteriológicos y de calidad del agua-ICA. Las variables más relacionadas con la coordenada 1 fueron las coliformes fecales y la dureza total; con la coordenada 2 se asociaron principalmente el sulfato, la saturación de oxígeno y la demanda biológica de oxígeno. Como se observa en este ordenamiento, los atributos de formación de filamentos y de presencia de exoesqueleto de sílice estuvieron muy asociados a la dureza total, en especial en los sitios Arroyo Alfaro y Ciénaga Alfaro. La presencia de flagelos se relacionó con el sulfato y la saturación de oxígeno en la Ciénaga Saloa. Los aerotopos se asociaron con el sitio Sempegua, pero sin un factor ambiental determinante. El biovolumen se vinculó con el ICA y tendió a ubicarse en dirección al Caño Patón, Montecarlo y la Ciénaga Candelaria. La presencia de mucílago se asoció al hierro y al fósforo total, sin ubicarse espacialmente en ningún lugar. Por su parte, la capacidad de formar colonias se asoció a mayores cantidades de bacterias coliformes fecales, y este vector mostró tendencia dirigirse hacia Sapatí, La Mata y la Zona limnética-Barrancones. Los demás rasgos morfofuncionales (dimensión lineal máxima, área superficial y relación S/V) no exhibieron patrones concluyentes de asociación con los factores ambientales ni con sitios específicos dentro del CCZ. En general, se puede decir que las estaciones con mejores condiciones de calidad fisicoquímica del agua (marcadas con cuadrados verdes en la Fig. 6), se ubicaron hacia la región izquierda del ordenamiento, mientras que aquellos sitios de menor calidad (triángulos rojos) se ubicaron de manera dispersa en el ordenamiento. Se destaca en este análisis NMDS el “stress” bajo (0,067), que indica un muy buen ajuste de los datos con el modelo estadístico obtenido.
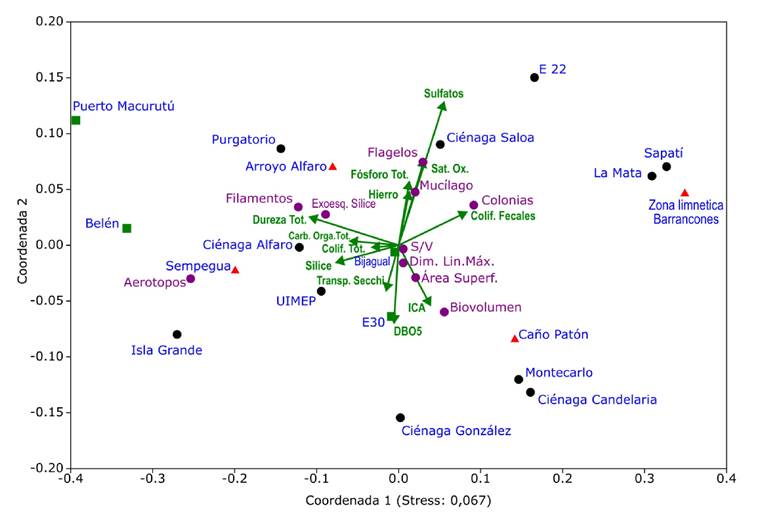
Figura 6 Análisis multidimensional no métrico (NMDS) teniendo en cuenta las 11 variables ambientales más determinantes, el índice ICA y las 10 características funcionales de la comunidad de ficoperifiton del CCZ. En el título del eje X se indica el “stress” o grado de ajuste de la ordenación. Los triángulos rojos corresponden a las estaciones probablemente más contaminadas, los cuadrados verdes a las aparentemente menos deterioradas y los puntos negros a los sitios con una degradación moderada.
Las correlaciones de Spearman mostraron resultados positivos y significativos entre el biovolumen y las coliformes totales (p = 0,04, r = 0,46) y entre éstas y el área superficial (p = 0,01, r = 0,54). De los rasgos cualitativos, tanto la presencia de mucílago como la organización en colonias se relacionaron inversamente con la dureza total (p = 0,01, r = -0,53 y p = 0,02, r = -0,51, respectivamente).
DISCUSIÓN
Los factores físicos, químicos y bacteriológicos de las aguas en los sistemas lénticos del CCZ evidencian un ambiente de clima cálido, relativamente enriquecido con materia orgánica y nutrientes provenientes probablemente de su cuenca hidrológica y de las actividades humanas (ganadería, agricultura, aguas residuales puntuales y difusas). Su estado general se puede considerar como eutrófico (Álvarez-S, 2012), característica que es la esperada en sistemas cenagosos asociados al plano de inundación de los grandes ríos. Durante la fase de campo, en varios de los sitios de colecta cercanos a la costa del sistema cenagoso, se visualizó un uso intensivo de suelo en actividades de ganadería y de agricultura. Además, se detectaron grandes tapetes de jacinto de agua (Eichhornia ENT#091;Kunth, 1843ENT#093; spp.) en el espejo de agua, los cuales se acumularon en las zonas litorales de la ciénaga, de acuerdo con la acción predominante del viento. Los efectos de la intervención antrópica se reflejan principalmente en la presencia notoria de bacterias coliformes, tanto totales como termo-tolerantes (fecales). Las coliformes, junto con el hierro y el grado de mineralización del agua, parecen tener algún grado de influencia sobre la estructura y distribución de las comunidades de algas perifíticas del CCZ.
Un aspecto destacado en estos resultados es la ausencia de grandes diferencias en las variables ambientales en todo el complejo cenagoso, con excepción de las bacterias coliformes (totales y fecales). Esta homogeneidad fue bastante generalizada, como se pudo ver en los datos del ICA, e impidió separar con mayor claridad los sitios más limpios de aquellos más degradados. Parte de esta respuesta homogénea del ICA podría obedecer los registros muy similares de los nutrientes (fósforo total, fosfato, nitrato, nitrógeno total) en todos los sitios del CCZ. Esto hace pensar que pudieron presentarse inconvenientes con los límites de detección de los análisis de nitrógeno y fósforo, un problema recurrente en los laboratorios del país que llama la atención sobre la necesidad de utilizar metodologías más precisas para establecer la concentración real de estos elementos, fundamentales para entender el funcionamiento ecológico y la salud de los sistemas acuáticos. No obstante, aunque no fue posible detectar un gradiente de nutrientes, si se observó un gradiente de mineralización y de transparencia; este último es muy importante por sus efectos en el régimen de luz para las algas en el ambiente acuático (Pacheco et al., 2022). De esta manera, hay cierta tendencia a que la región occidental del CCZ sea más transparente (y con menos contaminación fecal), mientras que la zona oriental se inclina a presentar aguas más turbias (y con mayores cantidades de coliformes).
Desde el punto de vista morfofuncional, las algas perifíticas del CCZ tienden a ser pequeñas y con una relación S/V moderadamente alta. Algunas algas filamentosas de gran tamaño (como Oedogonium y Melosira) parecen asociarse a lugares con una mayor concentración de coliformes totales (pero baja de coliformes fecales) y con menos sulfato y menos fósforo total. La propensión a los tamaños reducidos parece ser una respuesta de las algas bentónicas al enriquecimiento con nutrientes, especialmente con nitrógeno, como fue demostrado experimentalmente por Ferragut & Bicudo (2010). En el trabajo de dichos autores, la comunidad de algas perifíticas de un sistema oligotrófico pasó de estar compuesta por organismos nanoperifíticos (2-20 µm) al dominio de algas picoperifíticas (0,2-2 µm) cuando se adicionó nitrógeno al sistema. Esto parece darle ventaja a las algas cuando el fósforo es deficitario, como es el caso de Zapatosa, donde la relación N/P fue en promedio 20,3 (Tabla 2S), es decir, con limitación por fósforo. Reynolds et al. (2002) hallaron un comportamiento similar para las algas planctónicas, las cuales tienden a ser pequeñas (nano y picoplactónicas) en ambientes meso a eutróficos con profundidades de la capa superficial de mezcla inferiores a 3 metros y bajas concentraciones de fósforo.
Por otra parte, las tallas reducidas de las algas del CCZ podrían estar favorecidas por la herbivoría, ya que las comunidades de ficoperifiton muy pastoradas están dominadas generalmente por especies de algas pequeñas, adheridas o postradas sobre el sustrato, que son menos consumidas debido a su pequeño tamaño (Marks & Lowe, 1989). Esta es una suposición que requerirá hacer trabajos experimentales para comprobar su validez.
Como se sabe, las algas que tienen una alta relación S/V presentan una mayor área de contacto directo con el ambiente que las rodea, y con ello reciben la influencia de los factores físicos y químicos del agua de forma más rápida (Reynolds, 2006). De esta manera, las algas que tiene valores medios a altos de S/V son por lo general esféricas y pequeñas y poseen una alta capacidad de absorber nutrientes (Lewis, 1976; Foy, 1980), lo que les puede dar una ventaja competitiva (Friebele et al., 1978). Para el caso del CCZ esta ventaja podría favorecer a las algas pequeñas, dada la limitación por fósforo en el ecosistema. La correlación significativa hallada entre el biovolumen y el área superficial con los coliformes totales parece deberse a que en el sitio donde estas bacterias fueron más abundantes (Ciénaga Alfaro), los géneros grandes y voluminosos como Oscillatoria y Melosira tuvieron una alta representación (Fig. 5). Aunque la abundancia de coliformes no explica el comportamiento de las algas, la relación parece ser indirecta, dado que la presencia de altas densidades de coliformes implica una fuerte intervención humana, acompañada generalmente por mayores concentraciones de nutrientes. Es probable que estos nutrientes no fueran cuantificados por los métodos analíticos empleados o que no están disponibles en el ambiente, ya que su absorción en la columna de agua se atribuye a las macrófitas; además, los nutrientes que bombean estas plantas desde los sedimentos pueden a ser atrapados por las algas bentónicas que cubren las macrófitas antes de que alcancen la columna de agua (Stevenson, 1996).
La presencia de mucílago en muchos taxones es una estrategia común de adhesión al sustrato (Stevenson, 1996), pero también podría servir de protección contra la herbivoría, como se ha documentado para el fitoplancton (Reynolds, 2007), de resistencia a la digestión de los herbívoros cuando pasan a través del tracto intestinal (Gliwicz, 2003) o como mecanismo de dispersión, como se ha visto en microalgas bentónicas marinas (Caronni et al., 2016). En cuanto a la presencia de géneros coloniales y filamentosos, cuyas formas diversas y complicadas están muy bien adaptadas a las condiciones bentónicas (Stevenson, 1996), se han propuesto varias explicaciones a su predominancia. En primer lugar, sus estructuras complejas les permiten inmovilizar nutrientes y sedimentos en la matriz perifítica; asimismo, el crecimiento en filamentos posibilita utilizar mejor la luz y los nutrientes de la columna de agua, con lo cual superan a las formas subyacentes en la competencia por esos recursos (Stevenson, 1996). Además, las formas filamentosas prosperan mejor en condiciones de baja velocidad del agua (Ahn et al., 2013), como es el caso de los sistemas lénticos del CCZ. Por otra parte, la dureza del agua parece tener un efecto negativo sobre la abundancia de algas que producen mucílago y sobre la densidad de taxones formadores de colonias, como se deduce de las correlaciones halladas. Podría ser que estas correlaciones sean fortuitas, ya que hasta el momento no existen estudios que demuestren esta clase de afectaciones de la mineralización del agua sobre la abundancia de estos grupos funcionales de microalgas perifíticas. Igualmente, es probable que este resultado se deba una mayor abundancia de organismos que se alimentan de las algas, es decir, un incremento de la actividad de los herbívoros. Estos son temas que merecen investigarse en el futuro, preferiblemente a través de abordajes experimentales.
La presencia de aerotopos se halló solamente en dos géneros de cianobacterias (Anabaenopsis y Microcystis), por lo que esta característica parece tener menor relevancia en la ecología de la comunidad de ficoperifiton del CCZ. En el caso del ambiente planctónico, estas estructuras acumuladoras de gas mejoran la flotabilidad de las cianobacterias (Reynolds, 2006). Este no parecer ser un el caso de los aerotopos en los géneros perifíticos de los sistemas estudiados. Otra función que podrían cumplir estas vesículas gaseosas en los géneros perifíticos de Zapatosa es recolectar el dióxido de carbono producido por la descomposición interna de los carbohidratos dentro de las células para su reutilización en la fotosíntesis (Rae et al., 2013).
Aunque los rasgos morfofuncionales del ficoperifiton responden a las características del ambiente acuático, no parecen reflejar adecuadamente las condiciones de calidad sanitaria de los distintos sitios del CCZ, ya que no se observaron patrones claros de agrupamiento de los rasgos funcionales de las algas de acuerdo a las condiciones físicas, químicas o microbiológicas. Como ya se mencionó, esto podría obedecer a la falta de diferencias evidentes en la calidad del agua entre las distintas zonas del sistema cenagoso de Zapatosa. Aunque se buscó que los sitios de muestreo tuvieran características ambientales contrastantes, parece ser que estas diferencias no fueron tan grandes. Así se deduce de las respuestas bióticas de la comunidad de ficoperifiton y de los valores del ICA obtenidos en el complejo de ecosistemas estudiados. Probablemente, dicho índice no tiene un poder de resolución suficiente que permita separar las condiciones de calidad del agua de los distintos sitios del CCZ. Sin embargo, esta homogeneidad que se obtuvo en los valores del ICA (la mayoría correspondientes a situaciones aceptables de calidad y con un solo caso de características inadecuadas) podría deberse muy seguramente a que en general todos los subsistemas del CCZ están sometidos a presiones similares de deterioro. Esto a su vez implicaría que no existen realmente ambientes prístinos dentro del complejo cenagoso. Por supuesto, no pueden descartarse los efectos que podrían tener sobre los resultados los límites de detección inadecuados en los análisis de laboratorio de los nutrientes, ni el efecto del diseño muestral empleado (estratificado en lugar de aleatorio), aspectos que podrían influir parcialmente en la homogeneidad observada en los rasgos funcionales de las algas. Aun así, parece existir una uniformidad real en el ambiente fisicoquímico de todo el complejo cenagoso, por lo que las respuestas morfofuncionales de las comunidades ficoperifíticas tampoco fueron significativamente diferentes entre las distintas zonas del sistema. Esto parece explicar, al menos en parte, la falta de patrones claros en el ordenamiento de los atributos y de los rasgos de historias de vida de las algas perifíticas en el gradiente de disturbio del CCZ, como lo mostraron los análisis NMDS. Para el fitoplancton, Lobo et al. (2018) encontraron que los grupos funcionales basados en la morfología responden bien a los cambios en las variaciones ambientales provocados por los ciclos de inundación en lagos de la planicie amazónica; por lo tanto, es probable que en el CCZ los rasgos funcionales del ficoperifiton cambien notablemente en diferentes momentos del ciclo hidrológico, hipótesis que deberá probarse en próximos estudios.
Sobre el fitoplancton se ha investigado más que sobre el ficoperifiton. En sistemas de planos de inundación tropicales y subtropicales, las investigaciones han mostrado resultados contrastantes para las algas planctónicas; por una parte, se ha visto que la luz, los nutrientes y la temperatura son factores determinantes en la organización morfofuncional de la comunidad, tanto a la escala particular de un lago amazónico (De Souza et al., 2022), como en el ámbito regional al comparar lagos de inundación de zonas bajas con lagos de montaña tropical (Hernández et al., 2020), pero en otros casos no se han detectado relaciones entre los rasgos funcionales y la variabilidad ambiental (Silva et al., 2022). Para el caso de las algas perifíticas en estos ambientes inundables tropicales, los estudios son escasos; Dunck et al. (2015) demostraron que los rasgos funcionales del ficoperifiton responden a los cambios en los factores ambientales provocados por el pulso de inundación en lagos asociados a la cuenca del río Paraná en Brasil. Según estos autores, el pulso favoreció el predominio de formas de vida coloniales, pedunculadas y heterofilamentosas, una respuesta similar a la hallada en el presente estudio (muestreo de aguas en descenso del CCZ), en el que predominaron formas coloniales, mucilaginosas y filamentosas. A diferencia de nuestro estudio, en el plano de inundación del río Paraná las diatomeas fueron el grupo dominante (Bichoff et al., 2018), pero en ese trabajo los muestreos se hicieron principalmente en sistemas fluviales, lo que explicaría la dominancia de las algas con exoesqueleto de sílice; dichos autores hallaron una relación entre los rasgos funcionales (formas de vida, formas de adherencia) y las variables del gradiente ambiental (turbidez, temperatura, conductividad y concentraciones de nitrato), probablemente porque dicho gradiente, que abarcó una distancia de 200 km, fue muy marcado.
Finalmente, es importante recalcar que la información analizada correspondió a un conjunto limitado de datos y solamente a una de las fases hidrológicas del CCZ (aguas en descenso). Será necesario ampliar esta base de registros, tanto espacial como temporalmente, con lo cual se podrían obtener resultados más claros y contundentes sobre la respuesta morfofuncional de las algas perifíticas ante las variaciones y tensores ambientales. Igualmente, sería conveniente, en lo posible, buscar ecosistemas similares cercanos que tengan un elevado grado de conservación, que estén muy poco afectados por las actividades humanas y que sirvan de ambientes de referencia para determinar los rasgos funcionales típicos de sus comunidades perifíticas.
CONCLUSIONES
Los rasgos funcionales cualitativos (presencia o ausencia de valvas o exoesqueleto de sílice, organización o no en filamentos, presencia o ausencia de mucílago, movilidad mediante flagelos, capacidad de formar colonias, aparición de aerotopos) y los rasgos morfológicos (dimensión lineal máxima, biovolumen, área superficial, relación superficie/volumen) medidos en el ficoperifiton del CCZ aportan un primer acercamiento a la ecología funcional de esta comunidad. Por lo tanto, permiten aproximarse a entender la manera como las especies pueden ser exitosas para establecerse y desarrollarse en este ambiente cenagoso. Estas mediciones morfofuncionales, además de brindar herramientas para conocer las respuestas ecológicas de estos organismos, constituyen una línea base que servirá para valorar los cambios futuros que se produzcan en dichas algas ante las variaciones ambientales, tanto naturales como producidas por la acción humana.
Las condiciones de contaminación y deterioro de los distintos sitios evaluados en el complejo cenagoso fueron muy semejantes y no permitieron detectar claramente las respuestas de estos rasgos funcionales frente a los cambios en la calidad del agua. En consecuencia, si se quisieran emplear los atributos funcionales como medidas del grado de disturbio de los sistemas acuáticos, será necesario ampliar el rango ambiental, de manera que se incluyan sitios muy bien conservados y otros con un alto deterioro, esto con el fin de que tales rasgos recojan adecuadamente la variabilidad en un gradiente de alteración suficientemente amplio.
La suposición inicial de que las características morfofuncionales de las algas perifíticas reflejarían las condiciones ambientales del agua se pudo comprobar parcialmente, ya que los análisis estadísticos no fueron contundentes en el establecimiento de estas relaciones. Probablemente esto se debió, al menos en parte, a la mencionada tendencia a la homogeneidad en las variables físicas, químicas y bacteriológicas de los diferentes sitios estudiados en el CCZ.











 nova página do texto(beta)
nova página do texto(beta)