Introducción
El fósforo (P) es un nutrimento esencial para el crecimiento y productividad de los cultivos (Blackwell, Darch y Haslam, 2019). Sin embargo, en la mayoría de los suelos, sólo una pequeña fracción del P mineral es asimilable por la planta (van Doorn et al., 2024). Esto hace necesario aplicar fuentes fosfatadas para mantener concentraciones óptimas de P en la solución del suelo y evitar que se convierta en un factor limitante al crecimiento y productividad de las plantas cultivas. Se estima que una concentración adecuada de P en la solución del suelo, para la mayoría de los cultivos, varía entre 5 y 20 mg kg-¹ (McDowell, Pletnyakov y Haygarth, 2024).
La forma más rápida para incrementar la concentración de P en la solución del suelo es suministrarlo mediante el uso de fertilizantes fosfatados; sin embargo, el P soluble tiende a ser adsorbido por las partículas del suelo debido a diferentes procesos fisicoquímicos, lo que reduce su disponibilidad (Zhao, Li y Yang, 2021; Álvarez y Noellemeyer, 2022). En suelos ácidos el P inorgánico se precipita como fosfato de aluminio (P-Al), de hierro (P-Fe) o es adsorbido en las superficies de óxidos de Fe, de Al y en minerales arcillosos (Celi, Prati, Magnacca, Santoro y Martin, 2020). En suelos neutros o calcáreos el P se precipita como fosfatos de calcio (Ca-P) o es adsorbido en la superficie de las arcillas y en el carbonato de calcio (CaCO3) (Gai et al., 2024).
En algunas zonas agrícolas es común el uso del superfosfato triple de calcio (SFT) (Ca(H2PO4)2 H2O), fertilizante que, al disolverse con la humedad edáfica, genera ácido fosfórico (H3PO4) disminuyendo el pH del entorno inmediato, facilitando la solubilización de compuestos de Fe3+y Al3+, que luego reaccionan con el P, contribuyendo a su adsorción (Penn y Camberato, 2019). El pH del suelo influye en la transformación del H3PO4 en H2PO4 -, HPO4 2- y PO4 3- con un incremento en el pH y en las primeras semanas, después de su aplicación, se forman fosfatos dicálcicos dihidratados (CaHPO4 2H2O); entre 3 y 5 meses empieza a precipitarse como octofosfatos de calcio (Ca4H(PO4)3 2.5H2O) y después de 8 meses se forman eventualmente minerales de apatita (Ca5(PO4)3OH (Havlin, Beaton, Tisdale y Nelson, 2017). La liberación gradual de P de estos compuestos hacia la solución del suelo, determina la disponibilidad de P para las plantas. En suelos calcáreos, la adsorción de P puede ocurrir desde concentraciones en solución de 0.1 a 5 mg kg-¹, mientras que su precipitación como P-Ca tiene lugar en concentraciones de 400 y 600 mg kg-¹ (Zhou y Li, 2001). De hecho, las prácticas de manejo de fertilizantes influyen en las reacciones de adsorción y de precipitación, lo que afecta la distribución y disponibilidad del P en el suelo (Afif, Palencia y Oliveira, 2013). Para modelar la disminución de P en la solución, las isotermas de adsorción, como la de Langmuir, permiten relacionar la cantidad de P adsorbido con su concentración en equilibrio en la solución del suelo. Esto permite estimar las necesidades de fertilizante fosfatado en función de la capacidad máxima de adsorción del suelo. En suelos calcáreos de España se han reportan valores de máxima adsorción de P entre 150 a 2566 mg kg-¹ (López-Pineiro y Navarro, 1997), mientras que en suelos de Florida se pueden alcanzar valores hasta de 5556 mg kg-¹ (Zhou y Li, 2001).
Los vertisoles ocupan el 8.3% del territorio nacional y se consideran los suelos más productivos de México; sin embargo, presentan problemas de manejo en cuatro aspectos principales, a) mecanización; b) compactación, c) drenaje y d) fertilización (Torres-Guerrero, Gutiérrez, Ortiz y Gutiérrez, 2016). El estudio del comportamiento del fósforo en suelos Vertisols es particularmente relevante debido a su alta capacidad de adsorción del P, lo que afecta significativamente su disponibilidad para las plantas. En este contexto, este estudio tiene como objetivo determinar la capacidad máxima de adsorción de P en un suelo Vertisol y analizar el comportamiento de dos fertilizantes fosfatados.
Materiales y Métodos
Las muestras de suelo se recolectaron en el área agrícola del campo experimental Las Huastecas del INIFAP, ubicado en Villa Cuauhtémoc, Altamira Tamaulipas, México (22° 34’ 6” N, 98° 10’ 5” O), el suelo se clasifica como un Vertisol. Las muestras de suelo recolectadas a una profundidad de 0-25 cm, fueron caracterizadas conforme a Norma Oficial Mexicana NOM-021-SEMARNAT-2000 (NOM-021-SEMARNAT-2000, 2002). Se evaluaron las propiedades físicos y químicas iniciales del suelo, incluyendo textura (método de Bouyoucos); capacidad de campo (Olla de presión); punto de marchites permanente (Membrana de presión); pH en agua (suelo: solución 1:2); conductividad eléctrica (Pasta saturada); materia orgánica; CIC y cationes intercambiables (NH4OAc 1 M a pH 7), fósforo disponible (Olsen); micro nutrimentos extraídos en DTPA), carbonatos totales (Sokolovich, 1966); carbonatos activos (Loeppert, Hallmark y Koshy, 1984). Las propiedades iniciales del suelo se indican en el Cuadro 1.
Table 1: Physicochemical properties of the soil used in the study.
| Determinación | Valor |
| pH H2O 1:2 (suelo: solución) | 8.7 |
| P-Olsen mg kg-1 | 10.4 |
| CE (dSm-1) | 1.3 |
| Carbonatos totales (%) | 6.9 |
| Carbonatos activos (%) | 0.6 |
| Materia orgánica (%) | 1.1 |
| CIC (cmol (+) kg-1) | 52.5 |
| Cationes intercambiables (cmol (+) kg-1) | |
| K+ | 0.72 |
| Ca2+ | 35.2 |
| Mg2+ | 4.0 |
| Na+ | 1.4 |
| Micronutrimentos (mg kg-1) | |
| Fe2+ | 0.3 |
| Zn2+ | 5.5 |
| Mn2+ | 0.2 |
| Cu2+ | 1.2 |
| Capacidad de campo (%) | 42.6 |
| Punto de marchites permanente (%) | 20.6 |
| Clase textural | |
| Arena (%) | 26.9 |
| Limo (%) | 23.0 |
| Arcilla (%) | 50.1 |
Isotermas de Adsorción de Fosforo
Se evaluó la capacidad de adsorción de P del suelo mediante las siguientes determinaciones:
Adsorción máxima de P. Se tomaron muestras de 1 g de suelo, las cuales se colocaron en tubos de centrífuga de 50 mL. A cada tubo se le adicionaron 25 mL de una solución de CaCl2 0.01 mol L-1 con concentraciones de P de 0, 5, 10, 20, 40, 60, 80 y 100 mg kg-1. Se utilizó SFT y H3PO4 como fuente de fósforo. Cada tratamiento de P se realizó por triplicado. Los tubos se agitaron durante 24 horas a temperatura ambiente. Posteriormente, se centrifugaron a 1800 rpm durante 10 minutos, el sobrenadante se filtró en una membrana de 0.45 µm (Nair et al., 1984). El fósforo se determinó por colorimetría mediante un espectrofotómetro a 882 nm, el color se desarrolló con una solución combinada de ácido ascórbico-molibdato de amonio. La cantidad de P adsorbida por el suelo se calculó por la diferencia entre la concentración de la solución inicial y la concentración de P en la solución en equilibrio con el suelo.
Los valores de adsorción se determinaron mediante la ecuación de Langmuir que en su forma lineal es:
Donde: C = concentración de P en la solución en equilibrio con el suelo (mg mL-1), x/m = P adsorbido sobre la superficie del suelo (µg g-1 de suelo), b = cantidad máxima de P que puede ser adsorbido sobre la superficie (µg g-1 de suelo), k = constante de energía de retención (mL µg-1).
Fraccionamiento de P. En las muestras de suelo utilizadas en la determinación de la adsorción máxima de P y en las cuales parte del P aplicado a un gramo de suelo fue adsorbido, se determinaron las diferentes fracciones de P mediante el método de Petersen y Corey (1966); fosfatos solubles en agua (P-S) -(NH4Cl 1 N); fosfatos ligados al aluminio (P-Al) - (NH4F 0.5N pH 7.0); fosfatos ligados al hierro (P-Fe) - (NaOH 1 N); fosfatos ligados al Calcio (P-Ca) - (H2SO4 0.5 N).
Disponibilidad del P aplicado. Se colocaron 30 g de suelo en frascos de vidrio de 130 mL, después se aplicó por triplicado los tratamientos de 214, 275, 466, 847 y 1100 mg kg-1 de P proveniente del superfosfato triple de calcio, Ca(H2PO4)2. H2O (46% P2O5) y ácido fosfórico, H3PO4 (85% de pureza y densidad de 1.76 g mL-1). La cantidad de P aplicado representó 20, 26, 44, 80 y 100%, respectivamente de la adsorción máxima de P por el suelo.
Se estudiaron 10 tratamientos derivados de un arreglo factorial 2×5. El primer factor fue la fuente de P (Ca(H2PO4)2. H2O (46% P2O5) y H3PO4 (85% de pureza y densidad de 1.76 g mL-1) y el segundo factor fueron las dosis de P aplicadas (214, 275, 466, 847 y 1100 mg kg-1), las cuales fueron aplicadas en frascos de vidrio de 130 mL de capacidad que contenían 30 g de suelo. La cantidad de P aplicado representó 20, 26, 44, 80 y 100%, respectivamente de la adsorción máxima de P por el suelo. Cada tratamiento se replicó tres veces y se organizó bajo un diseño completamente al azar.
Las dosis del fertilizante fosfatado se aplicaron uniformemente en el suelo y se mezclaron para garantizar su distribución homogénea. Posteriormente se añadió agua a cada frasco hasta alcanzar la capacidad de campo, que se había determinado previamente en las muestras de suelo. Los frascos se colocaron en una incubadora, permaneciendo a 35 °C durante 36 días; periódicamente se aplicó el volumen de agua necesario para mantener la humedad de suelo. Se realizaron cinco evaluaciones del P aprovechable con el método Olsen, a 1, 3, 9, 18, 27, 36 días después de la incubación.
Análisis Estadístico
Los datos obtenidos fueron analizados estadísticamente utilizando software informático Statical Analysis System (SAS, 2011). Se utilizó un análisis de varianza, para evaluar la diferencia entre los tratamientos y las medias se compararon mediante la prueba de Tukey (P ≤ 0.05).
Resultados y discusión
Adsorción Máxima y Fraccionamiento de P
Las curvas de adsorción de P son fundamentales para entender su dinámica en el suelo, además permiten definir la estrategia más adecuada para la fertilización. En este estudio la adsorción de P por ambas fuentes fosfatadas mostró un buen ajuste a la ecuación de Langmuir con un coeficiente de determinación R2 = 0.93**. El P adsorbido por el suelo fue 1080 y 1030 mg kg-1 para el SFT y H3PO4, respectivamente (Cuadro 2). Estos valores indican que el P aplicado a través de los fertilizantes fosfatados no estará completamente disponible para las raíces de las plantas, lo anterior sugiere que su disponibilidad no depende únicamente de su concentración, sino de una serie de procesos fisicoquímicos del suelo (Muindi et al., 2015). Los valores de adsorción de P obtenidos en este estudio, son comparables con los reportados en vertisols de España (López-Pineiro y Navarro, 1997); no obstante, la capacidad de adsorción es cuatro veces inferior a la observada en Vertisols del sur de Florida (Zhou y Li, 2001), lo cual que puede deberse a diferencias en los minerales del suelo como caolinita, montmorillonita, illita y geotita, como fosfato de calcio, aluminio y fierro (Penn y Camberato, 2019).
Table 2: Parameters of the adsorption of P derived from the Langmuir isotherm.
| Fuente | Ecuación de la isoterma de adsorción de P | R2 | Adsorción máxima de P de suelo | Energía de adsorción |
| mg kg-1 | mg P g-1 | |||
| SFT | Y = 13.137 + 0.928 (C) | 0.93** | 1080 | 0.07 |
| H3PO4 | Y = 14.539 + 0.974 (C) | 0.93** | 1030 | 0.07 |
**altamente significativo (α ( 0.01); C = concentración de P mg mL-1 en equilibrio.
**Highly significant (α ≤ 0.01); C = equilibrium P concentration in mg mL⁻¹.
El P adsorbido fue liberado con relativa facilidad, lo que sugiere que la energía de adsorción en el suelo es similar para ambas fuentes fosfatadas. Estos resultados son consistentes con los hallazgos de Muindi et al. (2015), quienes reportaron que la liberación de P en suelos calcáreos está fuertemente influenciada por la mineralogía del suelo. En cuanto al P total aplicado, se adsorbió el 58% con SFT y el 71% con H3PO4. Con el SFT, 30% del fósforo adsorbido estuvo ligado al calcio y el 28% fue P soluble, mientras que con H3PO4 estos porcentajes fueron 40% y 31%, respectivamente. Las fracciones de P-Al, P-Fe no se detectaron (datos no mostrados).
Disponibilidad del P Aplicado como Fertilizante
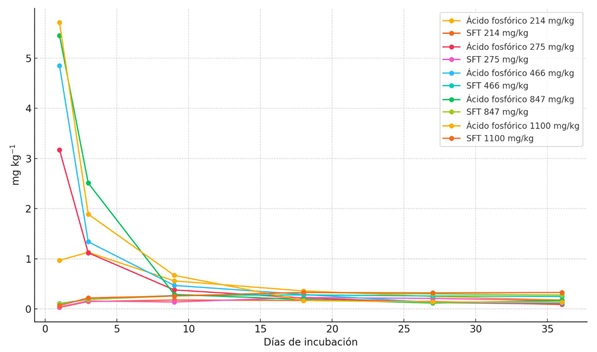
La disponibilidad del P en el estudio de incubación, fue significativamente afectada por la fuente, dosis aplicada y el tiempo de incubación (Figura 1). Hasta el noveno día posterior a la aplicación, los valores de P disponible en él fueron superiores cuando se utilizó H3PO4, con respecto a los del SFT, lo que indica una mayor disponibilidad de P en la solución del suelo con el uso del H3PO4. Aunque la disponibilidad de P aumentó con la dosis aplicada, las diferencias entre las dosis solo fueron significativas hasta el tercer día del estudio de incubación. A medida que el H3PO4 interactuó más tiempo con el suelo, su disponibilidad disminuyó progresivamente, reduciendo las diferencias inicialmente observadas entre ambas fuentes de P. Como se muestra en la Figura 1, la disponibilidad de P en el suelo se estabilizó durante los últimos 18 días del experimento, alcanzando niveles comparables tanto para el SFT como para el ácido fosfórico.
La mayor disponibilidad del P en la solución del suelo del H3PO4 y la liberación lenta de P por el SFT, confirma las limitaciones en la disponibilidad de P asociada al manejo tradicional de la fertilización fosfatada. El SFT, generalmente es aplicado antes del establecimiento de los cultivos, como fertilización de fondo, mientras que el H3PO4 se utiliza en sistemas de producción intensiva, en dosis bajas y con alta frecuencia como es la fertirrigación (Chtouki, Naciri y Oukarroum, 2024).
Mengel y Kirkby (2001), establecen que para mantener en la solución del suelo una concentración de P de 0.3 mg L-1, se requieren aplicaciones elevadas de SFT; dicha concentración en caso fue observada después de los 18 días y se mantuvo hasta el final del experimento, tras la aplicación de 847 y 1100 mg kg-1, de P, equivalentes a 2.5 y 3.3 Mg ha-1 de SFT, estos resultados resaltan la necesidad de realizar estudios adicionales sobre el periodo en el que el suelo puede mantener una concentración adecuada de P para nutrir adecuadamente a los cultivos.
Por otra parte, de acuerdo a los modelos de regresión generados (Cuadro 3), la disponibilidad inicial de P en la solución del suelo tras la aplicación de H3PO4, supera la concentración critica de 0.3 mg L-1 desde el momento de la aplicación hasta los 16 días posteriores. Este intervalo sugiere que dicha duración puede ser utilizada para determinar la frecuencia de la aplicación de los fertilizantes en los sistemas intensivos de producción.
Cuadro 3: Modelos de regresión y coeficientes de determinación ajustados al P-Olsen determinado durante el periodo de incubación utilizando el ácido fosfórico.
Table 3: Regression models and coefficients of determination adjusted to the P-Olsen determined during the incubation period using phosphoric acid.
| Dosis de P | Ecuación de regresión | R2 |
| mg L-1 | ||
| 214 | Y = 1.4266 X –0.5415 | 0.97 |
| 275 | Y = 2.6297 X –0.8191 | 0.98 |
| 468 | Y = 4.5696 X –1.0183 | 0.98 |
| 846 | Y = 5.3353 X –1.1147 | 0.93 |
| 1100 | Y = 7.4143 X –1.1881 | 0.97 |
X = dosis de P aplicado.
X = applied P dose.
La alta frecuencia de riego en los sistemas de riego localizado, como el goteo y micro goteo, permiten reducir las dosis de P inyectadas en el sistema. Estudios previos en vertisols indican que una dosis de 40 mg L-1 de P, es suficiente para alcanzar altos rendimientos en papa (Papadopoulos y Stylianou, 1991). Además, dado que el volumen de humedecimiento del suelo con este sistema de riego puede ser hasta 50% del volumen total del suelo, la cantidad de fertilizante se reduce en la misma proporción (Bar-Yosef, 1999). La combinación de ambas fuentes de P es conveniente debido a las diferencias en la liberación del P, ya que el SFT, lo libera de manera más lenta, lo cual es útil para aplicaciones de fondo, y el H3PO4, al tener una rápida disponibilidad es ideal para cubrir las necesidades inmediatas de los cultivos. Lo anterior sugiere que para un manejo adecuado del P en suelos vertisols, con sistemas de riego localizado, se requiere una fertilización inicial con materiales solubles, complementada con aplicaciones frecuentes de H3PO4, para asegurar un suministro constante de P. El presente estudio resalta la importancia de seleccionar las fuentes adecuadas de P y ajustar la frecuencia de aplicación para mantener niveles adecuados de P en la solución del suelo, donde las raíces de la planta absorben este nutrimento. Esto es particularmente relevante en áreas del suelo donde los emisores de riego no logran abastecer suficiente P, además para cultivos con un sistema radical poco desarrollado, la fertilización de fondo en banda permite asegurar una concentración de P adecuado de nutrimentos a las plantas (Bar-Yosef, Sagiv y Markovitch, 1989). Es importante destacar que, independientemente de la fuente y dosis el 94% del P fue adsorbido por el suelo dentro de las primeras 24 h tras su aplicación. En el caso de las dosis más altas como la de 1100 mg de P kg-1 de suelo, esto representó una adsorción equivalente a 3.3 toneladas de SFT en una capa arable de 0.25 m. los resultados muestran que, después de la aplicación del H3PO4, la cantidad de P disponible en la solución del suelo es más del doble que la cuantificada con el SFT (Cuadro 4). Esta diferencia en la disponibilidad sugiere que el H3PO4 es más eficiente en los sistemas de producción intensiva, mientras que el SFT es adecuado para sistemas de fertilización de fondo.
Cuadro 4: Total, de fósforo y porcentaje recuperado, estimado en el estudio de incubación en un suelo Vertisol.
Table 4: Total phosphorus and percentage recovered, estimated in the incubation study in a Vertisol soil.
| Dosis de P | Fuente de fósforo | |||
| H3PO4 | SFT | |||
| mg kg-1 | mg de P | % | mg de P | % |
| 214 | 13.843 | 6.47 | 5.458 | 2.6 |
| 275 | 15.206 | 5.53 | 7.290 | 2.6 |
| 466 | 19.019 | 4.08 | 9.272 | 2.0 |
| 847 | 21.113 | 2.49 | 10.435 | 1.2 |
| 1100 | 23.14 | 2.10 | 11.029 | 1.0 |
| Promedio | 18.46 | 4.14 | 8.70 | 1.88 |
En ambas fuentes de P, el incremento de la dosis aplicada generó un aumento en la concentración de P disponible. Sin embargo, el comportamiento relativo de la disponibilidad de P fue diferente entre ambas fuentes. El H3PO4 mostró una disponibilidad promedio del 4.14% mientras que el SFT tuvo una disponibilidad del 1.88 por ciento.
Conclusiones
La isoterma de Langmuir describió adecuadamente el proceso de adsorción de P en suelos Vertisols. Las fuentes fosfatadas mostraron diferencias en la capacidad de adsorción de P, con valores de 1080 mg kg-1 para el SFT y 1030 mg kg-1 para el H3PO4. Del P aplicado como SFT, 30% se encontró como P unido al Ca y 28% como P soluble, mientras que en el H3PO4 estos porcentajes fueron 40 y 31% respectivamente. El P proveniente del H3PO4 es inmediatamente disponible en concentraciones significativamente más altas que las del SFT. A las 24 horas de su aplicación el 94% del P fue adsorbido por el suelo, independientemente de la fuente o dosis utilizadas. El manejo eficiente del P en Vertisols se logra mediante una combinación de una aplicación inicial de SFT, complementada con aplicaciones frecuentes de H3PO4, lo que optimiza la disponibilidad del P para las plantas.











 nova página do texto(beta)
nova página do texto(beta)