Introducción
En el mundo existen aproximadamente 400 000 000 ha afectadas por la salinidad (FAO, 2005), siendo este incremento el causante principal de la degradación de los suelos en muchas partes del mundo. Teniendo en cuenta esta problemática, la identificación y uso de plantas adaptadas a ambientes salinos, es de importancia para que dichas áreas sigan siendo productivas (Abdelrahman, Burritt y Tran, 2018a; Abdelrahman, Jogaiah, Burritt y Tran, 2018b; Machado y Serralheiro, 2017; Wang, Tang, Wang y Shao, 2015).
Las leguminosas pratenses tienen un importante papel en las áreas dedicadas a la producción de pastos y forraje a nivel global, no solo por su habilidad de fijar el nitrógeno atmosférico (Lange et al., 2015; Maikhuri, Dangwal, Negi y Rawat, 2016), sino además en la recuperación de suelos salinos (Bruning et al., 2015) y en los indicadores químicos del suelo (Rivero-Herrada, Gutiérrez, Granados y Varas, 2020).
El estrés salino afecta el desarrollo normal de las plantas leguminosas (Flexas, Bota, Loreto, Cornic y Sharkey, 2004; Murillo-Amador et al., 2007), provocando desequilibrios nutritivos, los efectos osmóticos y la toxicidad de iones específicos (He et al., 2015; Patil et al., 2016); además reduce la capacidad de germinar y establecer plántulas en tierras salinas, esto es particularmente importante para las leguminosas de pasto anual, que deben repetir este proceso cada año (Nichols, Malik, Stockdale y Colmer, 2009). Por lo que resulta necesario profundizar en la comprensión de los procesos subyacentes que gobiernan la reacción de las leguminosas frente al estrés salino (Manchanda y Garg, 2008).
De acuerdo con Anwandter, Balocchi, López y Pinochet (2004), los pastos exhiben una extraordinaria habilidad para ajustarse a diversos entornos a través de modificaciones en su estructura, tamaño y funciones fisiológicas, un fenómeno conocido como plasticidad fenotípica. Asimismo, generan variantes genéticas denominadas ecotipos, que consisten en grupos de individuos de una misma especie con diferencias heredadas en cuanto a su crecimiento o resistencia ante condiciones ambientales adversas. Esta capacidad les facilita la colonización de una amplia variedad de hábitats.
La plasticidad fenotípica es ampliamente reconocida por su relevancia ecológica y evolutiva en organismos no móviles, como las plantas (Valladares, Martinez, Balaguer, Perez y Manrique, 2000). Esto se debe a que los hábitats de las especies vegetales suelen variar tanto en el tiempo como en el espacio. La habilidad de las plantas para modificar su morfología, en respuesta a estas condiciones ambientales cambiantes, puede verse como un mecanismo adicional que contribuye a su supervivencia y éxito en la reproducción.
La isla de Cuba no está ajena a este fenómeno, cerca de 42% de los suelos usados para la producción de pastos están afectados por la salinidad, lo cual provoca un decremento considerable del rendimiento de los pastos y de la producción animal (López-Sánchez, Eichler, Posada, Campos y Padilla, 2019). Aunque se han realizado estudios acerca del efecto del estrés por sales en algunas leguminosas pratenses en combinación con aislamientos de Rizobium (López-Sánchez, Eichler y Schnug, 2007; López-Sánchez et al., 2019; López-Sánchez, Eichler, Posada, Campos y Padilla, 2020), no se conoce la plasticidad fenotípica de especies de leguminosas pratenses, en ecosistemas tropicales, en respuesta al estrés por sales.
En este contexto, el propósito del presente estudio fue examinar la plasticidad fenotípica y la variación en los rasgos relacionados con la acumulación de biomasa, características histológicas y la acumulación de iones en siete leguminosas forrajeras, durante la fase de establecimiento bajo condiciones controladas en invernadero.
Materiales y Metodos
Se emplearon para el estudio siete especies de leguminosas pratenses: Leucaena leucocephala, Sesbania rostrata, Macroptillium lathyroides, Macroptillium atropurpureum, Clitoria ternatea, Canavalia ensiformis y Centrosema pubescens.
En condiciones semi controladas de invernadero se siguieron dos variantes experimentales: una con suelo normal (C.E -0.35 dS m-1) y otra con suelo fuertemente salino (C.E -10 dS m-1). La sal predominante era el NaCl. En cada maceta crecieron 5 plantas y para cada tratamiento se utilizaron 10 macetas, las cuales se rellenaron con 5 kg de suelo, previamente desinfectado con solución de formaldehído al 10% (formol) y se distribuyeron siguiendo un arreglo aleatorizado. No se inocularon con rizobio las semillas y no se aplicó fertilizantes a las plantas. Los riegos se realizaron sólo cuando se observaron síntomas de estrés hídrico.
A los 70 días, se llevó a cabo la recolección de muestras de plantas para evaluar la frecuencia estomática, grosor histológico de las hojas, así como longitud y ancho de los estomas. Se realizaron impresiones foliares utilizando acetato de celulosa diluido en ácido acético, específicamente de la zona central de la lámina foliar. Para la preparación de cortes histológicos, se utilizó una solución fijadora compuesta por formol, ácido acético y etanol (FAA) al 50%. Posteriormente, se siguió el método de inclusión en parafina, deshidratando los tejidos con una serie ascendente de alcohol butílico terciario y obteniendo cortes transversales de 7 µm de grosor con un micrótomo de deslizamiento horizontal. Para la tinción de los tejidos, se aplicó azul de toluidina a pH de 4.0. Además, se evaluaron características de acumulación de biomasa, como la materia seca de partes aéreas y raíces, así como la acumulación de iones, incluyendo el contenido de nitrógeno de las partes aéreas y, los niveles de sodio y potasio, siguiendo la metodología establecida por AOAC (1975).
Se determinó el Índice de Plasticidad Fenotípica (IPF) para los indicadores evaluados a través de la siguiente ecuación:
En tal sentido Max y Min son las medias de los valores máximos y mínimos de cada parámetro evaluado en cada especie de leguminosa pratense respectivamente (Valladares et al., 2000).
Para el estudio del efecto del estrés salino en las especies de leguminosas estudiadas se realizó prueba de t de Student y para la evaluación de la plasticidad fenotípica los datos recolectados fueron sometidos al análisis de varianza (ANOVA), seguido de la comparación de medias mediante la prueba de rango múltiple de Duncan, utilizando en ambos análisis el software STATISTICA (Tibco, 2020).
Resultados y Discusión
Efecto del estrés salino en las especies de leguminosas pratenses estudiadas
Las leguminosas pratenses mostraron diferencias significativas en todos los caracteres evaluados bajo condiciones de estrés salino. Dado que las plantas crecieron en condiciones semi controladas, estos resultados reflejan una variabilidad con base genética (Cuadro 1).
Cuadro 1: Efecto del estrés salino (S = salino y NS = no salino) en leguminosas pratenses sobre los caracteres materia seca de parte aérea (MSPA); materia seca de la raíz (MSR); largo de los estomas (LE); ancho de las estomas (AE); frecuencia estomática (FE); grosor histológico (GI); contenido de nitrógeno (N); potasio (K) y sodio (Na).
Table 1: Effect of salt stress (S = salt and NS = non-salt) in pasture legumes on characters of aerial part dry matter (MSPA); dry matter of the root (MSR); stomata length (LE); width of stomata (AE); stomatal frequency (FE); histological thickness (GI); nitrogen (N); potassium (K); and sodium content (Na).
| Parámetros evaluados | Niveles de salinidad | S. rostrata | L. leucocephala | M. lathyroides | C. ternatea | C. pubescens | C. ensiformis | M. atropurpureum |
| MSPA | S | 2.18 b | 2.3 b | 1.01 b | 2.56 b | 0.92 b | 1.07 b | 3.18 b |
| NS | 4.53 a | 3.61 a | 3.3 a | 6 a | 4.63 a | 1.83 a | 5.15 a | |
| MSR | S | 1.87 b | 1.97 b | 0.81 b | 2.1 b | 0.45 b | 0.95 b | 2.98 b |
| NS | 4.2 a | 3.42 a | 3 a | 5.4 a | 4.1 a | 1.67 a | 4.84 a | |
| LE | S | 13.4 b | 16 b | 15.6 b | 17.52 b | 14.2 b | 24.3 b | 10.84 b |
| NS | 15.57 a | 17.71 a | 19.2 a | 18.38 a | 16.75 a | 26.67 a | 15.82 a | |
| AE | S | 7 b | 9.82 b | 8.52 b | 8.62 b | 6.38 b | 14.1 b | 9.8 b |
| NS | 8.53 a | 10.67 a | 11.52 a | 9.17 a | 8.64 a | 16.11 a | 11.95 a | |
| FE | S | 215.2 a | 182.14 a | 252.42 a | 158.2 a | 270.82 a | 212.8 a | 334 a |
| NS | 213.1 b | 179.14 b | 247.23 b | 155.1 b | 266.76 b | 208.72 b | 332.15 b | |
| GH | S | 62.61 a | 81.8 a | 57.07 a | 75.73 a | 76.12 a | 83.6 a | 44.48 a |
| NS | 59.82 b | 79.8 b | 52.38 b | 73.7 b | 74.3 b | 80.5 b | 42.2 b | |
| N | S | 67.46 b | 65.23 b | 75.6 b | 64.5 b | 28.6 b | 47.51 b | 86.4 b |
| NS | 120.75 a | 128.46 a | 102.65 a | 171.96 a | 97.5 a | 81.54 a | 123.73 a | |
| K | S | 1.18 b | 1.16 b | 0.57 b | 0.4 b | 0.8 b | 1 b | 0.9 b |
| NS | 1.52 a | 1.52 a | 0.8 a | 0.64 a | 1.1 a | 1.3 a | 1.21 a | |
| Na | S | 2.58 a | 1.6 a | 1.92 a | 0.94 a | 2.92 a | 1.92 a | 2.1 a |
| NS | 2.21 b | 1.32 b | 1.2 b | 0.76 b | 2.45 b | 1.6 b | 1.74 b |
Letras distintas difieren significativamente para P ( 0.05 por la prueba de t de Student.
Letras distintas difieren significativamente para P ( 0.05 por la prueba de t de Student.
Los caracteres relacionados con la acumulación de biomasa (MSPA y MSR) fueron afectados significativamente por el estrés salino en todas las leguminosas estudiadas. En tanto, los indicadores anatómicos evaluados del comportamiento mostraron que el estrés salino provocó una disminución del ancho y largo de los estomas, aumento de la frecuencia estomática y grosor histológico (Cuadro 1). Similares resultados reportan Li, Wan, Zhou, Yang y Qin (2010), Praxedes, De Lacerda, DaMatta, Prisco y Gomes (2010) y Huang et al. (2014) los cuales señalan la reducción de biomasa total, biomasa foliar, biomasa del tallo y biomasa de la raíz son producto del efecto negativo del estrés salino.
El estudio del efecto del estrés por sales en la acumulación de iones muestra reducción significativa del contenido de nitrógeno y potasio e incremento significativo del contenido de sodio en todas las especies estudiadas (Cuadro 1).
Al analizar la acumulación de materia seca y la acumulación de nitrógeno (Cuadro 1) se observó disminución significativa de ambos indicadores en todas las especies estudiadas frente a la presencia del estrés salino. Este comportamiento podría deberse a la influencia del poder inhibitorio de la salinidad en los procesos fisiológicos de las leguminosas, el cual afecta los mecanismos de translocación de asimilatos.
La salinidad causó disminución leve pero significativa en longitud y ancho de los estomas, acompañada de incremento en su frecuencia y en el grosor histológico de las hojas (Cuadro 1). Estos resultados son consistentes con los hallazgos de varios autores en diferentes cultivos (El-Taher et al., 2021; Fonseca, González, López y Zamora, 1999), quienes indican que estas alteraciones en la anatomía foliar, asociadas a la formación de estructuras celulares en las plántulas bajo condiciones salinas, son consecuencia del impacto del estrés salino en el crecimiento celular.
El aumento en la frecuencia estomática podría ser resultado de la reducción en el tamaño de los estomas o de disminución en el área foliar de las plántulas sometidas a estrés salino (Fonseca et al., 1999). Por otro lado, el incremento en el grosor histológico de las hojas ha sido vinculado, por algunos autores, a la elongación del parénquima en empalizada, que se produce debido a los cambios asociados con la acumulación de iones tóxicos que afectan las relaciones hidro osmóticas de las células.
Disminución moderada en la apertura de los estomas bajo estas circunstancias podría ser benéfica para mitigar la pérdida excesiva de agua a través de la transpiración, sin comprometer la capacidad fotosintética, y en consecuencia, favorecer una mayor acumulación de biomasa (Mirza y Tariq, 1993; Botti, Palzkill, Muñoz y Prat, 1998).
En todas las especies el contenido de sodio se incrementó, mientras que el de potasio disminuyó (Cuadro 1). El antagonismo observado entre el sodio y el potasio ha sido descrito por varios autores (Yamanouchi, Tanaka y Fujiyama, 1997) quienes lo asocian a la competencia por un mismo sitio de acumulación en las células vegetales, lo cual puede ser una de las causas que afectan el crecimiento y desarrollo de las plantas bajo estas condiciones. El estrés salino impacta diversos aspectos del metabolismo de las plantas, lo que lleva a reducción en su crecimiento. Además, la fotosíntesis se ve comprometida debido a la afectación en la tasa de expansión foliar, área foliar y duración de las hojas. Esta disminución en el crecimiento asociado a la salinidad también se debe a que la energía se desvía del crecimiento hacia el mantenimiento de la planta (Manchanda y Garg, 2008).
Plasticidad fenotípica para el estrés salino en las leguminosas pratenses estudiadas
El análisis del Índice de Plasticidad Fenotípica arrojó que todas las leguminosas pratenses mostraron diferencias significativas calculadas a partir de los caracteres evaluados en los dos ambientes estudiados (Cuadro 2).
Cuadro 2: Índice de plasticidad fenotípica frente al estrés salino de siete especies de leguminosas pratenses, en los caracteres materia seca de parte aérea (MSPA); materia seca de la raíz (MSR); largo de las estomas (LE); ancho de las estomas (AE); frecuencia estomática (FE); grosor histológico (GI); contenido de nitrógeno (N); potasio (K) y sodio (Na).
Table 2: Phenotypic Plasticity Index in response to saline stress in seven species of grassland legumes in the characters: aerial part dry matter (MSPA); root dry matter (MSR); stomata length (LE); stomata width (AE); stomatal frequency (FE); histological thickness (GI); nitrogen (N); potassium (K); and sodium content (Na).
| Caracteres evaluados | S. rostrata | L. leucocephala | M. lathyroides | C. ternatea | C. pubescens | C. ensiformis | M. atropurpureum | |
| Acumulación de biomasa | MSPA | 0.51 c | 0.36 d | 0.69 b | 0.57 bc | 0.80 a | 0.41 d | 0.38 d |
| MSR | 0.55 c | 0.42 d | 0.73 b | 0.61 c | 0.89a | 0.43 d | 0.38 de | |
| Media | 0.53 d | 0.39 f | 0.71 b | 0.59 c | 0.84 a | 0.42 e | 0.38 f | |
| Histológicos | LE | 0.13 c | 0.09 d | 0.18 b | 0.04 e | 0.15 c | 0.08 d | 0.31 a |
| AE | 0.17 b | 0.07 d | 0.26 a | 0.05 d | 0.26 a | 0.12 c | 0.17 b | |
| FE | 0.009 c | 0.01 b | 0.02 b | 0.01 b | 0.01 b | 0.01 b | 0.05 a | |
| GH | 0.04 bc | 0.02 c | 0.08 a | 0.02 c | 0.02 c | 0.03 c | 0.05 b | |
| Media | 0.08 b | 0.04 bc | 0.13 a | 0.03 c | 0.11 a | 0.06 b | 0.14 a | |
| Acumulación de iones | N | 0.44 c | 0.49 c | 0.26 e | 0.62 b | 0.70 a | 0.41 c | 0.30 d |
| K | 0.22 c | 0.23 c | 0.28 b | 0.37 a | 0.27 b | 0.23 c | 0.25 bc | |
| Na | 0.18 b | 0.17 b | 0.37 a | 0.19 b | 0.16 b | 0.16 b | 0.17b | |
| Media | 0.28 b | 0.29 b | 0.30 b | 0.39 a | 0.37 a | 0.26 bc | 0.24 c |
Letras distintas difieren significativamente para P ≤ 0.05 por la prueba de Rangos Múltiples de Duncan.
Different letters differ significantly at P ≤ 0.05 according to Duncan's Multiple Range Test.
Las especies C. pubescens, M. lathyroides, C. ternatea, C. ensiformis y C. ternatea mostraron valores medios superiores a 0.40 para los caracteres relacionados con la acumulación de biomasa, las especies M. atropurpureum y L. leucocephala aunque presentan plasticidad, fueron las especies que mostraron los valores inferiores.
Por otra parte, para el total de los caracteres histológicos evaluados en todas las leguminosas tuvieron valores muy bajos de Plasticidad Fenotípica, aunque con diferencias significativas entre ellas. Aunque estas especies mostraron disminución del largo y ancho de los estomas y aumento de frecuencia estomática y grosor histológico; el cálculo de la plasticidad fenotípica denota que existe estabilidad de estos caracteres frente a estrés salino, por lo que pudiera no constituir parte de los mecanismos que emplean para lograr tolerancia al estrés por salinidad. Al respecto Abbruzzese et al. (2009) reportan que genotipos tolerantes a la salinidad de Popolus alba L. no mostraron afectaciones en la densidad estomática y en el índice de área de poros estomáticos para altos niveles de salinidad y concluyen que las afectaciones que incurren en las células, producto al estrés salino no está claro y que este comportamiento pudiera ser el resultado de la complicada interacción entre los componentes estomáticos de las plantas.
Para los caracteres de acumulación de iones, aunque la media de todos los indicadores denota valores medios de plasticidad, es necesario destacar los altos valores de plasticidad fenotípica encontrados para la acumulación de nitrógeno para las especies C. pubescens, C. ternatea, L. leucocephala, S. rostrata y C. ensiformis con valores más altos y significativamente mayores al resto de las otras especies estudiadas. Resulta interesante que las dos especies estudiadas del género Macroptillium presentan valores bajos para este indicador tan sensible a la presencia del estrés salino. Los caracteres acumulación de sodio y potasio, aunque mostraron diferencias significativas entre especies de leguminosas fueron los menos plásticos.
Al evaluar la plasticidad fenotípica, a partir de la media de todas las especies, para cada carácter en específico frente al factor estrés salino, los resultados arrojaron que los caracteres relacionados con la acumulación de biomasa y contenido de nitrógeno, fueron los que presentaron valores por encima de 0.4 y con diferencias significativa entre ellos y el resto de los caracteres evaluados, es decir, que fueron los caracteres más variables. Los caracteres histológicos y la acumulación de potasio y sodio mostraron los valores significativamente menores en cuanto a este indicador, siendo los caracteres que menos variaron frente a la presencia del estrés salino (Figura 1). Los resultados obtenidos referentes a los caracteres histológicos coinciden con los reportes de Alvarez (20061) en clones de la especie Populus spp. al considerar que la magnitud de la plasticidad anatómica fue menor que la plasticidad en la asignación de materia seca. Por otra parte, aunque las especies estudiadas son reportadas en el rango de especies medianamente tolerantes a la salinidad (Subbarao y Johansen, 1993; Mahmood, 1998; Mandal et al., 1998), presentan diferencias en las estrategias de aclimatación al estrés salino.
Figura 1: Índice de Plasticidad fenotípica promedio para todas las leguminosas pratenses estudiadas frente al factor estrés salino en los caracteres materia seca de parte aérea (MSPA), materia seca de la raíz (MSR), largo de los estomas (LE), ancho de las estomas (AE), frecuencia estomática (FE), grosor histológico (GI), contenido de nitrógeno (N), potasio (K) y sodio (Na). Literales diferentes difieren significativamente para P ≤ 0.05 por la prueba de Rangos Múltiples de Duncan.
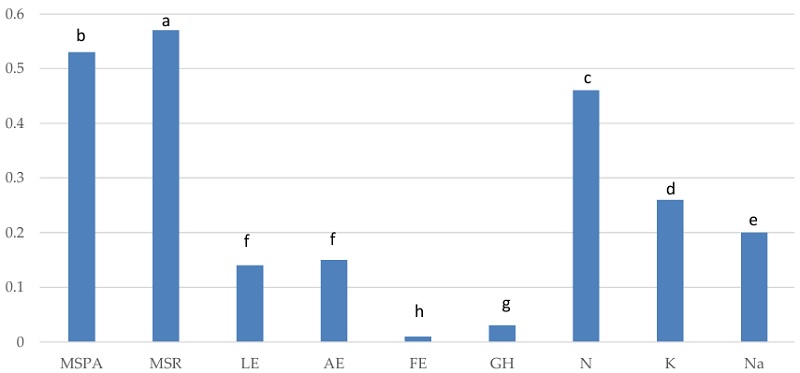
Figure 1: Average phenotypic Plasticity Index for all grassland legumes studied against the saline stress factor in the traits: aerial part dry matter (MSPA); root dry matter (MSR); stomatal length (LE); stomatal width (AE); stomatal frequency (FE); histological thickness (GI); nitrogen (N); potassium (K); and sodium (Na) content. Different literals differ significantly for P ≤ 0.05 by Duncan's Multiple Range test.
Aspinwall et al. (2015) subrayan la relevancia de la variabilidad en la plasticidad fenotípica para identificar genotipos que puedan incrementar o mantener su rendimiento en condiciones climáticas adversas o cambiantes. En la presente investigación, las especies S. rostrata, L. leucocephala, C. ternatea, C. pubescens y C. ensiformis demostraron adaptación notable al estrés salino, exhibiendo mayor plasticidad tanto en la biomasa aérea como en la radicular, así como en la acumulación de nitrógeno. En contraste, las especies M. lathytoires y M. atropurpureum mostraron comportamiento similar, aunque con diferencias en la acumulación de nitrógeno, que parece ser un rasgo más estable en relación con la fotosíntesis frente al estrés salino. Además, los caracteres histológicos y acumulación de sodio y potasio en los tejidos vegetales se mantuvieron bastante estables bajo condiciones de estrés salino en todas las especies analizadas.
Zunzunegui et al. (2009) reportan alta capacidad de aclimatación a entornos adversos está vinculada con alta plasticidad fisiológica, la base de este comportamiento es que, bajo diferentes condiciones de estrés abiótico, las plantas han creado muchas variantes de defensa que ayudan a la planta a mantener las funciones normales de la planta por adaptación y ajuste en procesos fisiológicos y bioquímicos (Hussain y Reigosa, 2011; Hussain et al., 2015; Hussain, Lyra, Farooq, Nikoloudakis y Khalid, 2016).
De acuerdo a los resultados, mantener la estabilidad en la exclusión de iones sodio de los tejido vegetales en ambientes normales y bajo estrés salino, pudiera ser una de las vías fundamentales que emplean estas especies para contrarrestar el estrés salino; esto coincide con lo reportados por Pirasteh-Anosheh, Ranjbar, Pakniyat y Emam (2016) al describir los diversos mecanismos que utilizan las plantas para la tolerancia a la salinidad, señalando que las plantas con tolerancia a la salinidad mostraron evidencias de exclusión de sodio e incluye a cultivos como el trigo, cebada, maíz, garbanzo, frijoles, así como algunas halófitas.
Según Valladares et al. (2000), para comprender cómo las plantas reaccionan a cambios en su entorno, es esencial analizar en profundidad las diversas características fenotípicas en la mayor cantidad de componentes posible. Dado que el presente experimento tuvo duración de solo 70 días, se considera fundamental investigar el comportamiento de estas especies de leguminosas durante un período más prolongado bajo estrés salino. Esto permitiría determinar si hay plasticidad fenotípica en otros rasgos estudiados e incorporar aquellos relacionados con la fotosíntesis, lo que facilitaría una evaluación más completa del desempeño de estas especies frente al estrés salino.
Conclusiones
Las especies S. rostrata, L. leucocephala, C. ternatea, C. pubescens y C. ensiformis mostraron frente al estrés salino el mayor índice de plasticidad fenotípica en materia seca de la parte aérea y de la raíz y la acumulación de nitrógeno resultaron ser los de mayor Índice de plasticidad fenotípica en presencia del estrés salino.
La estabilidad mostrada en la acumulación de sodio en todas las leguminosas sugiere que estas especies utilicen la exclusión de iones de sodio para tolerar el estrés salino.
Disponibilidad de Datos
Los conjuntos de datos generados o analizados durante el estudio actual no están disponibles públicamente debido [a regulaciones institucionales] pero están disponibles del autor correspondiente a solicitud razonable.
Contribución de los Autores
Conceptualización: R.C.L.S. y B.E.L. Metodología: R.C.L.S. y Y.V.E. Software: R.C.P. Validación: B.E.L., R.C.P. y G.C.P. Análisis formal: R.C.L.S. y L.R.L. Investigación: R.C.L.S. Recursos: R.C.L.S. Escritura, preparación del borrador original: R.C.L.S., B.E.L y L.R.L. Escritura: revisión y edición: R.C.L.S. y L.R.L.











 nova página do texto(beta)
nova página do texto(beta)



