Introducción
En la actualidad, uno de los cultivos con más importancia en la agricultura es el banano (Musa spp.), ocupa el segundo lugar en producción dentro de las frutas tropicales en México, tan solo en Michoacán en el 2023 se sembraron 5,803 ha con producción de 177,760.46 t y un rendimiento de 31.64 t ha -1 (SIAP, 2024). El banano tiene un elevado valor nutritivo en carbohidratos, fibra, proteína, minerales y vitaminas, por ello, es considerado como una de las frutas básicas en la alimentación humana (Fernández et al., 2021).
El cultivar cv. Gran enano tiene más de 30 años de presencia en la frontera entre los estados de Michoacán y Colima (Álvarez et al., 2011), este es afectado por diversas enfermedades, la más importante es Sigatoka negra (SN) causada por el hongo Mycosphaerella fijiensis (anamorfo = Pseudocercospora fijiensis, Cruz et al., 2020). P. fijiensis se multiplica y se dispersa mediante ascosporas y conidios, como inóculo inicial (Churchill, 2011); presenta los dos estados de reproducción sexual y asexual; en el caso de la fase asexual se caracteriza por desarrollar las primeras lesiones, presentándose estrías en el envés ocasionadas por esporas asexuales (conidiosporas), mientras que el estado sexual posee ascosporas que se encuentran en las ascas; estas se producen en el interior de los pseudotecios, los cuales se manifiestan en las hojas infectadas como puntos negros o manchas cenizadas en la etapa final de la enfermedad (Muimba, 2018). Las hojas con síntomas de SN manifiestan un retraso en el proceso de la fotosíntesis, provocando pérdidas económicas del 33 hasta un 69 % en la producción (Kablan et al., 2012).
El control químico con fungicidas es la estrategia de control más frecuentada
por los productores de banano, especialmente, en México, el Mancozeb (etilenbisditiocarbamato) es el fungicida más utilizado para el control de la SN (Mena y Couoh, 2015), debido a su espectro biológico y bajo costo. Sin embargo, se ha evidenciado que la etilentiourea, un metabolito que se forma al disociarse el en el agua en presencia de oxígeno y que posee alta movilidad en suelos, debido a su elevada solubilidad en agua, es la responsable de su toxicidad a largo plazo en humanos y en el ambiente (Alza et al., 2016). Por esta razón, el control biológico de la SN es una opción viable por su convivencia amigable con el ambiente. El género Trichoderma posee un amplio rango de control sobre fitopatógenos (Kumar et al., 2023), debido a sus mecanismos como la competencia, antibiosis, parasitismo y endofitisimo (Saeed, 2022), estas cualidades hacen que Trichoderma sea una opción para el control de agentes fitopatógenos, cualidad que no poseen los fungicidas químicos (Acosta et al., 2013).
También, Trichoderma spp. posee ventajas para su producción masiva, puesto que se puede producir a través de fermentación líquida, sólida y bifásica. La fermentación en estado sólido (FES) para la producción de conidiosporas de Trichoderma spp. se realiza en granos, cereales o con residuos agroindustriales (López et al., 2022). Los granos de arroz entero y quebrado han sido uno de los sustratos más empleados; sin embargo, resulta costoso por su alto valor económico si se compara con el maíz (Rini et al., 2018; Hernández et al., 2019).
Por otra parte, en el control biológico in vitro de P. fijiensis se han empleado bacterias (Chávez et al., 2020) y actinobacterias (Moreno et al., 2016), una de ellas es Streptomyces galilaeus, la cual es efectiva para inhibir el crecimiento in vitro de P. fijiensis (Castillo et al., 2007; Moreno et al., 2016). Sin embargo, estudios in situ para la evaluación de Streptomyces contra la epidemiología de la SN no se han realizado. Por lo tanto, el objetivo fue evaluar el rendimiento de cepas de Trichoderma spp. producidas en sustratos sólidos y determinar la epidemiología de la SN a través de aplicaciones de conidiosporas de Trichoderma sp. y Streptomyces sp. (Blitefree®) en el cultivo de banano cv. Gran enano.
Materiales y Métodos
Producción masiva de conidiosporas de Trichoderma spp.
Aislamiento e identificación de cepas de Trichoderma spp. Las cepas se aislaron de suelo rizosférico de plantas de banano (Musa spp.), ubicadas en un huerto orgánico en Tecomán, Colima, México (18°50’16.8” N, 103°50’06.4” O) con antecedentes de no aplicación de productos biológicos a base de Trichoderma. El muestreo se realizó en cuatro hectáreas en un rancho de 40 ha, las muestras se colectaron entre 15 a 20 cm de profundidad, se preparó una muestra compuesta (2 kg) por ha, a partir de cinco submuestras (0.4 kg), el suelo se depositó en bolsas ziplock y se transportó y conservó en nevera y refrigerador (5 °C) para su procesamiento antes de las 24 h después del muestreo. El aislamiento se realizó mediante el lavado de las partículas de suelo, que consistió en lavar 1 g de suelo con 3 L de agua destilada estéril utilizando tres tamices (Alcon®, México) de tamaño de malla decreciente, uno sobre otro, de 500, 250 y 150 μm, respectivamente. Las partículas lavadas (150 μm) se depositaron en discos de papel filtro estéril durante 5 h para eliminar el exceso de humedad. Diez partículas se sembraron en agar papa dextrosa (PDA) + cloranfenicol (150 ppm, SigmaAldrich®, EUA) (Bills et al., 2004). Se incubaron cinco placas de Petri a 25±3 °C, 75±5 % de humedad relativa (HR) y 12 h luz: oscuridad. Las colonias con características distintivas al género Trichoderma se purificaron mediante reaislamiento en PDA.
Los aislamientos de Trichoderma spp. fueron identificados a nivel género con las claves taxonómicas propuestas por Rifai (1969), Barnett y Hunter (1972) y Bissett et al. (2015). Las principales características morfológicas macroscópicas tomadas en cuenta fueron: color de micelio, textura de micelio y formación de anillos concéntricos. Mientras que las características microscópicas determinadas bajo un microscopio invertido (Axio vert A1, Zeiss®, Alemania) fueron: forma de conidios, fiálides y presencia de clamidosporas. Los aislamientos se depositaron en el cepario de la Facultad de Ciencias Biológicas y Agropecuarias de la Universidad de Colima. Para los experimentos se seleccionaron cuatro cepas nativas de Trichoderma spp. (T-82, T-85, T-94 y T-99), las cuales fueron mantenidos en tubos con PDA inclinado (25±3 °C, 75±5 % HR y 12 h luz: oscuridad), se emplearon colonias en los tubos de 10 días de edad para la producción masiva de conidiosporas en fermentación en estado sólido (FES).
Preparación del inóculo. Se utilizaron dos tubos inclinados con colonias de 10 días de edad por cada cepa de Trichoderma spp. para preparar 500 mL de suspensión de esporas por cepa. A cada tubo se le adición 10 mL de agua destilada estéril con Tween 80 (0.05%), la superficie de la colonia se raspó con un asa bacteriológica estéril y se transfirió a un matraz con 480 mL de agua destilada estéril con Tween 80 (0.05%), se emplearon dos tubos con colonias de Trichoderma por cada cepa, cuando la suspensión no alcanzó los 500 mL se aforó con agua destilada estéril. La concentración de la suspensión de esporas se cuantificó en cámara de Neubauer por cuatriplicado y se ajustó a 1.0×107 conidiosporas mL -1.
Preparación de los sustratos para la FES. Para el experimento en FES se estudiaron dos sustratos: arroz entero (AE) y maíz amarillo quebrado (MQ). El AE se lavó con agua potable tres veces hasta remover el polvo; posteriormente, se colocó en charolas para su secado al sol hasta obtener menos de 15 % de humedad. Después, el AE secó, se embolsaron 120 g en bolsas de polietileno de alta densidad de 2 kg y se esterilizaron en la autoclave a 120 °C (1.5 psi), durante 20 minutos. Cada bolsa fue inoculada con 5 mL de inóculo (1.2×107 conidiósporas mL -1), posteriormente se incubó durante 18 días a 24.7-29.6 °C con 12 horas luz: oscuridad.
Los granos de maíz amarillo se quebraron en un molino de grano seco (Molino del Rey 0.5 HP, México), después se tamizó para eliminar el polvo. Los granos quebrados se lavaron en cuatro ocasiones, la primera se realizó con agua potable, retirando la cáscara de maíz y granos vanos; en la segunda, se lavó con una solución de Fullgrow® (Agroscience, México) 1.5 mL L -1 de agua; en la tercera, se lavó con agua caliente (80 ºC) durante 10 min y, por último, se le añadió agua a temperatura ambiente como enjuague. Después el MQ se secó hasta obtener una humedad menor al 15%. El MQ se embolsó (120 g) en bolsas de polietileno de alta densidad de 2 kg y se esterilizó como se describió anteriormente. Cada bolsa fue inoculada con 5 mL de la suspensión de conidiosporas (1.2x107 conidiósporas mL -1), posteriormente se incubó (24.7-29.6 °C, 75±5 % HR y 12 horas luz: oscuridad) durante 18 días. La incubación consistió en 12 días para la colonización del sustrato, crecimiento micelial y esporulación, en los seis días restantes, las bolsas se abrieron en el cuarto de incubación y se les colocó un deshumificador (Delonghi®, USA) por 8 horas al día, con el fin de eliminar la humedad del sustrato.
Variable respuesta. El rendimiento se determinó (conidiosporas g -1 de sustrato colonizado) a los 18 días después de la inoculación e incubación de los sustratos. Se tomaron 4 g de sustrato colonizado (MQ o AE) y se depositaron en 36 mL de agua destilada estéril + Tween 80 0.05% en tubo cónico (50 mL). La mezcla se agitó en vórtex durante 1 min. La concentración de conidiosporas se contabilizó en una cámara de Neubauer en microscopio (Axio vert A1, Zeiss®, Alemania) a 40×. Se emplearon diluciones seriadas para cuando las esporas sobrepasaban las 250 conidiosporas por campo de conteo en la cámara de Neubauer.
Diseño experimental y análisis de datos. Se empleó un diseño completamente al azar con arreglo factorial A×B. El factor A consistió en la cepa de Trichoderma spp. (T-82, T-85, T-94 y T-99) y el factor B el sustrato (MQ y AE), resultaron ocho tratamientos (interacciones), cada uno con 10 repeticiones. Una repetición constó de una bolsa de 2 kg con 120 g de sustrato inoculado. Los datos se analizaron a través de un análisis de varianza bifactorial con una probabilidad del 95% (α=0.05). Posteriormente, se realizó una comparación de rango múltiple empleando la prueba de Tukey (α=0.05). Los análisis se realizaron con Statgraphics Plus® para Windows®.
Epidemiología de la Sigatoka negra en campo
Sitio experimental. El estudio se realizó de enero a abril del 2019 en un huerto de banano cv. Gran enano de 30 años (18°67´57.73” N y 103°67´12.89” O, Google Earth, 2018), en Coahuayana de Hidalgo, municipio de Coahuayana, Michoacán, con superficie de dos hectáreas y densidad de 1900 planta ha -1, con tipo de suelo fluvisol (INEGI, 2025) a una altura de 30 msnm. El clima predominante en la región es cálido subhúmedo A(w) con temperatura promedio de 26-30 °C y una precipitación de 1558 mm anuales.
Establecimiento del experimento in situ. El experimento consistió en cuatro tratamientos, dos cepas de Trichoderma spp. (T84 y T94), seleccionadas por haber sido las cepas con mayor producción de conidiosporas en el experimento en FES, además, de un producto biorracional Blitefree® (extracto de Streptomyces sp. De Altus Biopharm S. A. de C. V., dosis 1.5 L ha -1) y un químico (Mancozeb®, dosis 2 kg ha -1), ambos adquiridos en Proveedora Agrícola de Tecomán, Colima. En el experimento in situ, se utilizaron bloques (500 m2) al azar de 20 m de ancho por 25 m de largo; las aplicaciones de los tratamientos se realizaron cada semana durante tres meses y se tomaron datos de muestreo cada semana después de la primera aplicación. La parcela experimental presentaba presencia de SN con pequeñas lesiones o puntos de color blanco-amarillento a marrón, de 1 mm de longitud, denominadas pizcas, apenas visibles en el envés de las hojas (Torrado y Zapata, 2008).
Aplicación de los tratamientos. La aplicación de los tratamientos se realizó con un aspersor de motor con capacidad de 15 L marca STIHL® (México). Para el caso de Trichoderma sp. y Blitefree® se empleó aceite de soya (1 mL L -1) como adherente natural; para el Mancozeb se utilizó Innex® (1 mL L -1) como adherente, con un gasto para cada tratamiento y control químico de 100 L ha -1. La dosis del Blitefree® y Mancozeb fue de 2.5 g y 2.5 mL L -1, respectivamente. Para las aplicaciones de las cepas de Trichoderma spp. en campo se empleó una concentración de 1×107 conidiosporas mL -1 (2×1012 conidiosporas ha -1). Las aplicaciones de los tratamientos se realizaron semanalmente en horario de 16:00 a 20:00 horas en invierno (enero, 2018) - primavera (abril, 2019).
Variables de respuesta epidemiológicas
La severidad de la SN. Se evaluó en intervalos de siete días en todas las hojas de las plantas seleccionadas. Se utilizó la escala de Stover (1970) de seis categorías, donde: 1) hojas sin síntomas de la enfermedad y aquellas con hasta 10 manchas; 2) hojas con área foliar lesionada <5%; 3) hojas con 6-15% de área foliar lesionada;
4) hojas con 16-33% de área foliar lesionado; 5) hojas con 34-50% de área foliar lesionada y 6) hojas con un área foliar lesionada >50%.
Promedio ponderado de infección (PPI). Se evaluó dividiendo la hoja en dos partes iguales. La hoja que presentó la mitad del limbo foliar lesionado recibió la nota 5 (34-50%) y si presentó lesiones en la otra mitad de la hoja, recibió la nota 6 (>50%). Para obtener las notas 3 y 4, se dividió cada una de las mitades del limbo foliar en dos partes iguales, es decir ¼ de la hoja. Si la hoja presentó hasta la mitad de ¼ de limbo foliar lesionado recibió la nota 3 (6-15%) y si la hoja presentó más de ¼, de limbo foliar lesionado asumió la nota 4 (16-33%). Para la obtención de la nota 2 se dividió ¼ del limbo foliar en dos partes iguales. Si la hoja presentó hasta la mitad de ¼ del limbo foliar lesionado tomó la nota 2 (<5%). La nota 1 se asignó cuando la hoja presente hasta 10 manchas. Este procedimiento se repitió en cada una de las unidades experimentales (Martins et al., 2007). El PPI se calculó con la formula PPI = (suma de % hojas en cada grado × grado respectivo) /100.
Área bajo la curva del progreso de la enfermedad (ABCPE). Es un resumen cuantitativo útil de la intensidad de la enfermedad en el tiempo, ubicaciones o estrategias de manejo. El ABCPE en cada tratamiento se calculó utilizando la ecuación descrita por Shaner y Finney (1977).
Donde: Yi: intensidad de la enfermedad y t: periodo de evaluación en días.
Diseño experimental y análisis de datos. El experimento se estableció con un diseño de bloques al azar con cuatro tratamientos y tres repeticiones, dos tratamientos con cepas de Trichoderma spp. (T-94 y T-85), Blitefree® y el control químico (Mancozeb) como testigo. Los datos de la severidad, PPI y ABCPE se analizaron mediante un análisis de varianza y una prueba de Tukey (α = 0.05). Los análisis se realizaron con el software StatGraphics Plus para Windows®.
Resultados
Rendimiento de cepas de Trichoderma spp. en fermentación sólida. Trichoderma T-94 (1.41×108 conidiosporas g -1) significativamente (p=0.0050) produjo más conidiosporas que Trichoderma T-99 (7.13×107conidiosporas g -1) y T-82 (8.25×107 conidiosporas g -1), pero estadísticamente produjo la misma cantidad de conidiosporas que Trichoderma T-85 (1.20×108 conidiosporas g -1) (Cuadro 1). El MQ fue el mejor sustrato (p=0.0060) para las cepas de Trichoderma spp. (Cuadro 1), produjo 71% más conidiosporas (1.31×108 conidiosporas g -1) que el AE (7.66×107 conidiosporas g -1). Las interacciones Trichoderma T-94 - Maíz (1.55×108 conidiosporas g -1) y Trichoderma T-85 - Maíz (1.49×108 conidiosporas g -1) presentaron mayor esporulación (p=0.0015) comparado con las interacciones Trichoderma T-99 - Arroz (4.17×107 conidiosporas g -1) y Trichoderma T-82 - Arroz (4.57×107 conidiosporas g -1); sin embargo, resultaron estadísticamente iguales al resto de las interacciones (Cuadro 1).
Epidemiología de la sigatoka negra en campo
Severidad. En los muestreos a 7 (p=0.587), 14 (p=0.150) y 21 (p=0.440) días no existieron diferencias significativas entre los tratamientos. A los 28 días, con Blitefree® se presentó mayor severidad (1.43) (p=0.026), mientras que con las cepas de Trichoderma T-85 y Trichoderma T-94 la severidad fue de 1.10 y 1.12, respectivamente. En el muestreo a 35 (F=5.89, P=0.0014) días, Blitefree® y Mancozeb® permitieron las severidades mayores con 1.45 y 1.39, respectivamente; mientras que las cepas T-85 y T-94 mostraron los valores menores con 1.03 y 1.28, respectivamente (Cuadro 2). En los muestreos a 42 (F=8.68, p =0.0001), 49 (F=16.55, p=0.00001) y 56 (F=15.31, p=0.00001) días, Mancozeb obtuvo la mayor severidad con valores de 1.48, 1.61 y 1.58, respectivamente, mientras que Trichoderma T-85 obtuvo los menores valores de severidad con 1.09, 0.87 y 0.93, respectivamente (Cuadro 2).
Cuadro 1 Rendimiento de cepas de Trichoderma spp. en sustratos sólidos
| Factor | Esporulación |
|---|---|
| Cepa | Conidiosporas/g colonizado |
| Trichoderma T-85 | 1.20×108 ± 1.7×107 ab |
| Trichoderma T-94 | 1.41×108 ± 2.2×107 a |
| Trichoderma T-99 | 7.13×107 ± 1.2×107 b |
| TrichodermaT-82 | 8.25×107 ± 1.3×107 b |
| Sustrato | Conidiosporas /g colonizado |
| Arroz entero | 7.66×107 ± 1.0×107 b |
| Maíz quebrado | 1.31×108 ± 1.3×107 a |
| Interacción | Conidiosporas /g colonizado |
| Trichoderma T-85 - Arroz | 9.20×107 ± 1.9×107 ab |
| Trichoderma T-85 - Maíz | 1.49×108 ± 2.4×107 a |
| Trichoderma T-94 - Arroz | 1.32×108 ± 1.6×107 ab |
| Trichoderma T-94 - Maíz | 1.55×108 ± 4.1×107 a |
| Trichoderma T-99 - Arroz | 4.17×107 ± 5.3×106 b |
| Trichoderma T-99 - Maíz | 1.02×108 ± 1.1×107 ab |
| Trichoderma T-82 - Arroz | 4.57×107 ± 3.1×106 b |
| Trichoderma T-82 - Maíz | 1.20×108 ± 1.1×107 ab |
| Significancia | p-valor |
| Cepas | ** |
| Sustrato | ** |
| Interacciones | ** |
Medias (± error estándar) entre filas con diferente letra son significativamente diferentes
entre sí, de acuerdo con la prueba múltiple de rango Tukey p=0.05.
Trichoderma sp. T-94 en el monitoreo a los 63 días después de la aplicación (dda) (F=3.36, p=0.0248) obtuvo el mayor promedio de severidad con 1.58, Blitefree® (1.53) y Mancozeb (1.54) mostraron mayor severidad comparado con Trichoderma T-85 (1.31). En los muestreos a 70 (F=5.01, p=0.0038), 77 (F=4.97, p=0.0040) y 84 (F=4.69, p=0.0054) días, Trichoderma sp. T-85 permitió registrar la menor severidad en comparación con los otros tratamientos; por el contrario, Blitefree® y Trichoderma T-94 que permitieron los valores más altos de severidad en esos muestreos (Cuadro 2).
Cuadro 2 Severidad de la Sigatoka negra en banano cv. Gran enano a través de aplicaciones de Trichoderma spp.
| Tratamiento | Días de muestreo | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 7 | 14 | 21 | 28 | 35 | 42 | 49 | 56 | 63 | 70 | 77 | 84 | |
| Trichoderma T-94 | 0.93 | 1.03 | 1.02 | 1.12 b | 1.28 b | 1.24 c | 1.37 b | 1.23 c | 1.58 a | 1.80 a | 1.72 a | 1.70 a |
| Trichoderma T-85 | 1.10 | 1.15 | 1.18 | 1.10 c | 1.03 c | 1.09 d | 0.87 d | 0.93 d | 1.31 c | 1.39 c | 1.34 c | 1.35 c |
| Blitefree® | 1.12 | 1.26 | 1.18 | 1.43 a | 1.45 a | 1.45 b | 1.32 c | 1.45 b | 1.53 b | 1.72 a | 1.74 a | 1.72 a |
| Mancozeb | 0.98 | 1.01 | 1.17 | 1.23 b | 1.39 a | 1.48 a | 1.61 a | 1.58 a | 1.54 b | 1.60 b | 1.44 b | 1.53 b |
| p= | ns | ns | ns | * | ** | ** | ** | ** | * | ** | ** | ** |
Medias entre filas con diferente letra son significativamente diferentes entre sí (Tukey, p=0.05). ns=no significativo, *=significativo, **= altamente significativo.
Promedio ponderado de infección (PPI). El Cuadro 3 describe los PPI. En los muestreos a 35 y 42 días, Blitefree® y Mancozeb presentaron el mayor PPI (F=6.08, p=0.0185, F=5.40, p=0.0252) con valores de 0.65 y 0.62, respectivamente, por el contrario, Trichoderma T-85 presentó los valores de PPI más bajos con 0.45 (35 días) y 0.49 (42 días). En los dos subsecuentes muestreos a los 49 (0.38) y 56 (0.37) días, Trichoderma T-85 presentó los menores PPI comparado con los otros tratamientos Blitefree y Mancozeb con valores que oscilaron entre 0.53 y 0.60. Para el resto de los muestreos (63, 70, 77 y 84 días) no se encontraron diferencias significativas (p>0.05, Cuadro 3).
Área bajo la curva del progreso de la enfermedad. La Figura 1 presenta la suma general del ABCPE de la Sigatoka negra en banano cv. Gran enano, durante los 12 muestreos (84 días). Trichoderma T-85 estadísticamente (F=153.01, p=0.0001) obtuvo la menor ABCPE con 11.76, en comparación con los otros tratamientos, los cuales presentaron valores de 13.32 (Blitefree®), 13.03 (Mancozeb®) y 20.49 (Trichoderma T-94). La Figura 2 reafirma los resultados; se puede observar que Trichoderma T85. a partir del quinto muestreo (35 días), presentó el menor ABCPE, muy por debajo del tratamiento químico. El tratamiento de Trichoderma sp. T-94 obtuvo la mayor ABCPE distinguiéndose desde el primer monitoreo (7 días) ante los demás tratamientos. Mancozeb® presentó valores más bajos de ABCPE (F=153.01, P=0.0001) comparado con Blitefree® en los muestreos a 14, 28, 49 y 77 días.
Cuadro 3 Promedio ponderado de infección (PPI) de la Sigatoka negra en banano cv. Gran enano a través de aplicaciones de
| Tratamiento | Días de muestreo | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 7 | 14 | 21 | 28 | 35 | 42 | 49 | 56 | 63 | 70 | 77 | 84 | |
| TrichodermaT-94 | 0.49 | 0.53 | 0.49 | 0.52 | 0.57 b | 0.53 b | 0.53 a | 0.43 b | 0.54 | 0.61 | 0.56 | 0.52 |
| TrichodermaT-85 | 0.57 | 0.57 | 0.54 | 0.52 | 0.45 c | 0.49 c | 0.38 b | 0.37 b | 0.52 | 0.53 | 0.49 | 0.47 |
| Blitefree® | 0.54 | 0.60 | 0.54 | 0.64 | 0.65 a | 0.62 a | 0.53 a | 0.59 a | 0.54 | 0.59 | 0.56 | 0.49 |
| Mancozeb | 0.46 | 0.44 | 0.53 | 0.52 | 0.6 1b | 0.61 b | 0.60 a | 0.56 a | 0.55 | 0.54 | 0.47 | 0.54 |
| p= | ns | ns | ns | ns | * | * | ** | ** | ns | ns | ns | ns |
Medias entre filas con diferente literal son significativamente diferentes entre sí (Tukey, p=0.05). ns=no significativo, *=significativo, **= altamente significativo.
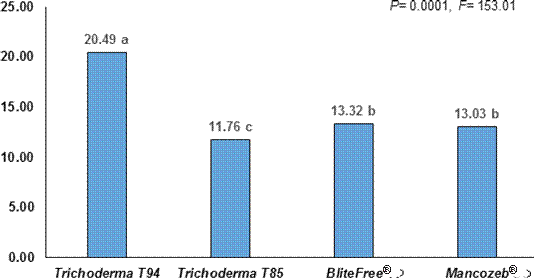
Figura 1 Suma general del área bajo la curva del progreso de la enfermedad (ABCPE) de la Sigatoka negra en banano cv. Gran enano a través de las aplicaciones de Trichoderma spp.
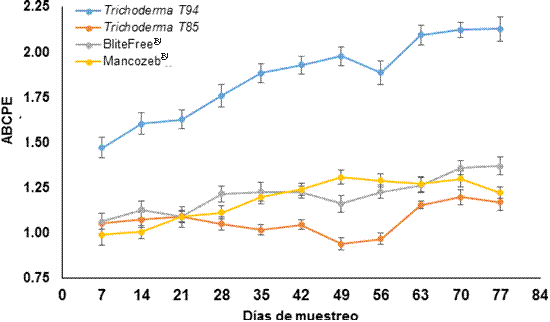
Figura 2 Comportamiento del área bajo la curva del progreso de la enfermedad (ABCPE) de la Sigatoka negra en banano cv. Gran enano a través de aplicaciones de Trichoderma spp.Discusión
Trichoderma spp. posee una amplia aceptación como agente de control biológico de hongos fitopatógenos por sus múltiples mecanismos de acción, de este modo, la producción a gran escala de Trichoderma spp. tiene potencial para uso comercial, a pesar de la existencia de productos formulados en el mercado, es idóneo explorar nuevas cepas dirigidos a fitopatógenos causantes de enfermedades específicas. Los micropropágulos de Trichoderma spp. en forma de conidiosporas son preferidos sobre clamidosporas y biomasa micelial debido a la viabilidad y estabilidad en la aplicación de campo (Cavalcante et al., 2008). En México, el sustrato más utilizado para la producción de conidiosporas de Trichoderma sp. son los granos de arroz entero y quebrado, cuyos costos actuales son de $30.0 y $18.0 pesos MXN, respectivamente, según el Sistema Nacional de Información e integración de Mercados (SNIIM, 2024). El presente trabajo demuestra que, en fermentación sólida, los granos de maíz quebrado son un mejor sustrato para la producción de conidiosporas de Trichoderma spp., y puede sustituir a los granos de arroz por su mejor rendimiento (71 % más) y menor precio ($9.0 M/N por kg según el SNIIM, 2024). El rendimiento de Trichoderma en FES depende de factores bióticos y abióticos.
Los bióticos corresponden a las especies y cepas de Trichoderma. Mientras que los abióticos corresponden a las características del sustrato como tipo, humedad, tamaño de partícula, lecho y volumen de fermentación y a las condiciones de incubación como luz, temperatura, humedad y tiempo de fermentación (Kumar et al., 2023). Algunos reportes describen rendimientos más altos que Trichoderma T-85 y T-94 cultivados en MQ, estos resultados podrían atribuirse a la temperatura y humedad de los sustratos, Arévalo et al. (2017) reportaron rendimientos de 3.63×109 y 1.45×109 conidiosporas g -1 en arroz entero y quebrado, respectivamente. Cavalcante et al. (2008) también reportaron altos rendimientos de Trichoderma spp. tanto en arroz entero (1.45 a 5.8 3.63×108 conidiosporas g -1) como en maíz quebrado (0.18 a 7.45×108 conidiosporas g -1) con Trichoderma harzianum, T. viride, T. koningii y T. polysporum. Por el contrario, otros reportes sugieren que Trichoderma spp. posee bajos rendimientos al emplear arroz entero o maíz quebrado, López et al. (2022) reportaron rendimientos en los rangos 0.33 a 9.20×107 conidiosporas g -1 y 0.14 a 3.70×107 conidiosporas g -1 en arroz entero y MQ, respectivamente para T. harzianum, T. longibrachiatum y Trichoderma sp. Asimismo, Gorotiza et al. (2023) reportaron rendimientos de 5.4×105 a 1.2×107 conidiosporas g -1 de Trichoderma spp. al combinar diferentes proporciones de arroz y MQ.
El contenido nutrimental del maíz puede ser la clave en la mejora del rendimiento de Trichoderma, el maíz posee mayor contenido de almidón que el arroz (Mex et al., 2016), el almidón está compuesto por dos polisacáridos, amilosa y amilopectina, ambos polímeros lineales de unidades de glucosa. Trichoderma sp. como micromiceto filamentoso prefiere crecer en medios o sustratos con alto contenido de carbono, puesto que es uno de sus principales nutrientes (Colina et al., 2009).
En cuanto a la epidemiología de la SN, Trichoderma T-85 fue la cepa con mayor control sobre la severidad y ABCPE. Trichoderma podría estar interactuando con la SN a través de sus mecanismos de acción como micoparasitismo y antibiosis. En estudios previos, Sagratzki et al. (2015) evaluaron el índice de severidad de la SN al utilizar cuatro cepas de Trichoderma y un fungicida químico (Azoxystrobin), los resultados indicaron que el Azoxystrobin redujo en mayor medida la severidad de la SN al 82%, seguido por Trichoderma viride con 66%. Este comportamiento no se encontró con Mancozeb, al permitir mayor severidad, PPI y ABCPE, si se compara con Trichoderma T-85. P. fijiensis como agente causal de la SN pudiera poseer resistencia, al respecto, Aguilar et al. (2014) reportaron que Mancozeb posee un valor alto de CL50 (entre 49.21 y 112.25 mg L -1) respecto a otros fungicidas como
Azoxystrobin (entre 13.25 y 51.8) y Propiconazole (entre 1.22 y 10.01), sugiriendo
que P. fijiensis posee resistencia al Mancozeb, incluyendo poblaciones aisladas del estado de Colima.
En otro estudio, Arzate (2006) evaluó el PPI de P. fijiensis en banano, utilizó cepas de Trichoderma sp. para control in situ de la SN, dos cepas de Trichoderma sp. fueron las mejores al obtener el menor PPI en el monitoreo a los 42 días después de la aplicación (dda); estos resultados concuerdan con el presente estudio, debido a que en los monitoreos a 35, 42 y 49 dda, Trichoderma sp. T-85 mostró el menor PPI, incluso comparado con el Mancozeb. Por el contrario, Agamez et al. (2012) estudiaron una cepa nativa de Trichoderma sp., un bioformulado a base de Trichoderma y Propiconazole como control químico para el control de SN en banano cv. Hartón, midieron el PPI y no encontraron diferencias significativas en el control de la SN entre los tratamientos. Asimismo, es posible que después de tres o cuatro aplicaciones de Trichoderma sp. en plantas con SN, sea un tratamiento adecuado para bajar el PPI y severidad, y que los resultados se observen en los 35 a 49 días; la efectividad de los productos biológicos requiere tiempo para establecerse y controlar el fitopatógeno o enfermedad. Además, es fundamental considerar las condiciones ambientales, ya que las épocas de aplicación (lluvias o sequía) son cruciales para lograr una efectividad positiva en el manejo de la SN en campo (Becker et al., 2021).
Por otra parte, el Blitefree® (Streptomyces spp.) permitió severidades y áreas bajo la curva del progreso de la enfermedad similares al Mancozeb, este producto contiene el extracto del actinomiceto, podría ser una de las razones por la cual no resultó más efectivo que Trichoderma sp., puesto que las conidiosporas aplicadas, podrían estar interactuando con mucha más facilidad con M. fijiensis a través del micoparasitismo, a comparación del extracto de Streptomyces; el cual podría ser efectivo a dosis más altas, siendo un objetivo de estudio a futuro bajo condiciones in situ, ya que estudios in vitro, indican que algunas especies como Streptomyces galilaeus CFFSUR-B12 poseen antagonismo contra M. fijiensis a través de la antibiosis, como resultado de la producción de quitinasas (Moreno et al., 2016).
Conclusiones
El maíz quebrado es mejor sustrato para obtener conidiosporas de Trichoderma spp. con 71 % más de rendimiento. Las cepas con mayor producción de conidiosporas fueron Trichoderma T-94 y Trichoderma T-85 y en la aplicación foliar semanal in situ solo Trichoderma T-85 redujo la severidad, PPI y ABCPE de la Sigatoka negra en banano cv. Gran enano, a partir de los 28 días después de las aplicaciones, Mancozeb y Blitefree® fueron menos efectivos.











 texto em
texto em 


