Introducción
El frijol común (Phaseolus vulgaris) es un cultivo alimenticio y comercial de suma importancia a nivel mundial. Este cultivo se encuentra ampliamente adaptado a ambientes con temperaturas de crecimiento moderadas y su popularidad se origina porque es fácil de producir (Foyer et al., 2016). Actualmente, la calidad, rendimiento y producción de este cultivo se ve afectado por numerosos problemas fitosanitarios, algunos generados por diversos microorganismos, que limitan la calidad de los productos agrícolas y son responsables de cuantiosas pérdidas económicas; además, representan una amenaza significativa para la seguridad alimentaria mundial (Sundin et al., 2016). Dentro de estos microorganismos se encuentra Pseudomonas syringae, uno de los fitopatógenos más importantes para este y otros cultivos como jitomate, kiwi, tabaco, limón, avena, trigo, soya, pepino, arroz, entre otros (Chen et al., 2022). La especie syringae incluye 62 patovares, dependiendo del hospedero al que infectan y entre ellos se encuentran la mayoría de los fitopatógenos del género Pseudomonas (Bull et al., 2010). El éxito de un fitopatógeno para infectar, colonizar e inducir una serie de síntomas en su hospedero, está directamente relacionado con su información genética. Esta información, representada por los genes, le permite sintetizar y secretar metabolitos deletéreos para la planta (Lamichhane et al., 2015). Los diversos patovares de P. syringae son reconocidos por producir un amplio espectro de metabolitos que actúan como factores de patogenicidad y virulencia; entre ellos se encuentran las fitotoxinas, que dañan directamente las células de las plantas e influyen en el desarrollo de la enfermedad. P. syringae pv. phaseolicola, es el agente causal de la enfermedad del
tizón de halo del frijol, la cual puede ser devastadora, especialmente cuando persisten las condiciones ambientales adversas. La presencia de un halo clorótico que caracteriza a esta enfermedad es justamente ocasionada por la faseolotoxina, una fitotoxina producida por P. syringae pv. phaseolicola (Arrebola et al., 2011). La genética relacionada con la síntesis de las fitotoxinas ha cobrado notable importancia, ya que los genes que codifican para las enzimas involucradas en el ensamblaje, la maduración e incluso, las necesarias para la secreción, se encuentran agrupados en fragmentos cromosómicos conocidos como islas genómicas. Estas islas contienen todos los elementos necesarios para transferirse de manera horizontal entre los diferentes patovares. Esto es de gran relevancia, dado que a través de estos mecanismos de transferencia genética, las bacterias adquieren nuevas habilidades patogénicas (Melnyk et al., 2019). El avance en el estudio genético de los factores de patogenicidad y virulencia, como son las fitotoxinas, favorece la comprensión de cómo los patógenos adquieren y producen el arsenal molecular necesario para el desarrollo de las enfermedades en los sistemas vegetales (Ichinose et al., 2013). Considerando que cada patovar de P. syringae produce una diversidad de fitotoxinas, esta revisión se enfocará en el análisis uno de esos casos: la genética involucrada en biosíntesis de la faseolotoxina producida por el patovar phaseolicola y su participación en el desarrollo del tizón de halo del frijol. Esta información contribuye esencialmente al entendimiento de cómo esta bacteria fitopatógena ha adquirido genes necesarios para sintetizar la faseolotoxina y cómo ha coordinado su sistema de regulación endógeno para este propósito. Adicionalmente, se analiza el potencial que han tenido este tipo de estudios genéticos para el desarrollo de es-
trategias destinadas al diagnóstico y manejo oportuno de las enfermedades.
P. syringae pv. phaseolicola
El tizón de halo es una de las principales enfermedades que afecta al cultivo de frijol y es causada por la bacteria P. syringae pv. phaseolicola. Esta bacteria persiste en la semilla y se activa después de su germinación; puede sobrevivir como parásito dentro del tejido vegetal y como epífita sobre la superficie de las hojas. La bacteria se ha observado en la mayoría de las regiones productoras de frijol en todo el mundo y se ha convertido en un fitopatógeno altamente destructivo para este cultivo, generando pérdidas que oscilan entre el 50 y 100 % de la producción (Arnold et al., 2011; Lépiz-Ildefonso et al., 2015). La bacteria se puede presentar en los diferentes estados fenológicos afectando hojas, tallo, vainas y semillas. En hojas, se observa la aparición pequeñas lesiones acuosas que posteriormente se vuelven necróticas; aproximadamente una semana después de la infección, una o más lesiones son rodeadas por un halo clorótico (Figura 1A y B). También en las vainas se desarrollan lesiones acuosas y hundidas de color marrón rojizo (Figura 1

Figura 1 Síntomas producidos por P. syringae pv. phaseolicola en el frijol. A y B, Síntomas en las hojas. C y D, Síntomas en las vainas. Fuente: Adaptada de Schwartz, 2008; Harveson, 2009.
C y D). Las infecciones de las vainas pueden transferirse a las semillas, causando que se contraigan, decoloren o sean más pequeñas de lo normal. La bacteria se desarrolla en un rango de 28-30 °C con una humedad relativa mayor al 80 %; sin embargo, a temperaturas que oscilan entre los 18 y 20 ºC se presentan síntomas más severos. El descenso de la temperatura induce la producción de faseolotoxina, que es la responsable de la formación del halo clorótico y del amarillamiento característico que se observa durante el desarrollo de la enfermedad (Arnold et al., 2011; Xin et al., 2018).
La faseolotoxina y su mecanismo de acción
Desde el punto de vista químico, la estructura de la faseolotoxina es inusual y tiene dos componentes distintos: un residuo inorgánico, Nδ(N’-Sulfodiaminofosfinil) y un tripéptido, L-ornitil-alanil-homoarginina (Figura 2) (Arrebola et al., 2011). Esta toxina actúa como un inhibidor reversible de la enzima ornitina carbamoiltransferasa (OCTasa EC 2.1.3.3.), codificada por el gen argF. La OCTasa cataliza la conversión de ornitina y carbamoilfosfato a citrulina en la ruta de la síntesis
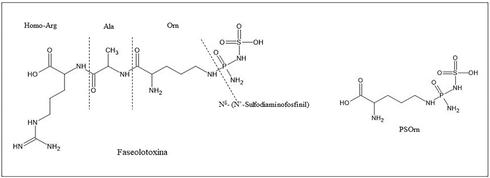
Figura 2 Estructura de la faseolotoxina y PSOrn, producto de la degradación de la faseolotoxina por peptidasas de la planta.
de arginina. Dentro de la célula vegetal, la faseolotoxina se hidroliza por la acción de peptidasas para producir Nδ-(N´-sulfodiaminofosfinil)-L-ornitina (denominada octicidina o PSOrn), que es un inhibidor irreversible de la OCTasa y que es la forma predominante en la que se encuentra la toxina en plantas de frijol infectadas (Sawada et al., 2002). Esta inhibición provoca una acumulación de ornitina y una deficiencia de arginina. A medida que la toxina se difunde a través del tejido foliar, altera la síntesis de la clorofila, causando clorosis e inhibición del crecimiento en tejidos vegetales y finalmente, ocasiona la muerte de las células del huésped. Adicionalmente, la invasión sistémica de la planta se ve facilitada por el efecto de la faseolotoxina, de manera que contribuye significativamente a la virulencia del patógeno (Arnold et al., 2011).
Originalmente, la faseolotoxina se consideró restringida a P. syringae pv. phaseolicola; sin embargo, también es producida por el patovar actinidiae que infecta al kiwi (Actinidia chinensis) (Fujikawa y Sawada, 2019), y por una cepa del patovar syringae, aislada de Vicia sativa (Tourte y Manceau, 1995). Diversos aislamientos pertenecientes al patovar phaseolicola sintetizan faseolotoxina cuando se cultivan a 18-20 °C, aunque su grado de producción puede variar entre aislamientos. Por otro lado, también se han identificado cepas pertenecientes al patovar phaseolicola que son incapaces de producirla, ya que carecen de todos o parte de los genes necesarios para su síntesis (Gonzalez et al., 2003).
Inmunidad a la faseolotoxina
Inicialmente, fue un misterio determinar cómo P. syringae pv. phaseolicola era inmune a su propia toxina. El efecto tóxico de la faseolotoxina era evidente ya que no solo inhibe a la OCTasa del frijol, sino a una gran variedad de OCTasas vegetales y bacterianas e incluso de mamíferos (Bender et al., 1999). En estos organismos
causa un fenotipo de auxotrofía a arginina, que es aliviado añadiendo arginina o citrulina al medio de cultivo. En contraste, cepas de P. syringae pv. phaseolicola productoras de faseolotoxina, son insensibles a su toxina y no requieren de suplementos de arginina o citrulina. Todo se esclareció cuando se identificó y caracterizó el gen argK, que codifica para una OCTasa resistente a la faseolotoxina (Mosqueda et al., 1990). De esta manera, se observó que P. syringae pv. phaseolicola presenta dos actividades de OCTasa, una sensible a la toxina que se produce a 28 °C y, la actividad de la OCTasa resistente, que garantiza el suministro óptimo de la arginina requerida para el crecimiento bacteriano, bajo las condiciones de síntesis de faseolotoxina (Lopez-Lopez et al., 2004). El conocimiento acerca de la resistencia bacteriana al efecto de sus toxinas se ha utilizado en varias estrategias para desarrollar plantas resistentes. Para el caso de la faseolotoxina, argK ha sido utilizado como transgen en plantas de tabaco (Nicotiana tabacum) y ha tenido éxito en el desarrollo de plantas resistentes al efecto de la faseolotoxina (De la Fuente-Martinez et al., 1992). Estudios como estos pueden extrapolarse a otros cultivos de interés agronómico, permitiendo generar cultivares resistentes al ataque de los patógenos.
La genética detrás de la biosíntesis de faseolotoxina
Diversos estudios se han enfocado en la química de la faseolotoxina, el modo de acción y su contribución a la patogenicidad, pero se sabe poco sobre su biosíntesis. A través de los análisis genéticos, se ha aportado información relevante para dilucidar cómo se sintetiza esta toxina. El primer indicio de los genes involucrados en la síntesis fue la identificación y caracterización de amtA y desI, estos genes codifican para una amidinotransferasa y una desaturasa de ácidos grasos, respectivamente (Hernandez-Guzman y Alvarez-Morales, 2001; Zhang y Patil, 1997). Actualmente, se cuenta con la descripción y el análisis de una región de 30,245 pb del cromosoma de P. syringae pv. phaseolicola NPS3121, denominada Región Pht (Figura 3A), la cual contiene 23 genes necesarios para la síntesis de faseolotoxina, incluyendo los genes argK, amtA y desI (Aguilera et al., 2007). La Región Pht está delimitada por secuencias de inserción y transposasas, sugiriendo que este fragmento constituye una isla genómica que pudo ser adquirida a través de eventos de transferencia horizontal (Murillo et al., 2011). La función precisa de los genes codificados dentro de la región Pht permanece incierta y solamente algunos de estos genes han sido estudiados más a fondo (Aguilera et al., 2012; Arai y Kino, 2008; Chen et al., 2015; Gonzalez-Villanueva et al., 2014). De esta manera, ha sido posible asignarles una función en el proceso de síntesis y regulación de la faseolotoxina (Cuadro 1).
La faseolotoxina se compone de un tripéptido y se ha propuesto que su síntesis es
a través de un mecanismo denominado síntesis no ribosómica de péptidos. En este proceso participan complejos enzimáticos como las péptido sintetasas no ribosomales (NRPS; por sus siglas en inglés, Non-ribosomal Peptide Synthetases) y/o las
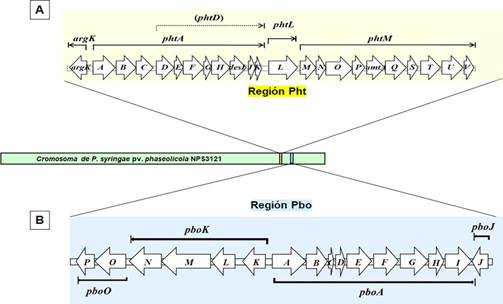
Figura 3 Representación gráfica de las Regiones Pht y Pbo en el cromosoma de P. syringae pv. phaseolicola. A, Operones de la Región Pht. B, Operones de la Región Pbo. Cada flecha representa cada gen, la dirección de la flecha indica la dirección de la transcripción.
Cuadro 1 Función de genes pht involucrados en la síntesis de faseolotoxina.
| Gen | Proteína codificada | Función | Referencia |
|---|---|---|---|
| argK | Ornitina carbamoil transferasa | Catalizar la reacción entre el carbamoil fosfato y la ornitina para formar citrulina bajo condiciones de síntesis de faseolotoxina. | Lopez-Lopez et al., 2004 |
| amtA | Amidinotransferasa | Catalizar la reacción de transferencia reversible de grupos amidino para sintetizar L-homoarginina. | Hernandez-Guzman y Alvarez-Morales, 2001 |
| desI | Desaturasa de ácidos grasos | Deshidrogenar ácidos grasos, creando dobles enlaces entre carbono-carbono; percepción de la temperatura. | Zhang y Patil, 1997 |
| phtU | L-aminoácido ligasa | Catalizar la condensación de aminoácidos. | Arai y Kino, 2008 |
| phtQ | Péptido ligasa | Catalizar la formación de enlaces peptídicos. | Chen et al., 2015 |
| phtL | Piruvatofosfato dicinasa | Transferir grupos fosfato del pirofosfato y del fosfoenolpiruvato a una molécula de AMP para sintetizar ATP, fosfato y piruvato. | Gonzalez-Villanueva et al., 2014 |
| phtA | Nucleósido trifosfato hidrolasa | Hidrolizar el enlace beta-gamma fosfato de un nucleósido trifosfato. | Aguilera et al., 2012 |
policétido sintetasas (PKS, por sus siglas en inglés, Polyketide Synthases). El gen PSPPH_4550, identificado como una NRPS, participa en la síntesis de faseolotoxina (De la Torre-Zavala et al., 2011). De manera interesante, el gen PSPPH_4550 se encuentra codificado fuera de la Región Pht y es parte de otra isla genómica,
denominada Región Pbo. Este fragmento contiene 16 genes (Figura 3B) y algunos de ellos, codifican para NRPS o PKS (Cuadro 2), sugiriendo su participación en la síntesis del tripéptido (Guardado-Valdivia et al., 2021).
Cuadro 2 Predicción de la función de genes pbo involucrados en la síntesis de faseolotoxina.
| Gen | Proteína codificada | Función | Referencia |
|---|---|---|---|
| pboO | Sintetasa c | Formar enlaces amida en el proceso de síntesis de péptidos no ribosomales. | Guardado-Valdivia et al., 2021 |
| pboM | Cetoacil transferasa | Catalizar las elongaciones de ácidos grasos en la síntesis de policétidos. | Guardado-Valdivia et al., 2021 |
| pboA | Enzima de unión a AMP | Condensar y adenilar en el proceso de síntesis de péptidos no ribosomales. | De la Torre-Zavala et al., 2011 |
| pboB | Cetoacil sintasa | Catalizar la condensación de Claisen descarboxiladora de ácidos grasos en la síntesis de policétidos. | Guardado-Valdivia et al., 2021 |
| pboC | Dominio de unión de fosfopanteína | Unir aminoácidos y ácidos grasos activados en la síntesis de péptidos no ribosomales. | Guardado-Valdivia et al., 2021 |
A la fecha, múltiples genes involucrados en la síntesis de faseolotoxina han sido identificados (Cuadro 1 y 2), y se han asignado funciones a algunos de ellos; sin embargo, aún queda mucho trabajo para dilucidar la función del resto de los genes y especialmente, cuáles son los genes involucrados en sintetizar el componente inorgánico de dicha toxina.
Regulación de la síntesis de faseolotoxina
Es evidente que los fitopatógenos requieren de mecanismos genéticos que les concedan la habilidad de adaptarse en respuesta a las condiciones en las que se encuentran. En bacterias fitopatógenas, los sistemas de regulación de dos componentes permiten la adaptación a diferentes condiciones en respuesta a las señales ambientales, transfiriendo la señal a factores de transcripción, los cuales activan la expresión de genes (Sultan et al., 2021). P. syringae pv. phaseolicola posee diversos sistemas de dos componentes; sin embargo, el sistema GacS/GacA es de gran importancia por su papel en el control de determinantes de virulencia y patogenicidad, adecuación ecológica, sistemas de Quorum sensing (Qs), y la síntesis de diversos metabolitos secundarios (Latour, 2020). El sistema GacS/GacA, controla a todos los genes conocidos hasta ahora, involucrados en la síntesis y regulación de la faseolotoxina en P. syringae pv. phaseolicola NPS3121 (De la Torre-Zavala et al., 2011; Ramirez-Zapata et al., 2020). Otros reguladores globales, como el factor transcripcional IHF, también participa en este proceso. La función de IHF como
regulador de la expresión de factores virulencia ha sido extensamente reportado (Arvizu-Gomez et al., 2011; Reverchon et al., 2021). Estos hallazgos revelan que algunos genes que se adquieren a través de eventos de transferencia horizontal, pueden ser integrados a los sistemas de regulación global preexistentes (RedondoSalvo et al., 2020). En este sentido, los genes involucrados en la biosíntesis de la faseolotoxina no fueron la excepción.
Para P. syringae pv. phaseolicola NPS3121, el descenso de la temperatura también es un factor determinante en la producción de la faseolotoxina. Este cambio controla la transcripción de los genes pht y pbo (Aguilera et al., 2007; GuardadoValdivia et al., 2021). La información recopilada hasta el momento, permite proponer un modelo de señalización y regulación de la biosíntesis de la faseolotoxina en P. syringae pv. phaseolicola NPS3121 (Figura 4), en el cual se representa de manera esquemática el estímulo y la cascada de señalización responsable de desencadenar la síntesis de faseolotoxina.
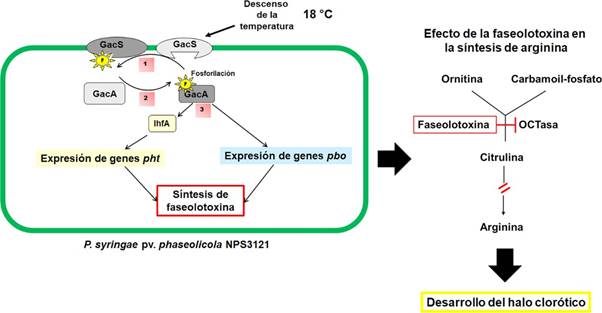
Figura 4 Modelo de señalización, regulación y efecto de la biosíntesis de la faseolotoxina producida por P. syringae pv. phaseolicola NPS3121. La temperatura se percibe por el sensor membranal GacS, que como consecuencia se autofosforila (1). GacS fosforilado transfiere el fosfato al regulador de respuesta GacA (2). GacA controla la expresión de los genes pht, mediada por el regulador IHF. GacA también controla la transcripción de los genes pbo 3). Finalmente, se sintetiza la faseolotoxina, que inhibe a la OCTasa del frijol, impidiendo la síntesis de arginina. Consecuentemente, se desarrolla el halo clorótico.
Transferencia de las Regiones Pht y Pbo entre patovares
En bacterias, la transferencia horizontal de genes a través de elementos genéticos accesorios como plásmidos, transposones, profagos o islas genómicas les permite adquirir y expresar genes provenientes de una amplia gama de especies (Carraro et al., 2017). Se ha sugerido que Región Pht constituye una isla genómica que P. syringae adquirió mediante mecanismos de transferencia horizontal. Esto se ha sustentado dada la similitud de la organización y la secuencia de las diferentes versiones de la Región Pht identificadas en los patovares phaseolicola y actinidae, que denotan claramente un origen común y una funcionalidad conservada (Murillo et al., 2011). Adicionalmente, el hallazgo de cepas de P. syringae pv. phaseolicola carentes de la Región Pht, ha dado sustento a esta propuesta (Gonzalez et al., 2003). En lo referente a la Región Pbo, también comprende otra isla genómica. A pesar de que ambas islas participan en la síntesis de la faseolotoxina, no existe una correlación entre la posesión de la Región Pbo y la Región Pht, sugiriendo que su adquisición se llevó a cabo de manera independiente y una vez que fueron adquiridas, se incorporaron en el cromosoma de P. syringae pv. phaseolicola, quedando bajo control de los sistemas de regulación global preexistentes (De la Torre-Zavala et al., 2011; Guardado-Valdivia et al., 2021). Las bacterias patogénicas han evolucionado a partir de organismos relacionados no patogénicos, debido a la adquisición de material genético que codifica para múltiples factores de patogenicidad y virulencia. En lo que se refiere a los patovares de P. syringae, es importante comprender cómo los mecanismos de movilidad genética han contribuido a su patogenicidad y virulencia, porque finalmente, esto es lo que ha convertido a esta especie, en una de las 10 bacterias fitopatógenas más importantes a nivel mundial (Mansfield et al., 2012). En lo que se refiere al patovar phaseolicola, los estudios sobre la genética molecular de su interacción con el frijol y la evolución de su patogenicidad y virulencia, han contribuido con importantes descubrimientos en el campo de las interacciones planta-microorganismo, por lo que actualmente P. syringae pv. phaseolicola es considerada un modelo de estudio de la interacción molecular planta-patógeno (Arnold et al., 2011).
Estrategias de detección molecular de Pseudomonas syringae pv. phaseolicola
Uno de los requerimientos más importantes para manejar las enfermedades en las plantas es la identificación oportuna del agente causal. Actualmente, existen técnicas biotecnológicas que aceleran la obtención de resultados y han permitido la identificación oportuna de bacterias fitopatógenas. Adicionalmente, han complementado los procesos tradicionales de diagnóstico como la examinación visual, cultivo del patógeno, la microscopía y las pruebas de patogenicidad.
En lo que se refiere a la detección e identificación de P. syringae pv. phaseolicola, se han desarrollado diversas estrategias moleculares, con la finalidad de llevar a cabo una detección precisa y oportuna. Dentro de las primeras estrategias reportadas, se encuentran los ensayos de inmunoadsorción ligado a enzima (ELISA, por sus siglas en inglés, Enzyme-Linked Immunosorbent Assay). Los antisueros obtenidos reconocieron de manera específica al patovar phaseolicola, sin mostrar reacción cruzada con otros patovares de P. syringae (Wyatt et al., 1989). En esa misma época, se desarrolló una estrategia basada en la hibridación de sondas de ADN que portaban genes involucrados en la síntesis de la faseolotoxina. Esta técnica permitió la detección e identificación del patovar phaseolicola a partir de semillas y de muestras maceradas de tejidos con lesiones (Schaad et al., 1989).
Con el desarrollo de la reacción en cadena de la polimerasa (PCR, por sus siglas en inglés, Polymerase Chain Reaction), se implementaron estrategias para detectar e identificar múltiples fitopatógenos y P. syringae pv. phaseolicola no fue la excepción. Para esto, se diseñaron oligonucleótidos específicos a partir de las secuencias disponibles de genes involucrados en la biosíntesis de faseolotoxina (MosquedaCano y Herrera-Estrella, 1997; Schaad et al., 1995; Schaad et al., 2007). En el Cuadro 3 se describen algunos de los oligonucleótidos empleados para la identificación y las regiones que amplifican.
Cuadro 3 Oligonucleótidos usados para identificar cepas de P. syringae pv. phaseolicola productoras de faseolotoxina.
| Nombre | Secuencia | Blanco | Referencia |
|---|---|---|---|
| BRL519 BRL520 | TTCATTCAAACCTCGCCCGTGTG TGAAAGGAGCCGCCGAAACTATTG | amtA | Aguilera et al., 2007 |
| PA5.1 PA3.1 | AGCTTCTCCTCAAAACACCTGC TGTTCGCCAGAGGCAGTCATG | desI | Schaad et al., 1995 |
| 62a 63a | CAATGAAGATTACAAGCCTG GCTAGCTATCAGGGGACGAC | argK | Mosqueda-Cano y Herrera-Estrella, 1997 |
| P3004L P3004R | CTGTCTGGCAGCCACTACAAAG GGCTGCAAATTGTGGGATTT | Región Tox- | Rico et al., 2006 |
| AVR1-F AVR1-R | CCGCCGTAGCAGGGCTTCAC GGACCAATCTCTTTTCTCAA | phtL | Gonzalez et al., 2003 |
| PHTE-F PHTE-R | AATATAGGCTTCAACTTCCTC CCAGGTCAACTCACTTCCG | phtE | Gonzalez et al., 2003 |
| P25156 Ptx1I5c | GCAAAAACGAAAACACCAGGCT ATCGCGCTGATCCGGAAAGG | phtA | Aguilera et al., 2017 |
| P12556 P11311 | TCCGGTTATCGCTTCAGGTCG GCAGTTTCTGATCTTGGGCCC | phtM-N | Aguilera et al., 2017 |
Es importante considerar la existencia de aislados de P. syringae pv. phaseolicola que no producen faseolotoxina y por lo tanto, no se pueden detectar utilizando estos oligonucleótidos (Rico et al., 2006). Además, la producción de faseolotoxina no es una característica específica de patovar phaseolicola, por lo que estos ensayos también podrían detectar otros patovares (Tamura et al., 2002). De acuerdo con esto, se han diseñado nuevas metodologías; por ejemplo, la PCR en tiempo real TaqMan, en la que se emplearon oligonucleótidos específicos, basados en el gen de la recombinasa específica de sitio. A través de esta estrategia se lograron diferenciar entre cepas de P. syringae pv. phaseolicola productoras y no productoras de faseolotoxina (Cho et al., 2010). Otra técnica de amplificación de ADN, conocida como amplificación isotérmica mediada por bucle (LAMP; por sus siglas en inglés, Loop-Mediated Isothermal Amplification), ha sido adaptada para facilitar la caracterización e identificación rápida y específica del patovar phaseolicola (Li et al., 2009). El diagnóstico molecular de P. syringae pv. phaseolicola es fundamental para el manejo eficaz del tizón de halo en cultivos de frijol. Aunque el diagnóstico molecular puede ser más costoso y requiere de infraestructura especializada, su alta precisión, rapidez y capacidad para detectar infecciones de manera temprana y cuantitativa, hacen que sea una herramienta indispensable en la lucha contra este patógeno. Con el tiempo, se espera que las tecnologías de diagnóstico molecular continúen mejorando y se hagan más accesibles, lo que permitirá un manejo más eficiente de las enfermedades bacterianas en la agricultura.
Estrategias moleculares para el manejo del tizón de halo del frijol. Una alternativa para la agricultura en México
En México, el manejo del tizón de halo en frijol se ha convertido en un desafío para los productores debido a la naturaleza agresiva de la enfermedad y la capacidad de propagación rápida (Félix-Gastélum et al., 2016). P. syringae pv. phaseolicola se encuentra ampliamente distribuida en el país (Figura 5), por lo es un riesgo para la producción nacional de frijol (Félix-Gastélum et al., 2016; Jiménez-Hernández et al., 2023; Navarrete y Acosta-Gallegos, 2000; Quiñones-Aguilar et al., 2018). Es por esto que para el manejo del tizón de halo, se han desarrollado estrategias como la aplicación de antibióticos agrícolas, la eliminación de residuos de la cosecha, la rotación de cultivos o el empleo de variedades de frijol resistentes; entre otras (Schwartz et al., 2005). Con la combinación de estas medidas ha sido posible controlar el desarrollo de la enfermedad; sin embargo, no ha sido suficiente.
A partir de los avances en la Biotecnología, las estrategias moleculares han emergido como una herramienta poderosa que pueden complementar las estrategias convencionales y lograr un manejo más eficiente y sostenible de los patógenos. La resistencia genética es una de las estrategias más efectivas para controlar las
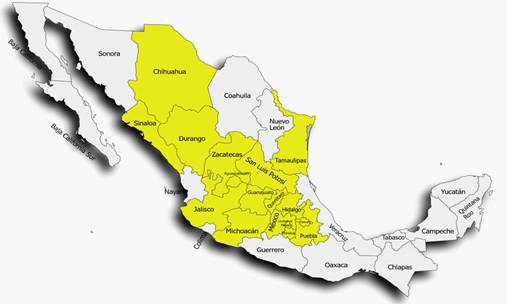
Figura 5 Mapa representativo de la distribución de P. syringae pv. phaseolicola en México. Los estados marcados con color amarillo indican la presencia de esta bacteria.
enfermedades en las plantas. En México, el uso de marcadores moleculares ha favorecido la identificación de variedades de frijol, como Flor de Mayo M38, San Rafael, Pinto Laguna 80 y Pinto Saltillo, que muestran resistencia contra P. syringae pv. phaseolicola (Jiménez-Hernández et al., 2023). A pesar de esto, la resistencia en las variedades comerciales disponibles en México sigue siendo limitada, por lo que el desarrollo de nuevas variedades resistentes, mediante técnicas moleculares novedosas como la edición genética CRISPR/Cas9 (Thomas et al., 2024), podría representar una alternativa para introducir de manera específica, genes de resistencia en las variedades de frijol. Adicionalmente, las tecnologías basadas en las llamadas “ciencias ómicas”, ofrecen información valiosa para comprender la interacción de P. syringae pv. phaseolicola con el frijol. Los análisis proteómicos de las variedades de frijol resistentes al tizón de halo, aportan información para entender la naturaleza de esa resistencia (Cooper et al., 2020; Oblessuc et al., 2022), además de generar información que podría ser utilizada para desarrollo de estrategias de control, basadas en los análisis de marcadores genéticos y proteicos de dichas variedades. El uso de bacteriófagos en el control biológico también es una alternativa prometedora y ecológica para el control de bacterias patógenas. En el 2018, Quiñones-Aguilar y cols., aislaron bacteriófagos nativos del estado de Zacatecas y evaluaron su actividad lítica contra cepas virulentas de P. syringae pv. phaseolico-
la. De esta manera, se identificó un bacteriófago capaz de disminuir hasta un 60% el daño provocado por el patovar phaseolicola en ejotes (Quiñones-Aguilar et al., 2018). En México, las técnicas moleculares enfocadas en el manejo del tizón de halo y demás enfermedades en los cultivos, son limitadas, por lo que es necesario impulsar el desarrollo de nuevas estrategias que complementen el manejo del tizón de halo del cultivo de frijol en la agricultura mexicana.
Conclusiones
Pseudomonas syringae pv. phaseolicola es una especie bacteriana con gran capacidad patogénica, por tal motivo, se ha convertido en un modelo de estudio para la comprensión de la interacción molecular planta-patógeno. Las regiones Pht y Pbo, que contienen genes involucrados en la biosíntesis de la faseolotoxina, juegan un papel clave en el desarrollo del tizón de halo. Las evidencias sustentan que la adquisición de las regiones Pht y Pbo se llevó a cabo a través de eventos de transferencia horizontal, una actividad común entre los fitopatógenos. De esta manera, adquieren material genético foráneo y lo controlan a través de su sistema de regulación endógeno; que para el caso de los genes pht y pbo, fueron incorporados a la regulación global del sistema de dos componentes, GacS/GacA y del regulador IHF. Para P. syringae pv. phaseolicola, la adquisición de las Regiones Pht y Pbo ha sido un evento favorable, ya que le permitió aumentar su grado de virulencia, de manera que el resultado de esta nueva habilidad es devastar con mayor eficiencia al cultivo de frijol. Los estudios a nivel molecular de los factores de patogenicidad y virulencia de P. syringae pv. phaseolicola, como es el caso de la faseolotoxina, ofrecen información valiosa para el diseño de estrategias de diagnóstico y manejo del tizón de halo. El desarrollo de nuevas estrategias moleculares favorecerá el diagnóstico temprano, la identificación de nuevas cepas patógenas y el desarrollo de cultivos resistentes, lo que a su vez reducirá el impacto económico de las enfermedades en cultivos de importancia agronómica como el frijol.











 texto em
texto em 


