Introducción
El músculo esquelético representa hasta el 40% de la masa corporal total y desempeña funciones esenciales, como la movilidad, la regulación de la temperatura corporal y el metabolismo de nutrientes como la glucosa y las proteínas.1 Este tejido se encuentra en un delicado equilibrio entre el anabolismo y el catabolismo, un balance que puede alterarse debido a factores como el envejecimiento, el estado nutricional y la presencia de enfermedades. En los adultos mayores, el envejecimiento fisiológico provoca inflamación crónica y daño oxidativo, lo que conduce a disminución de la actividad física, pérdida de apetito con menor ingesta de nutrientes de la dieta (principalmente proteínas) y mayor riesgo de fragilidad que los vuelve vulnerables a distintos padecimientos.2 El catabolismo predispone al desarrollo de sarcopenia, caracterizada por la pérdida progresiva de masa, fuerza y funcionalidad musculares, incrementando la morbilidad y la mortalidad.3 La sarcopenia se ha convertido en un problema de salud pública, exacerbado por el aumento en la esperanza de vida. La sarcopenia es una de las principales causas del síndrome de fragilidad en pacientes geriátricos, caracterizado por un deterioro sistémico con repercusiones físicas, psicológicas y sociales que incrementan la morbilidad y la mortalidad.
Actualmente existe gran interés por desarrollar nuevas estrategias que permitan recuperar el estado anabólico de los músculos. Estas estrategias pretenden complementar los tratamientos actuales, representados principalmente por programas de ejercicio físico de resistencia, planes de alimentación y suplementación a base de proteínas y micronutrientes que disminuyan el daño celular oxidativo y la inflamación. En los últimos años, la microbiota intestinal ha surgido como un área de interés debido a su papel en el desarrollo y la regulación del metabolismo muscular. La microbiota está compuesta por microorganismos (bacterias, virus, hongos y protozoos) que residen en el intestino humano y llevan a cabo funciones esenciales para la salud. Se sospecha que la microbiota está implicada en el desarrollo fisiopatológico de varios trastornos metabólicos, tales como la obesidad, la diabetes mellitus y las enfermedades cardiovasculares, que tienen como común denominador a la inflamación.4 La coincidencia de alteración de la composición de la microbiota intestinal, deterioro del estado fisiológico y estado de catabolismo muscular sugiere que la microbiota, de manera directa o indirecta, podría influir también en el estado y la regulación de la masa muscular a través del conocido «eje intestino-músculo», propuesto por distintos autores como elemento fundamental en la fisiopatología de la sarcopenia en los pacientes geriátricos.5,8 Lo anterior podría explicar las diversas estrategias terapéuticas implementadas por los investigadores para incidir sobre el metabolismo, específicamente durante la fase anabólica, y la función del tejido muscular.5,7 Entre dichas estrategias se encuentra la suplementación con probióticos, microorganismos que poseen efectos positivos sobre la salud si se administran en cantidades adecuadas. Cabe mencionar que el mecanismo exacto por el cual las distintas clases de probióticos residentes en la microbiota intestinal ejercen sus efectos sobre el músculo esquelético aún no es del todo comprendido.
El objetivo de esta revisión es examinar los mecanismos por los que la microbiota intestinal interactúa con el músculo esquelético y compilar las estrategias terapéuticas más recientes basadas en la suplementación con probióticos para corregir las alteraciones en la microbiota (disbiosis), y así prevenir o tratar la sarcopenia en pacientes geriátricos.
Metodología: criterios de búsqueda y selección
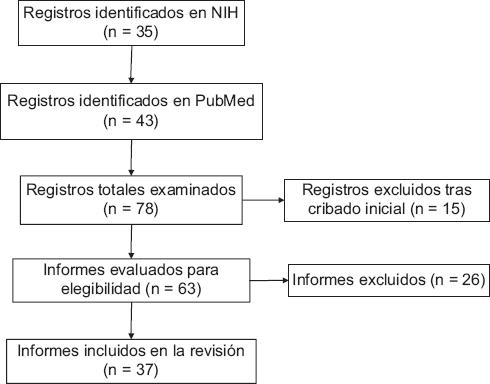
Se realizó una búsqueda sistemática en las bases de datos PubMed y NIH utilizando las palabras clave "sarcopenia", "microbiota intestinal" y "adulto mayor". Se identificaron 78 artículos relevantes (43 en PubMed y 35 en NIH), de los cuales se descartaron 15 tras un cribado inicial.
El diagrama PRISMA (Fig. 1) refleja el proceso de selección, en el cual 63 artículos fueron seleccionados tras excluir 26 que no cumplían con los criterios de elegibilidad, los cuales fueron que se tratara de estudios en inglés o español centrados en análisis sistemáticos, metaanálisis y ensayos clínicos, enfocados en pacientes geriátricos con sarcopenia o síndrome de fragilidad, en quienes se implementara una suplementación con probióticos.
Los 37 artículos finalmente incluidos en la revisión se utilizaron para definir conceptos generales, como la etiología y la fisiopatología de la sarcopenia, así como la fisiología de la microbiota intestinal y su posible relación con el desarrollo y la preservación de la función del músculo esquelético. Se analizaron estudios enfocados en vías metabólicas y de señalización implicadas en el eje intestino-músculo. Además, se evaluó cómo la incorporación de microorganismos específicos a la microbiota afecta la función muscular y el pronóstico de la sarcopenia.
El posible vínculo entre la microbiota intestinal y el músculo esquelético
La sarcopenia es frecuente en los pacientes geriátricos debido al envejecimiento fisiológico, pero también es un trastorno que puede ocurrir en cualquier individuo en estado de hipercatabolismo asociado a inflamación, trauma grave, fallo multiorgánico o procedimientos quirúrgicos mayores.
Debido al actual incremento en la esperanza de vida se estima que en aproximadamente el 20% de las personas mayores de 60 años prevalece cierto grado de sarcopenia.9 Para su diagnóstico se requiere la determinación de la fuerza muscular, así como la evaluación de la calidad y la cantidad de masa muscular, y de la capacidad para realizar actividad física como indicador de gravedad. La sarcopenia es un elemento central en el desarrollo del síndrome de fragilidad del adulto mayor, caracterizado por cambios sistémicos que provocan deterioro físico, pérdida de peso y disminución de la fuerza, con impactos psicológicos y sociales significativos.10 El envejecimiento está asociado con cambios en la composición y en la diversidad de la microbiota intestinal. Sorprendentemente, estas variaciones son más pronunciadas en pacientes con trastornos en comparación con adultos mayores sanos;11,13 por ejemplo, posterior a la evaluación de pacientes con síndrome de fragilidad se encontró una disminución de Prevotella y de Faecalibacterium prausnitzii.14 Estos microorganismos están relacionados con una salud intestinal óptima y con propiedades antiinflamatorias, principalmente a través de metabolitos como los ácidos grasos de cadena corta (AGCC). Así mismo, se ha reportado en estos pacientes un incremento de enterobacterias, las cuales están asociadas con problemas infecciosos como diarrea, dolor abdominal y deshidratación.14,16
Los estudios experimentales realizados en ratones sugieren una poderosa relación entre la microbiota intestinal y el músculo esquelético, pues ratones tratados con un esquema antibiótico a base de penicilina (1 µg por gramo de peso corporal durante 4 semanas) presentaron una disminución de la masa y la fuerza muscular en comparación con un grupo control al cual no se administró dicho esquema.17
Llama la atención que las alteraciones encontradas en la masa y la función musculares pueden restaurarse mediante la restitución de la microbiota después de un trasplante de microbiota fecal.17,19
Mecanismos fisiológicos del músculo esquelético que pueden ser explicados por el eje intestino-músculo
Diversos estudios han explorado la interacción de la microbiota y el tejido muscular, destacando su influencia en funciones como el metabolismo, la inflamación y el estrés oxidativo. Recientemente, algunas investigaciones han identificado vínculos adicionales mediados por moléculas sintetizadas por bacterias intestinales.1,20 A continuación, se describen los principales mecanismos regulatorios de la microbiota en el músculo esquelético.
Relevancia de los AGCC en la interacción intestino-músculo
Las implicaciones fisiológicas de los AGCC se descubrieron en estudios en modelos de roedores con resistencia a la insulina inducida con la dieta. Este efecto se ha confirmado en seres humanos mediante el trasplante de microbiota fecal de pacientes aparentemente sanos realizado a pacientes diagnosticados con síndrome metabólico, en los cuales se observó un incremento en la sensibilidad a la insulina por parte de los tejidos periféricos (músculo esquelético), reflejándose en una mejoría en la tasa de utilización de la glucosa; sin embargo, cabe destacar que no fue un efecto observado en todos los pacientes.4,21,22
Los AGCC se encuentran entre los principales metabolitos generadores de un probable vínculo entre la microbiota intestinal y la sensibilidad a la insulina del tejido muscular.
Los AGCC se producen mediante el metabolismo anaeróbico de fibra insoluble fermentada en el íleon distal y el colon. La fermentación genera AGCC en una proporción aproximada de 3:1:1 entre acetato, butirato y propionato, que en conjunto constituyen más del 90% del total. La mayoría de los AGCC son absorbidos y utilizados como sustratos energéticos por las células del colon (aproximadamente un 60-70%) y el resto son conducidos a través de la circulación portal hacia el hígado, en donde son utilizados como sustratos para las principales vías metabólicas del metabolismo energético. Una fracción menor de los AGCC llegan al tejido muscular a través de la circulación sanguínea, donde regulan funciones metabólicas clave (Fig. 2).13,23
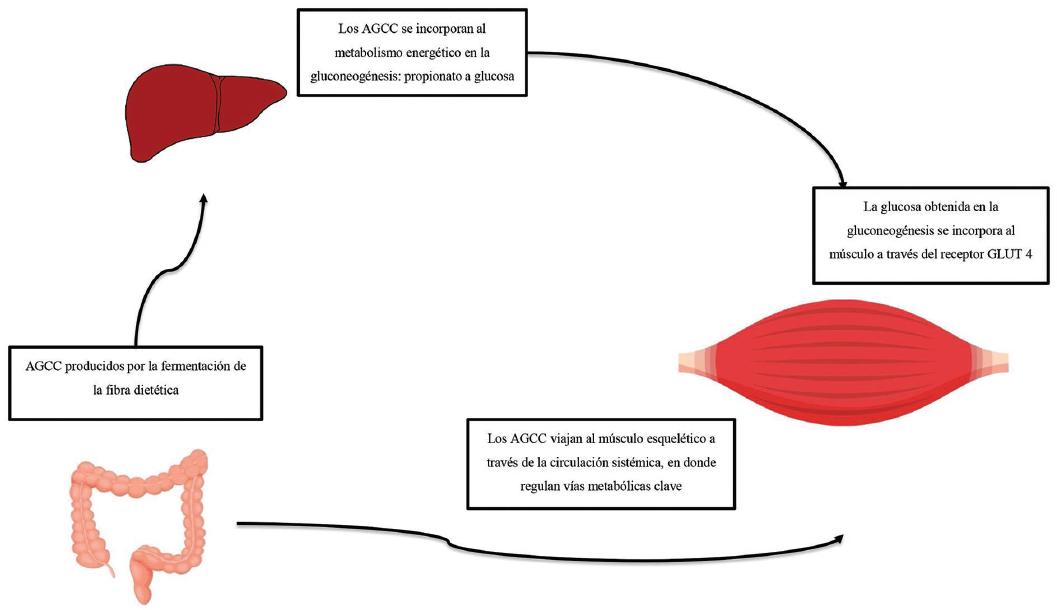
Figura 2 Cómo los probióticos están implicados en la homeostasis del músculo esquelético.13,23 AGCC: ácidos grasos de cadena corta; GLUT 4: transportador de glucosa tipo 4.
Los AGCC están implicados en el metabolismo muscular al mantener la homeostasis de la glucosa dentro de las células, así como regulando el metabolismo lipídico. La suplementación con acetato en ratones ha demostrado que aumenta la captación de glucosa por el músculo, favorece la formación de glucógeno y promueve la oxidación de ácidos grasos, disminuyendo el contenido lipídico de las células. Por otra parte, la administración exógena de butirato ha demostrado disminuir el estrés oxidativo, aumentar la función mitocondrial y favorecer la formación de fibras musculares de tipo I.24 La estimulación para la secreción del péptido similar al glucagón de tipo 1 (hormona que de forma indirecta regula los niveles de glucosa al promover la secreción de insulina), el incremento del flujo sanguíneo hacia los músculos, así como los efectos antiinflamatorios, son otras propiedades atribuidas a la suplementación con AGCC.25,26
El rol de los probióticos en la prevención del catabolismo muscular
Aunque se han identificado mecanismos que vinculan el intestino con el músculo, surge la pregunta de cómo los probióticos pueden utilizarse como estrategia terapéutica para abordar la pérdida progresiva de masa muscular asociada a la sarcopenia en adultos mayores. Aunque los probióticos no son una terapia única contra la sarcopenia, sus propiedades para mejorar la sensibilidad a la insulina, regular las vías metabólicas musculares y limitar la inflamación y el estrés oxidativo los convierten en un complemento valioso para otros tratamientos.27 Además, algunos probióticos tienen el aparente potencial de modular específicamente algunas funciones metabólicas. Por ejemplo, Lacticaseibacillus casei LC122 y Bifidobacterium longum BL986 han demostrado aumentar la masa muscular y la fuerza de agarre en modelos murinos jóvenes comparados con grupos control.28 Se comprobó que las dos especies bacterianas actúan por diferentes vías celulares: L. casei exhibió actividad antioxidante al incrementar las enzimas SOD y GPx en el músculo y el intestino, mientras que B. longum mostró un efecto antiinflamatorio al reducir citocinas proinflamatorias como el factor de necrosis tumoral alfa y las interleucinas 6 y 1β en el músculo y el colon (Fig. 3).28 Sin embargo, la eficiencia de los probióticos en la regulación del metabolismo muscular bajo condiciones de estrés sigue siendo incierta, tanto en modelos animales como en humanos.
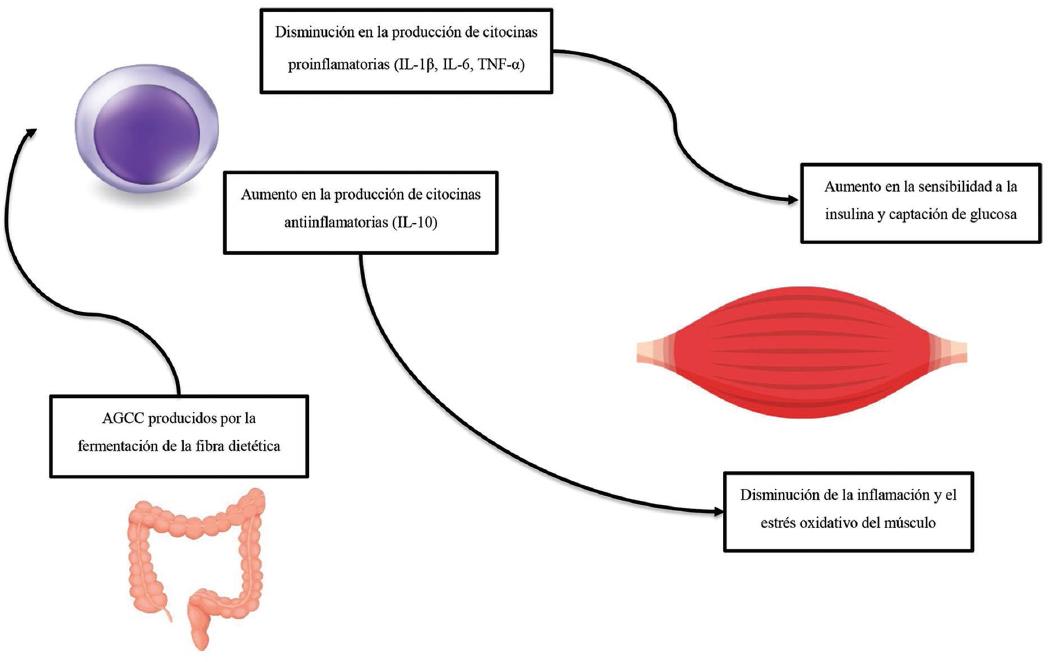
Figura 3 Interacción de la microbiota intestinal y el músculo esquelético, en el contexto de la inflamación.28 AGCC: ácidos grasos de cadena corta; IL: interleucina; TNF-α: factor de necrosis tumoral alfa.
Catabolismo muscular asociado a la edad en modelos animales
Diversos estudios han evaluado el efecto de la suplementación con probióticos en modelos murinos durante periodos variables. Se evaluó la suplementación con Limosilactobacillus reuteri ATCC-PTA6475 en ratones normales, analizando sus efectos sobre las características musculares y la esperanza de vida. La masa muscular, el tamaño de las fibras y la supervivencia de los animales aumentaron después del tratamiento con el probiótico cuando era ingerido durante un tiempo prolongado.29
Modelos murinos de envejecimiento acelerado inducidos por D-galactosa han permitido evaluar los efectos de los suplementos probióticos. En estos estudios se realizó una suplementación de 12 semanas con Lacticaseibacillus paracasei PS23 en ratones y se observó un incremento de la masa magra y de la fuerza muscular (fuerza de agarre). Esto se asoció con una mejora en el consumo de oxígeno en el músculo y en la biogénesis mitocondrial.30,31 En estos modelos, los mecanismos involucrados en el desarrollo muscular incluyen la estimulación de fibras por Factor de Crecimiento Similar a la Insulina tipo 1 (IGF-1), la activación de factores miogénicos, la regulación del estado energético muscular y la inhibición de la proteólisis y del estrés oxidativo.32 Además, se observó una reducción en la inflamación sistémica, evidenciada por el aumento de interleucina 10 plasmática y la disminución de citocinas proinflamatorias.32
El efecto de los probióticos en los estados catabólicos del músculo esquelético humano
A diferencia de los estudios en modelos murinos, la evidencia en humanos que relacione la microbiota intestinal con la preservación y el desarrollo musculares es limitada.
Los estudios disponibles en adultos mayores con síndrome de fragilidad, sarcopenia o cáncer muestran que la suplementación con probióticos reduce los microorganismos patogénicos en la microbiota intestinal.33,34 Además, algunos estudios han reportado un aumento en la citotoxicidad de las células NK y una mejora en el perfil de citocinas;35,36 sin embargo, no hay evidencia sólida sobre el impacto directo de los probióticos en el aumento o la preservación de la masa muscular en adultos mayores.37 Aun así, se cree que la diversidad y la composición de la microbiota tienen un potencial beneficio sobre el metabolismo del músculo esquelético, de forma indirecta, a través de la mejora en la respuesta inmunitaria y la diversificación de los microorganismos intestinales.
La heterogeneidad en el estado de salud y el estilo de vida de los adultos mayores puede influir significativamente en la respuesta a la suplementación con probióticos. Por lo anterior, la validez de los parámetros utilizados puede ser muy distinta, razón por la cual se requiere un método que permita determinar de una manera más efectiva el posible vínculo entre la composición de la microbiota intestinal y la preservación muscular en los humanos, por lo que este aspecto representa un área de oportunidad para futuras investigaciones.
Conclusiones
Los estudios en modelos experimentales han evidenciado una relación entre la microbiota intestinal y las células musculares esqueléticas, abriendo nuevas perspectivas para investigaciones en humanos. La suplementación con probióticos productores de AGCC ha mostrado eficacia en mejorar la función muscular en modelos de catabolismo inducido por el envejecimiento. Sin embargo, en los humanos los resultados son menos claros debido a la escasez de estudios, la variabilidad en el estado fisiológico de las poblaciones objetivo y la falta de métodos precisos para evaluar la función del músculo esquelético. Es posible que la respuesta a los probióticos en los humanos sea menos eficiente que en los modelos animales, lo cual requiere mayor estudio en investigaciones futuras.
La incorporación de prebióticos o de nutrientes específicos para las cepas utilizadas, junto con planes de alimentación y entrenamiento físico adaptados, podrían optimizar los efectos y aportar datos más precisos sobre el eje intestino-músculo.
La interacción de la microbiota intestinal y el músculo esquelético constituye una prometedora área de investigación en medicina. Explorar esta relación podría generar estrategias innovadoras para mejorar la salud de los adultos mayores, considerando las elevadas prevalencias de sarcopenia y de síndrome de fragilidad en esta población.











 nova página do texto(beta)
nova página do texto(beta)