Introducción
La vainilla (Vanilla planifolia Jacks.) es un cultivo originario de la región de Papantla localizada en la antigua región central-norte donde se encuentra ubicado hoy en día el estado de Veracruz. Datos más antiguos sugieren que el cultivo se encontraba disperso por la zona donde habitaron los Mayas conocida como Mesoamérica. Siendo Chiapas, Oaxaca, Veracruz, Quintana Roo, Belice y Guatemala las principales regiones reportadas (Lubinsky et al. 2008). Este cultivo se ha propagado a varias regiones del mundo por sus propiedades aromáticas, constituidas principalmente por el compuesto vainillina contenido en sus frutos. La vainilla se propaga clonalmente mediante esquejes, por lo que la variabilidad genética de las plantas es limitada, lo que dificulta el proceso de selección de los mejores genotipos que se adapten a las limitaciones abióticas y bióticas (Koyyappurath et al. 2015).
Entre los principales problemas que enfrenta el cultivo se encuentra el patógeno Fusarium oxysporum Schltdl., especie de amplia distribución listada entre los 10 hongos fitopatógenos más devastadores y de importancia económica en el mundo (Zhang y Ma 2017). En vainilla, F. oxysporum f. sp. vanillae (Fov) es el causante de la pudrición de raíz y tallo, que comienza con la generación de lesiones de color café y la muerte de las raíces subterráneas y aéreas, marchitez de hojas y tallo, y eventualmente ocurre el colapso total de la planta (Koyyappurath et al. 2015, Adame-García et al. 2016). En 2020, en la localidad Mesa de Guadalupe, Veracruz, México, el patógeno ocasionó la muerte de al menos el 95 % de las plantas de un cultivo intensivo bajo malla sombra.
Se ha indicado que la temperatura óptima de crecimiento para Fusarium spp. es de 25 a 28 °C (Nelson et al. 1981) y que F. oxysporum f. sp. vanillae presenta un buen desarrollo en el intervalo entre 20 y 30 °C, con un punto óptimo establecido a 25 °C (Gangadhara et al. 2010). Siendo la temperatura uno de los principales factores ambientales al cual se le atribuye ser detonante para el desarrollo de la enfermedad, por su coincidencia con las condiciones favorables para el cultivo de vainilla comprendidos entre 20 y 30 °C y humedad relativa sobre el 70 % (Hernández-Hernández 2011). La alta susceptibilidad de V. planifolia a Fov (cepa M21C5) a temperaturas desde 25 a 35 °C fue confirmada por Barreda-Castillo et al. (2022).
Sin embargo, surge la interrogante de cómo la amplia diversidad genética entre los aislados de F. oxysporum obtenidos a partir de V. planifolia reportada por Adame-García et al. (2015), Flores-de la Rosa et al. (2018) y González-Oviedo et al. (2022) responde a gradientes de temperatura, ante los escenarios fitosanitarios que se están generando para los agrosistemas en consecuencia del cambio climático. Para tal fin, en el presente trabajo se evaluaron aspectos del desarrollo in vitro de cepas de F. oxysporum con diversa capacidad patógena en V. planifolia, ante un gradiente térmico entre 23 y 32 ºC. Para la selección de este gradiente se tuvo en consideración, que por encima de los 32 °C las plantas de vainilla comienzan a manifestar otras alteraciones fisiológicas. Donde no solo interviene el factor temperatura sino también la humedad, estas son: amarillamiento, pérdida de viabilidad de polen y caída de frutos (Hernández-Hernández 2011, INIFAP 2016).
Materiales y métodos
Selección del material biológico
Se eligieron seis cepas de F. oxysporum con base en su capacidad patogénica: dos altamente patógenas (JAGH3 y N9), dos moderadamente patógenas (28R1 y V7M) y dos no patógenas (H2 y M22C2). Las cepas se aislaron a partir de Vanilla sp. de los estados de Veracruz, Nayarit y Oaxaca en México, y pertenecen a la colección del grupo de investigación sobre Fusarium del Laboratorio de Genética e Interacciones Planta Microorganismos de la Facultad de Ciencias Agrícolas de la Universidad Veracruzana.
Pruebas de patogenicidad de Fusarium oxysporum aisladas de Vanilla planifolia
Las cepas de F. oxysporum se reactivaron en medio agar papa dextrosa (PDA) incubadas a 27 ºC durante 7 días y se ratificó la capacidad patogénica de las cepas en hojas de V. planifolia en un período de 13 días de acuerdo con Solano-de la Cruz et al. (2019). Para ello, cada hoja de vainilla fue desinfectada mediante lavados con solución de detergente durante 10 min, enjuagues con agua estéril e inmersión en solución de cloro de uso doméstico (10 gotas por litro) durante 5 minutos, finalmente, enjuagues con abundante agua estéril. Este procedimiento se realizó en dos ocasiones. Después de la desinfección, se hizo una incisión no mayor a 5 mm sobre el haz de cada hoja con la punta de un bisturí estéril, donde se colocó una porción (≈3x3 mm) de agar con micelio de F. oxysporum, según la cepa en estudio. Cada hoja se colocó en una cámara húmeda individualmente y se mantuvo a 25 - 26 °C por 13 días, con observaciones cada 48 horas. La capacidad patogénica de cada cepa fue evaluada en dos bioensayos independientes. Los criterios para la clasificación de las cepas en patógenas (CP), moderadamente patogénicas (CMP) y no patógenas (CNP) se establecieron a partir del área dañada de la hoja con relación al tiempo (días) de la infección.
Preparación del inóculo
Para inducir la esporulación, las cepas de F. oxysporum se cultivaron en medio PDA y se incubaron a 27 ºC ± 1°C durante 15 días. Una vez concluido el tiempo de incubación se obtuvieron las esporas al agregar 4 mL de agua destilada estéril sobre el micelio, provocando inundación en toda la zona de crecimiento del hongo. Se extrajeron 0.8 mL de la suspensión y se colocaron en una “columna de filtración” estéril elaborada con un tubo de microcentrifugación de 1.5 mL con el fondo escindido, que en el interior contenía una membrana de algodón. Para la centrifugación, la columna de filtración se introdujo en un tubo de microcentifugación de 1.5 mL estéril y se aplicaron 10 000 rpm durante 5 min. A continuación, se retiró el sobrenadante y el precipitado (esporas) se resuspendió con 3 mL de agua destilada estéril. Se cuantificó el número de esporas utilizando la cámara de Neubauer y posteriormente se preparó una suspensión de esporas a 1×106 UFC x mL-1.
Desarrollo de F. oxysporum ante el gradiente térmico
Para evaluar el desarrollo de las cepas se cuantificó la biomasa por peso seco y se analizó la formación de esporas. Para ello, se establecieron cultivos en matraces Erlenmeyer de 250 mL en medio líquido formulado con 50 mL de caldo papa dextrosa adicionado con 5 µL de la suspensión de esporas (1×106 células/ mL) de cada cepa de F. oxysporum en estudio. Los cultivos se incubaron durante 15 días a temperatura constante, según el valor evaluado (23, 25, 28, 30 y 32 °C). Se emplearon cinco réplicas para cada cepa por cada temperatura evaluada. Las incubadoras microbiológicas usadas para las pruebas se calibraron mediante mediciones diarias con termómetros de mercurio calibrados durante un mes previo al desarrollo de las pruebas. La temperatura se monitoreó diariamente durante los bioensayos. A los 15 días de incubación se retiró 1 mL de medio de cada cultivo para realizar el conteo de esporas en cámara de NeuBauer; el volumen restante del cultivo se filtró al vacío con membranas de celulosa F1091chm. Previamente, se determinó el peso constante de cada pieza de membrana de filtración a 80 °C. El valor de la biomasa se obtuvo al calcular la diferencia entre el peso seco de la membrana de filtración con el micelio y el peso inicial de la membrana de filtración. Para cada temperatura evaluada se incorporó un tratamiento control de esterilidad del medio de cultivo que consistió en caldo papa dextrosa sin inóculo fúngico.
Análisis Estadístico
Se empleó un diseño completamente al azar estructurado con cinco valores de temperatura (23, 25, 28, 30 y 32 °C) para cada cepa evaluada, con cinco réplicas para el análisis del peso seco del micelio y tres réplicas para el número de esporas. Para determinar las diferencias entre los tratamientos se aplicó ANOVA de una vía y la prueba post hoc Tukey (P=0.05) cuando los datos cumplieron los supuestos de normalidad y homogeneidad de las varianzas. Los datos que no cumplieron estos supuestos fueron analizados por la prueba no paramétrica de Kruskal Wallis. Los análisis se desarrollaron con el software InfoStat versión 2020.
Resultados
Pruebas de patogenicidad realizadas en hojas de Vanilla planifolia
Se seleccionaron seis cepas en cuanto al grado de patogenicidad mostrado en hojas de V. planifolia. Aquellas cepas que al pasar los 13 días de evaluación no mostraron daño a la hoja y estas permanecieron verdes y turgentes se clasificaron en no patógenas, por su parte aquellas que mostraron un daño moderado comenzando la necrosis a los 9 días se clasificaron en cepas moderadamente patógenicas y aquellas que mostraron un daño acelerado a la hoja desde el día siete se clasificaron en cepas altamente patógenas (Figura 1).
Desarrollo de F. oxysporum ante el gradiente térmico
Se encontraron diferencias significativas (P<0.05) en el desarrollo de biomasa de las cepas de F. oxysporum N9, 28R1, V7M, H2 y M22C2 en el gradiente térmico evaluado, sin importar su carácter patogénico (Figura 2). Particularmente, cinco de las seis cepas tuvieron su punto óptimo de desarrollo entre 28 y 30 °C al alcanzar los valores mayores de biomasa. Temperaturas de 25 y 32 °C fueron menos favorables para la producción de micelio. Un caso extraordinario lo constituye la cepa JAGH3 (altamente patogénica) que mantuvo la producción de biomasa sin diferencias significativas en todas las temperaturas evaluadas (Figura 2F).
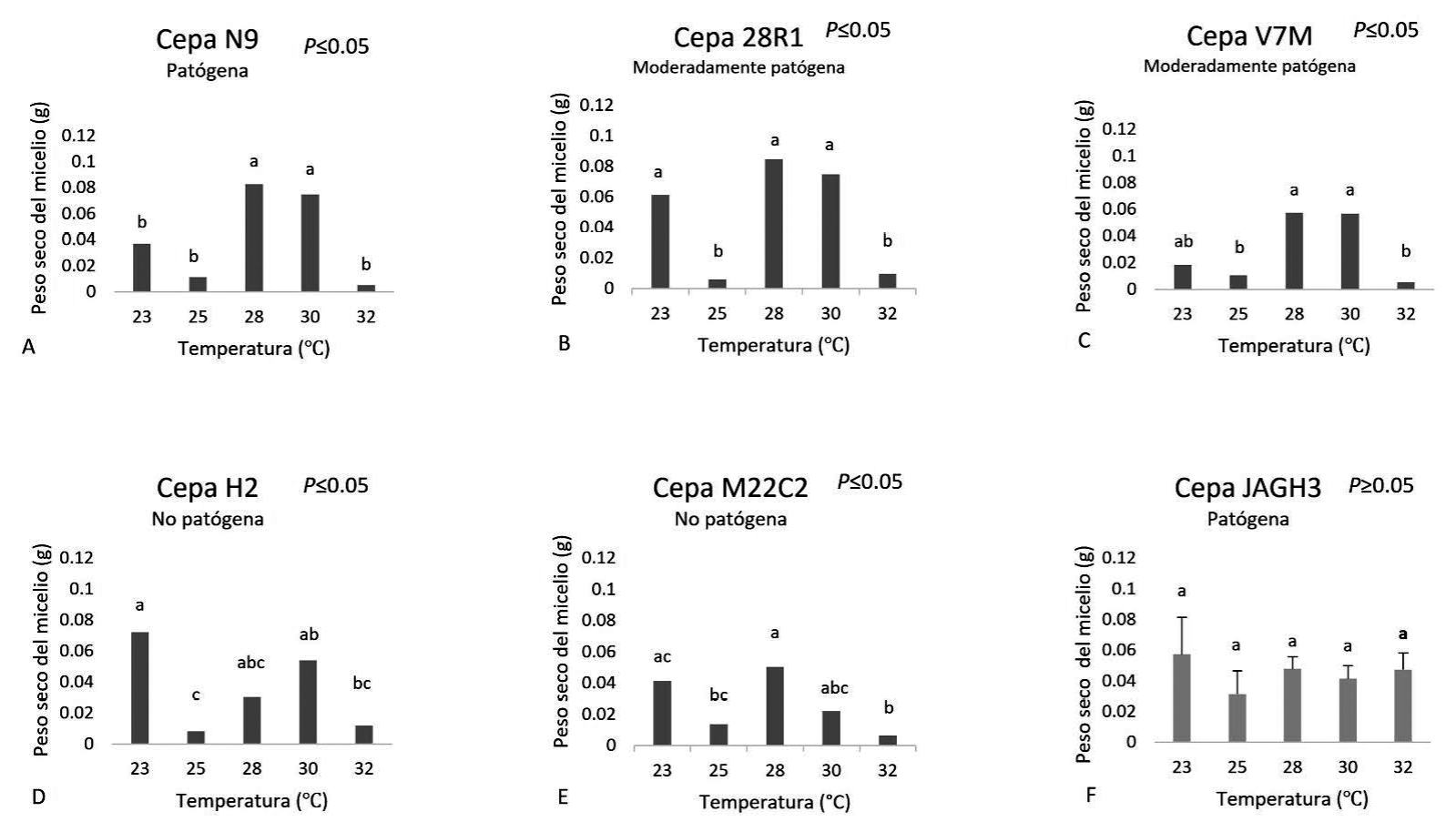
Figura 2 Peso seco del micelio (biomasa) de las cepas N9 (A), 28R1 (B), V7M (C), H2 (D), M22C2 (E) y JAGH3 (F) de F. oxysporum endófito de Vanillae sp. desarrolladas a 23, 25, 28, 30 y 32 °C en caldo papa dextrosa durante 15 días. Letras diferentes sobre las barras indican diferencias significativas entre los tratamientos (A, B, C, D y E, Kruskal Wallis, P ≤ 0.05; F, Tukey, P ≤ 0.05).
La producción de esporas mostró diferencias con significancia estadística para cinco de las cepas ante el gradiente térmico. De manera general, se observó que la producción de esporas se estimuló a 23 y 32 °C, y que la producción más baja se obtuvo entre los 28 y 30 °C (Figura 3). La cepa N9 se diferenció del resto de las cepas por generar mayor número de esporas a 25 y 32 °C.
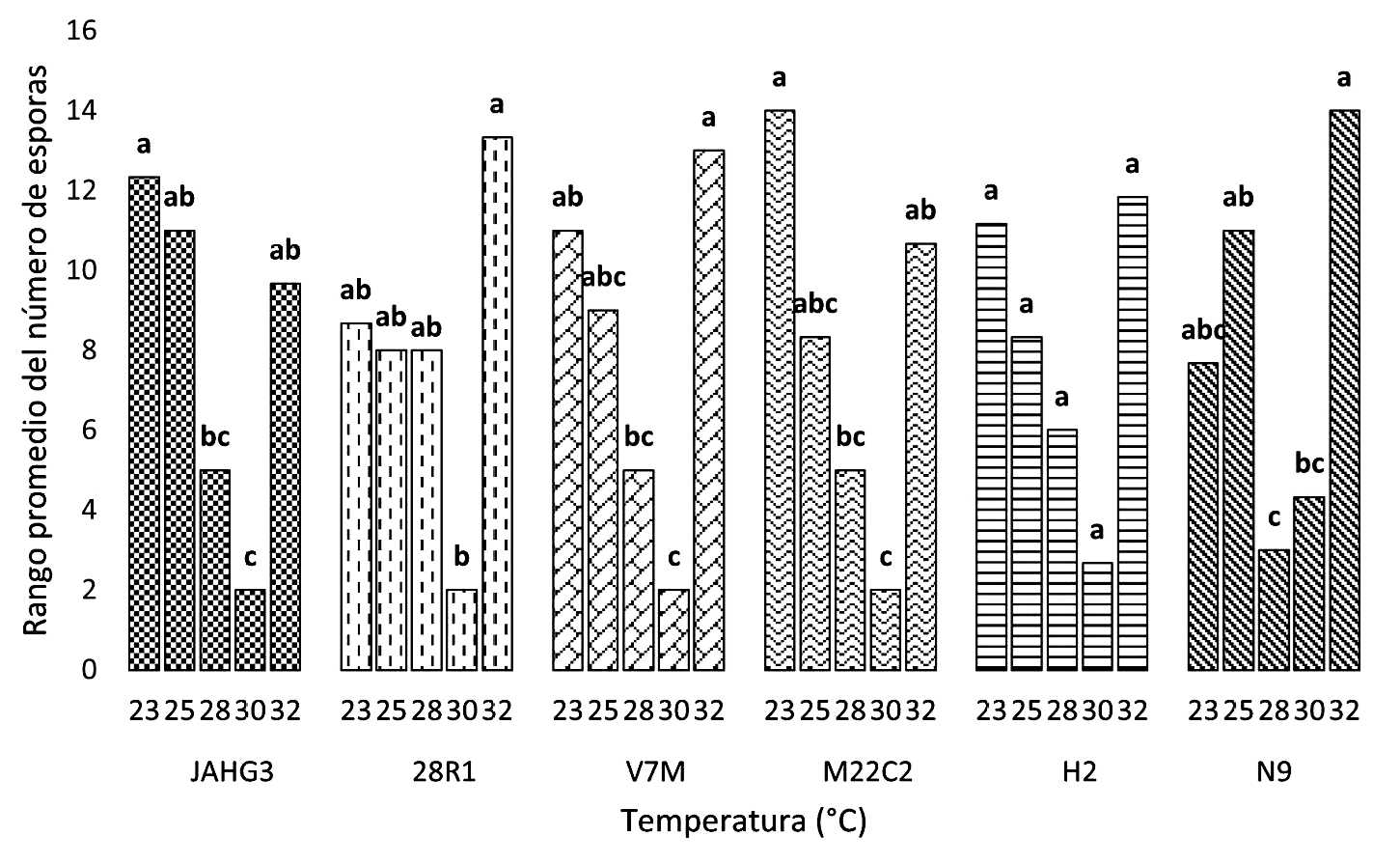
Figura 3 Número de esporas de las cepas de F. oxysporum N9, 28R1, V7M, H2, M22C2 y JAGH3 desarrolladas a 23, 25, 28, 30 y 32 °C en caldo papa dextrosa durante 15 días. Letras diferentes sobre las barras en un mismo grupo indican diferencias significativas entre los tratamientos Kruskal Wallis, P ≤ 0.05.
Discusión
La temperatura es un factor importante en el desarrollo de todo microorganismo, a medida que la temperatura disminuye o aumenta a partir del punto óptimo, los microorganismos disminuyen la velocidad a la que se desarrollan. En este estudio se observó que cinco de las seis cepas evaluadas tuvieron limitaciones en el desarrollo del micelio a 25 °C, por lo que se tienen elementos para proponer que, de manera general, las variantes de F. oxysporum aislados de V. planifolia, tienen un punto óptimo de desarrollo in vitro entre 28 y 30 ºC, sin importar el carácter patogénico, lo cual, en cierto grado difiere de la propuesta de Nelson et al. (1981) para el género y en mayor grado a la propuesta de Gangadhara et al. (2010) para F. oxysporum f. sp. vanillae quienes establecen el punto óptimo a 25 ºC.
Resultados similares de inhibición del crecimiento del micelio a 25 °C y estimulación a 30 °C fueron obtenidos por Veneros-Terrones et al. (2017) para el crecimiento in vitro de F. oxysporum ante el gradiente térmico de 8, 17, 25, 30 y 40 °C. Por su parte, Ezrari et al. (2021) encontraron que los cultivos de F. oxysporum y F. solani se desarrollaron mejor a 30 °C, al evaluar un rango térmico desde 5 a 40 °C. En formas especiales de F. oxysporum se ha comprobado un comportamiento distinto, Santamarina et al. (2003) determinaron que F. oxysporum f. sp. lycopersici tuvo mayor crecimiento a 25 °C, tal como se ha propuesto para especies como F. equiseti y F. brachygibbosum (Ezrari et al. 2021).
El comportamiento característico mostrado por la cepa JAGH3, que no tuvo limitaciones en su desarrollo a 32 ºC, demostró que existen cepas capaces de desarrollarse a temperaturas fuera del rango óptimo de crecimiento, como lo indicaron Ezrari et al. (2021), al observar que cepas de Fusarium sp. resultaron tolerantes a 35 °C con crecimiento óptimo del micelio a 30 °C. El hecho de que existan cepas de alta capacidad patogénica, aptas para tener un crecimiento normal a temperaturas superiores al punto óptimo, como lo demostró la cepa JAGH3, tiene importantes implicaciones sobre el cultivo de vainilla. Teniendo en cuenta que, en combinación con el incremento de la temperatura ambiental debido al cambio climático, puede representar un peligro potencial, considerando las alteraciones fisiológicas que presenta V. planifolia a temperaturas mayores de 32 ºC. Entre ellas se encuentran el amarillamiento reportado por Hernández-Hernández (2011) y la afectación del desarrollo de raíces reportado por Barreda-Castillo et al. (2022).
En este estudio se encontró discrepancia respecto a la declaración de Ramos-Quintana et al. (2017), quienes indicaron que a temperaturas mayores de 30 ºC se inhibe el desarrollo de Fov, sugiriendo a la vez, que hay menor probabilidad de que mantenga la capacidad de causar enfermedad. En este sentido, un estudio sobre el comportamiento de la patogenicidad de Fov en V. planifolia ante el gradiente térmico de 25, 30 y 35 °C demostró que a 25 y 30 °C el patógeno afecta considerablemente las plantas, hasta causar la muerte en el transcurso de 60 días y que a 35 °C las plantas no murieron, pero se provocó daño en el 50 % de la raíz, por lo que se postuló que la capacidad del patógeno persiste aún a temperaturas fuera de su rango óptimo de desarrollo (Barreda-Castillo et al. 2022). La generación de esporas es una estrategia de supervivencia de los hongos al estar limitados o en peligro. Entre los factores implicados en la esporulación se encuentran la temperatura, la actividad del agua y su interacción en el tiempo (Camardo et al. 2018). Se ha demostrado que valores de temperatura fuera del punto óptimo inducen una mayor esporulación en cultivos mixtos que en cultivos puros (Chauvet et al. 1998), sugiriendo que la respuesta de los hongos a la temperatura en condiciones naturales podría ser aún más compleja.
Conclusiones
Fusarium oxysporum f. sp. vanillae se desarrolla de forma óptima a 28 y 30 ºC en condiciones in vitro, con mayor esporulación a 23 y 32 ºC. En nuestro estudio se observó que sin importar el carácter patogénico las cepas se desarrollaron abundantemente ante estas temperaturas y excepcionalmente una cepa altamente patógena (JAGH3) creció sin diferencias estadísticas en todo el gradiente térmico probado. Por lo que se puede concluir que no se encontró una relación entre la patogenicidad y la adaptabilidad a las diferentes temperaturas.
La diversidad genética reportada para el patógeno contribuye a la existencia de cepas con alta capacidad patogénica aptas para crecer de manera normal a temperaturas superiores al punto óptimo, lo que genera interrogantes en relación con los beneficios que obtienen los individuos que presentan esta cualidad y su impacto en los cultivos de vainilla, bajo las proyecciones del incremento en la temperatura de los agrosistemas debido al cambio climático.











 nueva página del texto (beta)
nueva página del texto (beta)




