ANTECEDENTES
Lophomona spp es un protozoario, familia Excavata, clase Parabasalia, subespecie blattarum,1 es la única con capacidad de infestar al humano.2 Morfológicamente se presenta como trofozoito de forma piriforme, mide 20-60 micras de largo; en la parte anterior se insertan los flagelos cortos y abundantes, irregulares y proporcionan la movilidad, y en su forma quística que es circular u ovoidal, cuenta con abundantes membranas.3,4 Se alberga en el aparato digestivo de sus comensales, termitas y cucarachas.1,2,5,6 Se elimina en heces del portador, y entran en contacto con los humanos infectando la vía respiratoria por inhalación en forma de polvo 2. El primer caso fue reportado en China en 1993, y desde entonces se han reportado 307 casos a nivel mundial; el 75% de estos han sido en China y el resto en otros países, en México sólo se ha reportado 1 caso.7,8,9
Los síntomas mayormente descritos son: tos crónica con expectoración hemoptoica y fiebre.10 La similitud clínica que tiene con otras patologías respiratorias, como el asma, enfermedad pulmonar obstructiva crónica (EPOC), contribuye con el retraso diagnóstico y por ende su tratamiento. Los diagnósticos diferenciales son asma, neumonía y abscesos pulmonares.12 En pacientes con asma, existe mayor riesgo de infección por Lophomona blattarum, una de las hipótesis es el uso de esteroides inhalados que mantiene en inmunosupresión al paciente.11 Según Mizzazadeh F, et al,11 las proteasas producidas por el protozoario generan daño al epitelio bronquial y consecuentemente la sintomatología.
Infesta principalmente pacientes inmunosuprimidos, sin embargo, puede infestar pacientes sanos, como lo reportó Tyagi y cols en India y Bakshaee y cols en Irán.12,13
REPORTE DE CASO
Paciente masculino de 30 años de edad, sin antecedentes personales patológicos, que presenta padecimiento de 6 meses de evolución con tos húmeda en accesos, expectoración hemoptoica y disfonía, se le indicó antibioticoterapia sin mejoría clínica. Se agrega a la sintomatología fiebre de 40°C, y acude con médico neumólogo quien reporta en la exploración física estertores crepitantes anteriores en hemitórax derecho. Los estudios de laboratorio solicitados fueron cultivo bacteriano, cultivo para hongos con desarrollo abundante de Cándida spp, reacción en cadena de la polimerasa (PCR) para Mycobacterium tuberculosis y baciloscopia seriada; en estudios de gabinete se reportó en la radiografía de tórax opacidad parahiliar derecha y en la tomografía axial computarizada (TAC) cavitación en lóbulo superior derecho, llenado perilesional y en lóbulo medio nódulos en árbol de gemación bilateral de predominio derecho (el Cuadro 1 muestra los resultados de laboratorios y la Figura 1 los estudios de gabinete).
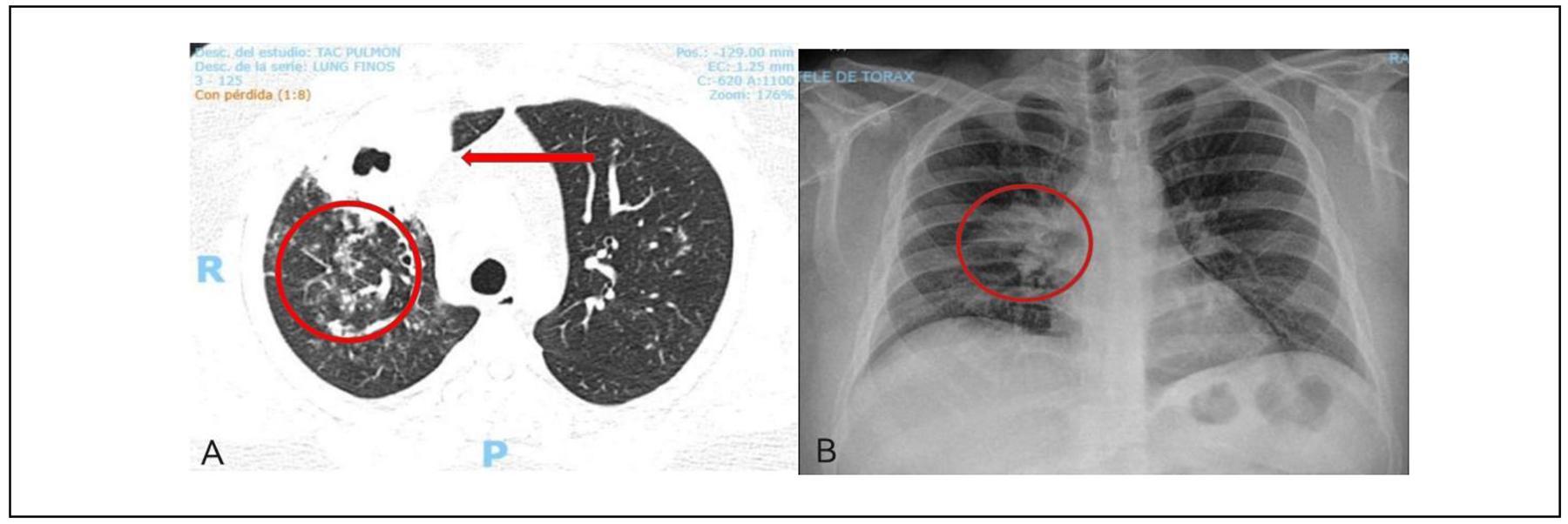
Figura 1. A) Tomografía Computarizada de tórax en donde se aprecia la cavitación en el lóbulo superior derecho con espesor de pared de 9 mm, así como medida transversal y de altura de 36 x 60 x 36 mm y media de 8 x 14 mm (flecha roja). Nódulos en árbol de gemación (círculo rojo). B) Radiografía de tórax con opacidad parahiliar derecha de morfología ovalada, con diámetro máximo de 4 cm (Círculo rojo).
Cuadro 1. Estudios de laboratorio del paciente. Cultivos de bacterias y hongos, PCR contra Mycobacterium tuberculosis y BAAR seriado: 22 de junio de 2023. Resto de los laboratorios solicitados en julio de 2023.
|
Cultivos de expectoración (en esputo) | |
| Bacteriológico | Microorganismos aislados: a) Streptococcus parasanguinis b) Streptococcus parabasalis c) Staphylococcus aureus Desarrollo escaso. |
| Hongos | Filamentosos: sin desarrollo. Levaduriformes: desarrollo abundante de Cándida albicans. |
| Detección de Mycobacterium tuberculosis por PCR (expectoración) | Sin observación |
| BAAR (baciloscopia, 3 muestras) | Sin observación de bacilos ácido alcohol resistentes. Células polimorfonucleares abundantes. Levaduras/hifas escasas. |
|
Biometría hemática | |
| Hemoglobina | 13.2 g/dL |
| Hematocrito | 41.3% |
| Plaquetas | 264.00 mcL |
| Leucocitos | 11,600 mcL |
| Neutrófilos | 68% (7,900 mcL) |
| Linfocitos | 23.5% (2700 mcL) |
| Eosinófilos | 0.5% (70 mcL) |
|
Química sanguínea | |
| Glucosa | 100 mg/dL |
| Urea | 38.5 mg/dl |
| Creatinina | 1.09 mg/dL |
|
Tiempos de coagulación | |
| Tiempos de protrombina | 10.4 seg |
| INR | 0.94 |
| Tiempo parcial de tromboplastina | 22.5 seg |
|
Quantiferón TB Gold | |
| Quantiferón TB Gold | Negativo |
| AG TB1 | 0.0 UI/mL |
| AG TB2 | 0.02 UI/mL |
| Mitógeno | >10 UI/mL |
| NIL | 0.08 UI/mL |
|
Anticuerpos anti-Aspergillus | |
| IgE específica Aspergillus niger | Negativo |
| IgG Aspergillus fumigatus | Negativo |
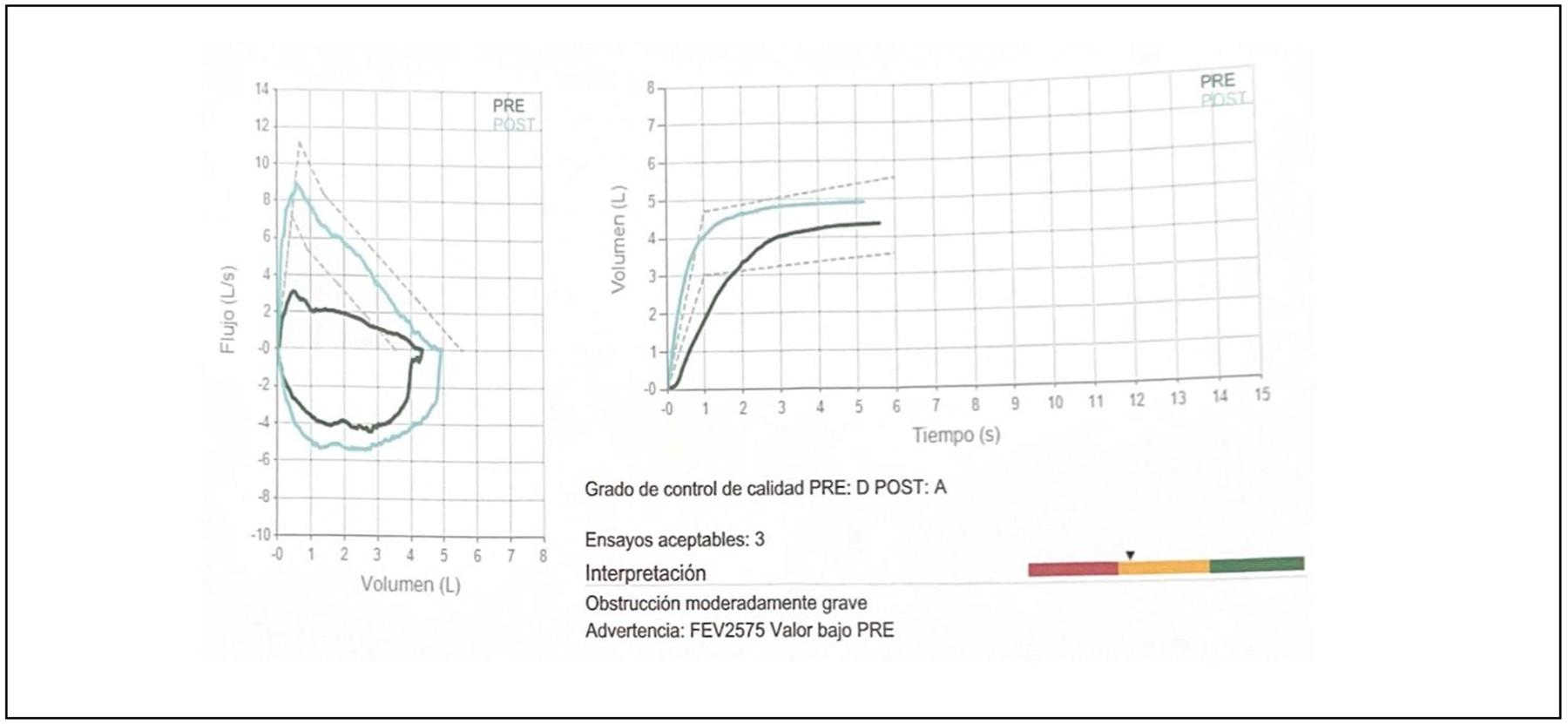
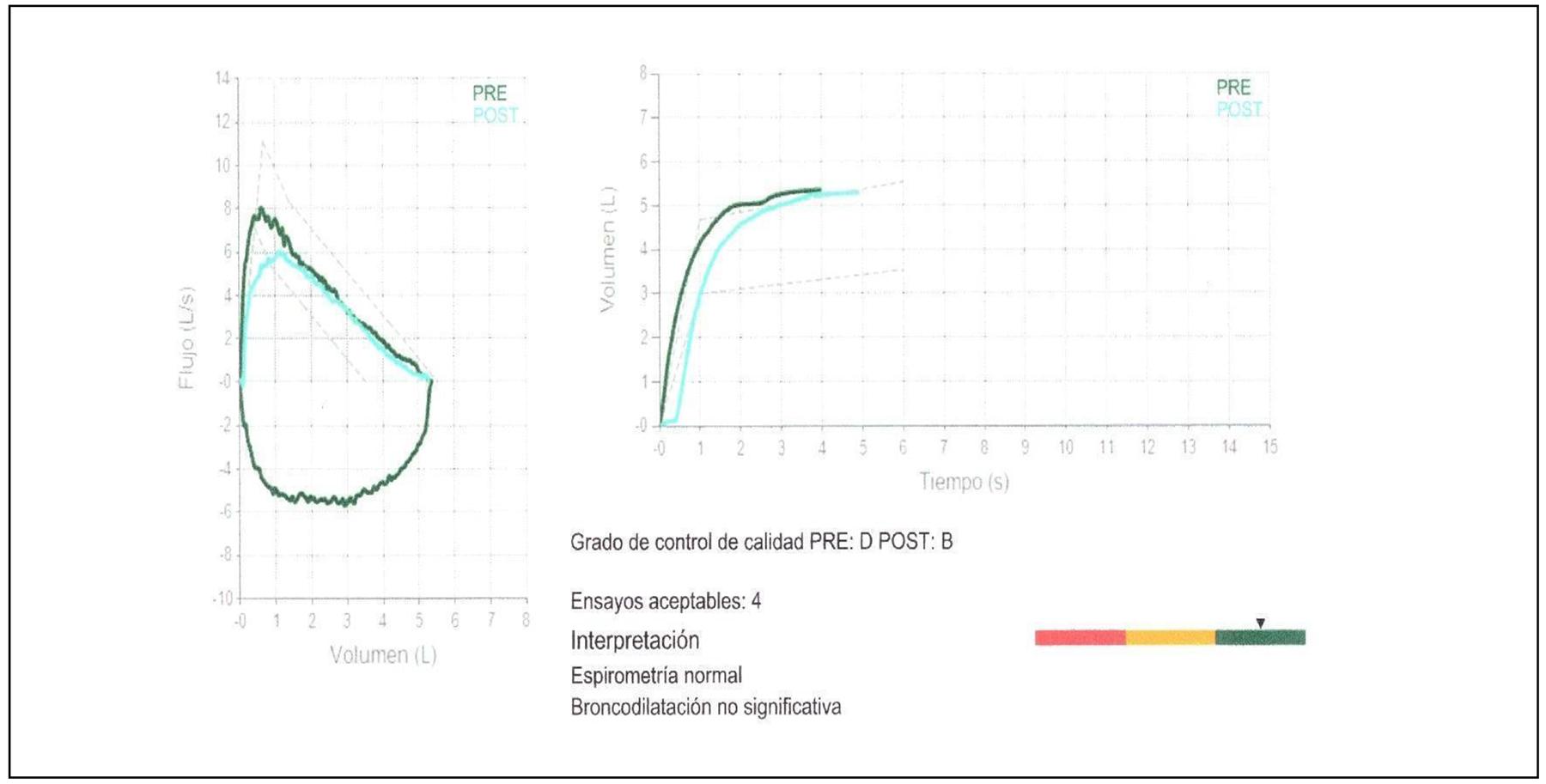
Es diagnosticado con neumonía adquirida en la comunidad e inicia antibioticoterapia, sin mejoría clínica, no se considera de importancia el inicio de antifúngico por médico tratante. Se inicia tratamiento con glucocorticoide inhalado (GCI), prednisona, acetilcisteína, broncodilatador de acción corta (BDAC) nebulizado y fisioterapia pulmonar, con mejoría parcial. Se detectó en la exploración física hipoventilación difusa en hemitórax derecho con presencia de estertores gruesos. Se realiza broncoscopia con lavado bronquial del lóbulo superior derecho y se encuentra mucosa edematosa, eritematosa, friable, con abundante secreción bronquial no purulenta. Se envían muestras para cultivo de bacterias y hongos y observación en fresco con tinción de lugol y azul de metileno y se identifica al protozoario Lophomonas blattarum, por lo que se diagnóstica lofomoniasis pulmonar. Inicia tratamiento con metronidazol tabletas de 500 mg durante 1 mes, persiste la tos húmeda. 6 meses después presenta expectoración hemoptoica y se repite la broncoscopia con lavado bronquial, que evidencia Lophomonas blattarum y repite tratamiento con metronidazol durante 1 mes con mejoría clínica. 7 meses después acude con médico alergólogo por persistencia de la tos, ahora seca e intermitente. La exploración física es normal. Se realiza espirometría que mostró patrón obstructivo moderado, la prueba de reversibilidad con salbutamol fue significativa. Es tratado con corticosteroide oral y BDAC por 10 días. Acude a su cita de control refiriendo remisión de la sintomatología y se ajusta el tratamiento a broncodilatador de acción prolongada con GCI (fumarato de formoterol/dipropionato de beclometasona 6 mcg/100 mcg). Al mes, persiste asintomático con mismo esquema de tratamiento. Un año después acude a consulta de seguimiento sin sintomatología y se realizan pruebas de control basadas en espirometría, que se reporta normal sin broncodilatación significativa; pruebas cutáneas a aeroalergenos positivas para alfalfa (+4), salsola kali (+3), mezcla de 6 gramíneas (+3); Fracción Exhalada de Óxido Nítrico (FeNO) con resultado de 17 ppm (NIOX-vero). Se cita anualmente a consulta para evaluación de su evolución.
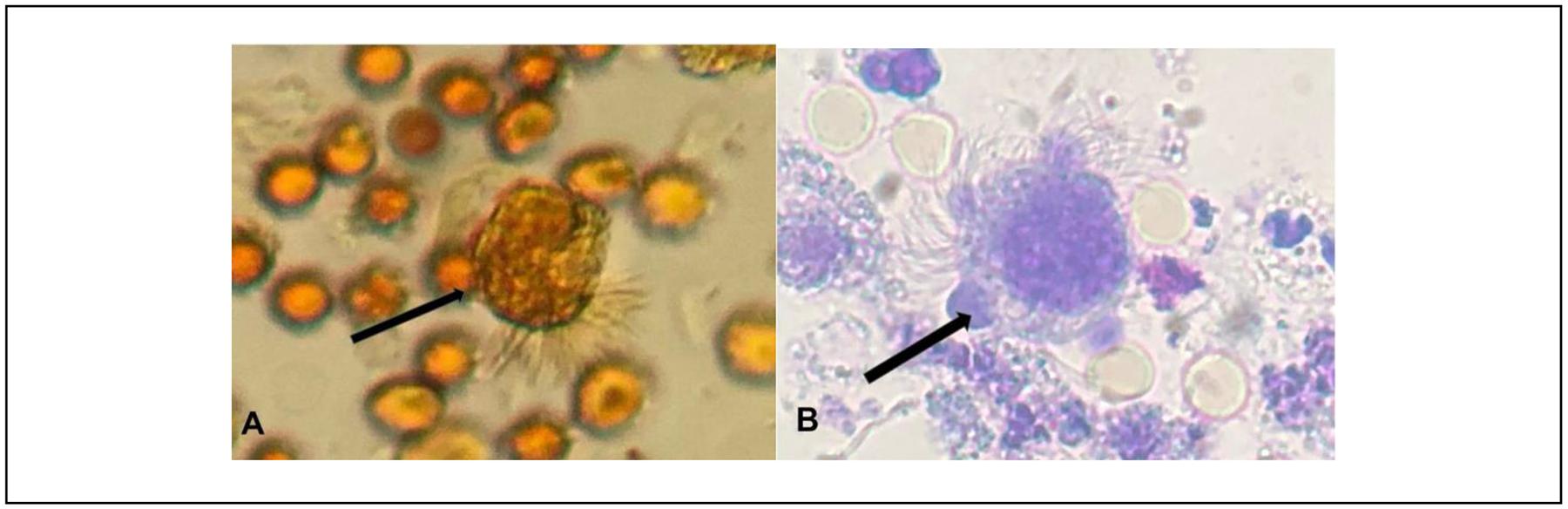
Figura 2. Identificación de Lophomona blattarum en material de lavado bronquial. A.Tinción de Lugol B.Tinción de azul de metileno. (Señalado con flechas negras).
Hallazgos clínicos clave
Broncoscopia con lavado bronquial: el material obtenido se estudió con microscopía simple con tinción de lugol y azul de metileno identificándose el protozoario Lophomona blattarum.
Espirometría: reportando patrón obstructivo moderado. Figuras 3 y 4
DISCUSIÓN
En este reporte de caso se presenta la infestación pulmonar por Lophomona blattarum en paciente sano y las complicaciones que causa en el epitelio respiratorio. En pacientes con enfermedades respiratorias subyacentes, como el asma, la característica son las exacerbaciones por el daño ya existente, los mecanismos que explican su mayor susceptibilidad aún no se esclarecen completamente.11 La fisiopatología del asma, con la liberación de distintas alarminas como TSLP (Linfopoyetina del estroma tímico), IL-25 e IL-33, que conlleva a una cascada de citocinas proinflamatorias, son las responsables de la aparición de los síntomas como la obstrucción del flujo aéreo por el aumento de la secreción de las glándulas mucosas, tos e hiperreactividad bronquial, todas ellas presentes en la lofomoniasis pulmonar.14,15 Van Woerden y cols.16 se han planteado que la inmunosupresión causada por GCI aumenta la susceptibilidad a las infecciones, sin embargo, esto no ha podido corroborarse.16
El diagnóstico se hace con la visualización directa del parásito por medio de microscopio de luz, teñido con diferentes técnicas; en nuestro paciente la confirmación diagnóstica se realizó utilizando las técnicas de lugol y azul de metileno.17 Otras tinciones que pueden utilizarse son la tricrómica de Weathley, de Papanicolau, y de Giemsa.18 La identificación del parásito puede prestarse a confusión ya que posee características morfológicas que son similares a células del epitelio respiratorio, pudiendo esto retrasar el inicio oportuno del tratamiento; si bien la mayoría de los pacientes evoluciona favorablemente con el tratamiento antiparasitario, en ciertos casos puede asociarse con desenlaces fatales.4,19,20,21 Alam-Eldin y cols, muestran en forma de cuadro comparativo las características de ambos para ayudar a diferenciarlas (Cuadro 2)18 Se ha reportado en la literatura aumento de los eosinófilos en la citometría hemática de los paciente con el padecimiento, se plantea la hipótesis de que aumentan con las infecciones parasitarias, encontrándose en pacientes inmunosuprimidos e inmunocompetentes.9,22,23,24,25
Cuadro 2. Descripción de las características de Lophomona blattarum y las células ciliadas del epitelio respiratorio. Alam-Eldin Y y cols.18 (Cuadro modificado).
| Características | Lophomonas b. | Células bronquiales |
|---|---|---|
| Tamaño | 20-35 micras | Mayor a 20 micras |
| Forma | Piriforme, redondeada u oval. | Columnar |
| Citoplasma | Gránulos citoplasmáticos y vacuolas. | Transparente |
| Núcleo | Vesicular, no visible fácilmente. | Núcleo localizado a nivel basal, con cromatina granular fina. |
| Flagelo/cilios | Larga Ondulada Varía en tamaño. No hay presencia de barra terminal En alguno de los extremos del protozoario. Movimiento en ondas que realiza la función de movimiento activo del parásito a la apreciación en microscopio. |
Corto Recto Tamaño uniforme. Barra terminal gruesa. En el borde luminal de la célula. Movimientos coordinados y sincrónicos que no realizan movimiento activo en las células a la apreciación en microscopio. |
Para explicar la fisiopatología del daño al epitelio respiratorio ocasionado por Lophomona blattarum se manejan dos hipótesis. La primera está basada en el mecanismo de daño mayormente estudiado en Acanthamoeba spp, centrándose en los receptores activados por proteasa (PAR’s, por sus siglas en inglés Protease-activated receptors) y culmina con la liberación de citocinas inflamatorias (IL-6, IL-8) que provocan el daño.26 La segunda hipótesis se enfoca en la barrera epitelial respiratoria con una alteración preexistente que conlleva a una descamación y denudación de las células, finalizado con la activación de la cascada inflamatoria y perpetúa el daño epitelial.26,27 Martínez-Girón y cols,26 refieren que existe una relación con la activación de los receptores PAR y el asma, específicamente los PAR-2, que se activan no sólo por la actividad de la Lophomona blattarum, sino que se encuentran activos previamente por el mecanismo inflamatorio del asma, amplificando la permeabilidad vascular, el reclutamiento de leucocitos y culminan en hiperreactividad bronquial aumentada. A su vez, el aumento de la producción de IL-8 y cisteínas contribuyen al daño epitelial, perpetuando la activación de citocinas inflamatorias.26
El fármaco indicado es metronidazol en dosis de 500 mg vía oral cada 8 horas durante 20-30 días en pacientes de más de 40 kilogramos de peso.28 Dependiendo de la gravedad se puede administrar vía intravenosa con dosis inicial de 15 mg/kg/hr y de mantenimiento 7.5 mg/kg cada 6 horas, como se reporta en el caso por Tyagi y cols.12,29 En un estudio publicado en Irán por Nasseri y cols30 reporta que los pacientes podrían beneficiarse del uso de tinidazol, sin embargo sus efectos adversos son frecuentes debido a las dosis altas que se requiere.30 En nuestro caso, la erradicación de Lophomona blattarum fue exitosa en la segunda administración del tratamiento con metronidazol, sin embargo, requirió manejo con GCI para los síntomas bronquiales debido al daño epitelial producido por el protozoario, lográndose la mejoría del paciente. Si bien el tratamiento con los imidazoles erradica la infestación pulmonar, no evita el daño epitelial. Por lo que es de importancia el control clínico del paciente.
CONCLUSIÓN
Se presenta en este reporte de caso, un paciente sin factores de riesgo identificados con infección pulmonar por Lophomona blattarum, constituyendo el primer caso en paciente aparentemente sano en reportarse en México. Aunque no es una enfermedad común, debe de considerarse como diagnóstico diferencial en los pacientes con síntomas pulmonares sometidos a diversos esquemas de tratamiento y que no se obtiene la mejoría esperada y que tengan factores de riesgo como el estado de inmunosupresión, hábitat rural, higiene deficiente, síntomas recurrentes, entre otros. Así mismo es importante sospechar e identificar patologías respiratorias de base, como lo es el paciente asmático con pobre control a esquemas de medicamento convencionales. Por lo anterior el seguimiento de los pacientes no debe de limitarse a la erradicación del protozoario, sino identificar una afección pulmonar coexistente, y en caso de que existiera, administrar un tratamiento pertinente. El control de la evolución debe incluir pruebas de función pulmonar y estudios de gabinete como radiografía de tórax, TAC de tórax, y cultivo de esputo para detectar un posible daño en el parénquima pulmonar.











 nueva página del texto (beta)
nueva página del texto (beta)