ANTECEDENTES
La Organización Mundial de la Salud (OMS) define un fármaco biológico al producto proteico bioterapéutico creado mediante tecnología de ácido desoxirribonucleico (ADN) recombinante.1 El nombre de un anticuerpo monoclonal se compone de: un prefijo específico, dos subelementos que indican el objetivo y la fuente del anticuerpo (“u” humano, “o” ratón, “xi” quimérico con 25% murino, “zu” humanizado con 2–5% murino), y el sufijo común “mab”.2
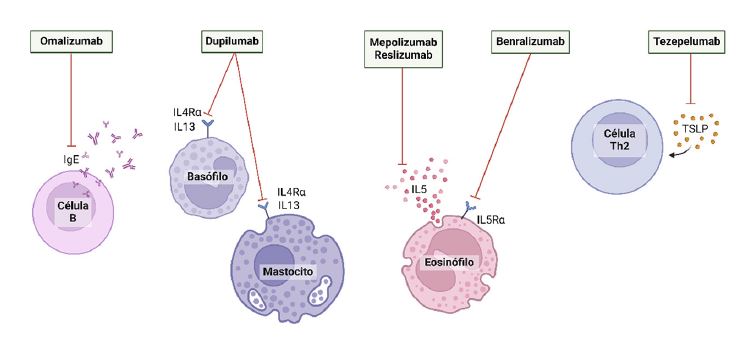
Los anticuerpos monoclonales representan una opción de tratamiento en pacientes con enfermedades alérgicas, autoinmunes, oncológicas, entre otras. Su función consiste en inhibir las interacciones entre moléculas efectoras y sus receptores específicos, o bloquear receptores funcionales.3 Figura 1
El aumento de su prescripción ha provocado un incremento de las reacciones adversas a medicamentos.2
Las reacciones adversas a medicamentos son respuestas perjudiciales, inesperadas e indeseadas de algún tratamiento, a dosis prescritas para prevención, diagnóstico o protocolo de tratamiento.4 Estas reacciones se clasifican en: 1) tipo A, que dependen de la acción del medicamento, dosis, farmacocinética, condiciones médicas e interacciones; y 2) tipo B, menos definidas y relacionadas con el sistema inmunológico, mayoritariamente reacciones de hipersensibilidad (tipos I, III y IV, que representan el 15% de todas las reacciones adversas a medicamentos).5
Las reacciones adversas de los fármacos biológicos, por su alta inmunogenicidad, difieren de las de los fármacos convencionales. Pichler propuso una nueva clasificación: Tipo alfa, por aumento de citocinas sistémicas, que se manifiestan con síndrome de liberación de citocinas y fiebre, fatiga, mialgia y síntomas gastrointestinales; Tipo beta, reacciones de hipersensibilidad mediadas por IgE, IgG, complemento o células T; Tipo gamma, por inmunosupresión del fármaco, facilitando infecciones o autoinmunidad; Tipo delta, por inhibición de moléculas sobreexpresadas en tumores; y Tipo épsilon, no relacionadas con el sistema inmunológico. 6
Las reacciones adversas por anticuerpos monoclonales son menos frecuentes en los completamente humanos o humanizados, pues generan menor respuesta inmunogénica. Dependen del mecanismo implicado o excipientes alergénicos. 7 La Sociedad Española de Reumatología reportó 16,361 reacciones adversas en 6754 pacientes que recibieron anticuerpos monoclonales, principalmente anti-TNF-α, de los que 2788 fueron graves y 215 mortales. 6
En la actualidad, por tratarse de estrategias de tratamiento personalizadas y específicas, se consideran prometedoras para el tratamiento de enfermedades alérgicas. Su indicación en pacientes con asma, dermatitis atópica, alergia alimentaria, urticaria, entre otras, ha mostrado un incremento significativo. 3
Con base en lo anterior, el objetivo de este estudio fue: describir la prescripción de anticuerpos monoclonales en el tratamiento de enfermedades alérgicas, abordando la farmacocinética, farmacodinámica, posología, contraindicaciones y reacciones adversas.
METODOLOGÍA
La búsqueda de información se llevó a cabo en las principales bases de datos médicas, acerca de la aplicación de anticuerpos monoclonales en el tratamiento de enfermedades alérgicas. La revisión de la bibliografía abarcó aspectos clave: farmacocinética, farmacodinámica, posología, contraindicaciones, y otros factores relevantes de los biológicos empleados en estas enfermedades. Se limitó la búsqueda para artículos originales, publicados entre 2014 y 2024, en las bases Scopus, Web of Science, MEDLINE y EMBASE, en idioma inglés y español.
Declaración de ética
La investigación se emprendió de acuerdo con la Declaración de Helsinki.
Omalizumab
Es un anticuerpo monoclonal humanizado, producido a partir de una línea celular mamífera de ovario de hámster chino, mediante tecnología de ADN recombinante. 8
Mecanismo de acción
Omalizumab es un anticuerpo monoclonal humanizado tipo Inmunoglobulina G1 (IgG1) kappa, que se une selectivamente a la IgE. Los efectos específicos del medicamento incluyen: 9-12
Reducción rápida de IgE libre sérica en el 99% de los casos después de dos horas de la administración.
Regulación negativa del receptor de alta afinidad para IgE (FcεRI) en basófilos, células dendríticas, mastocitos y monocitos en siete días.
Los receptores FcεRI en los basófilos disminuyen un 93% a los tres meses.
Disminución significativa de la cantidad de células dendríticas mieloides y plasmocitoides.
Disminución de la proliferación de células T dependientes de células dendríticas en cultivos estimulados con alérgeno de gato.
Disminución significativa de la capacidad de las células mononucleares en cultivo para liberar IL-5.
Reducción del aclaramiento de endotelina-1 en el aire exhalado de pacientes con asma.
Reducción del espesor de la pared bronquial y aumento del área endoluminal bronquial.
Reversibilidad de la remodelación en el epitelio ciliado y reducción en los espacios intracelulares y en el espesor de la membrana basal.
Nombre comercial y presentación
Xolair® 150 mg, solución inyectable con jeringa precargada
Xolair® 300 mg, solución inyectable con jeringa precargada
Xolair® 150 mg, solución inyectable con pluma precargada
Xolair® 300 mg, solución inyectable con pluma precargada
Indicaciones (Cuadro 1)
Cuadro 1 Principales indicaciones de omalizumab (aprobadas por la FDA y en estudio)
| Indicaciones aprobadas por la FDA | |||||
|---|---|---|---|---|---|
| Objetivo del tratamiento | Mecanismo de acción | Grupos de edad | Dosis y vía de administración | Eficacia | Principales efectos adversos |
| Asma alérgica grave (eosinofílica) | Impide la unión de la IgE al receptor de la IgE de alta afinidad en los basófilos y mastocitos. | Adolescentes mayores de 6 años y adultos. | La dosis deberá ajustarse según el peso y la concentración de IgE. La dosis máxima recomendada es de 600 mg cada dos semanas. | Disminución de la estimulación con el alérgeno en un 90%. Reducción de las exacerbaciones graves, visitas al servicio de urgencias, mejoría de la función pulmonar y mejoría en la calidad de vida. | Reacciones anafilácticas, en general en las primeras 3 aplicaciones; infecciones virales, enfermedad del suero; infecciones parasitarias. |
| Rinosinusitis crónica con pólipos nasales (RSCcPN) | Niños a partir de los 18 años. | La dosis deberá ajustarse según el peso y la concentración de IgE. La dosis máxima recomendada es de 600 mg cada dos semanas. | Disminución de SNOT, puntuación de pólipos (NPS), congestión nasal, eosinófilos, IgE, gravedad del asma y aumento de olfato. | ||
| Urticaria crónica espontánea | Pacientes mayores de 12 años. | 300 mg cada 4 semanas. | Disminución de IgE sérica libre en un 95%. Las concentraciones de IgE total en suero aumentaron debido a la formación de complejos omalizumab-IgE, con una velocidad de eliminación más lenta comparada con la IgE libre. | ||
| Indicaciones en estudio (off label) | |||||
| Pénfigo ampolloso | Impide la unión de la IgE al receptor de IgE de alta afinidad en los basófilos y mastocitos. | Pacientes mayores de 18 años. | La dosis deberá ajustarse según el peso y la concentración de IgE. Dosis entre 100 y 525 mg cada 2 a 8 semanas durante 20 meses. | Disminución de anticuerpos IgE. Disminución de la prescripción de corticosteroides e inmunosupresores. | Reacciones anafilácticas, en general en las primeras tres aplicaciones; enfermedad del suero; infecciones parasitarias; sensibilidad al látex. |
| Gastritis eosinofílica | A partir de los 18 años. | La dosis deberá ajustarse según el peso y la concentración de IgE. | Disminución de los síntomas y de la concentración de IgE, con reducción de la eosinofilia, no estadísticamente significativa. | ||
| Alergia alimentaria | Pacientes mayores de 18 años. | La dosis deberá ajustarse según el peso y la concentración de IgE. | Disminución de los síntomas y de la concentración de IgE, con reducción de la eosinofilia, con reducción significativa de la expresión de superficie de FcεRI en los basófilos y células dendríticas. | ||
| Mastocitosis cutánea | Pacientes mayores de 18 años. | La dosis deberá ajustarse según el peso y la concentración de IgE. | Disminución significativa de la expresión de superficie de FcεRI en los basófilos y células dendríticas. | ||
| Dermatitis atópica | Pacientes mayores de 18 años. | La dosis deberá ajustarse según el peso y la concentración de IgE. | Disminución de los síntomas (SCORAD) y mediciones de IgE, con reducción de la eosinofilia. | ||
Posología
La dosis recomendada en pacientes con asma es de 75 a 375 mg, por vía subcutánea; en rinosinusitis crónica y poliposis nasal, al igual que en los casos con alergia alimentaria mediada por IgE, 75 a 600 mg por vía subcutánea; en urticaria crónica espontánea de 150 a 300 mg por vía subcutánea, cada 2 a 4 semanas. La dosis se determina miligramos (mg) y la frecuencia por los valores de IgE total (IU/mL) medida antes del inicio del tratamiento y por peso en kilogramos (kg). Figura 2
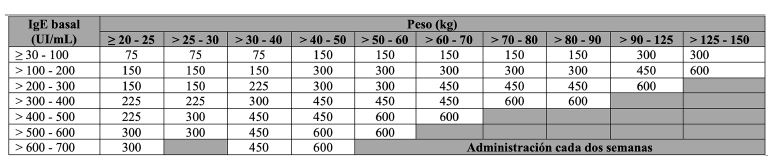
Figura 2 Dosis de omalizumab por vía subcutánea cada dos semanas, de acuerdo con el peso y la concentración sérica basal de IgE. 1
Advertencias y precauciones
No está indicada en exacerbaciones agudas del asma ni en enfermedades autoinmunes, insuficiencia renal o hepática preexistentes. Puede haber anafilaxia por mecanismos mediados por IgE.8-9
Se han reportado casos de enfermedad del suero por la formación de inmunocomplejos, debido a la producción de anticuerpos contra omalizumab con mecanismos de hipersensibilidad tipo III. Los pacientes pueden padecer fiebre, artralgias, eritema y infadenopatía.
Incluso se han informado eosinofilias sistémicas y cuadros de vasculitis, por ejemplo: granulomatosis eosinofílica con poliangeítis. Puede exacerbar enfermedades parasitarias por helmintos.
Interacciones con otros medicamentos
Omalizumab es medicamento seguro, la ficha técnica del fabricante refiere que no se elimina por bombas de flujo o mediante la vía del citocromo P450; por lo tanto, solo existe riesgo potencial para la interacción medicamento a medicamento.8 La eliminación de anticuerpos monoclonales se lleva a cabo por el sistema retículo endotelial, por lo que el complejo omalizumab-IgE se elimina de forma más lenta que la IgE sola. Existe evidencia con algunos anticuerpos monoclonales que los medicamentos inmunosupresores afectan su concentración sérica y tiempo de eliminación.18
Dentro de los efectos adversos se han reportado: aumento de infecciones virales y riesgo de enfermedades parasitarias; por tanto, debe vigilarse estrechamente a los pacientes que reciben este tipo de medicamentos.19 Aunque no se considera un medicamento, la inmunoterapia específica con alérgenos o venenos, concomitante con la indicación de omalizumab, ha informado disminución de efectos adversos con esta combinación.20
Fertilidad, embarazo y lactancia
Omalizumab es transportado a través de la placenta. Los estudios en animales informan que las alteraciones en la fertilidad no se han alterado, incluso con dosis diez veces mayores.1 Recientemente, los estudios EXPECT, entre otros, evaluaron a neonatos y mujeres embarazadas expuestas a omalizumab, al menos con una dosis dentro de las 8 semanas anteriores a la concepción, y no encontraron un aumento significativo en las anomalías congénitas, prematuridad ni bajo peso al nacimiento.21,22
Los estudios en monos Cynomolgus identificaron concentraciones de omalizumab en la leche materna del 0.15% de los valores séricos maternos; la indicación de omalizumab durante la lactancia no ha demostrado aumento de infecciones.8,23,24
Reacciones adversas
Omalizumab provoca reacciones sistémicas, efectos potenciales en malignidad, riesgo de enfermedad parasitaria y efectos inmunológicos; los más frecuentes son: reacciones en el sitio de inyección e infecciones virales, principalmente del sistema respiratorio.19
Las reacciones anafilácticas se han reportado en el 0.09% de los casos en las primeras dos horas de la aplicación, por lo que se recomienda vigilancia con las tres primeras aplicaciones. Otro tipo de reacción informada es la enfermedad del suero.25,26
Con el aumento de la prescripción de omalizumab se han evaluado a 40,000 pacientes por diferentes enfermedades, y aunque se han informado tumores en algunos casos, el riesgo de aparición no es mayor que el de la población general.27
Dupilumab
Dupilumab es un anticuerpo monoclonal inmunoglobulina G4 (IgG4) que se une a la subunidad alfa del receptor de Interleucina-4 (IL-4, IL-4Rα), inhibiendo la señalización de IL-4 a través del receptor Tipo I (IL-4Rα/γc) y, a su vez, a la interleucina 13 (IL-13) a través del receptor de Tipo II (IL-4Rα/IL-13Rα).28
El eje IL-4/IL-13/IL-4R promueve la diferenciación de las células TH2, por lo que la inhibición de esta vía regula negativamente la señalización de células TH2.
Mecanismo de acción
Los posibles mecanismos de acción incluyen: inhibición de la unión de IL-4 a IL-4Rα, inhibición del reclutamiento de γc a la cadena de IL-4Rα, e inhibición del reclutamiento de IL-4Rα a IL-13Rα1.29
Nombre comercial y presentación
En México se comercializa con el nombre DUPIXENT®, con dos presentaciones para aplicación subcutánea: plumas o jeringas precargadas, con dosis de 300 mg/2 mL y 200 mg/1.14 mL.30
Indicaciones (Cuadro 2)
Dupilumab se encuentra aprobado por la Food and Drug Administration (FDA) para el tratamiento de la dermatitis atópica, de moderada a grave, en pacientes no controlados; incluso en 2018 se aprobó para pacientes con asma moderada a grave (eosinófilos en sangre > 150 células/μL y/o FeNO > 25 ppb). Ha demostrado resultados prometedores en pacientes con rinosinusitis crónica y esofagitis eosinofílica.28
Cuadro 2 Principales indiciaciones de dupilumab (aprobadas por la FDA*)
| Objetivo del tratamiento | Mecanismo de acción | Grupos de edad | Dosis y vía de administración | Eficacia | Principales efectos adversos |
|---|---|---|---|---|---|
| Asma grave (eosinofílica)* | Unión a receptores IL-4Rα/γc y IL-4Rα/IL-13Rα impidiendo la unión de IL-4 e IL-13 en las células B, eosinófilos, células epiteliales (piel) y células del músculo liso respiratorio. | Adolescentes mayores de 12 años y pacientes adultos. | Dosis de carga inicial de 400 mg y dosis posterior de 200 mg cada 14 días por vía subcutánea. | Reducción de las exacerbaciones del asma y mejoría de la función pulmonar.12 | Infecciones helmínticas y reacciones de hipersensibilidad (enfermedad del suero).12 |
| Dermatitis atópica (moderada a grave)* | Niños a partir de 6 años adultos | Dosis inicial de 600 mg, seguida de 300 mg cada 14 días por vía subcutánea. | Disminución del prurito y los síntomas de ansiedad y depresión. | Conjuntivitis, blefaritis, queratitis, prurito ocular y ojo seco, eosinofilia transitoria (<2%), herpes zoster (<0.1%). Se han registrado dos casos de erupción cutánea después de su aplicación. | |
| Esofagitis eosinofílica* | Adolescentes >12 años y adultos (peso mayor a 40 kg) | Dosis semanal de 300 mg por vía subcutánea | Reducción de la disfagia entre la semana 10 y 12 de tratamiento. | Dolor en el sitio de la aplicación y nasofaringitis (único efecto reportado).16 | |
| Rinosinusitis crónica con poliposis* | Adultos | Dosis semanal de 300 mg por vía subcutánea | Reducción de los síntomas en pacientes con cirugías previas (aún se requieren estudios adicionales). | Tos, cefalea, eritema y dolor en el sitio de infección (3.6%).17 | |
| Neumopatía obstructiva crónica | Adultos | 300 mg cada dos semanas, vía subcutánea. | Reducción de las exacerbaciones, de moderadas a graves; mejoría de la función pulmonar y disminución de los síntomas en general. | No se han reportado. |
*Aprobadas por la FDA*
Posología
Dermatitis atópica: en adultos se recomienda una dosis inicial de 600 mg, seguida de 300 mg, administrada cada 14 días.
Asma: en pacientes mayores de 12 años se indica una dosis de carga inicial de 400 mg y posteriormente 200 mg cada 14 días.31
Rinosinusitis crónica con poliposis nasal: la dosis recomendada en adultos es de 300 mg, administrada cada dos semanas.
Esofagitis eosinofílica: en pacientes mayores de 12 años (con peso mínimo de 40 kg) se sugiere 300 mg cada semana.30,31
Contraindicaciones
Hipersensibilidad conocida a dupilumab o cualquier excipiente del fármaco.32 Debe considerarse la hipersensibilidad a la proteína de hámster, porque se produce en células ováricas de hámster chino. No se cuenta con suficiente información acerca de otras contraindicaciones; sin embargo, se puntualizan advertencias y precauciones en su prescripción.30
Precauciones
Las reacciones de hipersensibilidad ocurren en menos del 1% de los pacientes; debe haber especial cuidado en los casos con enfermedad del suero, urticaria, angioedema, eritemas cutáneo, nodoso o multiforme, y anafilaxia.31
Considerar la vigilancia de manifestación de novo o cuando empeora la artralgia.
Antes de iniciar el tratamiento con dupilumab deberá llevarse a cabo la valoración oftalmológica, debido al riesgo de conjuntivitis y queratitis, incluso diagnosticar y tratar infecciones parasitarias.
Prescribir con cautela en pacientes con eritema vasculítico, enfermedades pulmonares exacerbadas, neuropatía o quienes reciben corticosteroides.32
No se tiene información concreta, pero se recomienda evitar la aplicación de vacunas con virus vivos en pacientes que reciben dupilumab.30
Fertilidad, embarazo y lactancia
Es el fármaco de elección en pacientes embarazadas con dermatitis atópica que requieren tratamiento sistémico; sin embargo, se han reportado casos de embarazo heterotópico y aborto espontáneo en mujeres que concibieron mientras recibían dupilumab, por lo que es necesario valorar el riesgo-beneficio.31,33 No altera la fertilidad masculina.34
La excreción en la leche materna es mínima, debido a su alto peso molecular; no obstante, se requieren estudios adicionales para determinar sus efectos durante la lactancia.35
Reacciones adversas
Las más frecuentes son: nasofaringitis, bronquitis, cefalea y eritema en el sitio de aplicación; la inyección conjuntival moderada a severa es común en pacientes con dermatitis atópica, secundario a conjuntivitis, blefaritis, queratitis, prurito ocular y ojo seco. Dentro de los efectos adversos graves se reportan exacerbaciones de asma y neumonía.36
Otros efectos reportados son: herpes oral, eosinofilia, insomnio, gastritis, odontalgia, y artralgias.30 Se han informado dos casos de erupción facial, el más reciente en 2019, coincidiendo con cada administración de dupilumab; la causa aún no es clara, pero se consideran otras posibles etiologías como: dermatitis de contacto y erupción por microorganismos comensales (Pityrosporum) incluso alguna afección autoinmune; no obstante, se requieren nuevos estudios para demostrar este hecho.37
Mepolizumab
Mecanismo de acción
Mepolizumab es un anticuerpo monoclonal humanizado, producido por tecnología del ADN recombinante, que se une con alta afinidad y especificidad a IL-5, citocina reguladora de los eosinófilos en sangre periférica y tisular, bloqueando su interacción con el receptor, lo que inhibe la cascada de señalización y resulta en disminución de la inflamación eosinofílica.38
Nombre comercial y presentación
El producto comercial es Nucala® y se encuentra en las siguientes presentaciones:
Caja con 1 o 3 frascos ámpulas de 100 mg de polvo liofilizado cada uno.
Caja con 1 o 3 autoinyectores o con 1 o 3 jeringas prellenadas, cada una de 100 mg/1 mL.
Caja con 1 o 3 jeringas prellenadas de 40 mg/0.4 mL.39
Indicaciones (Cuadro 3)
Asma grave eosinofílica, como tratamiento adicional en pacientes adultos, adolescentes y niños a partir de 6 años.40,41
Rinosinusitis crónica con pólipos nasales, como tratamiento adicional con corticosteroides intranasales en adultos, en quienes los corticosteroides sistémicos y/o la cirugía no proporcionan control adecuado de la enfermedad.42
Granulomatosis eosinofílica con poliangeítis recurrente-remitente o resistente al tratamiento convencional en pacientes de 6 años o mayores.43
Síndrome hipereosinofílico no controlado adecuadamente, sin alguna causa secundaria hematológica identificable.44
Cuadro 3 Principales indiciaciones de mepolizumab2,8
| Objetivo del tratamiento | Mecanismo de acción | Grupos de edad | Dosis y vía de administración | Eficacia | Reacciones adversas |
|---|---|---|---|---|---|
| Asma grave (eosinofílica)** | Unión de alta especificidad a IL-5, citocina reguladora de los eosinófilos en sangre periférica y tisular. | Niños mayores de 6 años; adolescentes y adultos. | Pacientes pediátricos de 6-11 años: 40 mg cada 4 semanas, sin tiempo definido. Adolescentes y adultos: 100 mg cada 4 semanas sin tiempo definido. Aplicar por vía subcutánea en brazo proximal, la cara anterolateral del muslo o el abdomen. | Disminución del 20-40% de las exacerbaciones del asma, reducción mayor del 50% de la dosis diaria del corticosteroide inhalado respecto de la dosis basal. Incremento del FEV1 y reducción de FeNO. | Infección por Herpes zóster, enfermedades parasitarias, reacciones de hipersensibilidad. |
| Rinosinusitis crónica con pólipos nasales** | Niños mayores de 12 años; adolescentes y adultos. | 100 mg cada 4 semanas sin tiempo definido. Aplicar por vía subcutánea en brazo proximal, la cara anterolateral del muslo o el abdomen. | Disminución del tamaño de los pólipos nasales; reducción de la sensación de obstrucción nasal y del requerimiento de cirugía. | Infección por Herpes zóster, enfermedades parasitarias, reacciones de hipersensibilidad. | |
| Granulomatosis eosinofílica con poliangéitis** | Dosis total de 300 mg: 100 mg cada 4 semanas hasta completar tres dosis (5 cm de separación entre los sitios de aplicación). Aplicar por vía subcutánea en brazo proximal, la cara anterolateral del muslo o el abdomen. | Desaparición de los síntomas de vasculitis en 32% de los casos. | Infección por Herpes zóster, enfermedades parasitarias, reacciones de hipersensibilidad. | ||
| Síndrome hipereosinofílico** | Dosis total de 300 mg: 100 mg cada 4 semanas hasta completar tres dosis (5 cm de separación entre sitios de aplicación). Vía Subcutánea en brazo proximal, cara anterolateral de muslo y abdomen. | Disminución de las exacerbaciones del asma. | Infección por Herpes zóster, enfermedades parasitarias, reacciones de hipersensibilidad. | ||
| Esofagitis eosinofílica, gastritis eosinofílica, neumonitis eosinofílica | Pacientes adultos, de 16 a 75 años. | Dosis total de 900 mg: 300 mg cada 4 semanas por 3 meses. Vía Subcutánea en brazo proximal, cara anterolateral de muslo o abdomen. | Sin disminución de los síntomas relacionados con fibrosis o remodelamiento del tejido. En la endoscopia se observa disminución del infiltrado. | Infección por Herpes Zóster, enfermedades parasitarias, reacciones de hipersensibilidad. |
*Aprobados por FDA**
Posología
Mepolizumab se aplica por vía subcutánea y está autorizado en pacientes de 6 años o mayores. Se han establecido dos esquemas de dosis según la enfermedad, y en niños de 6 a 11 años sólo se ha definido la dosis para asma grave eosinofílica.39,45 Figura 1
Contraindicaciones
Está contraindicado en pacientes con antecedente de hipersensibilidad al fármaco o excipientes de la fórmula, por ejemplo: polisorbato 80, fosfato de sodio difásico heptahidrato y sacarosa.46 En cuanto a pacientes con enfermedad renal crónica, es seguro en quienes tienen tasa de filtración glomerular entre 50-80 mL/min o mayor.39
Advertencias y precauciones
Se han establecido las siguientes precauciones antes de su administración:
No debe prescribirse en pacientes con broncoespasmo o exacerbación del asma.
No suspender abruptamente los corticosteroides sistémicos o inhalados al iniciar el tratamiento. Es importante disminuir la dosis gradualmente.
No aplicar en pacientes con infección por helmintos y deberá tratarse la infección antes de prescribir el fármaco biológico.39,45,47
Interacciones con otros medicamentos
Se han descrito interacciones con deucravacitinib, efgartigimod alfa, fexinidazole, ritecitinib, rozanolixizumab y tejido alogénico tímico procesado.
Fertilidad, embarazo y lactancia
Mepolizumab tiene un peso molecular de 149,000 Da, y es capaz de cruzar la barrera placentaria. Su prescripción durante el segundo y tercer trimestres se relaciona con efectos adversos.48 Los estudios de seguridad del fármaco provienen de estudios en animales, y no han reportado efecto embriotóxicos ni teratogénicos durante el embarazo, parto o lactancia.
Un ensayo en una paciente embarazada reportó que su consumo continuo no demostró efectos adversos para el feto y la madre durante, incluso durante la lactancia.49 Se requieren investigaciones adicionales para confirmar su seguridad. En cuanto a la fertilidad, se ha demostrado que puede disminuir las condiciones generales durante el embarazo.50
Reacciones adversas
La mayor parte son leves a moderadas, un estudio informó que 9 (2.8%) de 321 pacientes que recibieron omalizumab manifestaron reacciones adversas, principalmente mujeres. 51 Las principales reacciones se asocian con: dolor en el sitio de aplicación, pirexia, dolor abdominal y torácica, y cefalea. 52
En cuanto al riesgo de infecciones en pacientes que reciben anticuerpos monoclonales anti-IL-5, un metaanálisis de 21 estudios, con población total de 9156 pacientes, no reportó diferencias significativas versus placebo en pacientes con nasofaringitis (OR: 0.90; IC95%: 0.76-1.07) faringitis (OR: 1.45; IC95%: 0.92 a 2.28), infección de vías respiratorias altas (OR: 0.97; IC95%: 0.82 a 1.15), rinitis (OR: 1.01; IC95%: 0.71-1.44), bronquitis (OR: 0.56; IC95%: 0.10 a 2.01), influenza (OR: 0.84; IC95%: 0.65-1.09). 43 La incidencia de trastornos del tejido conectivo y musculoesqueléticos relacionados fue del 1.6%. 52,53
El riesgo de infección por Herpes zoster es poco definido, aún así se recomienda la vacunación previa. El riesgo de infecciones parasitarias es incierto, debido a la función de los eosinófilos en la depuración de parásitos.46 Los pacientes con infecciones parasitarias preexistentes requieren tratamiento antes de iniciar el protocolo con mepolizumab. En caso de infección durante el tratamiento, o que no respondan a éste, deberá suspenderse el protocolo hasta que desaparezca el cuadro. Se recomienda la búsqueda previa y monitoreo de procesos parasitarios durante el tratamiento.39,45-47,51
Benralizumab
Mecanismo de acción
Es un anticuerpo monoclonal humanizado (IgG1, kappa), producido en las células de ovarios de hámster (COH) mediate tecnología de ADN recombinante. Funciona en el receptor de alta afinidad de la interleucina-5 humana (IL-5Rα), que ocasiona un descenso en la cuenta de eosinófilos, originada por apoptosis celular dependiente de anticuerpos.51
La IL-5 es la principal citoquina implicada en la activación de los eosinófilos y es decisiva para el desarrollo, maduración y supervivencia de los eosinófilos en los tejidos. Benralizumab se une a la subunidad α del IL-5Rα con alta afinidad y especificidad. El receptor de IL-5 se expresa de forma específica en la superficie de los eosinófilos y basófilos, bloqueando la vía de señalización de la IL5, inhibiendo la proliferación de líneas celulares dependientes de ésta.
Nombre comercial y presentación
Fasenra®
La jeringa prellenada contiene: Benralizumab 30 mg, Vehículo cbp 1 mL
La pluma precargada contiene: Benralizumab 30 mg, Vehículo cbp 1 mL55
Indicaciones (Cuadro 4)
Está indicado en el tratamiento de mantenimiento en pacientes mayores de 6 años con asma grave de fenotipo eosinofílico, y no controlado. Sin embargo, existen reportes de casos de "off label" en síndromes eosinofílicos resistentes al tratamiento, rinosinusitis con poliposis, granulomatosis eosinofílica con poliangeítis, síndromes eosinófilos resistentes al tratamiento.56,57
Cuadro 4 Principales indiciaciones de benralizumab
| Objetivo del tratamiento | Mecanismo de acción | Grupos de edad | Dosis y vía de administración | Eficacia | Principales efectos adversos |
|---|---|---|---|---|---|
| Asma grave (eosinofílica)* | Unión con la subunidad alfa del receptor de interleucina 5 (IL-5Rα) e inhibición de la proliferación de líneas celulares dependientes de ésta. | Recientemente aprobado en niños mayores de 6 años y en pacientes adultos. | Los pacientes por debajo de 35 kg deberán recibir dosis de 10 mg, y por arriba de 35 kg aplicar 30 mg cada 4 semanas las primeras tres dosis y luego cada 8 semanas. Aplicar por vía subcutánea. | Reducción de las exacerbaciones del asma y mejoría de la función pulmonar.12 | Cefalea y pirosis. Reportes de anafilaxia. No existen protocolos diagnósticos de reacciones de hipersensibilidad reportados. |
| Granulomatosis eosinofílica por poliangeítis (off label) | Pacientes mayores de 18 años. | Aplicar tres dosis de 30 mg cada 4 semanas y posteriormente cada 8 semanas. | El 67.1% de los casos se cura luego de un año de tratamiento. El 87.1% permanece libre de recaídas. Reducción del consumo de corticoesteroides. | Recaída en el 15% de los casos. | |
| Rinosinusitis crónica por pólipos nasales (off label) | Pacientes mayores de 18 años. | Aplicar tres dosis de 30 mg mensual y luego cada 8 semanas. | Mejoría de la disomia, reducción de la obstrucción nasal y del índice Nasal Polip Score. | NR |
Posología
Hace poco se aprobó para niños de 6 a 11años, la dosis recomendada es de 10 mg, con peso menor a 35 kg; en sujetos por arriba de este peso se recomienda una de 30 mg por vía subcutánea cada 4 semanas las primeras 3 dosis y luego cada 8 semanas.58,59
Contraindicaciones
En pacientes con hipersensibilidad conocida a cualquiera de sus excipientes: histidina, trehalosa dihidrato, polisorbato 20 (e432); anafilaxia con otros anticuerpos monoclonales de tipo IgG; embarazo y la lactancia.54,60,61
Advertencias y precauciones
Debe evitarse en exacerbaciones agudas del asma. No se recomienda la suspensión abrupta de los corticosteroides.
Interacciones con otros medicamentos
Hasta el momento no se han efectuado estudios formales de interacción farmacológica.
Fertilidad, embarazo y lactancia
En la actualidad no está autorizado durante el embarazo y la lactancia. Naftel y colaboradores evaluaron la función de benralizumab en diferentes etapas del embarazo y observaron eficacia del medicamento, sin efectos secundarios evidentes. Sin embargo, los datos de la exposición durante el embarazo procedentes de ensayos clínicos son insuficientes para informar el riesgo asociado con el fármaco, pero sugiere que atraviesan la barrera placentaria por lo que el feto se encuentra más expuesto a partir del segundo y tercer trimestres de embarazo, con reducción de la cuenta de eosinófilos hasta los 7 meses de edad, sin evidencia de efectos teratogénicos.61
Se desconoce si benralizumab o sus metabolitos se excretan en la leche materna de humanos o animales; por lo tanto, no se descarta el riesgo para el lactante.
Reacciones adversas
Liu y su grupo realizaron un metaanálisis donde evaluaron la incidencia de efectos adversos y efectos secundarios en general de benralizumab, y encontraron un riesgo bajo (RR: 0.94) y elevada incidencia de eventos adversos al compararlos con placebo.
En ensayos controlados aleatorizados, la incidencia de reacciones adversas graves fue del 10.52%. En pacientes que recibieron al menos una dosis de benralizumab, la exacerbación del asma fue el evento adverso más frecuentemente, seguido de cefalea (8.32%), pirosis (4.14%), bronquitis (7.61%) y sinusitis (5.21%).
Reslizumab
Mecanismo de acción
Reslizumab es un anticuerpo monoclonal humanizado dirigido contra IL-5, que bloquea la bioactividad y disminuye la concentración de IL-5 biológicamente disponible. Reslizumab se une a IL-5 circulante en la región ERRR (ácido glutámico, arginina, arginina, arginina) con posterior inhibición de la bioactividad de IL-5, encargada de estimular la producción, maduración y activación de eosinófilos al interactuar con el complejo del receptor de IL-5, localizado en la membrana celular de los eosinófilos. Al inhibir su unión, reslizumab bloquea la cascada de señalización e inflamación patológica.62
Indicaciones terapéuticas (Cuadro 5)
En la Unión Europea está indicado en adultos con asma eosinofílica grave, con mal control, aún con el consumo de corticosteroides inhalados en altas dosis, en combinación con otro medicamento para el tratamiento de mantenimiento.65 En Estados Unidos se prescribe en pacientes mayores de 18 años con asma grave y algún fenotipo eosinofílico.66
Cuadro 5 Principales indiciaciones de reslizumab
| Objetivo del tratamiento | Mecanismo de acción | Grupos de edad | Dosis y vía de administración | Eficacia | Principales efectos adversos |
|---|---|---|---|---|---|
| Asma grave (eosinofílica)1 | Función antagonista de IL-5, impidiendo la unión con eosinófilos y bloqueando la cascada de señalización. | Pacientes mayores de 18 años (aprobado por EMA y FDA).4,5 | Dosis de 3 mg/kg por vía intravenosa cada 4 semanas (ajustar en caso de cambio de peso). 2,4 Duración de la infusión entre 20-50 minutos (no administrar en bolo).5 Diluir en 50 mL de solución salina al 0.9%.6 Administrar a una temperatura de 15 a 25°C.6 Utilizar equipo de infusión con baja unión a proteínas.6 | Mejoría en las pruebas de función pulmonar (FEV1, FVC, y FEF25-75) y calidad de vida; disminución de los síntomas y control del asma (puntuaciones AQLO, ACQ, ASUI).7 | Anafilaxia en 0.3% de los pacientes, anticuerpos contra reslizumab (5%), dolor orofaríngeo (3%).3,5 Mecanismo inmunológico implicado, reacción de hipersensibilidad tipo I. 13 |
Posología
La dosis recomendada es de 3 mg/kg, administrada cada 4 semanas por vía intravenosa. La infusión debe aplicarse entre 20 y 50 minutos.65,66 La dosis se ajusta en caso de cambio del peso importante. 63
Poblaciones especiales: en pacientes con insuficiencia renal o hepática no se ajusta la dosis. En adultos mayores no se recomienda el ajuste; los datos son limitados en sujetos mayores de 75 años. En la población pediátrica, la eficacia y seguridad no se ha establecido y hasta la fecha no se han establecido recomendaciones en pacientes menores de 18 años.67
Advertencias y precauciones
Exacerbaciones: no indicado en el tratamiento de crisis de asma.
Reacciones de hipersensibilidad: se han reportado reacciones adversas agudas sistémicas y anafilaxia durante la administración o en los siguientes 20 minutos de finalizar la infusión. En caso de este tipo de complicaciones deberá suspenderse la infusión.68
Infecciones por parásitos: los pacientes deberán recibir tratamiento para la infección por parásitos antes de iniciar el protocolo con reslizumab; si durante el tratamiento el paciente requiere terapia antihelmíntica, sin buena respuesta a la misma, deberá valorarse la suspensión de reslizumab temporalmente, debido a la respuesta inmunológica de estos macroorganismos, donde existe participación de eosinófilos.64,66
Malignidad: algunos estudios reportaron neoplasias sin ningún predominio histológico, principalmente en los primeros seis meses de la exposición a reslizumab.68 En un estudio de extensión sin ocultación se reportaron 15 neoplasias en receptores de reslizumab. Se consideró poco probable que estuvieran relacionadas con el medicamento e involucraron sitios como colon, mama, próstata y pulmón.69
Otros: se ha relacionado con elevación transitoria de creatina-fosfocinasa (toxicidad muscular).70
Interacciones con otros medicamentos
Los medicamentos: efgartigimod-alfa y rozanolixizumab pueden disminuir el efecto de los agentes de unión al receptor de fracción cristalizable (Fc). Su administración concomitante con reslizumab supone un riesgo tipo C, lo que implica su vigilancia.
Fertilidad, embarazo y lactancia
Los datos relacionados con anticuerpos monoclonales en el tratamiento del asma grave durante el embarazo son limitados. La vida media de estos fármacos debe considerarse en mujeres que desean embarazarse.71 Los anticuerpos monoclonales pueden considerarse cuando el tratamiento con fármacos convencionales es insuficiente.48 De manera general, este tipo de medicamentos no debe iniciarse durante el embarazo. La decisión de prescribirlos durante el embarazo debe hacerse de manera conjunta entre el médico y el paciente.71 En esta situación puede optarse por una alternativa al reslizumab.48
Debido al peso molecular de 147,000 dalton (Da), es probable que reslizumab se encuentre en concentraciones bajas en la leche materna. De igual manera, es probable que la absorción a nivel gastrointestinal en el lactante sea mínima. Por estos motivos, un consenso de expertos encontró que reslizumab es posiblemente aceptable durante la lactancia materna, aunque debe indicarse con precaución hasta contar con más información.48
Reacciones adversas
Se reportó anafilaxia en el 0.3% de los pacientes con asma que reciben reslizumab en estudios controlados con placebo. Los cuadros clínicos aparecieron en los primeros 20 minutos de haber completado la infusión y se registraron desde la segunda aplicación. Por tanto, su administración debe vigilarse por un tiempo razonable.64,66
El mecanismo inmunológico implicado es una reacción de hipersensibilidad tipo I.72 El 5% de los pacientes producen anticuerpos contra reslizumab y el 3% ha reportado dolor orofaríngeo.62,73
Tezepelumab
Mecanismo de acción
Tezepelumab (IgG2λ) se centra en dirigirse a la proteína del estrato tímico, citocina liberada por el epitelio respiratorio en respuesta a estímulos alérgicos y no alérgicos, inhibiendo la activación de eosinófilos, ILC2, células dendríticas, linfocitos TH2, TH17, IL5, IL-13, IL-17, importantes en la inflamación e hiperactividad de las vías aéreas en pacientes con asma.31,74-78
Nombre comercial y presentación
Tezspire®: disponible en un ámpula de 210 mg, en 1.91 mL de solución para aplicación por vía subcutánea.79
Indicaciones terapéuticas (Cuadro 6)
Tratamiento de mantenimiento adicional en adultos y adolescentes a partir de los 12 años con asma grave no controlada.80-82
Aumenta el volumen espiratorio forzado en el primer segundo (FEV1), reduce la puntuación de los síntomas y el riesgo de exacerbaciones en pacientes con asma no controlada. Tiene efectos benéficos en los parámetros clínicos de FEV1, ACQ-6, y tasa de exacerbación.80-83
El ensayo DESTINATION reportó disminución de la concentración de eosinófilos en sangre, y las concentraciones séricas de IgE y FeNO permanecieron sostenidas hasta la semana 104.83-85
Cuadro 6 Principales indiciaciones de tezepelumab
| Objetivo del tratamiento | Mecanismo de acción | Grupos de edad | Dosis y vía de administración | Eficacia | Principales efectos adversos |
|---|---|---|---|---|---|
| Asma grave (cualquier endotipo) | Bloqueo de la Proteína del estrato tímico TSLP, inhibiendo la activación de eosinófilos, ILC2, células dendríticas, Linfocitos TH2, TH17, IL-5, IL-13, IL-17 | Adolescentes mayores de 12 años y pacientes adultos. | Dosis de 210 mg cada 4 semanas | Reducción de las exacerbaciones del asma en un 60-90% de los casos con AAER; Mejoría de FEV1, ACQ6 | Odinofagia (4%), artralgías (4%), lumbalgia (4%). Eventos cardiacos (poco frecuentes). Reacciones de hipersensibilidad (excepcionales) y menores a las provocadas por otros biológicos. |
| Asma grave con poliposis nasal | Adolescentes mayores de 12 años y pacientes adultos. | Dosis de 210 mg cada 4 semanas | Aún en estudio de fase IIb. Reducción de AAER (tasas anuales de exacerbación del asma) en un grado similar al de pacientes con y sin NP. Reducción de las concentraciones de biomarcadores inflamatorios T2 (eosinófilos en sangre, FeNO e IL-5 e IL-13 en suero). | ||
| Dermatitis atópica moderada a grave | Pacientes de 18 a 75 años. | Dosis de 280 mg cada 2 semanas en combinación con corticosteroides tópicos clase 3 | Aun en estudio de fase IIa. | Nasofaringitis (23.2%), diarrea (8.9%), cefalea (5.4%), eritema en el sitio de aplicación (5.4%), quiste dérmico infectado (1.8%). |
Posología
Se recomienda una dosis de 210 mg cada 4 semanas, con ajuste en función del control del asma.80,85
Contraindicaciones
No debe indicarse en exacerbaciones agudas del asma; durante el tratamiento pueden manifestarse síntomas o exacerbaciones relacionadas. En caso de empeoramiento de los síntomas deberá suspenderse el medicamento. Hasta el momento no existen datos disponibles de eficacia y seguridad en pacientes menores a 12 años.83,84
Advertencias y precauciones
Los estudios actuales no han informado aumento de infecciones graves;80,81 sin embargo, se recomienda vigilar la aparición de infecciones por helmintos y evitar la aplicación concomitante de vacunas con virus vivas, pues no existen estudios relacionados con su seguridad. En caso de infección grave deberá interrumpirse el tratamiento.
Se recomienda suspender los corticosteroides de manera gradual y con supervisión médica.
Se han observado eventos cardíacos graves en un pequeño porcentaje de pacientes que reciben terapelumab versus placebo. Sin embargo, no se ha establecido una relación directa, y se ha reportado una incidencia similar con otros biológicos. Se recomienda informar a los pacientes acerca de los signos y síntomas de algún evento cardíaco grave: dolor en el pecho, dificultad respiratoria, malestar, mareos o desmayos. En caso de algún evento cardíaco grave deberá interrumpirse el tratamiento.83,86,87
Interacciones con otros medicamentos
No se han realizado estudios formales de interacción farmacológica.
Fertilidad, embarazo y lactancia
No existen suficientes datos de tezepelumab en mujeres embarazadas. Los anticuerpos IgG humanos pueden atravesar la barrera placentaria y transmitirse al feto en desarrollo.
Se recomienda evitar su consumo durante el embarazo, a menos que los beneficios esperados para la madre superen los posibles riesgos para el feto. Se desconoce si se excreta en la leche materna, por lo que debe evaluarse la relación entre los beneficios durante la lactancia y el tratamiento para la madre. Debe investigarse más acerca de la fertilidad y la concentración del medicamento en el organismo.81
Reacciones adversas
En caso de reacción de hipersensibilidad grave se recomienda interrumpir el medicamento.85
La incidencia de reacciones locales es baja y similar en el grupo aleatorizado (2.40 vs 2.15 en pacientes del estudio NAVIGATOR, diferencia 0.25; IC95%: -1.33 a 1.73; y 0.00 en el grupo de TZP vs 1.00 placebo del estudio SOURCE, -1.00, -5.46 a 1.91).
No se informaron efectos adversos graves en los estudios NAVIGATOR, SOURCE Y DESTINATION, que representan los ensayos con más datos acerca de efectos adversos en grandes grupos de pacientes. El ensayo de fase II reportó un caso de Guillain-Barré contra ninguno en el de fase III. Los efectos adversos generales y graves fueron similares entre ambos grupos.80,82,88 Los efectos adversos más comunes incluyeron: dolor de cabeza, infección de la vía respiratoria superior, cefalea y asma, este último en el grupo placebo. No hubo diferencias en la incidencia de malignidad y displasia benigna.
En el ensayo CASCADE, ningún paciente manifestó enfermedad maligna durante el periodo de prueba. En el DESTINATION tampoco se observaron efectos adversos significativos en menos del 10% de los pacientes. La incidencia de mortalidad fue similar en ambos grupos, sin identificarse patrones claros de mortalidad ni relación provocados por la dosis del medicamento.86,87
A destacar que la información proporcionada se basa en los estudios mencionados y pueden variar en situaciones individuales. Se recomienda investigar más sobre la accesibilidad y concentración en el organismo.80,84
Según el análisis post hoc, después del inicio de la pandemia, no se reportó aumento en las tasas de incidencia de COVID-19 durante el tratamiento.83,86,87
CONCLUSIONES
La recopilación de datos acerca de medicamentos biológicos es fundamental para que la comunidad médica pueda desarrollar una comprensión exhaustiva y actualizada de los anticuerpos monoclonales y sus aplicaciones clínicas.
El conocimiento profundo de las reacciones adversas a medicamentos mejora la capacidad de diagnóstico e identificación de diversas enfermedades, además de optimizar la calidad de la atención médica proporcionada a los pacientes. La información obtenida permitirá la formulación de tratamientos más eficaces y seguros, lo que contribuirá a una mejor eficiencia terapéutica y reducción significativa de riesgos asociados con la prescripción de este tipo de medicamentos.











 nueva página del texto (beta)
nueva página del texto (beta)